下列有关速率和平衡说法正确的是
| A.已知反应:CaCO3(s)⇌CaO(s)+CO2(g),在密闭的反应炉内达到平衡后,若其他条件均不改变,将反应炉体积缩小一半,则达到新平衡时CO2(g)的浓度将升高 |
| B.H2、I2、HI平衡混合气体加压后颜色变深,能用勒夏特列原理解释 |
C.重铬酸钾溶液中存在: (橙色) (橙色) (黄色) (黄色) ,若滴加少量NaOH溶液,平衡正移,溶液由橙色变黄色 ,若滴加少量NaOH溶液,平衡正移,溶液由橙色变黄色 |
| D.使用正催化剂,改变了反应历程和∆H,降低了反应的活化能,增大了活化分子百分数,化学反应速率增大 |
更新时间:2023-11-21 10:33:46
|
相似题推荐
单选题
|
较易
(0.85)
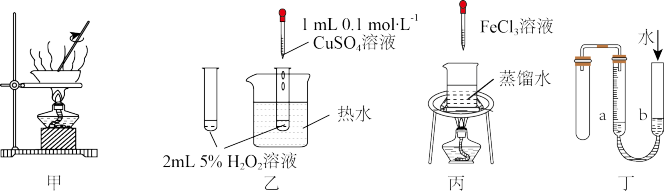
【推荐1】下列有关实验原理、装置、操作的描述中正确的是
| A | B | C | D |
 |  |  |  |
| pH试纸测量溶液的pH | 反应热的测定 | 研究催化剂对反应速率的影响 | 制取无水MgCl2 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
较易
(0.85)
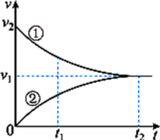
【推荐2】工业上苯乙烯的生产主要采用乙苯脱氢工艺:C6H5CH2CH3(g)  C6H5CH=CH2(g)+H2(g)。某条件下无催化剂存在时,该反应的正、逆反应速率v随时间t的变化关系如图所示。下列说法正确的是
C6H5CH=CH2(g)+H2(g)。某条件下无催化剂存在时,该反应的正、逆反应速率v随时间t的变化关系如图所示。下列说法正确的是
 C6H5CH=CH2(g)+H2(g)。某条件下无催化剂存在时,该反应的正、逆反应速率v随时间t的变化关系如图所示。下列说法正确的是
C6H5CH=CH2(g)+H2(g)。某条件下无催化剂存在时,该反应的正、逆反应速率v随时间t的变化关系如图所示。下列说法正确的是
| A.曲线①表示的是逆反应的v−t关系 | B.t1时刻体系处于平衡状态 |
| C.反应进行到t1时,Q>K(Q为浓度商) | D.当催化剂存在时,ν1、ν2都增大 |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐1】对于反应:CO2(g)+3H2(g) CH3OH(g)+H2O(g) △H<0,有利于提高平衡时CO2转化率的措施是
CH3OH(g)+H2O(g) △H<0,有利于提高平衡时CO2转化率的措施是
 CH3OH(g)+H2O(g) △H<0,有利于提高平衡时CO2转化率的措施是
CH3OH(g)+H2O(g) △H<0,有利于提高平衡时CO2转化率的措施是| A.使用催化剂 | B.加压 |
| C.增大CO2和H2的初始投料比 | D.升高温度 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐2】下列事实不能用勒夏特列原理解释的是
| A.在合成氨实际生产中,使气态氨变成液氨后及时从平衡混合物中分离出去,以提高原料的利用率 |
B. 、 、 、 、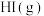 组成的平衡体系,加压后体系颜色变深 组成的平衡体系,加压后体系颜色变深 |
C.向重铬酸钾( )溶液中滴加少量NaOH溶液,溶液颜色由橙色变为黄色 )溶液中滴加少量NaOH溶液,溶液颜色由橙色变为黄色 |
| D.实验室中常用排饱和食盐水的方法收集氯气 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐1】下列说法中,能说明化学平衡一定向正反应方向移动的是( )
A.2HI(g) H2(g)+I2(g),改变某一条件后,气体颜色加深 H2(g)+I2(g),改变某一条件后,气体颜色加深 |
B.N2O4(g) 2NO2(g),单位时间内消耗 N2O4和 2NO2的物质的量之比大于 1:2 2NO2(g),单位时间内消耗 N2O4和 2NO2的物质的量之比大于 1:2 |
C.2SO2(g)+O2(g) 2SO3(g),改变某一条件后,SO3(g)的体积分数增加 2SO3(g),改变某一条件后,SO3(g)的体积分数增加 |
D.N2(g)+3H2(g) 2NH3(g),恒温恒压条件下,充入 He 2NH3(g),恒温恒压条件下,充入 He |
您最近一年使用:0次
【推荐2】一定条件下进行反应: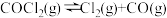 。向
。向 恒容密闭容器中加入
恒容密闭容器中加入
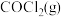 ,经过一段时间后达到平衡。反应过程中测得的有关数据见下表,下列说法正确的是
,经过一段时间后达到平衡。反应过程中测得的有关数据见下表,下列说法正确的是
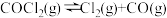 。向
。向 恒容密闭容器中加入
恒容密闭容器中加入
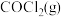 ,经过一段时间后达到平衡。反应过程中测得的有关数据见下表,下列说法正确的是
,经过一段时间后达到平衡。反应过程中测得的有关数据见下表,下列说法正确的是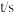 | 0 | 2 | 4 | 6 | 8 |
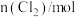 | 0 | 0.30 | 0.39 | 0.40 | 0.40 |
A.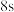 时加压,平衡向正反应方向移动 时加压,平衡向正反应方向移动 |
B.保持其他条件不变,升高温度,平衡时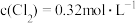 ,则反应的 ,则反应的 |
C.若在 恒容与外界没有热量变换的密闭容器中进行该反应,化学平衡常数不变 恒容与外界没有热量变换的密闭容器中进行该反应,化学平衡常数不变 |
D.保持其他条件不变,起始向容器中充入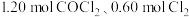 和 和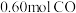 ,反应达到平衡前的速率: ,反应达到平衡前的速率: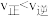 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐1】反应Fe(s)+CO2(g)⇌FeO(s)+CO(g),700℃时,k=1.47,900℃时,k=2.15.下列说法正确的是
| A.增加Fe用量可以提高速率 |
B.化学平衡常数表达式 |
| C.升高温度,正反应速率加快,逆反应速率降低 |
| D.该反应为吸热反应 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐2】已知:C(s)+H2O(g) CO(g)+H2(g) △H1 K1
CO(g)+H2(g) △H1 K1
CO(g)+H2O(g) CO2(g)+H2(g) △H2 K2
CO2(g)+H2(g) △H2 K2
CO2(g)+2H2(g)=C(s)+2H2O(g) △H3 K3
在同一温度下,下列关系正确的是
 CO(g)+H2(g) △H1 K1
CO(g)+H2(g) △H1 K1CO(g)+H2O(g)
 CO2(g)+H2(g) △H2 K2
CO2(g)+H2(g) △H2 K2CO2(g)+2H2(g)=C(s)+2H2O(g) △H3 K3
在同一温度下,下列关系正确的是
| A.△H3=-(△H1+△H2) K1·K2·K3=1 |
| B.△H3=△H1+△H2 K1+K2=K3 |
| C.△H3=-(△H1+△H2) K1·K2=K3 |
| D.△H3=△H1+△H2 K1·K2·K3=1 |
您最近一年使用:0次

 溶液制备无水
溶液制备无水 对
对 分解有催化作用
分解有催化作用
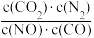
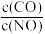 的值,NO的转化率下降
的值,NO的转化率下降

