名校
1 . 在二氧化碳合成甲醇的研究中,催化剂是研究的关键。目前国内外研究主要集中于铜基催化剂,有学者提出了如图CO2的转化过程。下列说法错误的是
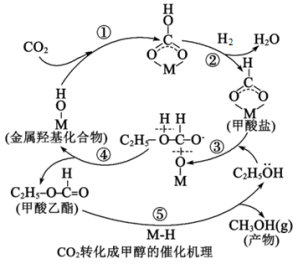

| A.铜元素位于周期表中的ds区 |
| B.步骤④中有化学键的断裂和形成 |
| C.甲酸乙酯是该过程的催化剂 |
D.总反应化学方程式为CO2+3H2 CH3OH+H2O CH3OH+H2O |
您最近一年使用:0次
2021-12-10更新
|
511次组卷
|
6卷引用:福建省南平高级中学2021-2022学年高三上学期12月月考化学试题
福建省南平高级中学2021-2022学年高三上学期12月月考化学试题湖北省十一校2021-2022学年高三上学期第一次联考(12月)化学试题(已下线)第十一单元 物质结构与性质(A卷 新题基础练)-2022年高考化学一轮复习单元滚动双测卷(新高考地区专用)(已下线)专题09 反应机理—2022年高考化学二轮复习讲练测(全国版)-测试(已下线)一轮巩固卷4-【赢在高考·黄金20卷】备战2022年高考化学模拟卷(湖北专用)四川省内江市第六中学2022-2023学年高二下学期入学考试化学试题
名校
解题方法
2 . 随着工业发展,空气污染也日益严重,其中NOx是主要污染源,最近科学家制备出了规整形貌的硫酸改性Fe2O3催化剂,该催化剂具有很好的NH3-SCR催化效果。研究表明,经过硫酸改性后的六方盘状Fe2O3催化活性和N2选择性都得到了极大的提升,催化流程如图所示。
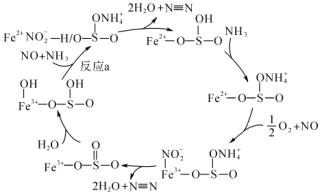
下列说法不正确的是

下列说法不正确的是
A.该反应的催化剂为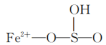 |
B.该过程可能发生的反应有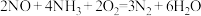 |
| C.反应a为化合反应 |
| D.硫酸改性后的六方盘状Fe2O3催化剂提高了NOx的去除率 |
您最近一年使用:0次
2021-11-19更新
|
184次组卷
|
3卷引用:福建省部分名校2021-2022学年高三上学期11月联合测评化学试题
名校
解题方法
3 . 常温下,向H2O2溶液中滴加少量Fe2(SO4)3溶液,反应原理如下图所示,下列说法不正确的是
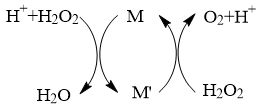

| A.该反应过程中,M是Fe3+, M’是Fe2+ |
B.该过程的总反应方程式为: 2H2O2 2H2O+O2↑ 2H2O+O2↑ |
| C.当反应中有1 mol O2生成时,转移电子数为2 mol |
| D.H2O2生产过程要严格避免混入Fe2+ |
您最近一年使用:0次
2021-11-17更新
|
333次组卷
|
3卷引用:福建省南安市侨光中学、昌财实验中学2021-2022学年高一上学期第二次阶段考化学试题
4 . 回答下列问题:
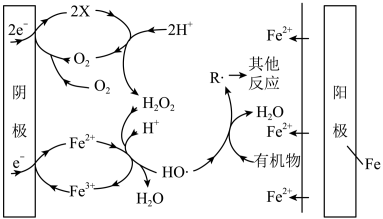
(1)EF、H2O2、FeOx,法可用于水体中有机污染物降解,其反应机理如图所示。阳极的电极反应式为____ ,X微粒的化学式为____ ,阴极附近Fe2+参与反应的离子方程式为___ 。
(2)将一定量的氢基甲酸铵置于恒容真空密闭容器中(固体试样体积忽略不计),在恒定温度下使其达到分解平衡:NH2COONH4(s) 2NH3(g)+CO2(g)。判断该分解反应已经达到化学平衡的是
2NH3(g)+CO2(g)。判断该分解反应已经达到化学平衡的是___ 。
a.2v正(NH3)=V逆(CO2)
b.密闭容器中c(NH3):c(CO2)=2:1
c.密闭容器中混合气体的密度不变
d.混合气体压强不再发生变化
e.气体的平均相对分子质量不变
(3)中科院化学所研究了下列反应的反应历程,如图所示:
CH3OH(g)+CO2(g)+H2(g) CH3COOH(g)+H2O(g)
CH3COOH(g)+H2O(g)
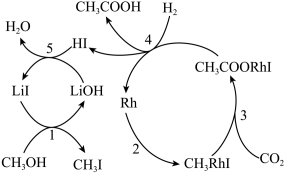
反应历程中,能降低反应活化能的物质有___ (填化学式);中间产物有___ 种。
(1)EF、H2O2、FeOx,法可用于水体中有机污染物降解,其反应机理如图所示。阳极的电极反应式为

(2)将一定量的氢基甲酸铵置于恒容真空密闭容器中(固体试样体积忽略不计),在恒定温度下使其达到分解平衡:NH2COONH4(s)
 2NH3(g)+CO2(g)。判断该分解反应已经达到化学平衡的是
2NH3(g)+CO2(g)。判断该分解反应已经达到化学平衡的是a.2v正(NH3)=V逆(CO2)
b.密闭容器中c(NH3):c(CO2)=2:1
c.密闭容器中混合气体的密度不变
d.混合气体压强不再发生变化
e.气体的平均相对分子质量不变
(3)中科院化学所研究了下列反应的反应历程,如图所示:
CH3OH(g)+CO2(g)+H2(g)
 CH3COOH(g)+H2O(g)
CH3COOH(g)+H2O(g)
反应历程中,能降低反应活化能的物质有
您最近一年使用:0次
名校
解题方法
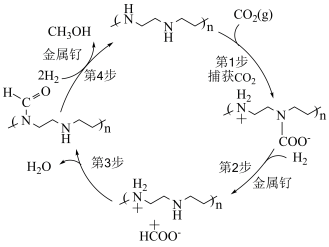
5 . 科学家致力于将大气中过多的 转化为有益于人类的物质,下图是一种可以从空气中捕获
转化为有益于人类的物质,下图是一种可以从空气中捕获 直接转化为甲醇的方法。下列说法正确的是。
直接转化为甲醇的方法。下列说法正确的是。
 转化为有益于人类的物质,下图是一种可以从空气中捕获
转化为有益于人类的物质,下图是一种可以从空气中捕获 直接转化为甲醇的方法。下列说法正确的是。
直接转化为甲醇的方法。下列说法正确的是。
A.从空气中每捕获 ,转移的电子数为 ,转移的电子数为 |
| B.第1步反应的原子利用率为100% |
| C.第4步反应中有极性键和非极性键的断裂和生成 |
D.该历程以金属钌、 作催化剂 作催化剂 |
您最近一年使用:0次
2021-10-12更新
|
358次组卷
|
5卷引用:福建省南平市高级中学2021-2022学年高三上学期第三次月考化学试题
福建省南平市高级中学2021-2022学年高三上学期第三次月考化学试题重庆市2022届高三第二次质量检测化学试题重庆市南开中学2022届高三第二次(10月)质量检测化学试题辽宁省渤海大学附属高级中学2021-2022学年高三上学期第三次考试化学试题(已下线)押新高考卷11题 反应机理分析-备战2022年高考化学临考题号押题(新高考通版)
名校
6 . 为了探究外界条件对过氧化氢分解速率的影响,某化学兴趣小组的同学做了以下实验。请回答下列问题:
(1)实验①的目的是___ 。
(2)实验②未观察到预期的实验现象,为了帮助该组同学达到实验目的,你提出的对上述操作的改进意见是____ (用实验中所提供的几种试剂)。
(3)对于H2O2分解反应,Cu2+也有一定的催化作用。为比较Fe3+和Cu2+对H2O2分解的催化效果,该兴趣化学小组的同学分别设计了如图所示的实验。请回答相关问题:
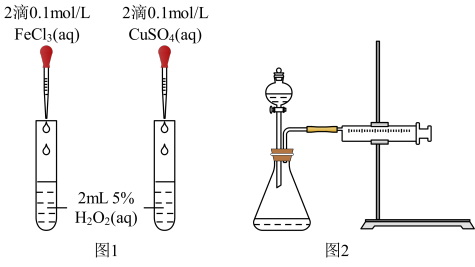
①定性分析:如图1可通过观察____ ,定性比较得出结论;该实验中将FeCl3溶液改为Fe2(SO4)3溶液的原因是___ 。
②定量分析:用图2所示装置做对照试验,实验时均以生成40mL气体为准,其它可能影响实验的因素均已忽略。实验中需要测量的数据是___ 。
(4)MnO2对H2O2分解反应也有催化作用,另一个同学用图2装置,将状态不同的1gMnO2分别加入盛有30mL等浓度的H2O2溶液的锥形瓶中,产生气体进入注射器针筒中,记录结果如下:
①实验结果表明,催化剂的催化效果与___ 有关。
②实验过程中放出气体的体积(标准状况)和时间的关系如图所示。解释反应速率变化的原因___ 。
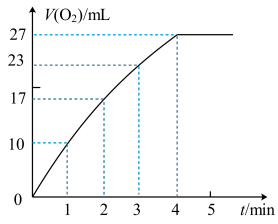
| 编号 | 实验操作 | 实验现象 |
| ① | 分别在试管A、B中加入5mL5%H2O2溶液,各滴入3滴FeCl3溶液。待试管中均有适量气泡出现时,将试管A放入盛有5℃右冷水的烧杯中浸泡;将试管B放入盛有40℃左右热水的烧杯中浸泡。 | 试管A中不再产生气泡;试管B中产生的气泡量增多 |
| ② | 另取两支试管分别加入5mL5%H2O2溶液和5mL10%H2O2溶液 | 两支试管中均未明显见到有气泡产生 |
(2)实验②未观察到预期的实验现象,为了帮助该组同学达到实验目的,你提出的对上述操作的改进意见是
(3)对于H2O2分解反应,Cu2+也有一定的催化作用。为比较Fe3+和Cu2+对H2O2分解的催化效果,该兴趣化学小组的同学分别设计了如图所示的实验。请回答相关问题:

①定性分析:如图1可通过观察
②定量分析:用图2所示装置做对照试验,实验时均以生成40mL气体为准,其它可能影响实验的因素均已忽略。实验中需要测量的数据是
(4)MnO2对H2O2分解反应也有催化作用,另一个同学用图2装置,将状态不同的1gMnO2分别加入盛有30mL等浓度的H2O2溶液的锥形瓶中,产生气体进入注射器针筒中,记录结果如下:
| MnO2状态 | 触摸锥形瓶情况 | 该温度下针筒内收集到气体的体积 | 所需时间 |
| 粉末状 | 很烫 | 30mL | 3min |
| 块状 | 微热 | 30mL | 9min |
②实验过程中放出气体的体积(标准状况)和时间的关系如图所示。解释反应速率变化的原因
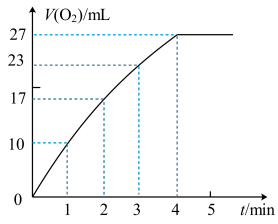
您最近一年使用:0次
名校
解题方法
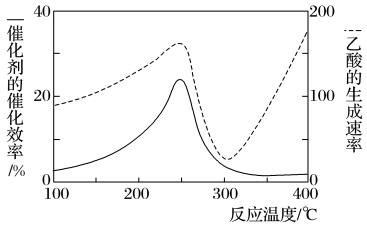
7 . 以二氧化钛表面覆盖Cu2Al2O4为催化剂,可将CO2和CH4直接转化成乙酸,如图为反应过程中催化剂的催化效率(实线)与乙酸的生成速率(虚线)随温度的变化情况。下列说法不正确的是

| A.该制备乙酸的反应中,原子利用率为100% |
| B.Cu2Al2O4写成氧化物的形式是Cu2O·Al2O3 |
| C.由图可知,工业上制备乙酸最适宜的温度应为250℃或者400℃ |
| D.250~300℃时,温度升高而乙酸的生成速率降低的主要原因是催化剂的催化效率降低 |
您最近一年使用:0次
8 . 某科研人员提出HCHO与O2在羟基磷灰石(HAP)表面催化氧化生成CO2、H2O的历程,该历程如图所示(图中只画出了HAP的部分结构,用18O标记羟基磷灰石中的羟基氧原子)。下列说法正确的是
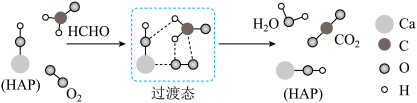

| A.反应物的键能之和大于生成物的键能之和 |
| B.经过该催化氧化过程后18O仍然在HAP中 |
| C.HAP改变了该反应的历程和焓变,加快了反应速率 |
| D.HAP降低了反应的活化能,提高活化分子百分数 |
您最近一年使用:0次
名校
解题方法
9 . 以二氧化钛表面覆盖Cu2Al2O4为催化剂,可以将CO2和CH4直接转化成乙酸。在不同温度下催化剂的催化效率与乙酸的生成速率如图所示。下列说法中错误的是
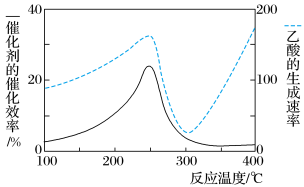

| A.250℃时,催化剂的活性最大 |
| B.250~300℃时,温度升高而乙酸的生成速率降低的原因是催化剂的催化效率降低 |
| C.300~400℃时,乙酸的生成速率升高的原因是催化剂效率增大 |
| D.300~400℃时,乙酸的生成速率升高的原因是温度升高 |
您最近一年使用:0次
2021-09-06更新
|
319次组卷
|
6卷引用:福建省宁德市第一中学2021-2022学年高二上学期10月月考化学试题
福建省宁德市第一中学2021-2022学年高二上学期10月月考化学试题【全国百强校】福建省莆田市第一中学2018-2019学年高二上学期期中考试化学试题福建省莆田第一中学2020-2021学年高二上学期期中考试化学试题江西省景德镇市昌江区景德镇一中2020-2021学年高二上学期期中考试化学试题(1班)(已下线)专题讲座(五)反应速率、平衡图像题解题策略(练) — 2022年高考化学一轮复习讲练测(新教材新高考)(已下线)第七章 化学反应速率与化学平衡 第45练 实际工业生产中图像问题分类突破
名校
解题方法
10 . 科学家结合实验和计算机模拟结果,研究了在贵重金属催化剂表面上的气态体系中,一个CO分子还原NO的能量变化与反应历程如图所示。下列说法错误 的是


| A.使用催化剂,不能改变反应的焓变 |
| B.决定整个反应速率快慢的是反应① |
| C.B物质比反应物和生成物都稳定 |
| D.该反应的热化学方程式为2CO(g)+2NO(g)=N2(g)+2CO2(g) ∆H=(Ed-Ea) kJ·mol−1 |
您最近一年使用:0次
2021-09-05更新
|
564次组卷
|
4卷引用:福建省龙岩市武平县第一中学2021-2022学年高二上学期9月月考化学试题



