解题方法
1 . 下列实验装置能达到相应实验目的的是
选项 | A | B | C | D |
实验装置 |
|
|
|
|
实验目的 | 验证牺牲阳极法保护铁 | 制备并收集氨气 | 验证 | 关闭a、打开b,可检查装置的气密性 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
2 . 下列图中的实验方案,能达到实验目的的是
| A | B | C | D | |
| 实验 方案 |
|
|
|
|
| 实验 目的 | 验证 对 对 分解反应有催化作用 分解反应有催化作用 | 实验室利用该装置制备少量氯气 | 验证非金属性: | 从碘的四氯化碳溶液中分离出碘单质 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2023-05-12更新
|
118次组卷
|
2卷引用:2024届湖南省益阳市安化县第二中学高三下学期三模化学试题
名校
3 . 利用如图实验装置进行相应实验,能达到实验目的的是
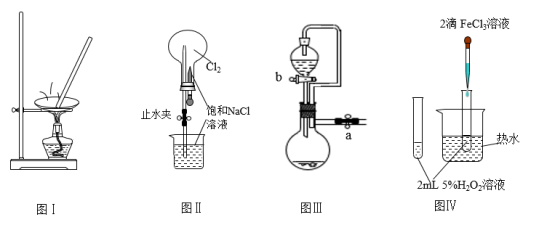

| A.利用图Ⅰ装置蒸发KCl溶液制备无水KCl |
| B.利用图Ⅱ装置进行喷泉实验 |
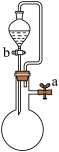
| C.图Ⅲ装置中,关闭a、打开b,可检查装置的气密性 |
D.利用图Ⅳ装置验证 分解反应有催化作用 分解反应有催化作用 |
您最近一年使用:0次
2021-10-11更新
|
395次组卷
|
5卷引用:福建省莆田市第二中学2022届高三10月月考化学试题
福建省莆田市第二中学2022届高三10月月考化学试题福建省泉州市城东中学2021-2022学年高三上学期10月月考化学试题(已下线)提升卷02-【新高考新题型】2022年高考化学选择题标准化练习20卷(山东专用)福建省福州市六校联考2022-2023学年高一下学期期末考试化学试题四川省宜宾市叙州区第二中学校2023-2024学年高二上学期12月月考化学试题
解题方法
4 . 下列操作或装置正确并能达到实验目的的是
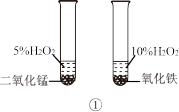

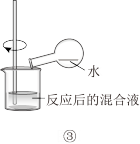





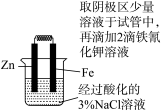
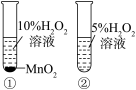
| A.图①用于比较二氧化锰和氧化铁的催化效果 |
| B.图②用此装置可制CaCO3沉淀 |
| C.图③用于检验铜与浓硫酸反应后的混合液中是否含有Cu2+ |
| D.图④用于制备Fe(OH)2沉淀 |
您最近一年使用:0次
5 . 用下列仪器或装置(图中夹持略)进行相应实验,能达到实验目的的是
| A | B | C | D |
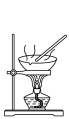 | 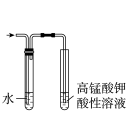 | 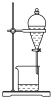 | 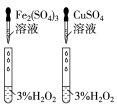 |
蒸发结晶制备 晶体 晶体 | 检验溴乙烷消去产物 | 分离苯和溴苯 | 探究不同催化剂 对  分解速率的影响 分解速率的影响 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2022-03-18更新
|
659次组卷
|
6卷引用:复旦大学附属中学2022届高三下学期 教学质量检测(二模)化学等级试卷
名校
6 . 下列设计的实验方案能达到实验目的的是
| A.制备Al(OH)3悬浊液:向1mol·L-1的AlCl3溶液中加过量的6mol·L-1NaOH溶液 |
| B.提纯含有少量乙酸的乙酸乙酯:向含有少量乙酸的乙酸乙酯中加入氢氧化钠溶液,振荡后静置分液,并除去有机相的水 |
| C.检验溶液中是否含有Fe3+:取少量待检验溶液,向其中加入少量新制氯水,再滴加KSCN溶液,观察实验现象 |
| D.探究催化剂对H2O2分解速率的影响:在相同条件下,向一支试管中加入2mL5%H2O2和1mLH2O,向另一支试管中加入2mL5%H2O2和1mLFeCl3溶液,观察并比较实验现象 |
您最近一年使用:0次
2016-12-09更新
|
199次组卷
|
6卷引用:2017届河南省部分重点中学高三上第一次联考化学试卷
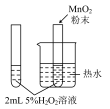
7 . 已知软锰矿和锰结核矿的主要成分均为MnO2,二氧化锰的制备和性质在生产生活和化学实验中有广泛应用。
二氧化锰的制备:
锰粉的主要成分为NH4Cl、C和MnO2,将锰粉进行如图所示操作后,可得到二氧化锰固体。
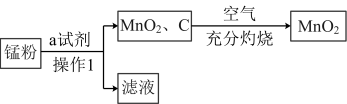
(1)某同学认为试剂a为蒸馏水,你认为______ (填“能”或“不能”)实现实验目的。
(2)操作1的名称是______ ,所用到的玻璃仪器有烧杯、玻璃棒和______ 。
(3)在空气中充分灼烧的目的是_________ 。
二氧化锰的性质检验:
Ⅰ.氧化性
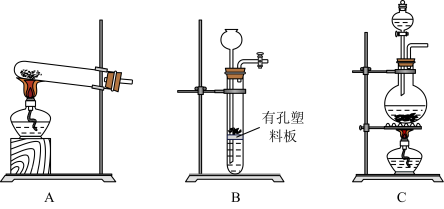
(4)实验室用MnO2与浓盐酸反应制备Cl2,可以选用的装置是______ (填字母)。
(5)将MnO2放在NH3气流中加热,可得到棕黑色的Mn2O3和N2,该反应的化学方程式为_______ 。
Ⅱ.还原性
(6)下列流程所发生的反应中,氧化剂与还原剂的物质的量之比为______ 。

Ⅲ.催化性
MnO2是实验室制取O2的催化剂。某同学设计实验探究双氧水分解的实验方案如下表所示。
(7)本实验的待测数据是___________ 。
(8)由实验①和②可得出的结论是______________________ 。
二氧化锰的制备:
锰粉的主要成分为NH4Cl、C和MnO2,将锰粉进行如图所示操作后,可得到二氧化锰固体。

(1)某同学认为试剂a为蒸馏水,你认为
(2)操作1的名称是
(3)在空气中充分灼烧的目的是
二氧化锰的性质检验:
Ⅰ.氧化性
(4)实验室用MnO2与浓盐酸反应制备Cl2,可以选用的装置是

(5)将MnO2放在NH3气流中加热,可得到棕黑色的Mn2O3和N2,该反应的化学方程式为
Ⅱ.还原性
(6)下列流程所发生的反应中,氧化剂与还原剂的物质的量之比为

Ⅲ.催化性
MnO2是实验室制取O2的催化剂。某同学设计实验探究双氧水分解的实验方案如下表所示。
| 实验序号 | w(H2O2)/% | 粉状MnO2/g | 温度/℃ | 待测数据 |
| ① | 5 | 0 | 20 | |
| ② | 5 | 1.0 | 20 |
(8)由实验①和②可得出的结论是
您最近一年使用:0次
名校
8 . 用下列装置进行的实验, 能达到相应实验目的的是
A. 配制一定浓度的硫酸溶液 配制一定浓度的硫酸溶液 | B.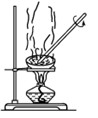 分离溶解在CCl4中的I2 分离溶解在CCl4中的I2 |
C. 制备和收集少量NH3 制备和收集少量NH3 | D.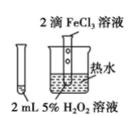 验证FeCl3 对 H2O2分解有催化作用 验证FeCl3 对 H2O2分解有催化作用 |
您最近一年使用:0次
2017-03-31更新
|
894次组卷
|
5卷引用:2017届四川省宜宾市高三第二次诊断理科综合能力测试化学试卷
2017届四川省宜宾市高三第二次诊断理科综合能力测试化学试卷江西省宜丰中学2019届高三上学期第三次月考理科综合化学试题广东省佛山市第一中学2021-2022学年高三上学期12月模拟考试化学试题江苏省沭阳县修远中学2018-2019学年高一下学期第二次月考(实验班)化学试题(已下线)江苏省沭阳县修远中学2018-2019学年高一下学期第二次月考化学试题
名校
解题方法
9 . 亚硝酰硫酸( )在重氮化反应中可以代替亚硝酸钠。实验室用如图所示装置(部分夹持仪器略)制备少量亚硝酰硫酸,并测定产品纯度。
)在重氮化反应中可以代替亚硝酸钠。实验室用如图所示装置(部分夹持仪器略)制备少量亚硝酰硫酸,并测定产品纯度。
已知:i.亚硝酰硫酸遇水分解为硫酸、硝酸和NO,溶于浓硫酸而不分解;
 .实验室制备亚硝酰硫酸的原理为
.实验室制备亚硝酰硫酸的原理为 ,
,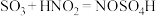 。
。
(1)仪器Ⅰ的名称为___________ ,按照气流从左到右的顺序,上述仪器的连接顺序为___________ (填仪器接口的字母,字母之间用“→”连接,部分仪器可以重复使用),C装置的作用为___________ 。
(2)反应需控制温度在25~40℃,采用的加热措施为___________ ,开始时反应缓慢,但某时刻反应速率明显加快,其原因可能是___________ 。
(3)测定亚硝酰硫酸的纯度:
步骤①:准确称取 产品,在特定条件下配制成
产品,在特定条件下配制成 溶液。
溶液。
步骤②:取 溶液于锥形瓶中,加入
溶液于锥形瓶中,加入 未知浓度
未知浓度 溶液(过量)和
溶液(过量)和 的
的 溶液,摇匀,发生反应
溶液,摇匀,发生反应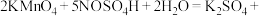
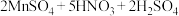
步骤③:向该溶液中滴加 标准溶液进行滴定,消耗
标准溶液进行滴定,消耗 溶液的体积为
溶液的体积为 。
。
步骤④:把亚硝酰硫酸溶液换为蒸馏水(空白实验),重复上述步骤,消耗 溶液的体积为
溶液的体积为 。
。
滴定终点时的现象为___________ ,亚硝酰硫酸的纯度为___________ (精确到 )。
)。
 )在重氮化反应中可以代替亚硝酸钠。实验室用如图所示装置(部分夹持仪器略)制备少量亚硝酰硫酸,并测定产品纯度。
)在重氮化反应中可以代替亚硝酸钠。实验室用如图所示装置(部分夹持仪器略)制备少量亚硝酰硫酸,并测定产品纯度。
已知:i.亚硝酰硫酸遇水分解为硫酸、硝酸和NO,溶于浓硫酸而不分解;
 .实验室制备亚硝酰硫酸的原理为
.实验室制备亚硝酰硫酸的原理为 ,
,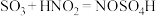 。
。(1)仪器Ⅰ的名称为
(2)反应需控制温度在25~40℃,采用的加热措施为
(3)测定亚硝酰硫酸的纯度:
步骤①:准确称取
 产品,在特定条件下配制成
产品,在特定条件下配制成 溶液。
溶液。步骤②:取
 溶液于锥形瓶中,加入
溶液于锥形瓶中,加入 未知浓度
未知浓度 溶液(过量)和
溶液(过量)和 的
的 溶液,摇匀,发生反应
溶液,摇匀,发生反应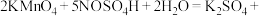
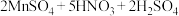
步骤③:向该溶液中滴加
 标准溶液进行滴定,消耗
标准溶液进行滴定,消耗 溶液的体积为
溶液的体积为 。
。步骤④:把亚硝酰硫酸溶液换为蒸馏水(空白实验),重复上述步骤,消耗
 溶液的体积为
溶液的体积为 。
。滴定终点时的现象为
 )。
)。
您最近一年使用:0次
2023-05-19更新
|
454次组卷
|
6卷引用:山东省聊城市百师联盟2023届高三下学期(二轮复习联考)模拟预测(三)化学试题
山东省聊城市百师联盟2023届高三下学期(二轮复习联考)模拟预测(三)化学试题山西省忻州市2023届高三下学期二轮复习联考(三)理综化学试题河南省开封市2022-2023学年高三下学期5月月考理综化学试题(已下线)实验探究题(已下线)第18练 化学实验综合题 -2023年【暑假分层作业】高二化学(2024届一轮复习通用)江西省丰城中学、新建二中2022-2023学年高二下学期期末联考化学试题
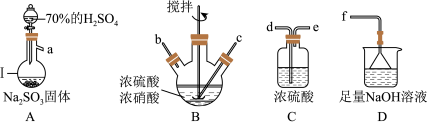
10 . 亚硝酰硫酸(NOSO4H)主要用于染料、医药等工业。实验室用如图装置(夹持装置略)制备少量NOSO4H,并测定产品的纯度。已知:NOSO4H遇水分解,但溶于浓硫酸而不分解。
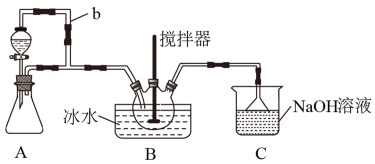
(1)装置A制取SO2
①A中反应的化学方程式为___ 。
②导管b的作用是___ 。
(2)装置B中浓HNO3与SO2在浓H2SO4作用下反应制得NOSO4H。
①该反应必须维持体系温度不得高于20℃,采取的措施除了冷水浴外,还可以是___ (只写1种)。
②开始反应缓慢,待生成少量NOSO4H后,温度变化不大,但反应速度明显加快,其原因是___ 。
(3)装置C的主要作用是___ (用离子方程式表示)。
(4)该实验装置存在可能导致NOSO4H产量降低的缺陷是___ 。
(5)测定亚硝酰硫酸NOSO4H的纯度
准确称取1.380g产品放入250mL的碘量瓶中,加入0.1000mol·L-1、60.00mL的KMnO4标准溶液和10mL25%H2SO4溶液,然后摇匀。用0.2500mol·L-1草酸钠标准溶液滴定,消耗草酸钠溶液的体积为20.00mL。
已知:2KMnO4+5NOSO4H+2H2O=K2SO4+2MnSO4+5HNO3+2H2SO4
①配平:__ MnO4-+__ C2O42-+__ =__ Mn2++__ +__ H2O
②滴定终点时的现象为___ 。
③亚硝酰硫酸的纯度=___ 。(精确到0.1%)[M(NOSO4H)=127g·mol-1]

(1)装置A制取SO2
①A中反应的化学方程式为
②导管b的作用是
(2)装置B中浓HNO3与SO2在浓H2SO4作用下反应制得NOSO4H。
①该反应必须维持体系温度不得高于20℃,采取的措施除了冷水浴外,还可以是
②开始反应缓慢,待生成少量NOSO4H后,温度变化不大,但反应速度明显加快,其原因是
(3)装置C的主要作用是
(4)该实验装置存在可能导致NOSO4H产量降低的缺陷是
(5)测定亚硝酰硫酸NOSO4H的纯度
准确称取1.380g产品放入250mL的碘量瓶中,加入0.1000mol·L-1、60.00mL的KMnO4标准溶液和10mL25%H2SO4溶液,然后摇匀。用0.2500mol·L-1草酸钠标准溶液滴定,消耗草酸钠溶液的体积为20.00mL。
已知:2KMnO4+5NOSO4H+2H2O=K2SO4+2MnSO4+5HNO3+2H2SO4
①配平:
②滴定终点时的现象为
③亚硝酰硫酸的纯度=
您最近一年使用:0次
2020-03-10更新
|
390次组卷
|
3卷引用:【市级联考】福建省泉州市2019届高三毕业班下学期第一次质量检查理科综合化学试题


 分解的催化剂
分解的催化剂