解题方法
1 . 下列实验中的现象与结论相对应正确的是
| 选项 | 实验 | 现象 | 结论 |
| A | 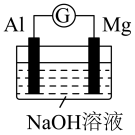 | 电流计指针偏转 | 形成了原电池,铝片作负极,镁片作正极 |
| B | 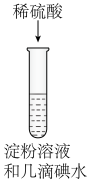 | 加热一段时间后溶液蓝色褪去 | 淀粉在酸性条件下水解,产物是葡萄糖 |
| C | 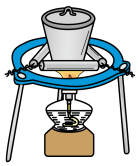 | 加热蒸发CuSO4溶液 | 制取硫酸铜蓝色晶体 |
| D | 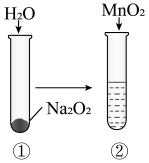 | ①和②中均迅速产生大量气泡 | MnO2一定是②中反应的催化剂 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
2 . 草酸与高锰酸钾在酸性条件下能够发生如下反应: +H2C2O4+H+=Mn2++CO2↑+H2O(未配平),用4mL 0.001mol•L﹣1KMnO4溶液与2mL 0.01mol•L﹣1 H2C2O4溶液,研究不同条件对化学反应速率的影响。改变的条件如下:回答下列问题:
+H2C2O4+H+=Mn2++CO2↑+H2O(未配平),用4mL 0.001mol•L﹣1KMnO4溶液与2mL 0.01mol•L﹣1 H2C2O4溶液,研究不同条件对化学反应速率的影响。改变的条件如下:回答下列问题:
(1)该反应中氧化剂和还原剂的物质的量之比为______ 。
(2)我们可以通过观察_____ ,来判断反应速率的大小
(3)如果研究催化剂对化学反应速率的影响,使用实验______ 和_____ (用Ⅰ~Ⅳ表示,下同),如果研究温度对化学反应速率的影响,使用实验_______ 和______ (用Ⅰ~Ⅳ表示,下同)。
(4)实验Ⅰ和Ⅳ研究浓度对反应速率的影响,Ⅳ中加入1mL蒸馏水的目的是_____ 。
(5)反应I、III、IV中都可观察到反应速率先慢后快的现象,引起这种现象的原因是_____ 。
 +H2C2O4+H+=Mn2++CO2↑+H2O(未配平),用4mL 0.001mol•L﹣1KMnO4溶液与2mL 0.01mol•L﹣1 H2C2O4溶液,研究不同条件对化学反应速率的影响。改变的条件如下:回答下列问题:
+H2C2O4+H+=Mn2++CO2↑+H2O(未配平),用4mL 0.001mol•L﹣1KMnO4溶液与2mL 0.01mol•L﹣1 H2C2O4溶液,研究不同条件对化学反应速率的影响。改变的条件如下:回答下列问题:组别 | 10%硫酸体积/mL | 温度/℃ | 其他物质 |
Ⅰ | 2 | 20 | |
Ⅱ | 2 | 20 | 5滴饱和MnSO4溶液 |
Ⅲ | 2 | 30 | |
Ⅳ | 1 | 20 | 1 mL蒸馏水 |
(2)我们可以通过观察
(3)如果研究催化剂对化学反应速率的影响,使用实验
(4)实验Ⅰ和Ⅳ研究浓度对反应速率的影响,Ⅳ中加入1mL蒸馏水的目的是
(5)反应I、III、IV中都可观察到反应速率先慢后快的现象,引起这种现象的原因是
您最近一年使用:0次
解题方法
3 . 为比较Fe3+、Cu2+和MnO2对H2O2分解反应的催化效果,某化学研究小组的同学分别设计了如图甲、乙、丙所示的实验。请回答相关问题:
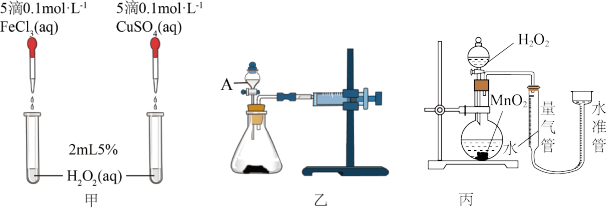
(1)同学X观察甲中两支试管产生气泡的快慢,由此得出Fe3+和Cu2+对H2O2分解的催化效果。其结论________ (填“合理”或“不合理”)。理由是_______ 。
(2)同学Y利用乙装置,测定相同时间内产生气体的体积,从而探究Fe3+和Cu2+对H2O2分解的催化效果。试回答下列问题:
① 仪器A的名称是________ 。
② 除了必要的试剂和图乙所示的仪器外,还有一样不能缺少的实验用品是___________ 。
③ 实验时组装好装置乙,关闭A的活塞,将注射器活塞向外拉出一段。这一操作的实验目的是_________ 。
(3)同学Z利用丙装置探究MnO2对H2O2分解的催化效果。将50 mL 双氧水一次性加入盛有0.10 mol MnO2粉末的烧瓶中,测得标准状况下由量气管读出气体的体积[V(量气管)]和时间(t/min)的关系如图所示。
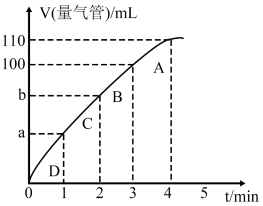
图中 b________ (填“大于”、“小于”或“等于”)90 mL

(1)同学X观察甲中两支试管产生气泡的快慢,由此得出Fe3+和Cu2+对H2O2分解的催化效果。其结论
(2)同学Y利用乙装置,测定相同时间内产生气体的体积,从而探究Fe3+和Cu2+对H2O2分解的催化效果。试回答下列问题:
① 仪器A的名称是
② 除了必要的试剂和图乙所示的仪器外,还有一样不能缺少的实验用品是
③ 实验时组装好装置乙,关闭A的活塞,将注射器活塞向外拉出一段。这一操作的实验目的是
(3)同学Z利用丙装置探究MnO2对H2O2分解的催化效果。将50 mL 双氧水一次性加入盛有0.10 mol MnO2粉末的烧瓶中,测得标准状况下由量气管读出气体的体积[V(量气管)]和时间(t/min)的关系如图所示。

图中 b
您最近一年使用:0次
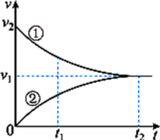
4 . 工业上苯乙烯的生产主要采用乙苯脱氢工艺:C6H5CH2CH3(g)  C6H5CH=CH2(g)+H2(g)。某条件下无催化剂存在时,该反应的正、逆反应速率v随时间t的变化关系如图所示。下列说法正确的是
C6H5CH=CH2(g)+H2(g)。某条件下无催化剂存在时,该反应的正、逆反应速率v随时间t的变化关系如图所示。下列说法正确的是
 C6H5CH=CH2(g)+H2(g)。某条件下无催化剂存在时,该反应的正、逆反应速率v随时间t的变化关系如图所示。下列说法正确的是
C6H5CH=CH2(g)+H2(g)。某条件下无催化剂存在时,该反应的正、逆反应速率v随时间t的变化关系如图所示。下列说法正确的是
| A.曲线①表示的是逆反应的v−t关系 | B.t1时刻体系处于平衡状态 |
| C.反应进行到t1时,Q>K(Q为浓度商) | D.当催化剂存在时,ν1、ν2都增大 |
您最近一年使用:0次
2024-01-27更新
|
50次组卷
|
2卷引用:湖南省岳阳市华容县2023-2024学年高二上学期期末考试化学试题
5 . CO2是一种重要的化学资源,基于Sabatier反应,中科院设计完成了在催化剂作用下CO2氧化 制取具有工业使用价值的
制取具有工业使用价值的 气体。回答下列问题:
气体。回答下列问题:
(1)已知:
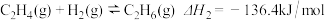
则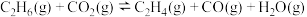

_____  。
。
(2)CO2氧化 制
制 的过程中,还存在反应:
的过程中,还存在反应: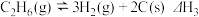 。
。
①随着反应进行,催化剂的活性明显降低,原因是_________________ ;
②若适当通入过量的CO2,则会明显减缓催化剂活性降低现象,原因是________________ 。
(3)CO2氧化 制
制 过程中,不同催化剂对反应物的转化率有不同影响,研究发现使用钴盐、铬盐作催化剂,未达到平衡时,其催化效果有如下结论:
过程中,不同催化剂对反应物的转化率有不同影响,研究发现使用钴盐、铬盐作催化剂,未达到平衡时,其催化效果有如下结论:
说明: 选择性是指转化的乙烷中生成乙烯的百分比;
选择性是指转化的乙烷中生成乙烯的百分比; 选择性是指转化的
选择性是指转化的 中生成
中生成 的百分比。该反应宜选取的催化剂为
的百分比。该反应宜选取的催化剂为______ ,理由是________________ 。
(4) 、
、 的某刚性容器中充入
的某刚性容器中充入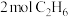 、
、 混合气体,压强为p,若仅发生如下反应:
混合气体,压强为p,若仅发生如下反应: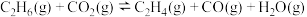 ,达到平衡时,
,达到平衡时, 的体积分数为0.2。
的体积分数为0.2。
①测得正反应速率为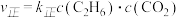 ,逆反应速率为
,逆反应速率为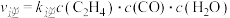 ,其中
,其中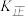 、
、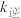 为速率常数,则
为速率常数,则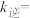
______ (以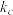 和
和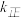 表示),
表示),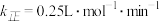 ,则平衡时
,则平衡时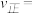
________ 。
②已知:气体分压=气体总压×体积分数,上述反应若应用平衡分压代替平衡浓度,所得的化学平衡常数
______ 。
 制取具有工业使用价值的
制取具有工业使用价值的 气体。回答下列问题:
气体。回答下列问题:(1)已知:

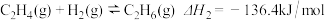
则
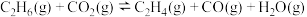

 。
。(2)CO2氧化
 制
制 的过程中,还存在反应:
的过程中,还存在反应: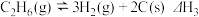 。
。①随着反应进行,催化剂的活性明显降低,原因是
②若适当通入过量的CO2,则会明显减缓催化剂活性降低现象,原因是
(3)CO2氧化
 制
制 过程中,不同催化剂对反应物的转化率有不同影响,研究发现使用钴盐、铬盐作催化剂,未达到平衡时,其催化效果有如下结论:
过程中,不同催化剂对反应物的转化率有不同影响,研究发现使用钴盐、铬盐作催化剂,未达到平衡时,其催化效果有如下结论:| 实验编号 |  | 催化剂 | 转化率/% | 选择性/% | ||
 | CO2 |  |  | |||
| Ⅰ | 650 | 钴盐 | 19.0 | 37.6 | 17.6 | 78.1 |
| Ⅱ | 650 | 铬盐 | 32.1 | 23.0 | 77.3 | 10.4 |
说明:
 选择性是指转化的乙烷中生成乙烯的百分比;
选择性是指转化的乙烷中生成乙烯的百分比; 选择性是指转化的
选择性是指转化的 中生成
中生成 的百分比。该反应宜选取的催化剂为
的百分比。该反应宜选取的催化剂为(4)
 、
、 的某刚性容器中充入
的某刚性容器中充入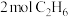 、
、 混合气体,压强为p,若仅发生如下反应:
混合气体,压强为p,若仅发生如下反应: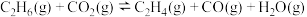 ,达到平衡时,
,达到平衡时, 的体积分数为0.2。
的体积分数为0.2。①测得正反应速率为
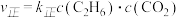 ,逆反应速率为
,逆反应速率为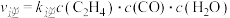 ,其中
,其中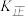 、
、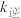 为速率常数,则
为速率常数,则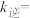
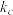 和
和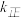 表示),
表示),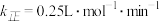 ,则平衡时
,则平衡时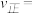
②已知:气体分压=气体总压×体积分数,上述反应若应用平衡分压代替平衡浓度,所得的化学平衡常数

您最近一年使用:0次
6 . NO和CO都是汽车尾气里的有害物质,它们能缓慢地起反应生成氮气和二氧化碳气体:2NO(g)+2CO(g) 2CO2(g)+N2(g)。对此反应,下列叙述正确的是
2CO2(g)+N2(g)。对此反应,下列叙述正确的是
 2CO2(g)+N2(g)。对此反应,下列叙述正确的是
2CO2(g)+N2(g)。对此反应,下列叙述正确的是| A.增大压强,正反应速率增大,逆反应速率减小 |
| B.使用催化剂,能提高反应速率和NO的转化率 |
| C.冬天气温低,反应速率降低,对人体危害减小 |
| D.体积不变充入He,CO的转化率不变 |
您最近一年使用:0次
2021-01-29更新
|
88次组卷
|
2卷引用:湖南省永州市2020-2021学年高二上学期期末考试化学试题
7 . 根据下列实验事实所推出的影响化学反应的因素不合理的是
| 序号 | 实验事实 | 影响化学反应的因素 |
| A | 铁丝在空气中很难燃烧,而在氧气中能剧烈燃烧 | 反应物的种类 |
| B | 碳在常温下不与氧气发生反应,而在点燃时能与氧气反应 | 反应温度 |
| C | 双氧水分解缓慢,而在加入二氧化锰后迅速分解 | 催化剂 |
| D |  粉与同浓度盐酸反应的速率比 粉与同浓度盐酸反应的速率比 粒快 粒快 | 反应物的表面积 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
8 . 分别进行下列操作,由现象得出的结论正确的是
选项 | 操作 | 现象 | 结论 |
A | 向某一溶液中滴加Ba(NO3)2和HNO3混合溶液 | 生成白色沉淀 | 原溶液中有SO42- |
B | 向盛有2mL0.1mol/LAgNO3溶液的试管中滴加1mL0.1mol/ LNaCl溶液,再向其中滴加4~5滴0.1mol/LKI溶液 | 先有白色沉淀成,后又产生黄色沉淀 | Ksp(AgCl)> Ksp(AgI) |
C | 室温下,取相同大小、形状和质量的Cu粒分别投入0.1mol/L的稀硝酸和10.0mol/L的浓硝酸中 | Cu粒与浓硝酸反应比与稀硝酸反应剧烈 | 探究浓度对化学反应速率的影响 |
D | 向某一溶液中滴加稀盐酸,将生成的气体通入澄清石灰水中 | 澄清石灰水变浑浊 | 生成的气体可能是SO2 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2017-05-24更新
|
825次组卷
|
2卷引用:湖南省衡阳市第八中学2017届高三第二次模拟(实验班)化学试题
名校
9 . CO2 + 4H2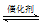 CH4 + 2H2O是CO2综合利用的一种方法。下列关于该反应的说法正确的是
CH4 + 2H2O是CO2综合利用的一种方法。下列关于该反应的说法正确的是
| A.适当升温能加快反应速率 | B.催化剂对反应速率无影响 |
| C.达到平衡时,正反应速率为0 | D.达到平衡时,CO2能100%转化为CH4 |
您最近一年使用:0次
2019-07-08更新
|
247次组卷
|
7卷引用:湖南省长沙市雨花区2019-2020学年高一下学期期末考试化学试题
名校
解题方法
10 . 紫外光照射时,不同催化剂作用下将CO2和H2O(g)转化为CH4和O2,CH4产量随光照时间的变化见图1,以TiO2/Cu2Al2O4为催化剂,可以将CO2和CH4直接转化成乙酸,不同温度下催化剂的催化效率与乙酸的生成速率的关系见图2。下列有关说法中正确的是
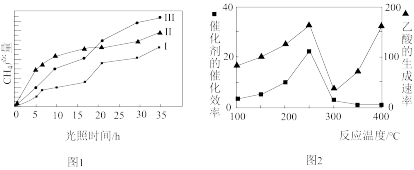

| A.由图1知,在0~15 h内,CH4的平均生成速率从大到小的顺序:Ⅲ>Ⅱ> I |
| B.由图1知,在25~35 h内,CH4的平均生成速率从大到小的顺序:Ⅱ>Ⅲ>I |
| C.由图2知,250 °C时催化剂的活性最高 |
| D.由图2知,乙酸的生成最佳温度范围:400 °C以上 |
您最近一年使用:0次
2021-11-19更新
|
103次组卷
|
2卷引用:湖南省常德市汉寿县第一中学2023-2024学年高二上学期1月期末化学试题



