名校
1 . 氢气既是一种清洁能源,又是重要的化工原料。回答下列问题:
(1)已知:断裂1molH-H、1molO=O、1molH-O键吸收的能量依次为436kJ、498kJ、467kJ,在2H2(g)+O2(g)=2H2O(g)反应中,44.8LH2(标准状况治好完全反应放出的能量为_____ kJ。
(2)实验室用纯净的铝片与稀硫酸反应制取氢气。
①实验过程如图所示,分析判断_____ 段化学反应速率最快(填OE、EF或FG)。
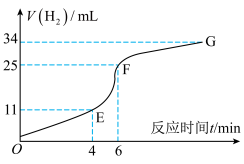
②将铝片投入盛有稀硫酸的烧杯中,刚开始时产生H2的速率逐渐加快,其原因是_____ 。
(3)要加快铝与硫酸溶液制H2的反应速率,小组成员提出一系列方案,比如:①加入某种催化剂;②加入蒸馏水:③将铝片换成铝粉;④增加硫酸的浓度至18mol/L;⑤_____ ;⑥_____ 。以上方案不合理的有_____ ;请你再补充两种合理方案,填入空白⑤⑥处。
(1)已知:断裂1molH-H、1molO=O、1molH-O键吸收的能量依次为436kJ、498kJ、467kJ,在2H2(g)+O2(g)=2H2O(g)反应中,44.8LH2(标准状况治好完全反应放出的能量为
(2)实验室用纯净的铝片与稀硫酸反应制取氢气。
①实验过程如图所示,分析判断

②将铝片投入盛有稀硫酸的烧杯中,刚开始时产生H2的速率逐渐加快,其原因是
(3)要加快铝与硫酸溶液制H2的反应速率,小组成员提出一系列方案,比如:①加入某种催化剂;②加入蒸馏水:③将铝片换成铝粉;④增加硫酸的浓度至18mol/L;⑤
您最近一年使用:0次
名校
解题方法
2 . 将玉米秸秆进行热化学裂解可制备出以CO、 、
、 、
、 为主要成分的生物质原料气,对原料气进行预处理后,可用于生产甲醇、乙醇等燃料。
为主要成分的生物质原料气,对原料气进行预处理后,可用于生产甲醇、乙醇等燃料。
(1)已知:几种常见共价键的键能如下表所示。
由此可估算反应 的焓变
的焓变
_______  。
。
(2)若在恒容绝热的密闭容器中进行上述反应,下列说法正确的是_______(填标号)。
(3) 和
和 合成乙醇的反应为
合成乙醇的反应为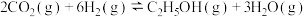 。将等物质的量的
。将等物质的量的 和
和 充入一刚性容器中,测得平衡时
充入一刚性容器中,测得平衡时 的体积分数随温度和压强的变化关系如图所示。
的体积分数随温度和压强的变化关系如图所示。
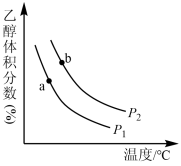
①压强
_______  (填“>”“<”或“=”,下同)。判断依据是
(填“>”“<”或“=”,下同)。判断依据是_______ 。
②a、b两点的平衡常数
_______  。
。
③已知Arrhenius经验公式为 (Ea为活化能,k为速率常数,R和C为常数),为探究m、n两种催化剂的催化效能,进行了实验探究,依据实验数据获得下图所示曲线。在m催化剂作用下,该反应的活化能Ea=
(Ea为活化能,k为速率常数,R和C为常数),为探究m、n两种催化剂的催化效能,进行了实验探究,依据实验数据获得下图所示曲线。在m催化剂作用下,该反应的活化能Ea=_______  。从图中信息获知催化效能较高的催化剂是
。从图中信息获知催化效能较高的催化剂是_______ (填“m”或“n”)。

 、
、 、
、 为主要成分的生物质原料气,对原料气进行预处理后,可用于生产甲醇、乙醇等燃料。
为主要成分的生物质原料气,对原料气进行预处理后,可用于生产甲醇、乙醇等燃料。(1)已知:几种常见共价键的键能如下表所示。
| 共价键 | C—H | C—O |  | H—H | O—H |
键能( ) ) | 413 | 358 | 839 | 436 | 467 |
 的焓变
的焓变
 。
。(2)若在恒容绝热的密闭容器中进行上述反应,下列说法正确的是_______(填标号)。
| A.体系温度不再发生变化时,反应达到化学平衡状态 |
B.平衡体系中, 和 和 的物质的量之比为2:1 的物质的量之比为2:1 |
C.加入催化剂,可以提高 的平衡产率 的平衡产率 |
D.其他条件不变,增大CO的浓度,能提高 的平衡转化率 的平衡转化率 |
 和
和 合成乙醇的反应为
合成乙醇的反应为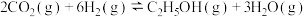 。将等物质的量的
。将等物质的量的 和
和 充入一刚性容器中,测得平衡时
充入一刚性容器中,测得平衡时 的体积分数随温度和压强的变化关系如图所示。
的体积分数随温度和压强的变化关系如图所示。
①压强

 (填“>”“<”或“=”,下同)。判断依据是
(填“>”“<”或“=”,下同)。判断依据是②a、b两点的平衡常数

 。
。③已知Arrhenius经验公式为
 (Ea为活化能,k为速率常数,R和C为常数),为探究m、n两种催化剂的催化效能,进行了实验探究,依据实验数据获得下图所示曲线。在m催化剂作用下,该反应的活化能Ea=
(Ea为活化能,k为速率常数,R和C为常数),为探究m、n两种催化剂的催化效能,进行了实验探究,依据实验数据获得下图所示曲线。在m催化剂作用下,该反应的活化能Ea= 。从图中信息获知催化效能较高的催化剂是
。从图中信息获知催化效能较高的催化剂是
您最近一年使用:0次
2022-05-17更新
|
1048次组卷
|
4卷引用:河北省张家口市2022届高三第三次模拟考试化学试题
河北省张家口市2022届高三第三次模拟考试化学试题(已下线)模拟卷03-2023年高三化学对接新高考全真模拟试卷(云南,安徽,黑龙江,山西,吉林五省通用)(已下线)考向4 原子守恒法巧解竞争反应计算问题2024届河南省安阳市第一中学高三上学期模拟检测化学试题(12月)
解题方法
3 . 运用化学反应原理研究氮及其化合物的反应有重要意义。
(1)铵态氮肥不能与含碳酸钾的草木灰混合使用,原因是_______ 。
(2)合成氨反应N2(g)+3H2(g) 2NH3(g) ΔH=-92.4 kJ·mol-1,在工业生产中温度常控制在480°C,而非常温。请从化学反应速率和催化剂的角度加以解释
2NH3(g) ΔH=-92.4 kJ·mol-1,在工业生产中温度常控制在480°C,而非常温。请从化学反应速率和催化剂的角度加以解释_______ 。
(3)合成氨过程中发生的反应机理如下:
I.2xFe+N2 2FexN (慢);
2FexN (慢);
II.2FexN+3H2 2xFe+2NH3 (快)
2xFe+2NH3 (快)
回答下列问题:
①合成氨反应的速率快慢主要取决于_______ (填“I”或“II”);
②合成氨反应的催化剂是_______ (填化学式):
③反应I的活化能_______ 反应II的活化能(填“>”“=”或“<”)。
④使用催化剂前后,合成氨反应的ΔH_______ (填“增大”“减小”或“不变”)。
(1)铵态氮肥不能与含碳酸钾的草木灰混合使用,原因是
(2)合成氨反应N2(g)+3H2(g)
 2NH3(g) ΔH=-92.4 kJ·mol-1,在工业生产中温度常控制在480°C,而非常温。请从化学反应速率和催化剂的角度加以解释
2NH3(g) ΔH=-92.4 kJ·mol-1,在工业生产中温度常控制在480°C,而非常温。请从化学反应速率和催化剂的角度加以解释(3)合成氨过程中发生的反应机理如下:
I.2xFe+N2
 2FexN (慢);
2FexN (慢);II.2FexN+3H2
 2xFe+2NH3 (快)
2xFe+2NH3 (快)回答下列问题:
①合成氨反应的速率快慢主要取决于
②合成氨反应的催化剂是
③反应I的活化能
④使用催化剂前后,合成氨反应的ΔH
您最近一年使用:0次
4 . 某学习小组同学研究过氧化氢溶液与氢碘酸反应,查到一组室温下的实验数据,如下表所示:
(1)过氧化氢溶液与氢碘酸反应的化学方程式为___________ ,该反应中的氧化产物为___________ (填化学式)。
(2)由表中编号为①、②、③的实验数据得到的结论是___________ 。
(3)若该反应的速率方程可表示为 ,对比表中数据可知a=
,对比表中数据可知a=___________ ,b=___________ 。
(4)资料显示编号①的反应进行至20s时,测得氢碘酸的浓度为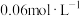 ,则20s内生成I2的平均速率
,则20s内生成I2的平均速率
___________ 。
(5)该实验小组同学将氢碘酸用碘化钾代替进行实验,控制其他条件不变,未观察到溶液变为棕黄色,却观察到有无色气体生成。该小组同学认为KI可能对过氧化氢的分解起到催化作用。为验证该猜想,该小组同学需要进行的实验操作是___________ 。
(6)该小组同学将实验编号④的温度升高,发现到一定温度下,溶液出现棕黄色所需时间变长,可能的原因是___________ 。
| 实验编号 | ① | ② | ③ | ④ | ⑤ |
 | 0.1 | 0.1 | 0.1 | 0.2 | 0.3 |
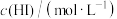 | 0.1 | 0.2 | 0.3 | 0.1 | 0.1 |
| 从混合至溶液出现棕黄色的时间/s | 13 | 6.5 | 4.3 | 6.6 | 4.4 |
(2)由表中编号为①、②、③的实验数据得到的结论是
(3)若该反应的速率方程可表示为
 ,对比表中数据可知a=
,对比表中数据可知a=(4)资料显示编号①的反应进行至20s时,测得氢碘酸的浓度为
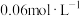 ,则20s内生成I2的平均速率
,则20s内生成I2的平均速率
(5)该实验小组同学将氢碘酸用碘化钾代替进行实验,控制其他条件不变,未观察到溶液变为棕黄色,却观察到有无色气体生成。该小组同学认为KI可能对过氧化氢的分解起到催化作用。为验证该猜想,该小组同学需要进行的实验操作是
(6)该小组同学将实验编号④的温度升高,发现到一定温度下,溶液出现棕黄色所需时间变长,可能的原因是
您最近一年使用:0次



