名校
解题方法
1 . 某校化学小组探究 与
与 溶液的反应,进行了如下实验(以下实验过程中溶液体积变化忽略不计):
溶液的反应,进行了如下实验(以下实验过程中溶液体积变化忽略不计):
(1)对比实验i、ii、iii,说明反应速率与___________ 有关。
(2)为了探究淡黄色固体的成分,甲同学进行实验:取实验iv试管壁上的淡黄色固体,发现其微溶于乙醇,易溶于 ,淡黄色固体是
,淡黄色固体是___________ 。
(3)根据上述实验现象,甲同学猜测一定有单质碘生成,猜测的理论依据是___________ ,但实验中溶液始终没有变蓝。
(4)利用如图装置继续实验,证实了单质碘可以生成。实验现象是___________ 。
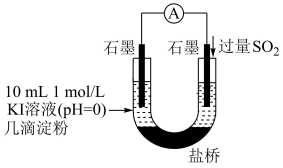
(5)对于实验i、ii、iii未能检测到单质碘,甲同学继续实验
根据(2)(4)(5)的实验现象,结合化学反应原理解释实验iv中始终未检测到单质碘的原因是___________ 。
(6)根据上述一系列实验,乙同学大胆猜测,整个反应中 起到了催化剂作用,为了证明乙同学的猜想正确,还需要的实验证据是
起到了催化剂作用,为了证明乙同学的猜想正确,还需要的实验证据是___________ 。
实验结果证实了猜想,则总反应的化学方程式是___________ 。
 与
与 溶液的反应,进行了如下实验(以下实验过程中溶液体积变化忽略不计):
溶液的反应,进行了如下实验(以下实验过程中溶液体积变化忽略不计):| 实验 | 实验操作 | 实验现象 |
| i | 取 淀粉 淀粉 溶液 溶液 ,通入 ,通入 至量 至量 | 溶液慢慢变为浅黄色 |
| ii | 取 淀粉 淀粉 溶液 溶液 ,通入 ,通入 至过量 至过量 | 溶液迅速变为黄色,略有浑浊 |
| iii | 取 淀粉 淀粉 溶液 溶液 (用盐酸酸化至 (用盐酸酸化至 ),通入 ),通入 至过量 至过量 | 溶液迅速变为黄色,有浑浊 |
| iv | 将实验iii中的黄色浊液进行离心分离 | 试管壁上附着淡黄色固体,溶液为黄色 |
(1)对比实验i、ii、iii,说明反应速率与
(2)为了探究淡黄色固体的成分,甲同学进行实验:取实验iv试管壁上的淡黄色固体,发现其微溶于乙醇,易溶于
 ,淡黄色固体是
,淡黄色固体是(3)根据上述实验现象,甲同学猜测一定有单质碘生成,猜测的理论依据是
(4)利用如图装置继续实验,证实了单质碘可以生成。实验现象是

(5)对于实验i、ii、iii未能检测到单质碘,甲同学继续实验
| 实验 | 实验操作 | 实验现象 |
| v | 将 通入蓝色的碘淀粉混合溶液中 通入蓝色的碘淀粉混合溶液中 | 溶液蓝色迅速褪去 |
| vi | 取实验iv离心后的黄色溶液少量,加入盐酸酸化的 溶液 溶液 | 生成白色沉淀 |
(6)根据上述一系列实验,乙同学大胆猜测,整个反应中
 起到了催化剂作用,为了证明乙同学的猜想正确,还需要的实验证据是
起到了催化剂作用,为了证明乙同学的猜想正确,还需要的实验证据是实验结果证实了猜想,则总反应的化学方程式是
您最近一年使用:0次
解题方法
2 . 研究 的转化可实现碳的循环利用。在反应器内
的转化可实现碳的循环利用。在反应器内 和
和 在催化剂作用下可发生如下反应:
在催化剂作用下可发生如下反应:
Ⅰ.

Ⅱ.

(1)反应I的历程如图1所示,其中吸附在催化剂表面上的物种用*标注。
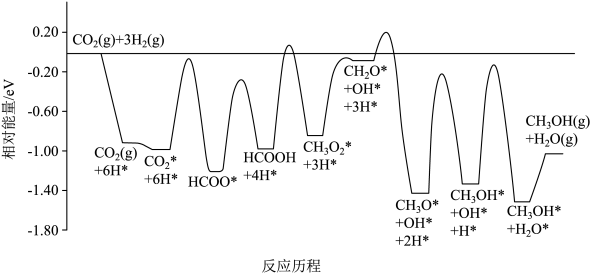
下列说法不正确的是 。
(2)若反应Ⅱ的正、逆反应速率分别表示为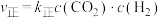 ,
,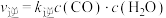 ,
, 、
、 分别为正、逆反应速率常数,c为物质的量浓度。
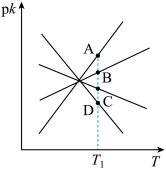
分别为正、逆反应速率常数,c为物质的量浓度。 ,如图2中有表示反应Ⅱ的正、逆反应速率常数随温度T变化的图像,若A、B、C、D点的纵坐标分别为
,如图2中有表示反应Ⅱ的正、逆反应速率常数随温度T变化的图像,若A、B、C、D点的纵坐标分别为 、
、 、
、 、
、 ,则温度
,则温度 时反应Ⅱ的化学平衡常数K=
时反应Ⅱ的化学平衡常数K=____________ 。
(3)一定条件下使 、
、 混合气体通过反应器,同时发生反应Ⅰ、Ⅱ,检测反应器出口气体的成分及其含量,计算
混合气体通过反应器,同时发生反应Ⅰ、Ⅱ,检测反应器出口气体的成分及其含量,计算 的转化率和
的转化率和 的选择性以评价催化剂的性能。
的选择性以评价催化剂的性能。
①220℃时,测得反应器出口气体中全部含碳物质的物质的量之比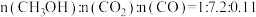 ,则该温度下
,则该温度下 转化率=
转化率=____________ 。(结果保留1位小数)
②其它条件相同时,反应温度对 的转化率和
的转化率和 的选择性的影响如图所示:
的选择性的影响如图所示:
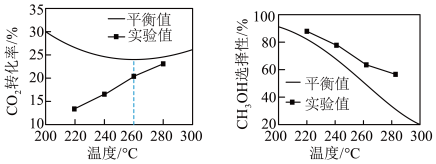
由图可知, 的转化率实验值低于其平衡值,而
的转化率实验值低于其平衡值,而 选择性的实验值却略高于其平衡值,请说明理由。
选择性的实验值却略高于其平衡值,请说明理由。__________ 。
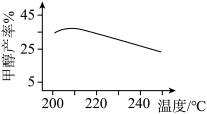
(4)恒压下, 和
和 以物质的量比1:3投料合成甲醇(不考虑反应II),在有分子筛膜时甲醇的产率随温度的变化如图所示,其中分子筛膜能选择性分离出
以物质的量比1:3投料合成甲醇(不考虑反应II),在有分子筛膜时甲醇的产率随温度的变化如图所示,其中分子筛膜能选择性分离出 。请在图中画出无分子筛膜时甲醇的平衡产率随温度的变化曲线
。请在图中画出无分子筛膜时甲醇的平衡产率随温度的变化曲线_________ 。
 的转化可实现碳的循环利用。在反应器内
的转化可实现碳的循环利用。在反应器内 和
和 在催化剂作用下可发生如下反应:
在催化剂作用下可发生如下反应:Ⅰ.


Ⅱ.


(1)反应I的历程如图1所示,其中吸附在催化剂表面上的物种用*标注。

下列说法不正确的是 。
A.该反应的 ,能低温自发 ,能低温自发 |
B.该历程中最小能垒(活化能)步骤的化学方程式为 |
| C.催化剂可以降低反应活化能和反应热,但对反应物的转化率无影响 |
D.最后一步是 (g)、 (g)、 (g)从催化剂表面的解吸过程, (g)从催化剂表面的解吸过程, |
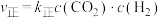 ,
,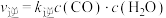 ,
, 、
、 分别为正、逆反应速率常数,c为物质的量浓度。
分别为正、逆反应速率常数,c为物质的量浓度。 ,如图2中有表示反应Ⅱ的正、逆反应速率常数随温度T变化的图像,若A、B、C、D点的纵坐标分别为
,如图2中有表示反应Ⅱ的正、逆反应速率常数随温度T变化的图像,若A、B、C、D点的纵坐标分别为 、
、 、
、 、
、 ,则温度
,则温度 时反应Ⅱ的化学平衡常数K=
时反应Ⅱ的化学平衡常数K=
(3)一定条件下使
 、
、 混合气体通过反应器,同时发生反应Ⅰ、Ⅱ,检测反应器出口气体的成分及其含量,计算
混合气体通过反应器,同时发生反应Ⅰ、Ⅱ,检测反应器出口气体的成分及其含量,计算 的转化率和
的转化率和 的选择性以评价催化剂的性能。
的选择性以评价催化剂的性能。
①220℃时,测得反应器出口气体中全部含碳物质的物质的量之比
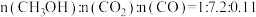 ,则该温度下
,则该温度下 转化率=
转化率=②其它条件相同时,反应温度对
 的转化率和
的转化率和 的选择性的影响如图所示:
的选择性的影响如图所示:
由图可知,
 的转化率实验值低于其平衡值,而
的转化率实验值低于其平衡值,而 选择性的实验值却略高于其平衡值,请说明理由。
选择性的实验值却略高于其平衡值,请说明理由。(4)恒压下,
 和
和 以物质的量比1:3投料合成甲醇(不考虑反应II),在有分子筛膜时甲醇的产率随温度的变化如图所示,其中分子筛膜能选择性分离出
以物质的量比1:3投料合成甲醇(不考虑反应II),在有分子筛膜时甲醇的产率随温度的变化如图所示,其中分子筛膜能选择性分离出 。请在图中画出无分子筛膜时甲醇的平衡产率随温度的变化曲线
。请在图中画出无分子筛膜时甲醇的平衡产率随温度的变化曲线
您最近一年使用:0次
名校
解题方法
3 . 回收利用含硫化合物有利于节约资源、保护环境。
(1)一种由含 的烟气回收硫磺的工艺为:将一部分含
的烟气回收硫磺的工艺为:将一部分含 的烟气在空气中燃烧,将燃烧所得产物与剩余烟气混合,冷却后可回收得到硫磺(
的烟气在空气中燃烧,将燃烧所得产物与剩余烟气混合,冷却后可回收得到硫磺( )。该工艺中涉及反应为:
)。该工艺中涉及反应为:
反应1:

反应2: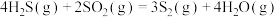
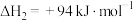
反应3:
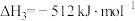
①反应 的△H=
的△H=_______ 。
②如果上述反应均能完全进行,为提高硫磺的产率,该工艺中需要控制的是_______ 。
(2)一种以 为原料,循环吸收烟气中
为原料,循环吸收烟气中 的物质转化关系如下:写出转化中由
的物质转化关系如下:写出转化中由 制
制 的化学反应方程式:
的化学反应方程式:_______ 。
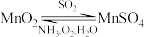
(3)一种以 为催化剂载体、
为催化剂载体、 为催化剂的
为催化剂的 还原烟气中
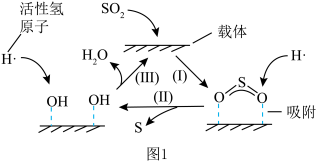
还原烟气中 制S的反应机理如图1和如图2所示:
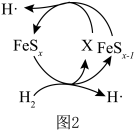
制S的反应机理如图1和如图2所示:
①如图1中所示转化可以描述为_______ 。
②如图2中X的电子式为_______ 。
③其他条件一定,改变起始时 与
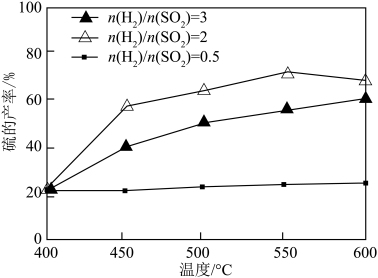
与 的比例,反应相同时间,测得S的产率与温度和
的比例,反应相同时间,测得S的产率与温度和 比值的关系如图所示。500℃时,
比值的关系如图所示。500℃时,  比值为3时硫的产率小于比值为2时的原因是
比值为3时硫的产率小于比值为2时的原因是_______ 。
(1)一种由含
 的烟气回收硫磺的工艺为:将一部分含
的烟气回收硫磺的工艺为:将一部分含 的烟气在空气中燃烧,将燃烧所得产物与剩余烟气混合,冷却后可回收得到硫磺(
的烟气在空气中燃烧,将燃烧所得产物与剩余烟气混合,冷却后可回收得到硫磺( )。该工艺中涉及反应为:
)。该工艺中涉及反应为:反应1:


反应2:
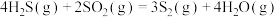
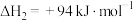
反应3:

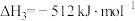
①反应
 的△H=
的△H=②如果上述反应均能完全进行,为提高硫磺的产率,该工艺中需要控制的是
(2)一种以
 为原料,循环吸收烟气中
为原料,循环吸收烟气中 的物质转化关系如下:写出转化中由
的物质转化关系如下:写出转化中由 制
制 的化学反应方程式:
的化学反应方程式: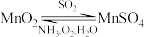
(3)一种以
 为催化剂载体、
为催化剂载体、 为催化剂的
为催化剂的 还原烟气中
还原烟气中 制S的反应机理如图1和如图2所示:
制S的反应机理如图1和如图2所示:①如图1中所示转化可以描述为

②如图2中X的电子式为

③其他条件一定,改变起始时
 与
与 的比例,反应相同时间,测得S的产率与温度和
的比例,反应相同时间,测得S的产率与温度和 比值的关系如图所示。500℃时,
比值的关系如图所示。500℃时,  比值为3时硫的产率小于比值为2时的原因是
比值为3时硫的产率小于比值为2时的原因是
您最近一年使用:0次
2023-04-16更新
|
523次组卷
|
2卷引用:江苏省南通市通州区2022-2023学年高三下学期4月月考化学试题
名校
解题方法
4 . 二甲醚是重要的有机合成原料:工业上常用合成气(主要成分为 、
、 )制备二甲醚,其主要反应如下:
)制备二甲醚,其主要反应如下:
反应ⅰ: ,
,
反应ⅱ: ,
,
反应ⅲ: ,
,
(1)已知 时,由稳定态单质生成
时,由稳定态单质生成 化合物的焓变称为该物质的标准摩尔生成焓
化合物的焓变称为该物质的标准摩尔生成焓 。几种物质的标准摩尔生成焓如下表所示,据此计算
。几种物质的标准摩尔生成焓如下表所示,据此计算
___________  。
。
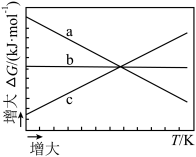
(2)已知 ,
, 随温度变化的三种趋势如下图中线条所示。能用来表示反应ⅰ的线条是
随温度变化的三种趋势如下图中线条所示。能用来表示反应ⅰ的线条是___________ (填线条字母)。
(3)在 催化剂的作用下发生反应ⅰ,其可能反应机理如下图所示。
催化剂的作用下发生反应ⅰ,其可能反应机理如下图所示。
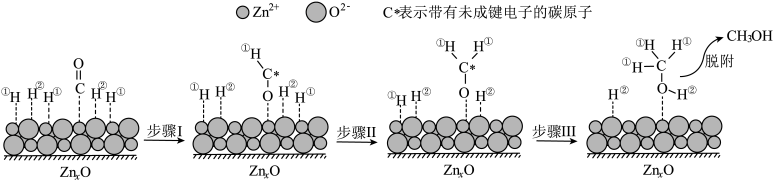
①根据元素电负性的变化规律,图中反应步骤Ⅲ可描述为___________ 。
②在合成甲醇过程中,需要不断分离出甲醇的原因为___________ (填选项字母)。
a.有利于平衡正向移动b.防止催化剂中毒c.提高正反应速率
(4)一定温度下,在体积为 的刚性容器中充入
的刚性容器中充入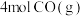 和
和 制备二甲醚,
制备二甲醚, 时达到平衡,平衡时
时达到平衡,平衡时 的转化率为80%,
的转化率为80%, ,且
,且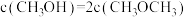 。
。
① 内,
内,
___________  。
。
②反应ⅲ的平衡常数
___________ (保留三位有效数字)。
(5)实际工业生产中,需要在260℃、压强恒为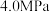 的反应釜中进行上述反应。初始时向反应釜中加入
的反应釜中进行上述反应。初始时向反应釜中加入 和
和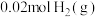 ,为确保反应的连续性,需向反应釜中以
,为确保反应的连续性,需向反应釜中以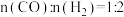 、进气流量
、进气流量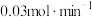 持续通入原料,同时控制出气流量。
持续通入原料,同时控制出气流量。
①需控制出气流量小于进气流量的原因为___________ 。
②已知出气流量为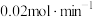 ,单位时间内
,单位时间内 的转化率为60%,则流出气体中
的转化率为60%,则流出气体中 的百分含量为
的百分含量为___________ 。
 、
、 )制备二甲醚,其主要反应如下:
)制备二甲醚,其主要反应如下:反应ⅰ:
 ,
,
反应ⅱ:
 ,
,
反应ⅲ:
 ,
,
(1)已知
 时,由稳定态单质生成
时,由稳定态单质生成 化合物的焓变称为该物质的标准摩尔生成焓
化合物的焓变称为该物质的标准摩尔生成焓 。几种物质的标准摩尔生成焓如下表所示,据此计算
。几种物质的标准摩尔生成焓如下表所示,据此计算
 。
。| 物质 |  |  |  |
 | 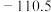 | 0.0 | 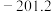 |
 ,
, 随温度变化的三种趋势如下图中线条所示。能用来表示反应ⅰ的线条是
随温度变化的三种趋势如下图中线条所示。能用来表示反应ⅰ的线条是
(3)在
 催化剂的作用下发生反应ⅰ,其可能反应机理如下图所示。
催化剂的作用下发生反应ⅰ,其可能反应机理如下图所示。
①根据元素电负性的变化规律,图中反应步骤Ⅲ可描述为
②在合成甲醇过程中,需要不断分离出甲醇的原因为
a.有利于平衡正向移动b.防止催化剂中毒c.提高正反应速率
(4)一定温度下,在体积为
 的刚性容器中充入
的刚性容器中充入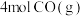 和
和 制备二甲醚,
制备二甲醚, 时达到平衡,平衡时
时达到平衡,平衡时 的转化率为80%,
的转化率为80%, ,且
,且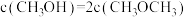 。
。①
 内,
内,
 。
。②反应ⅲ的平衡常数

(5)实际工业生产中,需要在260℃、压强恒为
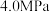 的反应釜中进行上述反应。初始时向反应釜中加入
的反应釜中进行上述反应。初始时向反应釜中加入 和
和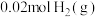 ,为确保反应的连续性,需向反应釜中以
,为确保反应的连续性,需向反应釜中以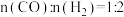 、进气流量
、进气流量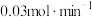 持续通入原料,同时控制出气流量。
持续通入原料,同时控制出气流量。①需控制出气流量小于进气流量的原因为
②已知出气流量为
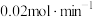 ,单位时间内
,单位时间内 的转化率为60%,则流出气体中
的转化率为60%,则流出气体中 的百分含量为
的百分含量为
您最近一年使用:0次
2023-03-09更新
|
938次组卷
|
4卷引用:河北省石家庄市2023届高中毕业年级教学质量检测(一)化学试题
河北省石家庄市2023届高中毕业年级教学质量检测(一)化学试题(已下线)河北省石家庄市2023届高中毕业年级教学质量检测(一模)变式题(原理综合题)(已下线)专题17 原理综合题河北i省石家庄市第二十四中学2023-2024学年高三上学期期末考试化学试题
解题方法
5 . 异丁烯是一种重要的化工原料,能用于生产甲基叔丁基醚、丁基橡胶、聚异丁烯和甲基丙烯酸酯等。它可由异丁烷通过如下反应催化脱氢制备: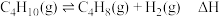 ,回答下列问题:
,回答下列问题:
(1)已知化学键的键能如下表所示,则
_______  。
。
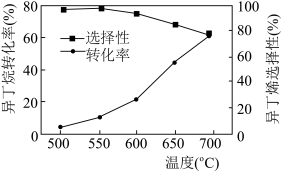
(2)异丁烷的转化率和异丁烯的选择性[ ]随着温度的变化如图所示。当温度升高时,异丁烯的选择性变化的原因是_______(填标号)。
]随着温度的变化如图所示。当温度升高时,异丁烯的选择性变化的原因是_______(填标号)。
(3)在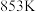 、
、 反应条件下,向反应器中加入氩气与异丁烷混合气体。
反应条件下,向反应器中加入氩气与异丁烷混合气体。
①异丁烷的平衡转化率随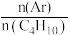 的增大而升高,其原因为
的增大而升高,其原因为_______ 。
②当 时,达到平衡所需时间为
时,达到平衡所需时间为 ,异丁烷的平衡转化率为66.67%,则异丁烷分压的平均变化率为
,异丁烷的平衡转化率为66.67%,则异丁烷分压的平均变化率为_______ 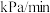 ,异丁烷脱氢反应的
,异丁烷脱氢反应的
_______  。
。
(4)“○”表示催化剂固体杂多酸盐,“…○”表示吸附在该催化剂表面,异丁烷脱氢反应的机理如下,请补充基元反应iii。
i.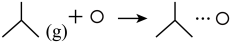
ii.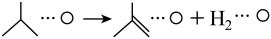
iii._______
iv.
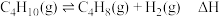 ,回答下列问题:
,回答下列问题:(1)已知化学键的键能如下表所示,则

 。
。| 化学键 |  |  |  | 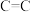 |
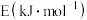 | 436 | 413 | 348 | 615 |
(2)异丁烷的转化率和异丁烯的选择性[
 ]随着温度的变化如图所示。当温度升高时,异丁烯的选择性变化的原因是_______(填标号)。
]随着温度的变化如图所示。当温度升高时,异丁烯的选择性变化的原因是_______(填标号)。
| A.催化剂的活性增大 | B.异丁烷裂解发生副反应 |
| C.异丁烯容易发生聚合反应 | D.平衡向逆反应方向移动 |
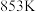 、
、 反应条件下,向反应器中加入氩气与异丁烷混合气体。
反应条件下,向反应器中加入氩气与异丁烷混合气体。①异丁烷的平衡转化率随
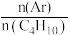 的增大而升高,其原因为
的增大而升高,其原因为②当
 时,达到平衡所需时间为
时,达到平衡所需时间为 ,异丁烷的平衡转化率为66.67%,则异丁烷分压的平均变化率为
,异丁烷的平衡转化率为66.67%,则异丁烷分压的平均变化率为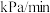 ,异丁烷脱氢反应的
,异丁烷脱氢反应的
 。
。(4)“○”表示催化剂固体杂多酸盐,“…○”表示吸附在该催化剂表面,异丁烷脱氢反应的机理如下,请补充基元反应iii。
i.
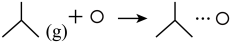
ii.

iii.
iv.

您最近一年使用:0次
6 . Ⅰ.碳热还原 过程中可能发生下列反应。
过程中可能发生下列反应。
ⅰ.

ⅱ.
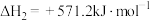
ⅲ.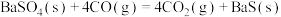
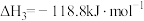
(1)
_______ ;温度升高, 平衡常数K将
平衡常数K将_______ (填“增大”、“减小”、“不变”)。
Ⅱ.乙炔的加成反应是众多科研工作者的研究对象。
(2)不同温度下,1.2
 与1
与1
 制氯乙烯(
制氯乙烯( ),在1L刚性容器中反应3h,实验数据如下图。
),在1L刚性容器中反应3h,实验数据如下图。

①135℃时,3h内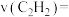
_______ (保留两位小数,下同)。
②该反应最适宜温度下平衡常数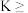
_______ 。
(3)《自然》杂志发表的一篇文章中,提出在催化剂 作用下上述反应的反应历程如图所示。“2→3”的化学方程式可表示为:
作用下上述反应的反应历程如图所示。“2→3”的化学方程式可表示为:

①“4→5”的化学方程式为_______ 。
②反应物在催化剂表面经历过程“扩散→吸附(活性位点)→表面反应→脱附”。若保持体系中 分压不变,
分压不变, 分压过高时反应催化效率降低的可能原因是
分压过高时反应催化效率降低的可能原因是_______ 。
(4)西北工业大学的张健教授、德累斯顿工业大学的冯新亮院士等人报道了一种电催化半氢化策略,在室温条件下,水溶液介质中可选择性地将 还原为
还原为 ,其原理示意图如下:
,其原理示意图如下:

①阴极的电极反应式为:_______ 。
②同温同压下,相同时间内,若进口处气体物质的量为a ,出口处气体的总体积为进口处的x倍,则
,出口处气体的总体积为进口处的x倍,则 转化率为
转化率为_______ 。
 过程中可能发生下列反应。
过程中可能发生下列反应。ⅰ.


ⅱ.

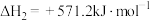
ⅲ.
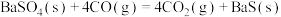
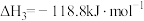
(1)

 平衡常数K将
平衡常数K将Ⅱ.乙炔的加成反应是众多科研工作者的研究对象。
(2)不同温度下,1.2

 与1
与1
 制氯乙烯(
制氯乙烯( ),在1L刚性容器中反应3h,实验数据如下图。
),在1L刚性容器中反应3h,实验数据如下图。
①135℃时,3h内
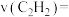
②该反应最适宜温度下平衡常数
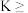
(3)《自然》杂志发表的一篇文章中,提出在催化剂
 作用下上述反应的反应历程如图所示。“2→3”的化学方程式可表示为:
作用下上述反应的反应历程如图所示。“2→3”的化学方程式可表示为:

①“4→5”的化学方程式为
②反应物在催化剂表面经历过程“扩散→吸附(活性位点)→表面反应→脱附”。若保持体系中
 分压不变,
分压不变, 分压过高时反应催化效率降低的可能原因是
分压过高时反应催化效率降低的可能原因是(4)西北工业大学的张健教授、德累斯顿工业大学的冯新亮院士等人报道了一种电催化半氢化策略,在室温条件下,水溶液介质中可选择性地将
 还原为
还原为 ,其原理示意图如下:
,其原理示意图如下:
①阴极的电极反应式为:
②同温同压下,相同时间内,若进口处气体物质的量为a
 ,出口处气体的总体积为进口处的x倍,则
,出口处气体的总体积为进口处的x倍,则 转化率为
转化率为
您最近一年使用:0次
2023-02-09更新
|
701次组卷
|
3卷引用:重庆市南开中学校2023届高三下学期第六次质量检测化学试题
名校
解题方法
7 . 研究含氮元素物质的反应对生产、生活、科研等方面具有重要的意义。
(1)发射“神舟十三”号的火箭推进剂为液态四氧化二氮和液态偏二甲肼(C2H8N2)。
已知:①C2H8N2(l)+4O2(g)=2CO2(g)+N2(g)+4H2O(l) ΔH1=-2765.0kJ/mol
②2O2(g) +N2(g)=N2O4(l) ΔH2=-19.5kJ/mol
③H2O(g)= H2O(l) ΔH3=-44.0kJ/mol
则C2H8N2(1)+2N2O4(1)=3N2(g)+2CO2(g)+4H2O(g)的ΔH为_______ 。
(2)碘蒸气存在能大幅度提高N2O的分解速率,反应历程为:
第一步:I2(g)→2I(g)(快反应)
第二步:I(g)+N2O(g)→N2(g)+IO(g)(慢反应)
第三步:IO(g)+N2O(g)→N2(g)+O2(g)+I2(g)(快反应)
实验表明,含碘时N2O分解速率方程v=k·c(N2O)·[c(I2)]0.5(k为速率常数)。下列表述正确的是_______
(3)为避免汽车尾气中的氮氧化合物对大气的污染,需给汽车安装尾气净化装置。在净化装置中CO和NO发生反应2NO(g)+2CO(g)=N2(g)+2CO2(g) ΔH=-746.8kJ-mol-1。实验测得:v正=k正·p2(NO)·p2(CO),v逆=k逆·p(N2)·p2(CO2)。其中k正、k逆分别为正、逆反应速率常数,只与温度有关;p为气体分压(分压=物质的量分数x总压)。
①达到平衡后,仅升高温度,k正增大的倍数_______ (填“大于”“小于”或“等于”)k逆增大的倍数。
②一定温度下在刚性密闭容器中充入CO、NO和N2物质的量之比为2:2:1,压强为p0kPa。达平衡时压强为0.9p0kPa,则
_______ 。
(4)我国科技人员计算了在一定温度范围内下列反应的平衡常数Kp:
①3N2H4(1)=4NH3(g)+N2(g) ΔH1 Kp1
②4NH3(g)=2N2(g)+6H2(g) ΔH2 Kp2
绘制pKp1-T和pKp2-T的线性关系图如图所示:(已知:pKp=-1gKp)
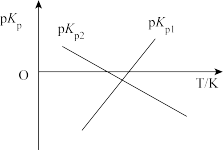
①由图可知,ΔH1_______ 0(填“>”或“<”)
②反应3N2H4(1)=3N2(g)+6H2(g)的K=_______ (用Kp1、Kp2表示);该反应的ΔH_______ 0(填“>”或“<”),写出推理过程_______
(1)发射“神舟十三”号的火箭推进剂为液态四氧化二氮和液态偏二甲肼(C2H8N2)。
已知:①C2H8N2(l)+4O2(g)=2CO2(g)+N2(g)+4H2O(l) ΔH1=-2765.0kJ/mol
②2O2(g) +N2(g)=N2O4(l) ΔH2=-19.5kJ/mol
③H2O(g)= H2O(l) ΔH3=-44.0kJ/mol
则C2H8N2(1)+2N2O4(1)=3N2(g)+2CO2(g)+4H2O(g)的ΔH为
(2)碘蒸气存在能大幅度提高N2O的分解速率,反应历程为:
第一步:I2(g)→2I(g)(快反应)
第二步:I(g)+N2O(g)→N2(g)+IO(g)(慢反应)
第三步:IO(g)+N2O(g)→N2(g)+O2(g)+I2(g)(快反应)
实验表明,含碘时N2O分解速率方程v=k·c(N2O)·[c(I2)]0.5(k为速率常数)。下列表述正确的是_______
| A.N2O分解反应中,k值与碘蒸气浓度大小有关 |
| B.v(第二步的逆反应)<v(第三步反应) |
| C.IO为反应的催化剂 |
| D.第二步活化能比第三步大 |
①达到平衡后,仅升高温度,k正增大的倍数
②一定温度下在刚性密闭容器中充入CO、NO和N2物质的量之比为2:2:1,压强为p0kPa。达平衡时压强为0.9p0kPa,则

(4)我国科技人员计算了在一定温度范围内下列反应的平衡常数Kp:
①3N2H4(1)=4NH3(g)+N2(g) ΔH1 Kp1
②4NH3(g)=2N2(g)+6H2(g) ΔH2 Kp2
绘制pKp1-T和pKp2-T的线性关系图如图所示:(已知:pKp=-1gKp)

①由图可知,ΔH1
②反应3N2H4(1)=3N2(g)+6H2(g)的K=
您最近一年使用:0次
2022-04-09更新
|
986次组卷
|
4卷引用:湖南省湘潭市第一中学2023届高三第六次月考化学试题



