1 . 如图实验装置和方法进行相应实验,装置和现象均正确且能达到实验目的的是
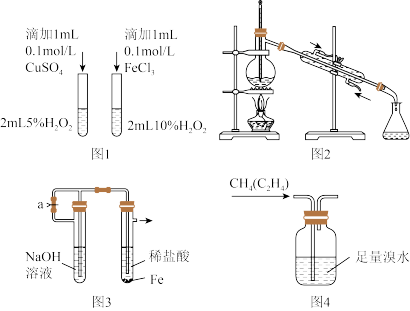

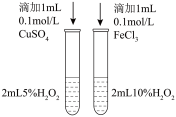
| A.图1比较Cu2+、Fe3+对反应速率的影响 |
| B.图2蒸馏海水得到淡水 |
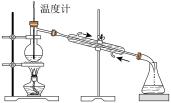
| C.图3制备少量Fe(OH)2沉淀 |
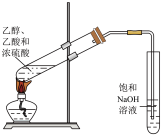
| D.图4除甲烷中的乙烯 |
您最近一年使用:0次
名校
2 . 如图实验装置和方法进行相应实验,装置和现象均正确且能 达到实验目的的是
| A | B | C | D |
 |  |  | 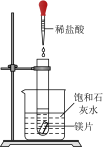 |
比较 、 、 对反应速率的影响 对反应速率的影响 | 蒸馏海水得到淡水 | 制取少量乙酸乙酯 | 验证镁片与稀盐酸反应放热 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
3 . 如图实验装置和方法进行相应实验,装置和现象均正确且能达到实验目的的是
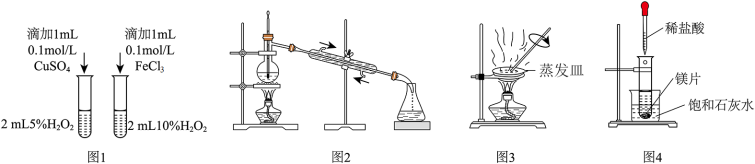

| A.图1是比较Cu2+、Fe3+对反应速率的影响 |
| B.图2是蒸馏海水得到淡水 |
| C.图3是蒸干NaHCO3溶液获得NaHCO3晶体 |
| D.图4是验证镁片与稀盐酸反应放热 |
您最近一年使用:0次
名校
4 . 利用如图实验装置进行相应实验,能达到实验目的的是
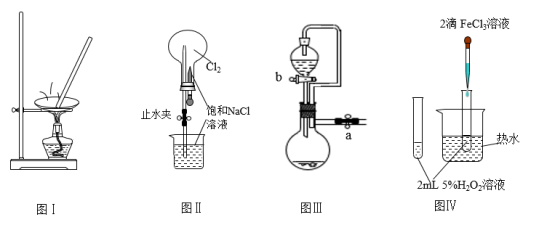

| A.利用图Ⅰ装置蒸发KCl溶液制备无水KCl |
| B.利用图Ⅱ装置进行喷泉实验 |
| C.图Ⅲ装置中,关闭a、打开b,可检查装置的气密性 |
D.利用图Ⅳ装置验证 分解反应有催化作用 分解反应有催化作用 |
您最近一年使用:0次
2021-10-11更新
|
380次组卷
|
5卷引用:福建省福州市六校联考2022-2023学年高一下学期期末考试化学试题
福建省福州市六校联考2022-2023学年高一下学期期末考试化学试题福建省莆田市第二中学2022届高三10月月考化学试题福建省泉州市城东中学2021-2022学年高三上学期10月月考化学试题四川省宜宾市叙州区第二中学校2023-2024学年高二上学期12月月考化学试题(已下线)提升卷02-【新高考新题型】2022年高考化学选择题标准化练习20卷(山东专用)
名校
5 . 亚硝酰硫酸(NOSO4H)主要用于染料、医药等工业,是一种浅黄色、遇水易分解的固体,但溶于浓硫酸后并不分解。某实验小组将在A中产生的SO2通入浓硫酸和浓硝酸的混合溶液中制备亚硝酰硫酸,并测定产品的纯度。
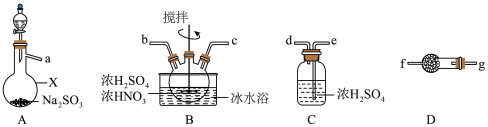
(1)仪器X的名称为___________ ;
(2)按气流从左到右的顺序,上述仪器的连接顺序为(填仪器接口字母)___________ 。
(3)①装置B中发生反应的化学方程式为___________ 。
②开始时反应缓慢,待生成少量NOSO4H后,温度变化不大,但反应速率明显加快,其可能原因是___________ 。
(4)装置B中维持反应体系温度不高于20℃的主要原因是___________ 。
(5)测定产品的纯度:称取4.5g产品放入锥形瓶中,加入100.00 mL 0.10mol/L的KMnO4溶液和适量H2SO4,摇匀,再将溶液加热至60~70℃(使生成的HNO3挥发逸出),冷却至室温,然后用0.20 mol/L的Na2C2O4标准溶液滴定至终点,消耗Na2C2O4溶液的体积为25.00 mL。
已知:2KMnO4+5NOSO4H+2H2O=K2SO4+2MnSO4+5HNO3+2H2SO4,2KMnO4+5Na2C2O4+8H2SO4=K2SO4+2MnSO4+10CO2+5Na2SO4+8H2O。
①滴定终点的现象为___________ 。
②该产品的纯度为___________ % (保留小数点后一位)。

(1)仪器X的名称为
(2)按气流从左到右的顺序,上述仪器的连接顺序为(填仪器接口字母)
(3)①装置B中发生反应的化学方程式为
②开始时反应缓慢,待生成少量NOSO4H后,温度变化不大,但反应速率明显加快,其可能原因是
(4)装置B中维持反应体系温度不高于20℃的主要原因是
(5)测定产品的纯度:称取4.5g产品放入锥形瓶中,加入100.00 mL 0.10mol/L的KMnO4溶液和适量H2SO4,摇匀,再将溶液加热至60~70℃(使生成的HNO3挥发逸出),冷却至室温,然后用0.20 mol/L的Na2C2O4标准溶液滴定至终点,消耗Na2C2O4溶液的体积为25.00 mL。
已知:2KMnO4+5NOSO4H+2H2O=K2SO4+2MnSO4+5HNO3+2H2SO4,2KMnO4+5Na2C2O4+8H2SO4=K2SO4+2MnSO4+10CO2+5Na2SO4+8H2O。
①滴定终点的现象为
②该产品的纯度为
您最近一年使用:0次
名校
6 . 用下列实验装置可以达到对应实验目的的是
| A | B | C | D | |
| 实验目的 | 制备“84”消毒液(电极均为惰性电极) | 将化学能转化为电能 | 测量盐酸和氢氧化钠反应的反应热 | 比较 、 、 对反应速率的影响 对反应速率的影响 |
| 实验装置 |  |  |  |  |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
7 . 下列图示装置不能达到实验目的的是


| A.图1:验证温度对化学平衡的影响 |
| B.图2:测定锌与稀硫酸的反应速率 |
| C.图3:验证FeCl3溶液对H2O2分解有催化作用 |
| D.图4:研究浓度对反应速率的影响 |
您最近一年使用:0次
2021-11-18更新
|
244次组卷
|
7卷引用:福建省宁德市部分达标中学2023-2024学年高二上学期期中考试化学试题
名校
8 . 下列实验操作规范且能达到实验目的的是
| 目的 | 操作 | |
| A | 测定醋酸钠溶液的pH | 用玻璃棒蘸 取溶液,点在湿润的pH试纸上 |
| B | 排除碱式滴定管尖嘴部分的气泡 | 将胶管弯曲使玻璃尖嘴斜向上,用两指捏住胶管,轻轻挤压玻璃珠,使溶液从尖嘴流出 |
| C | 由TiCl4制备TiO2∙xH2O | 在干燥的HCl气流中加热 |
| D | 研究催化剂对H2O2分解速率的影响 | 分别向两支试管中加入相同体积不同浓度的H2O2溶液,再向其中一支中加入少量MnO2 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2022-01-20更新
|
558次组卷
|
7卷引用:福建省莆田第一中学2022-2023学年高二上学期期末考试化学试题
名校
9 . “化学多米诺实验“即只需控制第一个反应,利用反应中气体产生的压力和虹吸作用原理使若干化学实验依次发生。如图是一个“化学多米诺实验”。
已知:①Cu2++4NH3·H2O=4H2O+[Cu(NH3)4]2+(该反应产物可作为H2O2分解的催化剂)
②A和C中的硫酸溶液浓度相同
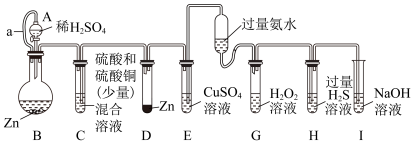
下列有关分析错误的是
已知:①Cu2++4NH3·H2O=4H2O+[Cu(NH3)4]2+(该反应产物可作为H2O2分解的催化剂)
②A和C中的硫酸溶液浓度相同

下列有关分析错误的是
| A.B装置中反应速率大于D装置中反应速率 |
| B.E装置中现象为试管内蓝色液面下降 |
| C.H装置中出现浅黄色浑浊 |
| D.该实验成功的重要条件是整套装置气密性良好 |
您最近一年使用:0次
2023-09-02更新
|
182次组卷
|
2卷引用:福建省政和县第一中学2023-2024学年高三上学期第一次月考化学试题
10 . 工业制硫酸的过程中, 转化为
转化为 是关键的一步,其反应方程式为:
是关键的一步,其反应方程式为: 。
。
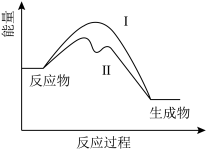
(1)在使用催化剂和未使用催化剂时, 转化为
转化为 的反应过程能量变化如下图所示,过程Ⅰ释放的能量
的反应过程能量变化如下图所示,过程Ⅰ释放的能量___________ 过程Ⅱ释放的能量(填“大于”“小于”或“等于”)。
(2)一定温度下,在2L的恒容容器中发生以上转化,反应过程中部分数据见下表:
① 的平均反应速率
的平均反应速率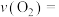
___________  。
。
②平衡时气体压强与初始时气体压强比为___________ 。
③能说明 转化为
转化为 的反应已达平衡状态的是
的反应已达平衡状态的是___________ 。
a. b.
b.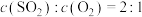
c.容器内压强保持不变 d.单位时间内消耗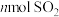 同时生成
同时生成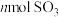
(3)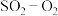 燃料电池可实现在能量利用的同时制备硫酸,其装置如下图所示。
燃料电池可实现在能量利用的同时制备硫酸,其装置如下图所示。
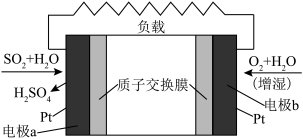
①该装置可以将___________ 能转化为___________ 能。
②电池工作时,电子导体中电子移动方向为___________ (选填“a到b”或“b到a”)
 转化为
转化为 是关键的一步,其反应方程式为:
是关键的一步,其反应方程式为: 。
。(1)在使用催化剂和未使用催化剂时,
 转化为
转化为 的反应过程能量变化如下图所示,过程Ⅰ释放的能量
的反应过程能量变化如下图所示,过程Ⅰ释放的能量
(2)一定温度下,在2L的恒容容器中发生以上转化,反应过程中部分数据见下表:
| 反应时间/min |  | 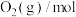 | 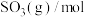 |
| 0 | 4 | 2 | 0 |
| 5 | 1.5 | ||
| 10 | 2 | ||
| 15 | 1 |
 的平均反应速率
的平均反应速率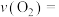
 。
。②平衡时气体压强与初始时气体压强比为
③能说明
 转化为
转化为 的反应已达平衡状态的是
的反应已达平衡状态的是a.
 b.
b.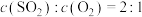
c.容器内压强保持不变 d.单位时间内消耗
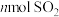 同时生成
同时生成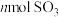
(3)
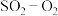 燃料电池可实现在能量利用的同时制备硫酸,其装置如下图所示。
燃料电池可实现在能量利用的同时制备硫酸,其装置如下图所示。
①该装置可以将
②电池工作时,电子导体中电子移动方向为
您最近一年使用:0次



