名校
1 . 工业上采用高温热分解H2S的方法制取H2。在恒容密闭容器中,控制不同温度进行一定量的H₂S分解:
 ,实验过程中测得H2S的平衡转化率、经过相同时间时H2S的转化率变化如图所示。下列说法错误的是
,实验过程中测得H2S的平衡转化率、经过相同时间时H2S的转化率变化如图所示。下列说法错误的是

 ,实验过程中测得H2S的平衡转化率、经过相同时间时H2S的转化率变化如图所示。下列说法错误的是
,实验过程中测得H2S的平衡转化率、经过相同时间时H2S的转化率变化如图所示。下列说法错误的是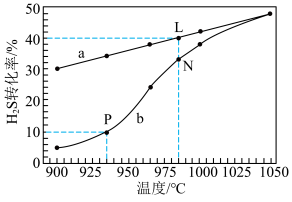
A.P、N、L三点,L点的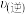 最大 最大 |
| B.曲线a表示H2S的平衡转化率随温度变化曲线 |
| C.随温度的升高,曲线b逐渐向a靠近的原因是反应达到平衡所需时间缩短 |
| D.若恒温、恒压条件下,充入1mol H2S进行上述反应,欲将H2S平衡转化率由20%提升至40%,可向反应器中充入34mol Ar作为稀释气 |
您最近一年使用:0次
名校
2 . 向体积为 的两密闭容器中各通入
的两密闭容器中各通入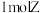 ,分别在恒温、绝热条件下发生:
,分别在恒温、绝热条件下发生: ,测得反应过程中体系压强随时间变化如图。下列说法不正确的是
,测得反应过程中体系压强随时间变化如图。下列说法不正确的是
 的两密闭容器中各通入
的两密闭容器中各通入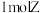 ,分别在恒温、绝热条件下发生:
,分别在恒温、绝热条件下发生: ,测得反应过程中体系压强随时间变化如图。下列说法不正确的是
,测得反应过程中体系压强随时间变化如图。下列说法不正确的是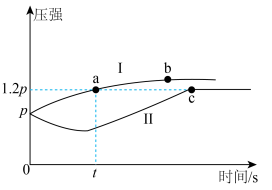
| A.曲线Ⅱ对应绝热条件 | B.曲线I、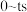 内: 内: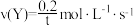 |
C.转化率: | D.平衡常数: |
您最近一年使用:0次
名校
解题方法
3 . 乙酰苯胺是一种无色有闪光的小叶状固体或白色晶性粉末,是磺胺类药物的原料,可用作止痛剂、退热剂、防腐剂。乙酰苯胺的一种制备原理为:
实验步骤:
【步骤1】如图所示,在圆底烧瓶中加入无水苯胺 、冰醋酸
、冰醋酸 、锌粉
、锌粉 ,安装仪器,加入沸石,调节加热温度,使温度计温度控制在
,安装仪器,加入沸石,调节加热温度,使温度计温度控制在 左右,反应约
左右,反应约 ,当反应基本完成时,停止加热。
,当反应基本完成时,停止加热。 水,搅拌加热至沸腾,使粗品完全溶解。
水,搅拌加热至沸腾,使粗品完全溶解。
【步骤3】稍冷后,加入 活性炭,并煮沸
活性炭,并煮沸 ,趁热抽滤除去活性炭。
,趁热抽滤除去活性炭。
【步骤4】将滤液倒入烧杯中,自然冷却,析出晶体。抽滤、洗涤、干燥得产品,称其质量。
回答下列问题:
(1)仪器a的名称_____ 。
(2)【步骤1】加热可用_____ (填“水浴”或“油浴”)。
(3)制备过程中加入锌粉的作用为_____ 。
(4)从化学平衡的角度分析,使用刺形分馏柱并控制分馏柱上端的温度在 左右的原因:
左右的原因:_____ 。
(5)乙酰苯胺粗品因含杂质而显色,【步骤3】中加入活性炭吸附有色杂质,加入活性炭需要待沸腾的溶液稍冷却后再加入,其目的是_____ 。
(6)该实验最终得到纯品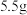 ,则乙酰苯胺的产率为
,则乙酰苯胺的产率为_____ (保留一位小数)。
(7)乙酰苯胺可以在 热溶液中发生水解,写出其反应方程式:
热溶液中发生水解,写出其反应方程式:_____ 。
(8)当制备少量乙酰苯胺时,常用图所示的微型仪器组装成实验装置制备。当观察到_____ 现象时,反应基本结束。
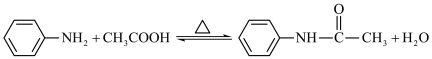
| 名称 | 相对分子质量 | 性状 | 密度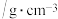 | 沸点/℃ | 溶解度 | 备注 |
| 苯胺 | 93 | 无色油状液体 | 1.02 | 184.4 | 微溶于水,易溶于乙醇、乙醚 | 易被氧化 |
| 乙酸 | 60 | 无色液体 | 1.05 | 118.1 | 易溶于水,易溶于乙醇、乙醚 | |
| 乙酰苯胺 | 135 | 白色晶体 | 1.22 | 304 | 微溶于冷水,溶于热水,易溶于乙醇、乙醚 |
【步骤1】如图所示,在圆底烧瓶中加入无水苯胺
 、冰醋酸
、冰醋酸 、锌粉
、锌粉 ,安装仪器,加入沸石,调节加热温度,使温度计温度控制在
,安装仪器,加入沸石,调节加热温度,使温度计温度控制在 左右,反应约
左右,反应约 ,当反应基本完成时,停止加热。
,当反应基本完成时,停止加热。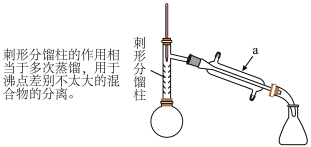
 水,搅拌加热至沸腾,使粗品完全溶解。
水,搅拌加热至沸腾,使粗品完全溶解。【步骤3】稍冷后,加入
 活性炭,并煮沸
活性炭,并煮沸 ,趁热抽滤除去活性炭。
,趁热抽滤除去活性炭。【步骤4】将滤液倒入烧杯中,自然冷却,析出晶体。抽滤、洗涤、干燥得产品,称其质量。
回答下列问题:
(1)仪器a的名称
(2)【步骤1】加热可用
(3)制备过程中加入锌粉的作用为
(4)从化学平衡的角度分析,使用刺形分馏柱并控制分馏柱上端的温度在
 左右的原因:
左右的原因:(5)乙酰苯胺粗品因含杂质而显色,【步骤3】中加入活性炭吸附有色杂质,加入活性炭需要待沸腾的溶液稍冷却后再加入,其目的是
(6)该实验最终得到纯品
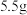 ,则乙酰苯胺的产率为
,则乙酰苯胺的产率为(7)乙酰苯胺可以在
 热溶液中发生水解,写出其反应方程式:
热溶液中发生水解,写出其反应方程式:(8)当制备少量乙酰苯胺时,常用图所示的微型仪器组装成实验装置制备。当观察到

您最近一年使用:0次
名校
4 . 25℃下,分别向体积均为1L的容器甲(恒温)、容器乙(绝热)中加入2molA和2molB,发生反应 ,两容器中A的转化率随时间的变化如图.下列说法正确的是
,两容器中A的转化率随时间的变化如图.下列说法正确的是
 ,两容器中A的转化率随时间的变化如图.下列说法正确的是
,两容器中A的转化率随时间的变化如图.下列说法正确的是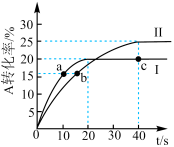
A.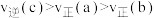 |
| B.曲线Ⅰ代表容器乙中A的转化率随时间变化 |
C.0~40s内,曲线Ⅱ中C的反应速率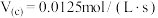 |
| D.容器乙达平衡后,缩小容器体积,达新平衡后C的物质的量增大 |
您最近一年使用:0次
名校
5 . 科学家研究利用反应 处理污染气体,向两个体积相同的恒容密闭容器中分别通入
处理污染气体,向两个体积相同的恒容密闭容器中分别通入 和
和 发生反应,反应体系的总压强随时间变化如图所示。下列说法正确的是
发生反应,反应体系的总压强随时间变化如图所示。下列说法正确的是
 处理污染气体,向两个体积相同的恒容密闭容器中分别通入
处理污染气体,向两个体积相同的恒容密闭容器中分别通入 和
和 发生反应,反应体系的总压强随时间变化如图所示。下列说法正确的是
发生反应,反应体系的总压强随时间变化如图所示。下列说法正确的是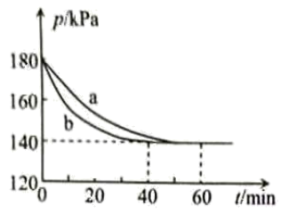
| A.b中反应温度比a中反应温度更高 |
B.向平衡后的b中加入 和 和 ,平衡向逆向移动 ,平衡向逆向移动 |
C.a中, 内 内 的平均反应速率约为 的平均反应速率约为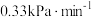 |
D.若开始时将b容积压缩到一半,则b平衡时总压大于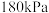 |
您最近一年使用:0次
名校
6 . 下列装置和操作能达到实验预期目的的是
|
|
A.实验室制 | B.实验室制氯气 |
|
|
C. ,颜色加深说明平衡逆移 ,颜色加深说明平衡逆移 | D.验证过氧化钠与水的反应是放热反应 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
7 . 一定条件下, 将NO还原成
将NO还原成 的反应为:
的反应为: 。在恒容密闭容器中按体积比为1∶1充入反应物,反应后有关数据如图。下列说法正确的是
。在恒容密闭容器中按体积比为1∶1充入反应物,反应后有关数据如图。下列说法正确的是
 将NO还原成
将NO还原成 的反应为:
的反应为: 。在恒容密闭容器中按体积比为1∶1充入反应物,反应后有关数据如图。下列说法正确的是
。在恒容密闭容器中按体积比为1∶1充入反应物,反应后有关数据如图。下列说法正确的是
| A.该反应的正反应为吸热反应 |
| B.其他条件不变时,在容器中充入Ar,可提高NO的转化率 |
| C.400℃后,催化效率降低的原因可能是温度过高催化剂失活 |
| D.使用催化剂,O点的平衡转化率可提高到M点 |
您最近一年使用:0次
2024-05-02更新
|
167次组卷
|
3卷引用:重庆市渝西中学2023-2024学年高三下学期4月月考化学试题
重庆市渝西中学2023-2024学年高三下学期4月月考化学试题安徽省六安市裕安区新安中学2023-2024学年高二下学期第一次月考化学试题(已下线)提升练04 化学平衡图像分析-【查漏补缺】2024年高考化学复习冲刺过关(新高考专用)
名校
8 . 在 催化作用下发生反应:
催化作用下发生反应: 。其反应的机理如下图所示。下列说法不正确的是
。其反应的机理如下图所示。下列说法不正确的是
 催化作用下发生反应:
催化作用下发生反应: 。其反应的机理如下图所示。下列说法不正确的是
。其反应的机理如下图所示。下列说法不正确的是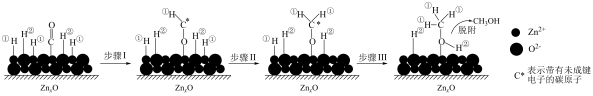
A.吸附在 上的H带正电荷 上的H带正电荷 |
| B.步骤Ⅰ、Ⅱ、Ⅲ均吸收能量 |
C.该过程中有s—  键的形成 键的形成 |
D.合成 过程中不断分离出 过程中不断分离出 ,有利于平衡正向移动 ,有利于平衡正向移动 |
您最近一年使用:0次
名校
9 . 下列实验目的、实验操作及现象与对应结论都正确的是
选项 | 实验目的 | 实验操作及现象 | 结论 |
A | 检验蔗糖是否水解 | 向蔗糖溶液中滴加稀硫酸,水浴加热,加入新制的 ,无砖红色沉淀 ,无砖红色沉淀 | 蔗糖未发生水解 |
B | 探究镁和铝的金属活泼性 | 向盛有浓 溶液的两支试管中分别加入除去氧化膜的镁带和铝片,加入镁带的试管中迅速产生红棕色气体,加入铝片试管中无明显现象 溶液的两支试管中分别加入除去氧化膜的镁带和铝片,加入镁带的试管中迅速产生红棕色气体,加入铝片试管中无明显现象 | 金属活泼性: 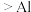 |
C | 探究氢离子浓度对 、 、 相互转化的影响 相互转化的影响 | 向 溶液中缓慢滴加浓硫酸,溶液黄色变为橙红色 溶液中缓慢滴加浓硫酸,溶液黄色变为橙红色 | 增大氢离子浓度,平衡向生成 的方向移动 的方向移动 |
D | 探究在相同条件下 和 和 的溶解度大小 的溶解度大小 | 向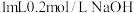 溶液中滴入2滴 溶液中滴入2滴 溶液,产生白色沉淀后,再滴加2滴 溶液,产生白色沉淀后,再滴加2滴 溶液,又生成红褐色沉淀 溶液,又生成红褐色沉淀 | 证明在相同条件下,溶解度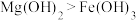 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
10 . 在恒容密闭容器中发生反应: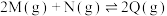
 ,在容器中以
,在容器中以 通入两种反应物,
通入两种反应物, 后M在不同温度下转化率如下表所示,且
后M在不同温度下转化率如下表所示,且 ,则下列说法正确的是
,则下列说法正确的是
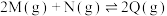
 ,在容器中以
,在容器中以 通入两种反应物,
通入两种反应物, 后M在不同温度下转化率如下表所示,且
后M在不同温度下转化率如下表所示,且 ,则下列说法正确的是
,则下列说法正确的是温度 |
|
|
|
|
转化率 | 10% | 60% | 60% | 50% |
A.根据上述信息可知 |
B. 温度下,若 温度下,若 后反应继续进行,N的转化率大于60% 后反应继续进行,N的转化率大于60% |
C. 温度下( 温度下(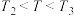 ),N的转化率是30% ),N的转化率是30% |
D. 温度下,充入一定量惰性气体一定可以提高Q的平衡产率 温度下,充入一定量惰性气体一定可以提高Q的平衡产率 |
您最近一年使用:0次









