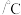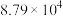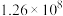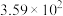名校
1 . 工业上采用高温热分解H2S的方法制取H2。在恒容密闭容器中,控制不同温度进行一定量的H₂S分解:
 ,实验过程中测得H2S的平衡转化率、经过相同时间时H2S的转化率变化如图所示。下列说法错误的是
,实验过程中测得H2S的平衡转化率、经过相同时间时H2S的转化率变化如图所示。下列说法错误的是

 ,实验过程中测得H2S的平衡转化率、经过相同时间时H2S的转化率变化如图所示。下列说法错误的是
,实验过程中测得H2S的平衡转化率、经过相同时间时H2S的转化率变化如图所示。下列说法错误的是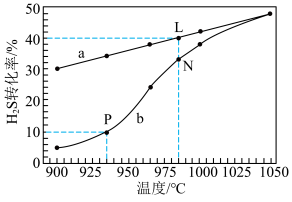
A.P、N、L三点,L点的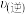 最大 最大 |
| B.曲线a表示H2S的平衡转化率随温度变化曲线 |
| C.随温度的升高,曲线b逐渐向a靠近的原因是反应达到平衡所需时间缩短 |
| D.若恒温、恒压条件下,充入1mol H2S进行上述反应,欲将H2S平衡转化率由20%提升至40%,可向反应器中充入34mol Ar作为稀释气 |
您最近一年使用:0次
名校
2 . 向体积为 的两密闭容器中各通入
的两密闭容器中各通入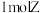 ,分别在恒温、绝热条件下发生:
,分别在恒温、绝热条件下发生: ,测得反应过程中体系压强随时间变化如图。下列说法不正确的是
,测得反应过程中体系压强随时间变化如图。下列说法不正确的是
 的两密闭容器中各通入
的两密闭容器中各通入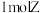 ,分别在恒温、绝热条件下发生:
,分别在恒温、绝热条件下发生: ,测得反应过程中体系压强随时间变化如图。下列说法不正确的是
,测得反应过程中体系压强随时间变化如图。下列说法不正确的是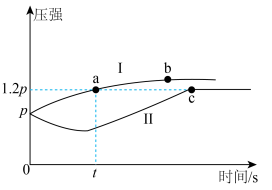
| A.曲线Ⅱ对应绝热条件 | B.曲线I、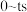 内: 内: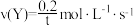 |
C.转化率: | D.平衡常数: |
您最近一年使用:0次
名校
3 . 向某恒容密闭容器中充入一定量的Xe和 ,发生反应
,发生反应 。
。

不同温度下平衡常数如表,平衡时的分布分数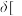 如
如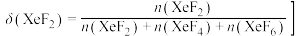 随温度的变化如图。下列说法不正确的是
随温度的变化如图。下列说法不正确的是
 ,发生反应
,发生反应 。
。
温度 |
|
|
250 |
|
|
400 |
|
|
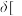 如
如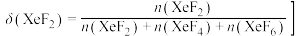 随温度的变化如图。下列说法不正确的是
随温度的变化如图。下列说法不正确的是
| A.反应ⅲ低温自发 |
B.当 与 与 的投料比为1:1时,平衡转化率: 的投料比为1:1时,平衡转化率: 大于Xe 大于Xe |
C.升高温度,平衡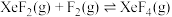 正向移动 正向移动 |
D.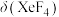 在 在 后减小的原因是反应ⅱ逆向移动的程度较大 后减小的原因是反应ⅱ逆向移动的程度较大 |
您最近一年使用:0次
2024-05-16更新
|
128次组卷
|
2卷引用:2024届重庆市南开中学校高三下学期5月月考化学试题
名校
4 . 25℃下,分别向体积均为1L的容器甲(恒温)、容器乙(绝热)中加入2molA和2molB,发生反应 ,两容器中A的转化率随时间的变化如图.下列说法正确的是
,两容器中A的转化率随时间的变化如图.下列说法正确的是
 ,两容器中A的转化率随时间的变化如图.下列说法正确的是
,两容器中A的转化率随时间的变化如图.下列说法正确的是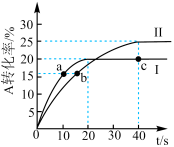
A.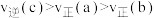 |
| B.曲线Ⅰ代表容器乙中A的转化率随时间变化 |
C.0~40s内,曲线Ⅱ中C的反应速率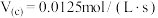 |
| D.容器乙达平衡后,缩小容器体积,达新平衡后C的物质的量增大 |
您最近一年使用:0次
名校
5 . 下列生活情境的化学解释不正确的是
| A.在青铜器、铁器保存中流传着“干千年,湿万年,不干不湿就半年”的说法,原因是它们在不干不湿的空气中容易构成原电池而腐蚀损耗 |
B.关节滑液中存在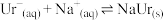 ,寒冷季节NaUr晶体的形成是诱发关节炎的原因,由此判断该反应为放热反应 ,寒冷季节NaUr晶体的形成是诱发关节炎的原因,由此判断该反应为放热反应 |
| C.通常采用真空包装进行食品保鲜,因为降低氧气浓度可以减慢食物变质速率 |
D.大力推广无氟制冷剂,因为制冷剂释放的 进入大气会破坏臭氧层 进入大气会破坏臭氧层 |
您最近一年使用:0次
名校
6 . 科学家研究利用反应 处理污染气体,向两个体积相同的恒容密闭容器中分别通入
处理污染气体,向两个体积相同的恒容密闭容器中分别通入 和
和 发生反应,反应体系的总压强随时间变化如图所示。下列说法正确的是
发生反应,反应体系的总压强随时间变化如图所示。下列说法正确的是
 处理污染气体,向两个体积相同的恒容密闭容器中分别通入
处理污染气体,向两个体积相同的恒容密闭容器中分别通入 和
和 发生反应,反应体系的总压强随时间变化如图所示。下列说法正确的是
发生反应,反应体系的总压强随时间变化如图所示。下列说法正确的是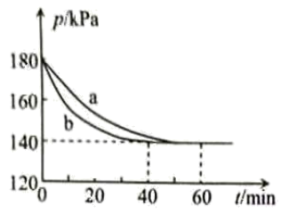
| A.b中反应温度比a中反应温度更高 |
B.向平衡后的b中加入 和 和 ,平衡向逆向移动 ,平衡向逆向移动 |
C.a中, 内 内 的平均反应速率约为 的平均反应速率约为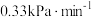 |
D.若开始时将b容积压缩到一半,则b平衡时总压大于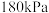 |
您最近一年使用:0次
名校
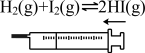
7 . 下列装置和操作能达到实验预期目的的是
|
|
A.实验室制 | B.实验室制氯气 |
|
|
C. ,颜色加深说明平衡逆移 ,颜色加深说明平衡逆移 | D.验证过氧化钠与水的反应是放热反应 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
8 . 已知反应:2NO2(红棕色)⇌N2O4(无色),该反应为放热反应。将一定量的NO2充入注射器中后封口,如图是在拉伸和压缩注射器的过程中气体透光率随时间的变化(气体颜色越深,透光率越小)。下列说法正确的是
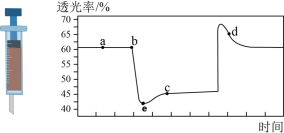
| A.b点的操作是压缩注射器 |
| B.b点v正>c点v正 |
| C.c点与a点相比,c(NO2)增大,c(N2O4)减小 |
| D.e点是平衡状态 |
您最近一年使用:0次
名校
解题方法
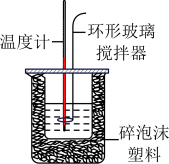
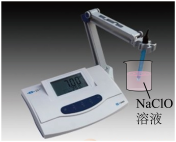
9 . 下列实验方案不能达到目的的是
|
|
|
|
| A.测定中和热 | B.探究压强对平衡移动的影响 | C.排出碱式滴定管中的气泡 | D.测定NaClO溶液的pH |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
10 . 一定条件下, 将NO还原成
将NO还原成 的反应为:
的反应为: 。在恒容密闭容器中按体积比为1∶1充入反应物,反应后有关数据如图。下列说法正确的是
。在恒容密闭容器中按体积比为1∶1充入反应物,反应后有关数据如图。下列说法正确的是
 将NO还原成
将NO还原成 的反应为:
的反应为: 。在恒容密闭容器中按体积比为1∶1充入反应物,反应后有关数据如图。下列说法正确的是
。在恒容密闭容器中按体积比为1∶1充入反应物,反应后有关数据如图。下列说法正确的是
| A.该反应的正反应为吸热反应 |
| B.其他条件不变时,在容器中充入Ar,可提高NO的转化率 |
| C.400℃后,催化效率降低的原因可能是温度过高催化剂失活 |
| D.使用催化剂,O点的平衡转化率可提高到M点 |
您最近一年使用:0次
2024-05-02更新
|
164次组卷
|
3卷引用:重庆市渝西中学2023-2024学年高三下学期4月月考化学试题
重庆市渝西中学2023-2024学年高三下学期4月月考化学试题安徽省六安市裕安区新安中学2023-2024学年高二下学期第一次月考化学试题(已下线)提升练04 化学平衡图像分析-【查漏补缺】2024年高考化学复习冲刺过关(新高考专用)