1 . 完成下列问题。
(1)化学键的键能是形成(或断裂)1 mol化学键时释放(或吸收)的能量。以下是部分共价键键能的数据:H-S:364 kJ·mol-1,S-S:266 kJ·mol-1,S=O:522 kJ·mol-1,H-O:463 kJ·mol-1,试根据这些数据计算下列反应的反应热:2H2S(g)+SO2(g)= 3S(s)+2H2O(l) ΔH=-Q kJ·mol-1,反应产物中的S实为S8,实际分子是一个八元环状分子(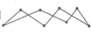 ),则Q=
),则Q=______ 。
(2)已知反应aA(g)+bB(g) cC(g),某温度下,在2 L的密闭容器中投入一定量的A、B,两种气体的物的量浓度随时间变化的曲线如图所示。
cC(g),某温度下,在2 L的密闭容器中投入一定量的A、B,两种气体的物的量浓度随时间变化的曲线如图所示。_____ 。
②经测定,前4 s内v(C)=0.05 mol·L-1·s-1,则该反应的化学方程式为______ 。
③若上述反应分别在甲、乙、丙三个相同的密闭容器中进行,经同一段时间后,测得三个容器中的反应速率分别为甲:v(A)=0.3 mol·L-1·s-1,乙:v(B)=0.12 mol·L-1·s-1,丙:v(C)=9.6 mol·L-1·min-1,则甲、乙、丙三个容器中反应速率由快到慢的顺序为_______ 。
(3)向某容积不变的密闭容器中充入一定量的NO2,发生反应2NO2(g) N2O4(g) ΔH<0,达到平衡后,若分别单独改变下列条件,下列判断正确的是_____。
N2O4(g) ΔH<0,达到平衡后,若分别单独改变下列条件,下列判断正确的是_____。
(4)工业上常用甲烷水蒸气重整制备氢气,体系中发生如下反应:
Ⅰ.CH4(g)+H2O(g) CO(g)+3H2(g) Ⅱ.CO(g)+H2O(g)
CO(g)+3H2(g) Ⅱ.CO(g)+H2O(g)  CO2(g)+H2(g)
CO2(g)+H2(g)
①下列操作中,能提高CH4(g)平衡转化率的是____ (填标号)。
A.增加CH4 (g)用量 B.恒温恒压下通入惰性气体
C.移除CO(g) D.加入催化剂
②恒温恒压条件下,1 mol CH4 (g)和1 mol H2O(g)反应达平衡时,CH4 (g)的转化率为α,CO2(g)的物质的量为b mol,则反应Ⅰ的平衡常数Kx=____ [写出含有α、b的计算式;对于反应mA(g)+nB(g) pC(g)+qD(g),Kx=
pC(g)+qD(g),Kx=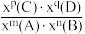 ,x为物质的量分数]。
,x为物质的量分数]。
(1)化学键的键能是形成(或断裂)1 mol化学键时释放(或吸收)的能量。以下是部分共价键键能的数据:H-S:364 kJ·mol-1,S-S:266 kJ·mol-1,S=O:522 kJ·mol-1,H-O:463 kJ·mol-1,试根据这些数据计算下列反应的反应热:2H2S(g)+SO2(g)= 3S(s)+2H2O(l) ΔH=-Q kJ·mol-1,反应产物中的S实为S8,实际分子是一个八元环状分子(
 ),则Q=
),则Q=(2)已知反应aA(g)+bB(g)
 cC(g),某温度下,在2 L的密闭容器中投入一定量的A、B,两种气体的物的量浓度随时间变化的曲线如图所示。
cC(g),某温度下,在2 L的密闭容器中投入一定量的A、B,两种气体的物的量浓度随时间变化的曲线如图所示。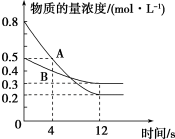
②经测定,前4 s内v(C)=0.05 mol·L-1·s-1,则该反应的化学方程式为
③若上述反应分别在甲、乙、丙三个相同的密闭容器中进行,经同一段时间后,测得三个容器中的反应速率分别为甲:v(A)=0.3 mol·L-1·s-1,乙:v(B)=0.12 mol·L-1·s-1,丙:v(C)=9.6 mol·L-1·min-1,则甲、乙、丙三个容器中反应速率由快到慢的顺序为
(3)向某容积不变的密闭容器中充入一定量的NO2,发生反应2NO2(g)
 N2O4(g) ΔH<0,达到平衡后,若分别单独改变下列条件,下列判断正确的是_____。
N2O4(g) ΔH<0,达到平衡后,若分别单独改变下列条件,下列判断正确的是_____。| A.升高温度,混合气体的颜色变浅 |
| B.通入NO2,化学平衡常数增大 |
| C.通入NO2,重新达到平衡后混合气体的平均相对分子质量增大 |
| D.增大压强,平衡向正反应方向移动,混合气体的颜色变浅 |
Ⅰ.CH4(g)+H2O(g)
 CO(g)+3H2(g) Ⅱ.CO(g)+H2O(g)
CO(g)+3H2(g) Ⅱ.CO(g)+H2O(g)  CO2(g)+H2(g)
CO2(g)+H2(g)①下列操作中,能提高CH4(g)平衡转化率的是
A.增加CH4 (g)用量 B.恒温恒压下通入惰性气体
C.移除CO(g) D.加入催化剂
②恒温恒压条件下,1 mol CH4 (g)和1 mol H2O(g)反应达平衡时,CH4 (g)的转化率为α,CO2(g)的物质的量为b mol,则反应Ⅰ的平衡常数Kx=
 pC(g)+qD(g),Kx=
pC(g)+qD(g),Kx=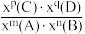 ,x为物质的量分数]。
,x为物质的量分数]。
您最近一年使用:0次
解题方法
2 . 回答下列问题。
(1)一定条件下,在 密闭容器中充入
密闭容器中充入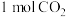 和
和 ,发生反应:
,发生反应: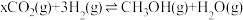 。测得
。测得 和
和 的物质的量随时间变化如图所示。
的物质的量随时间变化如图所示。
___________ ; 内
内 的平均反应速率
的平均反应速率
___________ 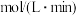 ,平衡时
,平衡时 的转化率为
的转化率为___________ 。
(2)下列措施能提高正反应速率的是___________(填正确答案的字母)。
(3)工业上常以水煤气( 和
和 )为原料合成甲醇。已知:
)为原料合成甲醇。已知: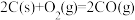
 ;
;
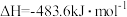 ,则
,则 与
与 制备水煤气的热化学方程式为
制备水煤气的热化学方程式为___________ 。
(1)一定条件下,在
 密闭容器中充入
密闭容器中充入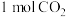 和
和 ,发生反应:
,发生反应: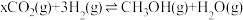 。测得
。测得 和
和 的物质的量随时间变化如图所示。
的物质的量随时间变化如图所示。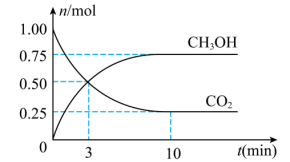

 内
内 的平均反应速率
的平均反应速率
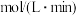 ,平衡时
,平衡时 的转化率为
的转化率为(2)下列措施能提高正反应速率的是___________(填正确答案的字母)。
| A.降低温度 | B.增加 的量 的量 | C.使用催化剂 | D.及时分离出甲醇 |
 和
和 )为原料合成甲醇。已知:
)为原料合成甲醇。已知: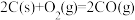
 ;
;
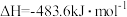 ,则
,则 与
与 制备水煤气的热化学方程式为
制备水煤气的热化学方程式为
您最近一年使用:0次
3 . 已知:A(g)+3B(g) 2C(g) ΔH<0,有甲乙两个容积为0.5L的密闭容器,向甲中加入1molA和3molB,5min时达到平衡,放出热量为Q1kJ;相同条件下,向乙中加入2molC,达到平衡时吸收热量为Q2kJ。已知Q2=3Q1,下列说法正确的是
2C(g) ΔH<0,有甲乙两个容积为0.5L的密闭容器,向甲中加入1molA和3molB,5min时达到平衡,放出热量为Q1kJ;相同条件下,向乙中加入2molC,达到平衡时吸收热量为Q2kJ。已知Q2=3Q1,下列说法正确的是
 2C(g) ΔH<0,有甲乙两个容积为0.5L的密闭容器,向甲中加入1molA和3molB,5min时达到平衡,放出热量为Q1kJ;相同条件下,向乙中加入2molC,达到平衡时吸收热量为Q2kJ。已知Q2=3Q1,下列说法正确的是
2C(g) ΔH<0,有甲乙两个容积为0.5L的密闭容器,向甲中加入1molA和3molB,5min时达到平衡,放出热量为Q1kJ;相同条件下,向乙中加入2molC,达到平衡时吸收热量为Q2kJ。已知Q2=3Q1,下列说法正确的是| A.甲中达平衡时,用B的浓度变化表示5min内的平均反应速率为0.15 mol・L-1・min-1 |
B.乙中的热化学方程式为2C(g) A(g)+3B(g):ΔH= A(g)+3B(g):ΔH=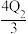 kJ/mol kJ/mol |
| C.乙中达到平衡后,再加入0.25molA、0.75molB、1.5molC,平衡不移动 |
| D.乙中平衡时C的转化率为75% |
您最近一年使用:0次
名校
解题方法
4 . 神舟十五号顺利发射升空,标志着我国航天事业的飞速发展。
Ⅰ.火箭推进剂的研究是航天工业中的重要课题,常见推进剂的燃料包括汽油液肼(N2H4)、液氢等,具有不同的推进效能。回答下列问题:
(1)火箭推进剂可用N2H4作燃料,N2O4作氧化剂,反应的热化学方程式可表示为2N2H4(l)+N2O4(g)=3N2(g)+4H2O(g) ∆H1。
相关物质的摩尔生成焓∆HfHm如下表所示。
注:一定温度下,由元素的最稳定单质生成1mol纯物质的热效应称为该物质的摩尔生成焓,用∆HfHm表示。如N2H4(1)的摩尔生成焓:N2(g)+2H2(g)=N2H4(l) ∆HfHm =+165.8kJ/mol
①∆H1=___________ kJ/mol。
②结合化学反应原理分析,N2H4(l)作推近剂燃料可与N2O4(g)自发进行反应的原因是___________ 。
(2)火箭推进器内氢氧燃烧的简化反应历程如下图所示,分析其反应机理。
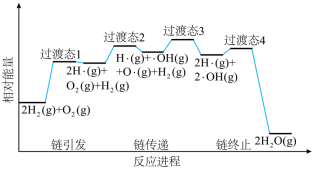
该历程分步进行,其中氢氧燃烧决速步对应的反应方程式为___________ 。
Ⅱ.在温度T下,容积固定的密闭容器中充入3 mol NO和2 mol H2发生2H2(g)+2NO(g) N2(g)+2H2O(g),起始压强为p0,一段时间后,反应达到平衡,此时压强p=0.9p0,
N2(g)+2H2O(g),起始压强为p0,一段时间后,反应达到平衡,此时压强p=0.9p0,
(3)则NO的平衡转化率α(NO)=___________ (结果保留三位有效数字),该反应的平衡常数Kp=___________ (用含P0的代数式表示)
Ⅰ.火箭推进剂的研究是航天工业中的重要课题,常见推进剂的燃料包括汽油液肼(N2H4)、液氢等,具有不同的推进效能。回答下列问题:
(1)火箭推进剂可用N2H4作燃料,N2O4作氧化剂,反应的热化学方程式可表示为2N2H4(l)+N2O4(g)=3N2(g)+4H2O(g) ∆H1。
相关物质的摩尔生成焓∆HfHm如下表所示。
| 物质 | N2O4(g) | N2H4(l) | H2O(g) |
| 摩尔生成焓∆HfHm(kJ/mol) | +10.8 | +165.8. | -242.0 |
①∆H1=
②结合化学反应原理分析,N2H4(l)作推近剂燃料可与N2O4(g)自发进行反应的原因是
(2)火箭推进器内氢氧燃烧的简化反应历程如下图所示,分析其反应机理。

该历程分步进行,其中氢氧燃烧决速步对应的反应方程式为
Ⅱ.在温度T下,容积固定的密闭容器中充入3 mol NO和2 mol H2发生2H2(g)+2NO(g)
 N2(g)+2H2O(g),起始压强为p0,一段时间后,反应达到平衡,此时压强p=0.9p0,
N2(g)+2H2O(g),起始压强为p0,一段时间后,反应达到平衡,此时压强p=0.9p0,(3)则NO的平衡转化率α(NO)=
您最近一年使用:0次
名校
解题方法
5 . 回答下列问题
I.肼( )可用做发射卫星的火箭燃料。已知:
)可用做发射卫星的火箭燃料。已知:
①
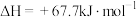
②
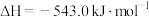
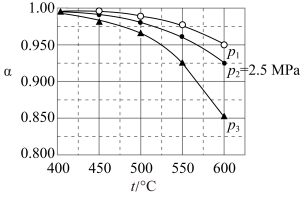
(1)写出气态肼和 生成氮气和水蒸气的热化学方程式
生成氮气和水蒸气的热化学方程式_______ 。
Ⅱ.硫酸是一种重要的基础化工产品,接触法制硫酸生产中的关键工序是SO2的催化氧化: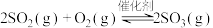
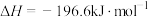 。回答下列问题。
。回答下列问题。
(2)某温度下,在体积为2L的刚性密闭容器中投入2molSO2和3.5molO2,下图是n(SO2)和n(SO3)随时间的变化曲线。

①0~10min,v(SO3)=_______ 。
②反应达到平衡时,平衡常数K=_______  。(保留3位
。(保留3位
有效数字)
③下列情况不能说明反应达到化学平衡状态的是_______ 。
A.v(SO3)=2v(O2)
B.混合气体的相对分子质量不再变化
C.体系的压强不再发生改变
D.混合气体的密度保持不变
(3)当SO2(g)、O2(g)和N2(g)起始的物质的量分数分别为7.5%、10.5%和82%时,在0.5MPa、2.5MPa和5.0MPa压强下,SO2平衡转化率α随温度的变化如下图所示。反应在5.0MPa、550℃时的α=_______ ,影响α的因素有温度、压强和_______ 。
I.肼(
 )可用做发射卫星的火箭燃料。已知:
)可用做发射卫星的火箭燃料。已知:①

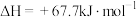
②

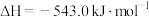
(1)写出气态肼和
 生成氮气和水蒸气的热化学方程式
生成氮气和水蒸气的热化学方程式Ⅱ.硫酸是一种重要的基础化工产品,接触法制硫酸生产中的关键工序是SO2的催化氧化:
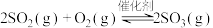
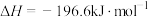 。回答下列问题。
。回答下列问题。(2)某温度下,在体积为2L的刚性密闭容器中投入2molSO2和3.5molO2,下图是n(SO2)和n(SO3)随时间的变化曲线。

①0~10min,v(SO3)=
②反应达到平衡时,平衡常数K=
 。(保留3位
。(保留3位有效数字)
③下列情况不能说明反应达到化学平衡状态的是
A.v(SO3)=2v(O2)
B.混合气体的相对分子质量不再变化
C.体系的压强不再发生改变
D.混合气体的密度保持不变
(3)当SO2(g)、O2(g)和N2(g)起始的物质的量分数分别为7.5%、10.5%和82%时,在0.5MPa、2.5MPa和5.0MPa压强下,SO2平衡转化率α随温度的变化如下图所示。反应在5.0MPa、550℃时的α=

您最近一年使用:0次
名校
6 . 将等物质的量的A、B混合于2L的密闭容器中,发生反应: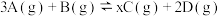 ,经2min后测得D的浓度为0.5mol/L,
,经2min后测得D的浓度为0.5mol/L, ,以C表示的平均反应速率
,以C表示的平均反应速率 ,下列说法错误的是
,下列说法错误的是
| A.反应速率为v(B)=0.125mol·L-1·min-1 | B.该化学方程式中,x=2 |
C. 时, 时, 的物质的量为 的物质的量为 | D. 时, 时, 的转化率为 的转化率为 |
您最近一年使用:0次
2024-01-20更新
|
1071次组卷
|
5卷引用:宁夏石嘴山市第三中学2022-2023学年高一下学期期末考试化学试题
名校
解题方法
7 . H2S与CO2在高温下发生反应:H2S(g)+CO2(g) COS(g)+H2O(g)。在610 K时,将0.10 mol CO2与0.40 mol H2S充入2.5 L 的空钢瓶中,反应平衡后水的物质的量分数为0.02。
COS(g)+H2O(g)。在610 K时,将0.10 mol CO2与0.40 mol H2S充入2.5 L 的空钢瓶中,反应平衡后水的物质的量分数为0.02。
(1)H2S的平衡转化率a1=___________ %,反应平衡常数K=___________ 。
(2)在620 K重复实验,平衡后水的物质的量分数为0.03,H2S的转化率a2___________ (填“>”“<”或“=”,下同)a1,该反应的ΔH___________ 0。
(3)向反应器中再分别充入下列气体,能使H2S转化率增大的是___________(填字母)。
 COS(g)+H2O(g)。在610 K时,将0.10 mol CO2与0.40 mol H2S充入2.5 L 的空钢瓶中,反应平衡后水的物质的量分数为0.02。
COS(g)+H2O(g)。在610 K时,将0.10 mol CO2与0.40 mol H2S充入2.5 L 的空钢瓶中,反应平衡后水的物质的量分数为0.02。(1)H2S的平衡转化率a1=
(2)在620 K重复实验,平衡后水的物质的量分数为0.03,H2S的转化率a2
(3)向反应器中再分别充入下列气体,能使H2S转化率增大的是___________(填字母)。
| A.H2S | B.CO2 |
| C.COS | D.N2 |
您最近一年使用:0次
2023-08-27更新
|
652次组卷
|
22卷引用:宁夏青铜峡市高级中学2021-2022学年高二下学期开学考试化学试题
宁夏青铜峡市高级中学2021-2022学年高二下学期开学考试化学试题2018-2019学年鲁科版高中化学选修四:第2章检测题山东省德州市夏津一中2018-2019学年高二上学期第一次月考化学试题(已下线)2019年9月18日《每日一题》选修4—— 平衡转化率的判断山东省济南外国语学校三箭分校2019-2020学年高二上学期期中考试化学试题(已下线)专题7.3 化学平衡常数 化学反应进行的方向(练)-《2020年高考一轮复习讲练测》(已下线)专题7.3 化学平衡常数 化学反应进行的方向(讲)-《2020年高考一轮复习讲练测》(已下线)专题十一 化学反应速率和化学平衡(真题汇编)-2020年高考二轮模块化复习之《化学基本原理》名师讲案与提分特训鲁科版(2019)选择性必修1 第2章 化学反应的方向、限度与速率 第2节 化学反应的限度(已下线)易错13 化学反应速率和化学平衡计算-备战2021年高考化学一轮复习易错题鲁科版(2019)高二选择性必修第一册第2章 化学反应的方向、限度与速率 高考挑战区 过高考山东省临沂市费县第二中学2020-2021学年高二上学期11月月考化学试题(已下线)第20讲 化学平衡常数及转化率的计算(讲) — 2022年高考化学一轮复习讲练测(新教材新高考)江西省遂川中学2021-2022学年高二上学期第二次月考化学(A卷)试题(已下线)2.2.1 化学平衡常数-【帮课堂】2022-2023学年高二化学同步精品讲义(沪科版2020选择性必修第一册)湖南省长沙市雅礼中学2022-2023学年高二上学期入学考试化学试题(已下线)第20讲 化学平衡常数及转化率的计算(讲)-2023年高考化学一轮复习讲练测(新教材新高考)(已下线)题型123 平衡转化率的计算章末检测卷(二)化学反应的方向、限度与速率(已下线)上海市华东师范大学第二附属中2023-2024学年高三上学期9月考试化学试题吉林省长春市东北师范大学附属中学2023-2024学年高二上学期第一次月考化学试题湖南省衡阳县第四中学2023-2024年高二上学期期中考试化学B卷
名校
8 .  是主要的温室气体。利用
是主要的温室气体。利用 制甲烷(
制甲烷( )、甲醇(
)、甲醇( )、CO等燃料,可实现能源再生和
)、CO等燃料,可实现能源再生和 的资源化利用。
的资源化利用。
Ⅰ.利用太阳能分解水获得氢气,再通过 加氢制甲醇,反应如下:
加氢制甲醇,反应如下:
①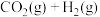


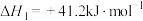
②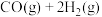


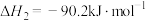
(1)反应①的平衡常数表达式
_______ ;
(2) 催化加氢制取
催化加氢制取 和
和 的热化学方程式是
的热化学方程式是_______ 。
Ⅱ.利用 与氢气反应制取甲烷。对于反应
与氢气反应制取甲烷。对于反应 ,不同温度下经过相同反应时间
,不同温度下经过相同反应时间 转化率的变化曲线如图所示。
转化率的变化曲线如图所示。

(3)请描述曲线( 转化率随着温度)变化趋势:
转化率随着温度)变化趋势:_______ ,该反应是_______ 反应(填“吸热”或“放热”)。
Ⅲ.甲烷的温室效应约为 的25倍,利用
的25倍,利用 重整技术能将二者同时转化为合成气CO和
重整技术能将二者同时转化为合成气CO和 而广受关注。该重整技术涉及的主要反应为:
而广受关注。该重整技术涉及的主要反应为:
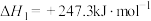 。
。
(4)为提高 的平衡转化率,可采取的措施为
的平衡转化率,可采取的措施为_______ (写出一条即可)。
(5)某温度下,向恒容容器中通入等物质的量的 和
和 ,初始总压强为p,反应达到平衡后,总压强变为1.6p,则该条件下的平衡常数
,初始总压强为p,反应达到平衡后,总压强变为1.6p,则该条件下的平衡常数
_______ (以分压表示,分压=总压×物质的量分数)。
 是主要的温室气体。利用
是主要的温室气体。利用 制甲烷(
制甲烷( )、甲醇(
)、甲醇( )、CO等燃料,可实现能源再生和
)、CO等燃料,可实现能源再生和 的资源化利用。
的资源化利用。Ⅰ.利用太阳能分解水获得氢气,再通过
 加氢制甲醇,反应如下:
加氢制甲醇,反应如下:①
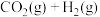


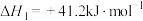
②
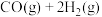


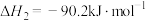
(1)反应①的平衡常数表达式

(2)
 催化加氢制取
催化加氢制取 和
和 的热化学方程式是
的热化学方程式是Ⅱ.利用
 与氢气反应制取甲烷。对于反应
与氢气反应制取甲烷。对于反应 ,不同温度下经过相同反应时间
,不同温度下经过相同反应时间 转化率的变化曲线如图所示。
转化率的变化曲线如图所示。
(3)请描述曲线(
 转化率随着温度)变化趋势:
转化率随着温度)变化趋势:Ⅲ.甲烷的温室效应约为
 的25倍,利用
的25倍,利用 重整技术能将二者同时转化为合成气CO和
重整技术能将二者同时转化为合成气CO和 而广受关注。该重整技术涉及的主要反应为:
而广受关注。该重整技术涉及的主要反应为:
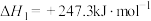 。
。(4)为提高
 的平衡转化率,可采取的措施为
的平衡转化率,可采取的措施为(5)某温度下,向恒容容器中通入等物质的量的
 和
和 ,初始总压强为p,反应达到平衡后,总压强变为1.6p,则该条件下的平衡常数
,初始总压强为p,反应达到平衡后,总压强变为1.6p,则该条件下的平衡常数
您最近一年使用:0次
2023-07-16更新
|
129次组卷
|
2卷引用:宁夏银川二中2023-2024学年高二上学期月考二化学试题
9 . 纳米碗 是一种奇特的碗状共轭体系。高温条件下,
是一种奇特的碗状共轭体系。高温条件下, 可以由
可以由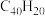 分子经过连续5步氢抽提和闭环脱氢反应生成。
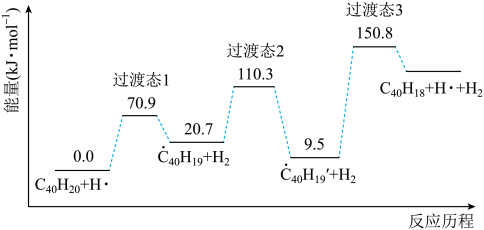
分子经过连续5步氢抽提和闭环脱氢反应生成。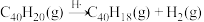 的反应机理和能量变化如下:
的反应机理和能量变化如下:
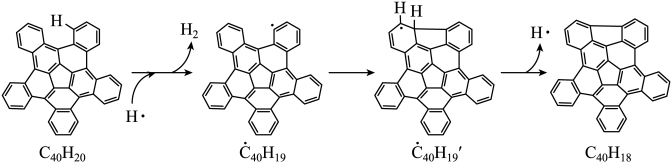
(1)已知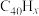 中的碳氢键和碳碳键的键能分别为
中的碳氢键和碳碳键的键能分别为 和
和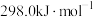 ,H-H键能为
,H-H键能为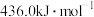 。估算
。估算 的
的
_______  。
。
(2)图示历程包含_______ 个基元反应,其中速率最慢的是第_______ 个。
(3) 纳米碗中五元环和六元环结构的数目分别为
纳米碗中五元环和六元环结构的数目分别为_______ 、_______ 。
(4)1200K时,假定体系内只有反应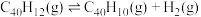 发生,反应过程中压强恒定为
发生,反应过程中压强恒定为 (即
(即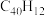 的初始压强),平衡转化率为α,该反应的平衡常数
的初始压强),平衡转化率为α,该反应的平衡常数 为
为_______ (用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
(5)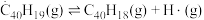 及
及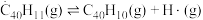 反应的
反应的 (
( 为平衡常数)随温度倒数的关系如图所示。已知本实验条件下,
为平衡常数)随温度倒数的关系如图所示。已知本实验条件下,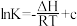 (R为理想气体常数,c为截距)。图中两条线几乎平行,从结构的角度分析其原因是
(R为理想气体常数,c为截距)。图中两条线几乎平行,从结构的角度分析其原因是_______ 。 的反应速率的是
的反应速率的是_______ (填标号)。
a.升高温度 b.增大压强 c.加入催化剂
 是一种奇特的碗状共轭体系。高温条件下,
是一种奇特的碗状共轭体系。高温条件下, 可以由
可以由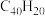 分子经过连续5步氢抽提和闭环脱氢反应生成。
分子经过连续5步氢抽提和闭环脱氢反应生成。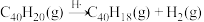 的反应机理和能量变化如下:
的反应机理和能量变化如下: 
(1)已知
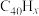 中的碳氢键和碳碳键的键能分别为
中的碳氢键和碳碳键的键能分别为 和
和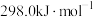 ,H-H键能为
,H-H键能为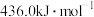 。估算
。估算 的
的
 。
。(2)图示历程包含
(3)
 纳米碗中五元环和六元环结构的数目分别为
纳米碗中五元环和六元环结构的数目分别为(4)1200K时,假定体系内只有反应
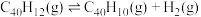 发生,反应过程中压强恒定为
发生,反应过程中压强恒定为 (即
(即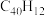 的初始压强),平衡转化率为α,该反应的平衡常数
的初始压强),平衡转化率为α,该反应的平衡常数 为
为(5)
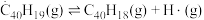 及
及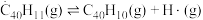 反应的
反应的 (
( 为平衡常数)随温度倒数的关系如图所示。已知本实验条件下,
为平衡常数)随温度倒数的关系如图所示。已知本实验条件下,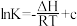 (R为理想气体常数,c为截距)。图中两条线几乎平行,从结构的角度分析其原因是
(R为理想气体常数,c为截距)。图中两条线几乎平行,从结构的角度分析其原因是
 的反应速率的是
的反应速率的是a.升高温度 b.增大压强 c.加入催化剂
您最近一年使用:0次
2023-06-14更新
|
9096次组卷
|
10卷引用:宁夏回族自治区银川一中2024届高三下学期考前热身训练化学试卷2
宁夏回族自治区银川一中2024届高三下学期考前热身训练化学试卷22023年高考湖北卷化学真题(已下线)专题17 原理综合题(已下线)T19-原理综合题(已下线)专题17 原理综合题(已下线)专题17 原理综合题(已下线)专题14 化学反应原理综合题-2023年高考化学真题题源解密(新高考专用)(已下线)专题15 化学反应原理综合题-2023年高考化学真题题源解密(全国通用)河南省开封市祥符高级中学2023-2024学年高二上学期第一次月考化学试题湖北省恩施高中2023-2024学年高一下学期入学考试化学试题
名校
10 . 甲醇脱氢法制HCOOCH3工艺过程涉及如下反应:
反应Ⅰ:2CH3OH(g) HCOOCH3(g)+2H2(g) ΔH1=+135.4 kJ·mol-1
HCOOCH3(g)+2H2(g) ΔH1=+135.4 kJ·mol-1
反应Ⅱ:CH3OH(g) CO(g)+2H2(g) ΔH2=+106.0 kJ·mol-1
CO(g)+2H2(g) ΔH2=+106.0 kJ·mol-1
向容积为10 L的恒容密闭容器中通入1 mol CH3OH(g)发生上述反应,反应相同时间,测得CH3OH的转化率和HCOOCH3的选择性随温度变化如图所示。(已知:HCOOCH3的选择性= )
)
下列说法错误 的是

反应Ⅰ:2CH3OH(g)
 HCOOCH3(g)+2H2(g) ΔH1=+135.4 kJ·mol-1
HCOOCH3(g)+2H2(g) ΔH1=+135.4 kJ·mol-1 反应Ⅱ:CH3OH(g)
 CO(g)+2H2(g) ΔH2=+106.0 kJ·mol-1
CO(g)+2H2(g) ΔH2=+106.0 kJ·mol-1 向容积为10 L的恒容密闭容器中通入1 mol CH3OH(g)发生上述反应,反应相同时间,测得CH3OH的转化率和HCOOCH3的选择性随温度变化如图所示。(已知:HCOOCH3的选择性=
 )
)下列说法

A.HCOOCH3(g)  2CO(g)+2H2(g) ΔH=+76.6 kJ·mol-1 2CO(g)+2H2(g) ΔH=+76.6 kJ·mol-1 |
| B.实线代表的是CH3OH的转化率 |
| C.553 K时,H2的体积分数为0.25 |
| D.高于553 K时,虚线趋势下降可能是因为HCOOCH3分解 |
您最近一年使用:0次
2023-05-06更新
|
239次组卷
|
4卷引用:宁夏石嘴山市第三中学2022-2023学年高二下学期期末理科化学试题



