名校
解题方法
1 . 过氧乙酸(CH3CO3H)是一种广谱高效消毒剂,不稳定、易分解,高浓度易爆炸。常用于空气器材的消毒,可由乙酸与 在硫酸催化下反应制得,热化学方程式为:
在硫酸催化下反应制得,热化学方程式为: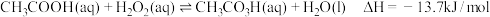
(1)市售过氧乙酸的浓度一般不超过21%,原因是___________ 。
(2)以下措施中能提高乙酸平衡转化率的措施有___________。
(3)取质量相等的冰醋酸和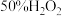 溶液混合均匀,在一定量硫酸催化下进行如下实验。
溶液混合均匀,在一定量硫酸催化下进行如下实验。
实验1:在 下,测定不同时间所得溶液中过氧乙酸的质量分数。数据如图1所示。
下,测定不同时间所得溶液中过氧乙酸的质量分数。数据如图1所示。
实验2:在不同温度下反应,测定24小时所得溶液中过氧乙酸的质量分数。数据如图2所示。
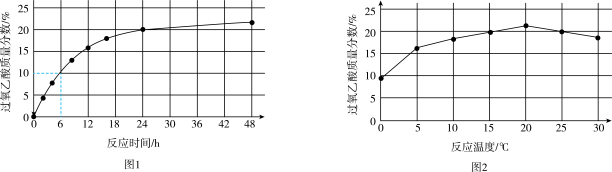
①实验1中,若反应混合液的总质量为 ,依据图1数据计算,在
,依据图1数据计算,在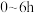 间,
间,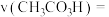
___________ 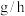 。(用含m的代数式表示)
。(用含m的代数式表示)
②综合图1、图2分析,与 相比,
相比, 时过氧乙酸产率降低的可能原因是
时过氧乙酸产率降低的可能原因是___________ (写出2条)。
(4)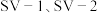 是两种常用于实验研究的病毒,病毒在水中可能会聚集成团簇。不同
是两种常用于实验研究的病毒,病毒在水中可能会聚集成团簇。不同 下,病毒团簇粒径及过氧乙酸对两种病毒的相对杀灭速率分别如图3、图4所示。
下,病毒团簇粒径及过氧乙酸对两种病毒的相对杀灭速率分别如图3、图4所示。
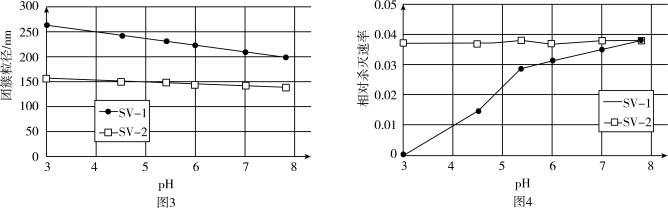
依据图3、图4分析,过氧乙酸对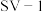 的杀灭速率随
的杀灭速率随 增大而增大的原因可能是
增大而增大的原因可能是___________ 。
 在硫酸催化下反应制得,热化学方程式为:
在硫酸催化下反应制得,热化学方程式为: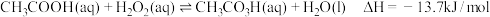
(1)市售过氧乙酸的浓度一般不超过21%,原因是
(2)以下措施中能提高乙酸平衡转化率的措施有___________。
| A.降低温度 | B.增加 用量(溶液体积不变) 用量(溶液体积不变) |
| C.加水稀释溶液 | D.增加乙酸的用量(溶液体积不变) |
(3)取质量相等的冰醋酸和
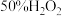 溶液混合均匀,在一定量硫酸催化下进行如下实验。
溶液混合均匀,在一定量硫酸催化下进行如下实验。实验1:在
 下,测定不同时间所得溶液中过氧乙酸的质量分数。数据如图1所示。
下,测定不同时间所得溶液中过氧乙酸的质量分数。数据如图1所示。实验2:在不同温度下反应,测定24小时所得溶液中过氧乙酸的质量分数。数据如图2所示。

①实验1中,若反应混合液的总质量为
 ,依据图1数据计算,在
,依据图1数据计算,在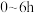 间,
间,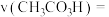
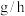 。(用含m的代数式表示)
。(用含m的代数式表示)②综合图1、图2分析,与
 相比,
相比, 时过氧乙酸产率降低的可能原因是
时过氧乙酸产率降低的可能原因是(4)
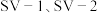 是两种常用于实验研究的病毒,病毒在水中可能会聚集成团簇。不同
是两种常用于实验研究的病毒,病毒在水中可能会聚集成团簇。不同 下,病毒团簇粒径及过氧乙酸对两种病毒的相对杀灭速率分别如图3、图4所示。
下,病毒团簇粒径及过氧乙酸对两种病毒的相对杀灭速率分别如图3、图4所示。
依据图3、图4分析,过氧乙酸对
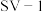 的杀灭速率随
的杀灭速率随 增大而增大的原因可能是
增大而增大的原因可能是
您最近一年使用:0次
名校
2 . 现有反应aA(g)+bB(g) pC(g),达到平衡后,当升高温度时,B的浓度减小;当减小压强时,混合体系中C的质量分数也减小,则:
pC(g),达到平衡后,当升高温度时,B的浓度减小;当减小压强时,混合体系中C的质量分数也减小,则:
(1)该反应是___________ 热反应,且a+b___________ p(填“>”“<”或“=”)。
(2)减压时,A的质量分数___________ (填“增大”“减小”或“不变”,下同),正反应速率___________ 。
(3)若降低温度,则平衡时,B、C的浓度之比c(B)/c(C) 将___________ 。
(4)若加入催化剂,平衡时气体混合物的总物质的量___________ 。
(5)若B是有色物质,A、C均为无色物质,则加入C(体积不变)时混合物的颜色___________ ,而维持容器内气体的压强不变,充入氖气时,混合物的颜色___________ 。(填“变浅”“变深”或“不变”)
 pC(g),达到平衡后,当升高温度时,B的浓度减小;当减小压强时,混合体系中C的质量分数也减小,则:
pC(g),达到平衡后,当升高温度时,B的浓度减小;当减小压强时,混合体系中C的质量分数也减小,则:(1)该反应是
(2)减压时,A的质量分数
(3)若降低温度,则平衡时,B、C的浓度之比c(B)/c(C) 将
(4)若加入催化剂,平衡时气体混合物的总物质的量
(5)若B是有色物质,A、C均为无色物质,则加入C(体积不变)时混合物的颜色
您最近一年使用:0次
名校
解题方法
3 . 在一定温度下,将 和2moB两种气体相混合于容积为
和2moB两种气体相混合于容积为 的某密闭容器中,发生如下反应:
的某密闭容器中,发生如下反应: ,
, 末反应达到平衡状态,此时测得D的浓度为
末反应达到平衡状态,此时测得D的浓度为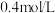 ,用C表示的反应速率为
,用C表示的反应速率为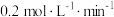 请填写下列空白:
请填写下列空白:
(1)x值等于___________ 。
(2)A的转化率为___________ 。
(3)如果增大反应体系的压强,则平衡体系中C的质量分数___________ (增大、减小或不变)。
(4)在此温度下,该化学反应的平衡常数K=___________ 。
(5)在此条件下,向该容器内加入 、
、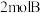 、
、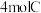 、
、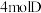 后,
后,
___________ (填“>”“<”或“=”) 。
。
(6)在此条件下, 末再向容器内加入
末再向容器内加入 、
、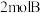 ,则平衡移动的方向
,则平衡移动的方向___________ ,再次达到平衡后A的转化率___________ (增大、减小或不变),C的物质的量分数___________ (增大、减小或不变)。
 和2moB两种气体相混合于容积为
和2moB两种气体相混合于容积为 的某密闭容器中,发生如下反应:
的某密闭容器中,发生如下反应: ,
, 末反应达到平衡状态,此时测得D的浓度为
末反应达到平衡状态,此时测得D的浓度为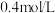 ,用C表示的反应速率为
,用C表示的反应速率为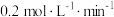 请填写下列空白:
请填写下列空白:(1)x值等于
(2)A的转化率为
(3)如果增大反应体系的压强,则平衡体系中C的质量分数
(4)在此温度下,该化学反应的平衡常数K=
(5)在此条件下,向该容器内加入
 、
、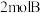 、
、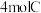 、
、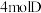 后,
后,
 。
。(6)在此条件下,
 末再向容器内加入
末再向容器内加入 、
、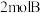 ,则平衡移动的方向
,则平衡移动的方向
您最近一年使用:0次
名校
4 . 现有反应:mA(g)+nB(g)  pC(g),达到平衡后,当升高温度时,B的转化率变大;当减小压强时,混合体系中C的质量分数也减小,则:
pC(g),达到平衡后,当升高温度时,B的转化率变大;当减小压强时,混合体系中C的质量分数也减小,则:
(1)该反应的逆反应为_______ 热反应,且m+n ______ p (填“>”、“<”或“=”)。
(2)减压时,A 的质量分数_______ (填“增大”、“减小”或“不变”,下同)。
(3)若加入 B(体积不变),则A的转化率__________ 。
(4)若升高温度,则平衡时B、C的浓度之比[B]/[C]将_______ 。
(5)若加入催化剂,平衡时气体混合物的总物质的量_______ 。
 pC(g),达到平衡后,当升高温度时,B的转化率变大;当减小压强时,混合体系中C的质量分数也减小,则:
pC(g),达到平衡后,当升高温度时,B的转化率变大;当减小压强时,混合体系中C的质量分数也减小,则:(1)该反应的逆反应为
(2)减压时,A 的质量分数
(3)若加入 B(体积不变),则A的转化率
(4)若升高温度,则平衡时B、C的浓度之比[B]/[C]将
(5)若加入催化剂,平衡时气体混合物的总物质的量
您最近一年使用:0次
2023-02-07更新
|
247次组卷
|
7卷引用:2016-2017学年河南省新乡市延津县中学高二上第一次月考化学卷
名校
解题方法
5 . 定条件下,发生反应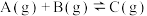
 ,达到平衡后根据下列图像判断:
,达到平衡后根据下列图像判断:
A.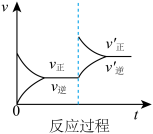 B.
B.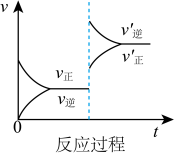 C.
C.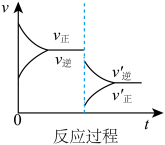 D.
D.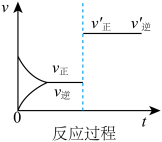 E.
E.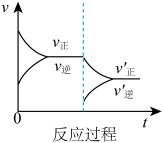
(1)表示升高温度,达到新平衡的是_______ (填“A”、“B”、“C”、“D”或“E”,下同),新平衡中C的质量分数_______ (填“增大”、“减小”或“不变”,下同)。
(2)表示降低压强,达到新平衡的是_______ ,A的转化率_______ 。
(3)表示减少C的浓度,达到新平衡的是_______ 。
(4)增加A的浓度,达到平衡后A的转化率_______ 。
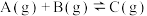
 ,达到平衡后根据下列图像判断:
,达到平衡后根据下列图像判断:A.
 B.
B. C.
C. D.
D. E.
E.
(1)表示升高温度,达到新平衡的是
(2)表示降低压强,达到新平衡的是
(3)表示减少C的浓度,达到新平衡的是
(4)增加A的浓度,达到平衡后A的转化率
您最近一年使用:0次
6 . 现有反应:mA(g)+nB(g)⇌pC(g),达到平衡后,当升高温度时,B的转化率变大;当减小压强时,混合体系中C的质量分数也减小,则:
(1)该反应的正反应为_______ 反应(填“吸热”或“放热”),且m+n_______ p(填“>”“=”“<”)。
(2)使容器体积减小压强增大时,A的质量分数_______ 。(填“增大”“减小”或“不变”,下同)
(3)若升高温度,则平衡时B、C的浓度之比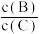 将
将_______ 。
(4)维持容器内压强不变,充入氖气后平衡将向_______ (填“正向移动”“逆向移动”或“不移动”)
(1)该反应的正反应为
(2)使容器体积减小压强增大时,A的质量分数
(3)若升高温度,则平衡时B、C的浓度之比
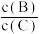 将
将(4)维持容器内压强不变,充入氖气后平衡将向
您最近一年使用:0次
名校
7 . 我国提出“ 排放力争于2030年前达到峰值,努力争取2060年前实现碳中和”。研发
排放力争于2030年前达到峰值,努力争取2060年前实现碳中和”。研发 的利用技术,降低空气中
的利用技术,降低空气中 的含量是实现该目标的重要途径。
的含量是实现该目标的重要途径。
(1)下面是用 捕捉
捕捉 时发生的两个反应:
时发生的两个反应:
I.

II.

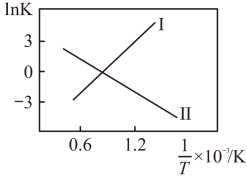
①反应I、II的 随
随 的变化如图所示,则
的变化如图所示,则
___________ 0(填“>”“<”或“=”)0;有利于该反应自发进行的温度是___________ (填“高温”或“低温”)。
②将一定量的 和
和 的混合气体充入密闭容器中,
的混合气体充入密闭容器中, 、
、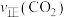 与温度的关系如下图所示,400℃之后
与温度的关系如下图所示,400℃之后 降低的原因是
降低的原因是___________ ,而速率仍然增大的可能原因是___________ 。

③220℃时,将4mol 与1mol
与1mol 的混合气体充入2L反应器中,气体初始总压强为p,10分钟后体系达到平衡,
的混合气体充入2L反应器中,气体初始总压强为p,10分钟后体系达到平衡, 的转化率为80%,
的转化率为80%, 的选择性为33.3%,则生成的
的选择性为33.3%,则生成的 平均速率为
平均速率为___________ (保留两位有效数字),反应II的平衡常数 为
为___________ [已知: 的选择性
的选择性 ]
]
(2)利用化学链将高炉废气中的 转化为CO的示意图如下。
转化为CO的示意图如下。
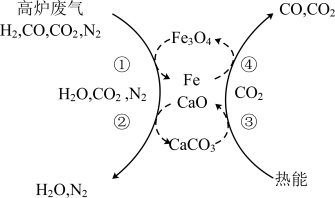
此过程中可循环利用的物质有___________ ,该化学链的总反应是___________ 。
 排放力争于2030年前达到峰值,努力争取2060年前实现碳中和”。研发
排放力争于2030年前达到峰值,努力争取2060年前实现碳中和”。研发 的利用技术,降低空气中
的利用技术,降低空气中 的含量是实现该目标的重要途径。
的含量是实现该目标的重要途径。(1)下面是用
 捕捉
捕捉 时发生的两个反应:
时发生的两个反应:I.


II.


①反应I、II的
 随
随 的变化如图所示,则
的变化如图所示,则

②将一定量的
 和
和 的混合气体充入密闭容器中,
的混合气体充入密闭容器中, 、
、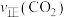 与温度的关系如下图所示,400℃之后
与温度的关系如下图所示,400℃之后 降低的原因是
降低的原因是
③220℃时,将4mol
 与1mol
与1mol 的混合气体充入2L反应器中,气体初始总压强为p,10分钟后体系达到平衡,
的混合气体充入2L反应器中,气体初始总压强为p,10分钟后体系达到平衡, 的转化率为80%,
的转化率为80%, 的选择性为33.3%,则生成的
的选择性为33.3%,则生成的 平均速率为
平均速率为 为
为 的选择性
的选择性 ]
](2)利用化学链将高炉废气中的
 转化为CO的示意图如下。
转化为CO的示意图如下。
此过程中可循环利用的物质有
您最近一年使用:0次
2023-04-09更新
|
568次组卷
|
2卷引用:湖南省长沙市雅礼中学2022-2023学年高三下学期4月份第八次月考化学试题
8 . 现有反应aA(g)+bB(g) pC(g),达到平衡后,当降低温度时,B的转化率变大;当减小压强时,混合体系中C的质量分数减小,则:
pC(g),达到平衡后,当降低温度时,B的转化率变大;当减小压强时,混合体系中C的质量分数减小,则:
(1)该反应的正反应是_______ 热反应,且a+b _______ p (填”>““<“或”=“)。
(2)减压时,A的质量分数_______ (填”增大”“减小”或”不变”,下同),正反应速率_______ 。
(3)若加入B(体积不变),则A的转化率_______ ,B的转化率_______ 。
(4)若升高温度,则平衡时,B、C的浓度之比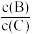 将
将_______ 。
(5)若加入催化剂,平衡时气体压强_______ 。
(6)若B是有色物质,A、C均为无色物质,则加入C(体积不变)时混合物的颜色_______ ,而维持容器体积不变,充入氖气时,混合物的颜色_______ 。(填”变浅”“变深”或”不变”)
 pC(g),达到平衡后,当降低温度时,B的转化率变大;当减小压强时,混合体系中C的质量分数减小,则:
pC(g),达到平衡后,当降低温度时,B的转化率变大;当减小压强时,混合体系中C的质量分数减小,则:(1)该反应的正反应是
(2)减压时,A的质量分数
(3)若加入B(体积不变),则A的转化率
(4)若升高温度,则平衡时,B、C的浓度之比
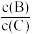 将
将(5)若加入催化剂,平衡时气体压强
(6)若B是有色物质,A、C均为无色物质,则加入C(体积不变)时混合物的颜色
您最近一年使用:0次
名校
解题方法
9 . 现有反应:mA(g)+nB(g)⇌pC(g),达到平衡后,当升高温度时,B的转化率变小;当减小压强时,混合体系中C的质量分数也减小,则:
(1)该反应的逆反应为_______ 热反应,(填“吸”或“放”)且m+n_______ p(填“>”“=”“<”)。
(2)减压时,A的质量分数_______ 。(填“增大”“减小”或“不变”,下同)
(3)若加入B(体积不变),则A的转化率_______ ,B的转化率_______ 。
(4)若B是有色物质,A、C均无色,则加入C(体积不变)时混合物颜色_______ ;而维持容器内压强不变,充入氖气时,混合物颜色_______ (填“变深”“变浅”或“不变”)。
(1)该反应的逆反应为
(2)减压时,A的质量分数
(3)若加入B(体积不变),则A的转化率
(4)若B是有色物质,A、C均无色,则加入C(体积不变)时混合物颜色
您最近一年使用:0次
2021-06-23更新
|
281次组卷
|
3卷引用:江西省赣州市信丰中学2020-2021学年高二上学期入学考试化学试题
江西省赣州市信丰中学2020-2021学年高二上学期入学考试化学试题(已下线)第二章 第三节化学平衡(第2课时 化学平衡的影响因素)(备作业)-【上好课】2021-2022学年高二化学同步备课系列(人教版选修4)(原卷版)吉林省长春市希望高中2021-2022学年高二上学期期中考试化学试题
解题方法
10 . 大气、水体常见污染元素主要有氮、硫。含氮废气、废液处理是化学学科重要研究课题。
(1)在含 、
、 废水中加入镁矿工业废水(含Mg2+),以除去N、P,其反应离子方程为Mg2++
废水中加入镁矿工业废水(含Mg2+),以除去N、P,其反应离子方程为Mg2++ +
+
 MgNH4PO4↓,该方法除N、P需要控制污水的pH在适当范围,原因是
MgNH4PO4↓,该方法除N、P需要控制污水的pH在适当范围,原因是___ 。
(2)用NaClO可以将氨氮(NH3、NH )氧化为N2脱离溶液,NaClO去除NH3反应的化学方程式
)氧化为N2脱离溶液,NaClO去除NH3反应的化学方程式___ 。
(3)目前,科学家正在研究一种以乙烯作为还原剂的脱硝(NO)方法,脱硝率与温度、负载率(分子筛中催化剂的质量分数)的关系如图1所示。
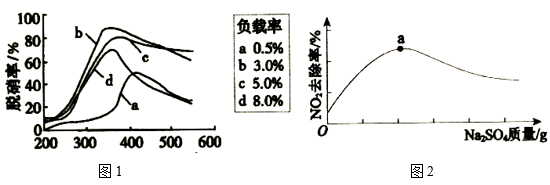
为达到最佳的脱硝效果,应采取的反应条件为___ (填温度和负载率数值)。
(4)CaSO3与Na2SO4混合浆液可用于脱除NO2,反应过程为:
Ⅰ.CaSO3(s)+ (aq)
(aq) CaSO4(s)+
CaSO4(s)+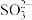 (aq)
(aq)
Ⅱ.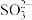 (aq)+2NO2(g)+H2O(l)
(aq)+2NO2(g)+H2O(l)
 (aq)+2
(aq)+2 (aq)+2H+( aq)
(aq)+2H+( aq)
浆液中CaSO3质量一定时,Na2SO4的质量与NO2的去除率变化趋势如图2所示。a点后NO2去除率降低的原因是___ 。
(1)在含
 、
、 废水中加入镁矿工业废水(含Mg2+),以除去N、P,其反应离子方程为Mg2++
废水中加入镁矿工业废水(含Mg2+),以除去N、P,其反应离子方程为Mg2++ +
+
 MgNH4PO4↓,该方法除N、P需要控制污水的pH在适当范围,原因是
MgNH4PO4↓,该方法除N、P需要控制污水的pH在适当范围,原因是(2)用NaClO可以将氨氮(NH3、NH
 )氧化为N2脱离溶液,NaClO去除NH3反应的化学方程式
)氧化为N2脱离溶液,NaClO去除NH3反应的化学方程式(3)目前,科学家正在研究一种以乙烯作为还原剂的脱硝(NO)方法,脱硝率与温度、负载率(分子筛中催化剂的质量分数)的关系如图1所示。

为达到最佳的脱硝效果,应采取的反应条件为
(4)CaSO3与Na2SO4混合浆液可用于脱除NO2,反应过程为:
Ⅰ.CaSO3(s)+
 (aq)
(aq) CaSO4(s)+
CaSO4(s)+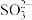 (aq)
(aq)Ⅱ.
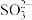 (aq)+2NO2(g)+H2O(l)
(aq)+2NO2(g)+H2O(l)
 (aq)+2
(aq)+2 (aq)+2H+( aq)
(aq)+2H+( aq) 浆液中CaSO3质量一定时,Na2SO4的质量与NO2的去除率变化趋势如图2所示。a点后NO2去除率降低的原因是
您最近一年使用:0次
2021-06-30更新
|
141次组卷
|
2卷引用:江苏省宿迁市2020-2021学年高二下学期期末考试化学试题



