解题方法
1 . 从某铋(Bi)、锌的冶炼厂的高铟烟灰(主要含ZnO、 、
、 、
、 、
、 )中提取铟和铋的流程如图:
)中提取铟和铋的流程如图:
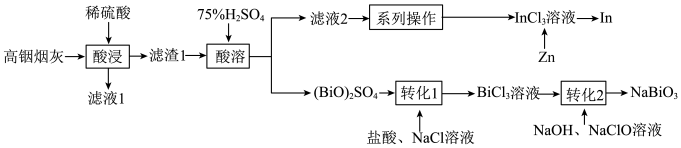
已知: 不溶于稀硫酸;
不溶于稀硫酸; 难溶于水。
难溶于水。
回答下列问题:
(1)“滤液1”中含有的金属阳离子有_______ (填离子符号)。
(2)“酸浸”过程中使用稀硫酸而不用75%的) 溶液,其原因是
溶液,其原因是_______ 。
(3)“酸溶”生成的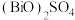 中,Bi元素的化合价为
中,Bi元素的化合价为_______ 。
(4)“转化2”时发生反应的化学方程式为_______ 。
(5)“系列操作”的流程如下:
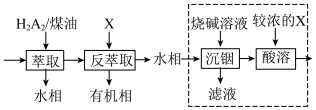
已知:“萃取”时发生反应: (金属阳离子)
(金属阳离子)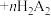 (有机液)
(有机液) (有机液)
(有机液)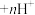 ;
; 与
与 相似,易水解。
相似,易水解。
①试剂X的名称为_______ ,“萃取”和“反萃取”的目的是_______ 。
②关于虚线框内的实验步骤,下列说法正确的是_______ (填标号)。
A.可以提高 溶液的浓度
溶液的浓度
B.烧碱溶液可用纯碱溶液代替
C.需用到分液漏斗、烧杯、玻璃棒等仪器
(6)akg的高铟烟灰经上述流程后,得到 质量分数为w的产品bg,则高铟烟灰中Bi的百分含量为
质量分数为w的产品bg,则高铟烟灰中Bi的百分含量为_______ (用含a、b、w的计算式表示)。
 、
、 、
、 、
、 )中提取铟和铋的流程如图:
)中提取铟和铋的流程如图:
已知:
 不溶于稀硫酸;
不溶于稀硫酸; 难溶于水。
难溶于水。回答下列问题:
(1)“滤液1”中含有的金属阳离子有
(2)“酸浸”过程中使用稀硫酸而不用75%的)
 溶液,其原因是
溶液,其原因是(3)“酸溶”生成的
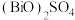 中,Bi元素的化合价为
中,Bi元素的化合价为(4)“转化2”时发生反应的化学方程式为
(5)“系列操作”的流程如下:

已知:“萃取”时发生反应:
 (金属阳离子)
(金属阳离子)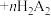 (有机液)
(有机液) (有机液)
(有机液)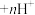 ;
; 与
与 相似,易水解。
相似,易水解。①试剂X的名称为
②关于虚线框内的实验步骤,下列说法正确的是
A.可以提高
 溶液的浓度
溶液的浓度B.烧碱溶液可用纯碱溶液代替
C.需用到分液漏斗、烧杯、玻璃棒等仪器
(6)akg的高铟烟灰经上述流程后,得到
 质量分数为w的产品bg,则高铟烟灰中Bi的百分含量为
质量分数为w的产品bg,则高铟烟灰中Bi的百分含量为
您最近一年使用:0次
21-22高二·浙江·期中
解题方法
2 . CH3COOH是食醋的主要成分,用化学反应原理可以研究其性质。
(1)气态CH3COOH中存在平衡2CH3COOH (CH3COOH)2 △H<0, 若要准确测定CH3COOH的相对分子质量,应选用的条件是___________。
(CH3COOH)2 △H<0, 若要准确测定CH3COOH的相对分子质量,应选用的条件是___________。
(2)用滴定法可以测定食醋中醋酸的含量,用酸式滴定管取10.00mL这种市售食醋,置于已知烧杯中称得其质量为12.50g,再稀释至100mL,滴定时每次取20.00 mL于锥形瓶中,选用的标准溶液是0.1125 mol/LNaOH溶液滴定至终点,平均每次消耗NaOH溶液20.00mL。
①该实验中的指示剂应选择___________ (填“酚酞”、“甲基橙”或“石蕊”),滴定终点的现象为___________ 。
②该食醋中CH3COOH的质量分数为___________ (CH3COOH的相对分子质量为60,结果保留三位有效数字)。
③滴定过程中下列操作会导致测定的CH3COOH的质量分数偏小的是(其它操作均正确)___________ 。
A.碱式滴定管在装液前未用待测NaOH溶液润洗2~3次
B.滴定开始前碱式滴定管尖嘴部分无气泡,在滴定终点读数时发现气泡
C.达到滴定终点时,俯视溶液凹液面最低点读数
D.滴定过程中,部分NaOH溶液滴到锥形瓶外
(1)气态CH3COOH中存在平衡2CH3COOH
 (CH3COOH)2 △H<0, 若要准确测定CH3COOH的相对分子质量,应选用的条件是___________。
(CH3COOH)2 △H<0, 若要准确测定CH3COOH的相对分子质量,应选用的条件是___________。| A.低温低压 | B.低温高压 | C.高温低压 | D.高温高压 |
①该实验中的指示剂应选择
②该食醋中CH3COOH的质量分数为
③滴定过程中下列操作会导致测定的CH3COOH的质量分数偏小的是(其它操作均正确)
A.碱式滴定管在装液前未用待测NaOH溶液润洗2~3次
B.滴定开始前碱式滴定管尖嘴部分无气泡,在滴定终点读数时发现气泡
C.达到滴定终点时,俯视溶液凹液面最低点读数
D.滴定过程中,部分NaOH溶液滴到锥形瓶外
您最近一年使用:0次
解题方法
3 . 煤焦油、煤和海砂中氯离子含量高会破坏金属的钝化膜,导致铁制设备和钢管等被腐蚀。
(1)铁接触氧气和水后会发生电化学腐蚀,其负极的电极反应式为_______ 。
(2)测定煤中氯离子含量的两种方法。
方法一:在高温下,通入水蒸气将煤样中无机盐转化为HCl,再滴定氯离子。
方法二:取a g煤样,处理后得到含氯离子的样品溶液,加入 溶液,以
溶液,以 作指示剂,用
作指示剂,用 溶液滴定过量的
溶液滴定过量的 溶液,共消耗KSCN溶液
溶液,共消耗KSCN溶液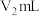 。
。
已知: 能与KSCN反应生成AgSCN沉淀。
能与KSCN反应生成AgSCN沉淀。
①结合化学用语,从化学平衡的角度解释方法一中无机盐中 生成HCl的原因
生成HCl的原因_______ 。
②方法二中,滴定终点的现象为_______ 。
③利用方法二,测得煤样中氯元素的质量分数为_______ 。
(3)快速检测法测定海砂中氯离子含量的过程如下。
i.配制固定组分的铬酸银( )浑浊液;
)浑浊液;
ii.将待测海砂样品与i中浑浊液混合,溶液的颜色会随着氯离子含量的变化而变化。
已知: ;
; ;
; 溶液为黄色,
溶液为黄色, 固体为砖红色。
固体为砖红色。
① 时,沉淀仍然为砖红色的原因是
时,沉淀仍然为砖红色的原因是_______ 。
②写出砖红色沉淀变为白色的离子方程式_______ 。
(1)铁接触氧气和水后会发生电化学腐蚀,其负极的电极反应式为
(2)测定煤中氯离子含量的两种方法。
方法一:在高温下,通入水蒸气将煤样中无机盐转化为HCl,再滴定氯离子。
方法二:取a g煤样,处理后得到含氯离子的样品溶液,加入
 溶液,以
溶液,以 作指示剂,用
作指示剂,用 溶液滴定过量的
溶液滴定过量的 溶液,共消耗KSCN溶液
溶液,共消耗KSCN溶液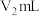 。
。已知:
 能与KSCN反应生成AgSCN沉淀。
能与KSCN反应生成AgSCN沉淀。①结合化学用语,从化学平衡的角度解释方法一中无机盐中
 生成HCl的原因
生成HCl的原因②方法二中,滴定终点的现象为
③利用方法二,测得煤样中氯元素的质量分数为
(3)快速检测法测定海砂中氯离子含量的过程如下。
i.配制固定组分的铬酸银(
 )浑浊液;
)浑浊液;ii.将待测海砂样品与i中浑浊液混合,溶液的颜色会随着氯离子含量的变化而变化。
| 氯离子含量x |  |  |  |
| ii中现象 | 沉淀仍然为砖红色 | 砖红色沉淀部分变为白色,溶液逐渐转变为黄色 | 砖红色沉淀完全变为白色,溶液完全转变为黄色 |
 ;
; ;
; 溶液为黄色,
溶液为黄色, 固体为砖红色。
固体为砖红色。①
 时,沉淀仍然为砖红色的原因是
时,沉淀仍然为砖红色的原因是②写出砖红色沉淀变为白色的离子方程式
您最近一年使用:0次
4 . 回答下列问题:
(1)现有反应:mA(g)+nB(g) pC(g),达到平衡后,当升高温度时,B的转化率变大;当减小压强时,混合体系中C的质量分数减小,则:
pC(g),达到平衡后,当升高温度时,B的转化率变大;当减小压强时,混合体系中C的质量分数减小,则:
①该反应的逆反应为___ 反应(填“吸热”或“放热“),且m+n___ p(填“>”“=”或“<”)。
②减压使容器体积增大时,A的质量分数___ 。(填“增大”、“减小”或“不变”,下同),平均相对分子质量___ 。
③若加入B(维持体积不变),则A的转化率___ ;B的百分含量___ 。
④若升高温度,则平衡时B、C的浓度之比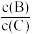 将
将___ 。
⑤若加入催化剂,平衡时气体混合物的总物质的量___ 。
Ⅱ.在一个体积为2L的密闭容器中,高温下发生反应:Fe(s)+CO2(g) FeO(s)+CO(g)。其中CO2、CO的物质的量(mol)随时间(min)的变化关系如图所示。
FeO(s)+CO(g)。其中CO2、CO的物质的量(mol)随时间(min)的变化关系如图所示。

(2)反应在1min时第一次达到平衡状态,固体的质量增加了3.2g。用CO2的浓度变化表示的反应速率v(CO2)=___ 。
(3)反应进行至2min时,若只改变温度,曲线发生的变化如图所示,3min时再次达到平衡,则ΔH__ 0(填“>”“<”或“=”)。
(4)5min时再充入一定量的CO(g),平衡发生移动。下列说法正确的是___ (填写编号)。
A.v(正)先增大后减小 B.v(正)先减小后增大
C.v(逆)先增大后减小 D.v(逆)先减小后增大
表示n(CO2)变化的曲线是___ (填写图中曲线的字母编号)。
(5)请用固态物质的有关物理量来说明该反应已经达到化学平衡状态:___ 。
(1)现有反应:mA(g)+nB(g)
 pC(g),达到平衡后,当升高温度时,B的转化率变大;当减小压强时,混合体系中C的质量分数减小,则:
pC(g),达到平衡后,当升高温度时,B的转化率变大;当减小压强时,混合体系中C的质量分数减小,则:①该反应的逆反应为
②减压使容器体积增大时,A的质量分数
③若加入B(维持体积不变),则A的转化率
④若升高温度,则平衡时B、C的浓度之比
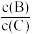 将
将⑤若加入催化剂,平衡时气体混合物的总物质的量
Ⅱ.在一个体积为2L的密闭容器中,高温下发生反应:Fe(s)+CO2(g)
 FeO(s)+CO(g)。其中CO2、CO的物质的量(mol)随时间(min)的变化关系如图所示。
FeO(s)+CO(g)。其中CO2、CO的物质的量(mol)随时间(min)的变化关系如图所示。
(2)反应在1min时第一次达到平衡状态,固体的质量增加了3.2g。用CO2的浓度变化表示的反应速率v(CO2)=
(3)反应进行至2min时,若只改变温度,曲线发生的变化如图所示,3min时再次达到平衡,则ΔH
(4)5min时再充入一定量的CO(g),平衡发生移动。下列说法正确的是
A.v(正)先增大后减小 B.v(正)先减小后增大
C.v(逆)先增大后减小 D.v(逆)先减小后增大
表示n(CO2)变化的曲线是
(5)请用固态物质的有关物理量来说明该反应已经达到化学平衡状态:
您最近一年使用:0次
解题方法
5 . 过氧化钙是一种在水产养殖中广泛使用的供氧剂.实验室以碳酸钙为原料制备过氧化钙的流程如图。

已知:273K时,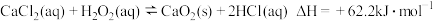
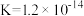
(1)“煮沸”的目的是_______ 。
(2)“冰水浴”的作用是_______ 。
(3)结合平衡移动原理,分析NaOH溶液的作用_______ 。
(4)NaOH用量过多,会产生大量_______ (填化学式),与CaO2共沉淀,造成产品纯度降低。
(5)常采用碘量法测定产品中CaO2含量,具体操作步骤如下:准确称取ag产品于碘量瓶中,加入适量蒸馏水和过量的bgKI晶体,再用稀盐酸酸化,充分反应后,以淀粉作指示剂,用c mol·L-1Na2S2O3溶液滴定至终点,记录数据.重复上述操作2~3次,平均消耗Na2S2O3溶液的体积为VmL。
①Na2S2O3溶液装于_______ 式滴定管。
②酸化过程中,稀盐酸不宜加入过多的原因是_______ 。
③CaO2的质量分数为_______ (用字母表示).(已知: )
)

已知:273K时,
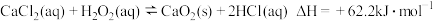
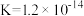
(1)“煮沸”的目的是
(2)“冰水浴”的作用是
(3)结合平衡移动原理,分析NaOH溶液的作用
(4)NaOH用量过多,会产生大量
(5)常采用碘量法测定产品中CaO2含量,具体操作步骤如下:准确称取ag产品于碘量瓶中,加入适量蒸馏水和过量的bgKI晶体,再用稀盐酸酸化,充分反应后,以淀粉作指示剂,用c mol·L-1Na2S2O3溶液滴定至终点,记录数据.重复上述操作2~3次,平均消耗Na2S2O3溶液的体积为VmL。
①Na2S2O3溶液装于
②酸化过程中,稀盐酸不宜加入过多的原因是
③CaO2的质量分数为
 )
)
您最近一年使用:0次
名校
解题方法
6 . 工业上利用锌焙砂(主要成分为 ,含有少量
,含有少量 、
、 、
、 等)生产高纯
等)生产高纯 的流程示意图如下。
的流程示意图如下。 溶液和氨水“浸出”锌焙砂。
溶液和氨水“浸出”锌焙砂。
①“浸出”前,锌焙砂预先粉碎的目的是_____ 。
②通过“浸出”步骤,锌焙砂中的 转化为
转化为 ,该反应的离子方程式为
,该反应的离子方程式为_____ 。
(2)“浸出”时 转化为
转化为 。“除砷”步骤①中用
。“除砷”步骤①中用 作氧化剂。
作氧化剂。
i.指出 中
中 与
与 的化合价:
的化合价:_____ 。
ii.步骤①的离子方程式为_____ 。
(3)“除重金属”时加入 溶液。滤渣Ⅱ中含有的主要物质是
溶液。滤渣Ⅱ中含有的主要物质是_____ 和 。
。
(4)“蒸氨”时会出现白色固体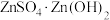 ,运用平衡移动原理解释原因:
,运用平衡移动原理解释原因:_____ 。
(5)“沉锌”步骤①中加入足量 溶液将白色固体转化为
溶液将白色固体转化为 的离子方程式为
的离子方程式为_____ 。
(6)“煅烧”步骤中,不同温度下, 分解的失重曲线和产品
分解的失重曲线和产品 的比表面积变化情况如图甲、图乙所示。
的比表面积变化情况如图甲、图乙所示。
已知:i.固体失重质量分数=
ii.比表面积指单位质量固体所具有的总面积;比表面积越大,产品 的活性越高。
的活性越高。 ,300min后固体失重质量分数为33.3%,则
,300min后固体失重质量分数为33.3%,则 的分解率为
的分解率为_____ %(保留到小数点后一位)。
②根据图1和图2,获得高产率( 分解率
分解率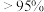 )、高活性(
)、高活性( 比表面积
比表面积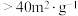 )产品
)产品 的最佳条件是
的最佳条件是_____ (填字母序号)。
a.恒温280℃,60~120min
b.恒温300℃,240~300min
c.恒温350℃,240~300min
d.恒温550℃,60~120min
(7)该流程中可循环利用的物质有_____ 。
 ,含有少量
,含有少量 、
、 、
、 等)生产高纯
等)生产高纯 的流程示意图如下。
的流程示意图如下。
已知: 结构如图所示
结构如图所示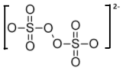
 溶液和氨水“浸出”锌焙砂。
溶液和氨水“浸出”锌焙砂。①“浸出”前,锌焙砂预先粉碎的目的是
②通过“浸出”步骤,锌焙砂中的
 转化为
转化为 ,该反应的离子方程式为
,该反应的离子方程式为(2)“浸出”时
 转化为
转化为 。“除砷”步骤①中用
。“除砷”步骤①中用 作氧化剂。
作氧化剂。i.指出
 中
中 与
与 的化合价:
的化合价:ii.步骤①的离子方程式为
(3)“除重金属”时加入
 溶液。滤渣Ⅱ中含有的主要物质是
溶液。滤渣Ⅱ中含有的主要物质是 。
。(4)“蒸氨”时会出现白色固体
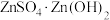 ,运用平衡移动原理解释原因:
,运用平衡移动原理解释原因:(5)“沉锌”步骤①中加入足量
 溶液将白色固体转化为
溶液将白色固体转化为 的离子方程式为
的离子方程式为(6)“煅烧”步骤中,不同温度下,
 分解的失重曲线和产品
分解的失重曲线和产品 的比表面积变化情况如图甲、图乙所示。
的比表面积变化情况如图甲、图乙所示。已知:i.固体失重质量分数=

ii.比表面积指单位质量固体所具有的总面积;比表面积越大,产品
 的活性越高。
的活性越高。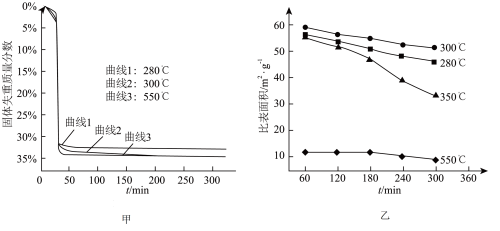
 ,300min后固体失重质量分数为33.3%,则
,300min后固体失重质量分数为33.3%,则 的分解率为
的分解率为②根据图1和图2,获得高产率(
 分解率
分解率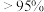 )、高活性(
)、高活性( 比表面积
比表面积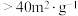 )产品
)产品 的最佳条件是
的最佳条件是a.恒温280℃,60~120min
b.恒温300℃,240~300min
c.恒温350℃,240~300min
d.恒温550℃,60~120min
(7)该流程中可循环利用的物质有
您最近一年使用:0次
真题
解题方法
7 . 磷酸二氢钾在工农业生产及国防工业等领域都有广泛的应用。某研究小组用质量分数为85%的磷酸与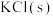 反应制备
反应制备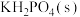 ,反应方程式为
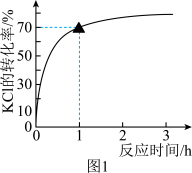
,反应方程式为 一定条件下的实验结果如图1所示。
一定条件下的实验结果如图1所示。
回答问题:
(1)该条件下,反应至1h时KCl的转化率为_______ 。
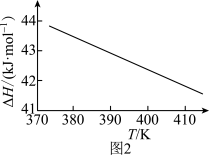
(2)该制备反应的 随温度变化关系如图2所示。该条件下反应为
随温度变化关系如图2所示。该条件下反应为_______ 反应(填“吸热”或“放热”),且反应热随温度升高而_______ 。
(3)该小组为提高转化率采用的措施中有:使用浓磷酸作反应物、向系统中不断通入水蒸气等。它们能提高转化率的原因是:不使用稀磷酸_______ ;通入水蒸气_______ 。
(4)298K时,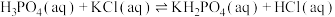 的平衡常数
的平衡常数
_______ 。(已知 的
的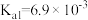 )
)
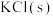 反应制备
反应制备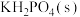 ,反应方程式为
,反应方程式为 一定条件下的实验结果如图1所示。
一定条件下的实验结果如图1所示。
回答问题:
(1)该条件下,反应至1h时KCl的转化率为
(2)该制备反应的
 随温度变化关系如图2所示。该条件下反应为
随温度变化关系如图2所示。该条件下反应为
(3)该小组为提高转化率采用的措施中有:使用浓磷酸作反应物、向系统中不断通入水蒸气等。它们能提高转化率的原因是:不使用稀磷酸
(4)298K时,
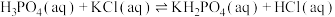 的平衡常数
的平衡常数
 的
的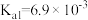 )
)
您最近一年使用:0次
8 . 某小组同学探究铜和浓硝酸的反应,进行如下实验:
实验1:分别取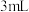 浓硝酸与不同质量的铜粉充分反应,铜粉完全溶解,溶液颜色如下:
浓硝酸与不同质量的铜粉充分反应,铜粉完全溶解,溶液颜色如下:
(1)写出铜和浓硝酸反应的离子反应方程式:_______ 。
(2)小组同学认为溶液呈绿色的可能原因是:
猜想1:硝酸铜质量分数较高,溶液呈绿色;
猜想2: 溶解在硝酸铜溶液中,溶液呈绿色。
溶解在硝酸铜溶液中,溶液呈绿色。
依据实验1中的现象,判断猜想1是否合理,并说明理由:_____ 。
(3)取⑤中溶液,_____ (填操作和现象),证实猜想2成立。
(4)小组同学进行如下实验也证实了猜想2成立。
实验2:向①中溶液以相同流速分别通入N2和空气,观察现象。
结合物质性质和上述实验现象,下列推测合理的是_______(填字母序号)。
(5)小组同学继续探究实验2中现象的差异,并查阅文献知:
i.“可溶性铜盐中溶解亚硝酸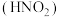 ”可能是实验①中溶液显绿色的主要原因
”可能是实验①中溶液显绿色的主要原因
ii. 在溶液中存在:
在溶液中存在:
反应1: (慢)
(慢)
反应2: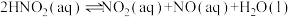 (快)
(快)
结合信息及反应原理解释实验2中“通入氮气变蓝慢,通入空气变蓝快”的原因_______ 。
(6)小组同学为确认亚硝酸参与了形成绿色溶液的过程,继续进行实验。
实验3:取3份等体积的①中绿色溶液,分别加入不同物质,观察现象。
实验中加入的固体物质是_______ (填化学式),加入 后溶液迅速变蓝可能的原因是化学方程式表示):
后溶液迅速变蓝可能的原因是化学方程式表示):  ,
,_______ ,_______ 。
实验1:分别取
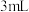 浓硝酸与不同质量的铜粉充分反应,铜粉完全溶解,溶液颜色如下:
浓硝酸与不同质量的铜粉充分反应,铜粉完全溶解,溶液颜色如下:| 编号 | ① | ② | ③ | ④ | ⑤ |
| 铜粉质量 | 0.1 | 0.2 | 0.3 | 0.4 | 0.5 |
| 溶液颜色 | 绿色 | 草绿色 | 蓝绿色偏绿 | 蓝绿色偏蓝 | 蓝色 |
(2)小组同学认为溶液呈绿色的可能原因是:
猜想1:硝酸铜质量分数较高,溶液呈绿色;
猜想2:
 溶解在硝酸铜溶液中,溶液呈绿色。
溶解在硝酸铜溶液中,溶液呈绿色。依据实验1中的现象,判断猜想1是否合理,并说明理由:
(3)取⑤中溶液,
(4)小组同学进行如下实验也证实了猜想2成立。
实验2:向①中溶液以相同流速分别通入N2和空气,观察现象。
| 通入气体 | 氮气 | 空气 |
| 现象 | 液面上方出现明显的红棕色气体,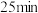 后溶液变为蓝色 后溶液变为蓝色 | 液面上方出现明显的红棕色气体, 后溶液变为蓝 后溶液变为蓝 |
A.(1)中溶液通入 时, 时, 被缓慢氧化为 被缓慢氧化为 |
| B.(1)中溶液里某还原性微粒与绿色有关,通入空气时较快被氧化 |
C.空气中的 溶于水显酸性,促进了溶液变蓝色 溶于水显酸性,促进了溶液变蓝色 |
| D.加热溶液①后,能观察到溶液变蓝的现象 |
i.“可溶性铜盐中溶解亚硝酸
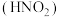 ”可能是实验①中溶液显绿色的主要原因
”可能是实验①中溶液显绿色的主要原因ii.
 在溶液中存在:
在溶液中存在:反应1:
 (慢)
(慢)反应2:
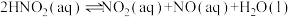 (快)
(快)结合信息及反应原理解释实验2中“通入氮气变蓝慢,通入空气变蓝快”的原因
(6)小组同学为确认亚硝酸参与了形成绿色溶液的过程,继续进行实验。
实验3:取3份等体积的①中绿色溶液,分别加入不同物质,观察现象。
| 加入物质 | _______固体 | 3滴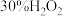 溶液 溶液 | 3滴水 |
| 现象 | 溶液绿色变深 | 溶液迅速变为蓝色 | 溶液颜色几乎不变 |
 后溶液迅速变蓝可能的原因是化学方程式表示):
后溶液迅速变蓝可能的原因是化学方程式表示):  ,
,
您最近一年使用:0次
2024高三·全国·专题练习
解题方法
9 . 下面是制备硫酸的工业流程:

(1) 的晶体类型是
的晶体类型是_______ 。
(2)第一步时,硫粉液化并与氧气共热生成二氧化硫。若反应温度超过硫粉沸点,部分硫粉会转化为硫蒸气,与生成的二氧化硫一同参加第二步反应,关于这种情况说法正确的是_______ 。
a.硫粉消耗会增大 b.二氧化硫生成率降低 c. 二氧化硫生成率增大
(3)若每生成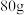 气体三氧化硫,放出
气体三氧化硫,放出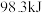 能量,写出生成三氧化硫的反应的热化学方程式:
能量,写出生成三氧化硫的反应的热化学方程式:_______ ,若反应温度升高,则二氧化硫转化率_______ (填“升高”或“降低”)。
(4)第二步反应中,从能量角度分析催化剂意义:_______ 。
在第二步反应中,首先将反应物加热到 ,通入催化剂层,进行第一轮反应,反应后体系温度升高,导出产物与剩余反应物,与其他反应物进行热交换降温,随后再次通入催化剂层,如此进行四轮反应,使反应转化率接近平衡转化率,得到较高产率的三氧化硫。
,通入催化剂层,进行第一轮反应,反应后体系温度升高,导出产物与剩余反应物,与其他反应物进行热交换降温,随后再次通入催化剂层,如此进行四轮反应,使反应转化率接近平衡转化率,得到较高产率的三氧化硫。
(5)通入催化剂层后,体系(剩余反应物与生成物)温度升高的原因在于_______ ;每轮反应后进行热交换降温的目的是_______ 。
(6)关于四轮反应,说法正确的是_______ 。
a.这一流程保证了在反应速率较大的情况下,转化率尽可能大
b.这一流程使这一反应最终达到平衡转化率
c.这一流程节约了能源
(7)如图是吸收三氧化硫时浓硫酸浓度、温度对吸收率影响曲线,读图可知,最适合吸收三氧化硫的浓硫酸质量分数为_______ ,最适合吸收的温度为_______ 。

(8)一批32吨含硫元素 的硫粉,参加反应,在第一步反应中硫元素损失了
的硫粉,参加反应,在第一步反应中硫元素损失了 ,二氧化硫在第二步反应中
,二氧化硫在第二步反应中 转化为了三氧化硫,三氧化硫在第三步反应中被吸收时,视作全部吸收,那么这批硫粉总计可以生产
转化为了三氧化硫,三氧化硫在第三步反应中被吸收时,视作全部吸收,那么这批硫粉总计可以生产 的浓硫酸
的浓硫酸_______ 吨。

(1)
 的晶体类型是
的晶体类型是(2)第一步时,硫粉液化并与氧气共热生成二氧化硫。若反应温度超过硫粉沸点,部分硫粉会转化为硫蒸气,与生成的二氧化硫一同参加第二步反应,关于这种情况说法正确的是
a.硫粉消耗会增大 b.二氧化硫生成率降低 c. 二氧化硫生成率增大
(3)若每生成
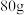 气体三氧化硫,放出
气体三氧化硫,放出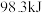 能量,写出生成三氧化硫的反应的热化学方程式:
能量,写出生成三氧化硫的反应的热化学方程式:(4)第二步反应中,从能量角度分析催化剂意义:
在第二步反应中,首先将反应物加热到
 ,通入催化剂层,进行第一轮反应,反应后体系温度升高,导出产物与剩余反应物,与其他反应物进行热交换降温,随后再次通入催化剂层,如此进行四轮反应,使反应转化率接近平衡转化率,得到较高产率的三氧化硫。
,通入催化剂层,进行第一轮反应,反应后体系温度升高,导出产物与剩余反应物,与其他反应物进行热交换降温,随后再次通入催化剂层,如此进行四轮反应,使反应转化率接近平衡转化率,得到较高产率的三氧化硫。(5)通入催化剂层后,体系(剩余反应物与生成物)温度升高的原因在于
(6)关于四轮反应,说法正确的是
a.这一流程保证了在反应速率较大的情况下,转化率尽可能大
b.这一流程使这一反应最终达到平衡转化率
c.这一流程节约了能源
(7)如图是吸收三氧化硫时浓硫酸浓度、温度对吸收率影响曲线,读图可知,最适合吸收三氧化硫的浓硫酸质量分数为

(8)一批32吨含硫元素
 的硫粉,参加反应,在第一步反应中硫元素损失了
的硫粉,参加反应,在第一步反应中硫元素损失了 ,二氧化硫在第二步反应中
,二氧化硫在第二步反应中 转化为了三氧化硫,三氧化硫在第三步反应中被吸收时,视作全部吸收,那么这批硫粉总计可以生产
转化为了三氧化硫,三氧化硫在第三步反应中被吸收时,视作全部吸收,那么这批硫粉总计可以生产 的浓硫酸
的浓硫酸
您最近一年使用:0次
10 . 氯化亚铜( )广泛应用于冶金工业,也用作催化剂和杀菌剂。以硫化铜精矿为原料生产
)广泛应用于冶金工业,也用作催化剂和杀菌剂。以硫化铜精矿为原料生产 的工艺如下:
的工艺如下: 难溶于醇和水,溶于
难溶于醇和水,溶于 较大的体系
较大的体系 ,潮湿空气中易水解氧化。
,潮湿空气中易水解氧化。
(1)步骤1是“氧化酸浸”的过程,该过程生成蓝色溶液和浅黄色沉淀,化学方程式是___________ 。
(2)步骤2是溶解过程,溶解时反应的离子方程式___________ 。
(3)步骤3为主反应, 的沉淀率与加入的
的沉淀率与加入的 的量关系如图所示。
的量关系如图所示。___________ ;
②比较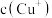 相对大小:A点
相对大小:A点___________ C点(填“>”、“<”或“=”);
③提高C点状态混合物中 沉淀率的措施是
沉淀率的措施是___________ ;
(4)步骤4进行的实验操作是___________ ;
(5)洗涤过程中不能用硝酸代替硫酸进行“酸洗”,理由是___________ 。用乙醇洗涤的目的是___________ 。
(6)产品纯度测定:称取 产品a g于锥形瓶中,加入足量的酸性
产品a g于锥形瓶中,加入足量的酸性 溶液使其充分溶解,然后用
溶液使其充分溶解,然后用
 标准溶液滴定
标准溶液滴定 ,消耗
,消耗 溶液b mL。(本实验中
溶液b mL。(本实验中 的被还原为
的被还原为 ,不与产品中杂质和
,不与产品中杂质和 反应)。
反应)。
① 溶于
溶于 溶液的离子方程式是
溶液的离子方程式是___________ 。
②产品中 (摩尔质量为99g/mol)的质量分数为
(摩尔质量为99g/mol)的质量分数为___________ 。
 )广泛应用于冶金工业,也用作催化剂和杀菌剂。以硫化铜精矿为原料生产
)广泛应用于冶金工业,也用作催化剂和杀菌剂。以硫化铜精矿为原料生产 的工艺如下:
的工艺如下:
 难溶于醇和水,溶于
难溶于醇和水,溶于 较大的体系
较大的体系 ,潮湿空气中易水解氧化。
,潮湿空气中易水解氧化。(1)步骤1是“氧化酸浸”的过程,该过程生成蓝色溶液和浅黄色沉淀,化学方程式是
(2)步骤2是溶解过程,溶解时反应的离子方程式
(3)步骤3为主反应,
 的沉淀率与加入的
的沉淀率与加入的 的量关系如图所示。
的量关系如图所示。
②比较
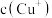 相对大小:A点
相对大小:A点③提高C点状态混合物中
 沉淀率的措施是
沉淀率的措施是(4)步骤4进行的实验操作是
(5)洗涤过程中不能用硝酸代替硫酸进行“酸洗”,理由是
(6)产品纯度测定:称取
 产品a g于锥形瓶中,加入足量的酸性
产品a g于锥形瓶中,加入足量的酸性 溶液使其充分溶解,然后用
溶液使其充分溶解,然后用
 标准溶液滴定
标准溶液滴定 ,消耗
,消耗 溶液b mL。(本实验中
溶液b mL。(本实验中 的被还原为
的被还原为 ,不与产品中杂质和
,不与产品中杂质和 反应)。
反应)。①
 溶于
溶于 溶液的离子方程式是
溶液的离子方程式是②产品中
 (摩尔质量为99g/mol)的质量分数为
(摩尔质量为99g/mol)的质量分数为
您最近一年使用:0次
2023-05-31更新
|
711次组卷
|
7卷引用:北京市朝阳区2023届高三下学期三模化学试题



