名校
1 . 某学习小组欲利用 平衡体系探究影响平衡的因素,将220 mL 0.005 mol⋅L
平衡体系探究影响平衡的因素,将220 mL 0.005 mol⋅L
 溶液和20 mL 0.015 mol⋅L
溶液和20 mL 0.015 mol⋅L KSCN溶液混合,得血红色溶液X,进行下列实验:
KSCN溶液混合,得血红色溶液X,进行下列实验:
实验Ⅰ.改变 、
、 、
、 、
、 等离子浓度对平衡的影响
等离子浓度对平衡的影响
(1)取2 mL溶液X,加入5滴0.01 mol⋅L KSCN溶液,溶液红色
KSCN溶液,溶液红色_______ (填“变深”、“变浅”或“不变”,下同);取2 mL溶液X,插入经砂纸打磨过的铁丝,溶液红色_______ 。基于上述两个实验可以得到的结论是_______ 。
(2)取2 mL溶液X,加入5滴0.03 mol⋅L KCl溶液,观察到溶液红色变浅,产生该现象的原因可能是
KCl溶液,观察到溶液红色变浅,产生该现象的原因可能是_______ 或者不直接参与平衡体系的 或
或 对平衡产生了影响。
对平衡产生了影响。
实验Ⅱ.探究KCl对 平衡体系的影响为了确定KCl是否对平衡产生影响,学习小组同学进行如下探究:各取2mL溶液X放入3支比色皿中,分别滴加5滴不同浓度的KCl溶液,并测定各溶液的透射率随时间的变化(已知溶液颜色越深,透射率越小),结果如图所示。
平衡体系的影响为了确定KCl是否对平衡产生影响,学习小组同学进行如下探究:各取2mL溶液X放入3支比色皿中,分别滴加5滴不同浓度的KCl溶液,并测定各溶液的透射率随时间的变化(已知溶液颜色越深,透射率越小),结果如图所示。
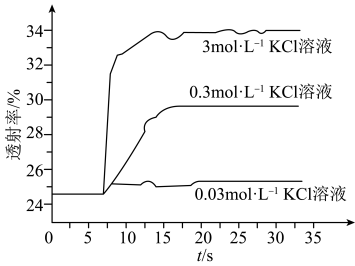
(3)上述实验可以得到以下结论:一是KCl对 平衡有影响,且KCl浓度越大,影响
平衡有影响,且KCl浓度越大,影响_______ 。二是_______ 。
(4)针对产生上述影响的可能原因,学习小组同学提出以下猜想:
猜想①: 产生的影响。
产生的影响。
猜想②: 产生的影响。
产生的影响。
猜想③:_______ 。
实验Ⅲ.探究盐对 和
和 平衡体系产生的影响
平衡体系产生的影响
资料信息:
a.溶液中的离子会受到周围带有异性电荷离子的屏蔽,使该离子的有效浓度降低,这种影响称为盐效应。
b.在 溶液中存在反应
溶液中存在反应 。
。
(5)根据上述信息,学习小组同学各取2 mL溶液X,分别加入5滴①去离子水、②0.3 mol⋅L KCl溶液、③0.3 mol⋅L
KCl溶液、③0.3 mol⋅L NaCl溶液、④0.3 mol⋅L
NaCl溶液、④0.3 mol⋅L
 溶液、⑤3 mol⋅L
溶液、⑤3 mol⋅L HCl溶液进行实验,测得各溶液的透射率随时间的变化如图所示。
HCl溶液进行实验,测得各溶液的透射率随时间的变化如图所示。

上述实验能证明阳离子盐效应影响 平衡体系的实验组是
平衡体系的实验组是_______ 。盐效应影响较大的阳离子是_______ 。
A.实验①②③ B.实验①②④ C.实验①③④
(6)解释出现实验⑤现象的原因:_______ 。
 平衡体系探究影响平衡的因素,将220 mL 0.005 mol⋅L
平衡体系探究影响平衡的因素,将220 mL 0.005 mol⋅L
 溶液和20 mL 0.015 mol⋅L
溶液和20 mL 0.015 mol⋅L KSCN溶液混合,得血红色溶液X,进行下列实验:
KSCN溶液混合,得血红色溶液X,进行下列实验:实验Ⅰ.改变
 、
、 、
、 、
、 等离子浓度对平衡的影响
等离子浓度对平衡的影响(1)取2 mL溶液X,加入5滴0.01 mol⋅L
 KSCN溶液,溶液红色
KSCN溶液,溶液红色(2)取2 mL溶液X,加入5滴0.03 mol⋅L
 KCl溶液,观察到溶液红色变浅,产生该现象的原因可能是
KCl溶液,观察到溶液红色变浅,产生该现象的原因可能是 或
或 对平衡产生了影响。
对平衡产生了影响。实验Ⅱ.探究KCl对
 平衡体系的影响为了确定KCl是否对平衡产生影响,学习小组同学进行如下探究:各取2mL溶液X放入3支比色皿中,分别滴加5滴不同浓度的KCl溶液,并测定各溶液的透射率随时间的变化(已知溶液颜色越深,透射率越小),结果如图所示。
平衡体系的影响为了确定KCl是否对平衡产生影响,学习小组同学进行如下探究:各取2mL溶液X放入3支比色皿中,分别滴加5滴不同浓度的KCl溶液,并测定各溶液的透射率随时间的变化(已知溶液颜色越深,透射率越小),结果如图所示。
(3)上述实验可以得到以下结论:一是KCl对
 平衡有影响,且KCl浓度越大,影响
平衡有影响,且KCl浓度越大,影响(4)针对产生上述影响的可能原因,学习小组同学提出以下猜想:
猜想①:
 产生的影响。
产生的影响。猜想②:
 产生的影响。
产生的影响。猜想③:
实验Ⅲ.探究盐对
 和
和 平衡体系产生的影响
平衡体系产生的影响资料信息:
a.溶液中的离子会受到周围带有异性电荷离子的屏蔽,使该离子的有效浓度降低,这种影响称为盐效应。
b.在
 溶液中存在反应
溶液中存在反应 。
。(5)根据上述信息,学习小组同学各取2 mL溶液X,分别加入5滴①去离子水、②0.3 mol⋅L
 KCl溶液、③0.3 mol⋅L
KCl溶液、③0.3 mol⋅L NaCl溶液、④0.3 mol⋅L
NaCl溶液、④0.3 mol⋅L
 溶液、⑤3 mol⋅L
溶液、⑤3 mol⋅L HCl溶液进行实验,测得各溶液的透射率随时间的变化如图所示。
HCl溶液进行实验,测得各溶液的透射率随时间的变化如图所示。
上述实验能证明阳离子盐效应影响
 平衡体系的实验组是
平衡体系的实验组是A.实验①②③ B.实验①②④ C.实验①③④
(6)解释出现实验⑤现象的原因:
您最近一年使用:0次
2023-05-21更新
|
327次组卷
|
2卷引用:山东省泰安市2023届高三下学期三模化学试题
2 .  是制备新能源汽车钴酸锂电池的重要原料。某化学学习小组设计如图实验装置制备
是制备新能源汽车钴酸锂电池的重要原料。某化学学习小组设计如图实验装置制备 ,并探究其有关性质。
,并探究其有关性质。

已知:ⅰ.无水 为蓝色,易溶于水及乙醇等有机溶剂。
为蓝色,易溶于水及乙醇等有机溶剂。
ⅱ. 常用作吸水剂,遇水剧烈水解生成
常用作吸水剂,遇水剧烈水解生成 和
和 ,其熔点
,其熔点 ,沸点
,沸点 ,
, 以上时易分解。
以上时易分解。
回答下列问题:
(1)仪器a的名称是_______ 。
(2)滴加 ,一段时间后容器A中充满白雾,发生反应的化学方程式为
,一段时间后容器A中充满白雾,发生反应的化学方程式为_______ 。
(3)无水 的作用是
的作用是_______ 。
(4)将A中反应混合物隔绝空气减压蒸馏,得到无水 晶体。下列装置适合作为冷凝和接收装置的是
晶体。下列装置适合作为冷凝和接收装置的是_______ (填序号)。

(5)某同学向无水氯化钴中加入95%乙醇溶液,得到蓝色溶液,滴加蒸馏水溶液由蓝色变为粉红色【查阅资料得知 为蓝色、
为蓝色、 为粉红色】。
为粉红色】。
①变色过程中发生反应的离子方程式为_______ 。
②资料显示变色反应为可逆反成,请选取合适试剂设计实验进行证明,简述实验方案_______ (可进用的试剂,浓盐酸、蒸馏水、稀硫酸)。
 是制备新能源汽车钴酸锂电池的重要原料。某化学学习小组设计如图实验装置制备
是制备新能源汽车钴酸锂电池的重要原料。某化学学习小组设计如图实验装置制备 ,并探究其有关性质。
,并探究其有关性质。
已知:ⅰ.无水
 为蓝色,易溶于水及乙醇等有机溶剂。
为蓝色,易溶于水及乙醇等有机溶剂。ⅱ.
 常用作吸水剂,遇水剧烈水解生成
常用作吸水剂,遇水剧烈水解生成 和
和 ,其熔点
,其熔点 ,沸点
,沸点 ,
, 以上时易分解。
以上时易分解。回答下列问题:
(1)仪器a的名称是
(2)滴加
 ,一段时间后容器A中充满白雾,发生反应的化学方程式为
,一段时间后容器A中充满白雾,发生反应的化学方程式为(3)无水
 的作用是
的作用是(4)将A中反应混合物隔绝空气减压蒸馏,得到无水
 晶体。下列装置适合作为冷凝和接收装置的是
晶体。下列装置适合作为冷凝和接收装置的是
(5)某同学向无水氯化钴中加入95%乙醇溶液,得到蓝色溶液,滴加蒸馏水溶液由蓝色变为粉红色【查阅资料得知
 为蓝色、
为蓝色、 为粉红色】。
为粉红色】。①变色过程中发生反应的离子方程式为
②资料显示变色反应为可逆反成,请选取合适试剂设计实验进行证明,简述实验方案
您最近一年使用:0次
名校
3 . 研究发现 时,
时, 表面易脱除O原子形成
表面易脱除O原子形成 (氧空穴)。氧空穴越多,催化效果越好,
(氧空穴)。氧空穴越多,催化效果越好, 催化
催化 和
和 合成甲醇的机理如图。下列说法错误的是
合成甲醇的机理如图。下列说法错误的是
 时,
时, 表面易脱除O原子形成
表面易脱除O原子形成 (氧空穴)。氧空穴越多,催化效果越好,
(氧空穴)。氧空穴越多,催化效果越好, 催化
催化 和
和 合成甲醇的机理如图。下列说法错误的是
合成甲醇的机理如图。下列说法错误的是
| A.温度较低时.催化剂的活性降低 |
B.增加 的用量, 的用量, 的平衡转化率不变 的平衡转化率不变 |
C.增大气体流速带走多余的 ,可提高催化效率 ,可提高催化效率 |
D.若 和 和 的混合气中混有 的混合气中混有 的催化效果增强 的催化效果增强 |
您最近一年使用:0次
2024-05-21更新
|
110次组卷
|
2卷引用:2024届山东省高三下学期联合模拟考试模拟预测化学试题
4 . 只要善于观察和发现,化学之美随处可见。下列说法错误的是
| A.“日照香炉生紫烟”涉及胶体的丁达尔效应 |
| B.石蕊遇到碱性溶液变为蓝色与平衡移动有关 |
| C.五彩缤纷的烟花,是电子由基态跃迁到激发态时,能量以光的形式释放出来 |
| D.晶莹剔透的大块水晶是由熔融态的二氧化硅缓慢冷却得到的 |
您最近一年使用:0次
名校
解题方法
5 . 相变离子液体体系因节能潜力大被认为是新一代 吸收剂,某新型相变离子液体X吸收
吸收剂,某新型相变离子液体X吸收 的过程如图,已知X的阴离子中所有原子共平面,下列说法错误的是
的过程如图,已知X的阴离子中所有原子共平面,下列说法错误的是
 吸收剂,某新型相变离子液体X吸收
吸收剂,某新型相变离子液体X吸收 的过程如图,已知X的阴离子中所有原子共平面,下列说法错误的是
的过程如图,已知X的阴离子中所有原子共平面,下列说法错误的是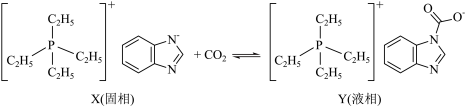
| A.X的阳离子中所有原子(除H外)均达到最外层8电子稳定状态 |
B.真空条件下有利于Y解析出 |
| C.X的阴离子中所有N均提供2个电子参与大π键的形成 |
| D.Y的熔点比X的低,可推知阴离子半径:Y>X |
您最近一年使用:0次
2024-04-07更新
|
424次组卷
|
3卷引用:2024届山东省泰安肥城市高考仿真模拟(二)化学试题
6 . 已知 ,在酸化的KI溶液中通入
,在酸化的KI溶液中通入 ,观察到溶液变为棕色并出现混浊,继续通入
,观察到溶液变为棕色并出现混浊,继续通入 ,直到溶液棕色恰好褪去,发生的反应分别为:
,直到溶液棕色恰好褪去,发生的反应分别为: ,
, ,下列说法错误的是
,下列说法错误的是
 ,在酸化的KI溶液中通入
,在酸化的KI溶液中通入 ,观察到溶液变为棕色并出现混浊,继续通入
,观察到溶液变为棕色并出现混浊,继续通入 ,直到溶液棕色恰好褪去,发生的反应分别为:
,直到溶液棕色恰好褪去,发生的反应分别为: ,
, ,下列说法错误的是
,下列说法错误的是A. 和水在KI的催化下可以发生氧化还原反应 和水在KI的催化下可以发生氧化还原反应 |
| B.物质的氧化性或还原性强弱与浓度有关 |
C.整个过程中被氧化的 和被还原的 和被还原的 物质的量比为1:2 物质的量比为1:2 |
| D.配制碘酒时可以加入一定量KI |
您最近一年使用:0次
名校
解题方法
7 .  的配位化合物较稳定且运用广泛。它可与
的配位化合物较稳定且运用广泛。它可与 、
、 、
、 、
、 等形成配离子使溶液显色。如:显浅紫色的
等形成配离子使溶液显色。如:显浅紫色的 、红色的
、红色的 、黄色的
、黄色的 、无色的
、无色的 。某同学按如下步骤完成实验:
。某同学按如下步骤完成实验:

已知 与
与 、
、 在溶液中存在以下平衡:
在溶液中存在以下平衡: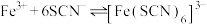 (红色);
(红色);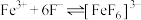 (无色)。
(无色)。
下列说法不正确的是
 的配位化合物较稳定且运用广泛。它可与
的配位化合物较稳定且运用广泛。它可与 、
、 、
、 、
、 等形成配离子使溶液显色。如:显浅紫色的
等形成配离子使溶液显色。如:显浅紫色的 、红色的
、红色的 、黄色的
、黄色的 、无色的
、无色的 。某同学按如下步骤完成实验:
。某同学按如下步骤完成实验:
已知
 与
与 、
、 在溶液中存在以下平衡:
在溶液中存在以下平衡: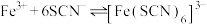 (红色);
(红色);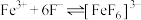 (无色)。
(无色)。下列说法不正确的是
A.Ⅰ中溶液呈黄色可能是由 水解产物的颜色引起的 水解产物的颜色引起的 |
B. 与 与 的配位能力强于 的配位能力强于 |
C.为了能观察到溶液Ⅰ中 的颜色,可向该溶液中加入稀盐酸 的颜色,可向该溶液中加入稀盐酸 |
| D.向溶液Ⅲ中加入足量的KSCN固体,溶液可能再次变为红色 |
您最近一年使用:0次
2023-03-25更新
|
603次组卷
|
8卷引用:山东省菏泽市2023届高三一模考试化学试题
解题方法
8 . 铬与铝性质相似,但活泼性比铝弱、熔点比铝高。下列说法错误的是
| A.可用铝热反应制备铬 |
| B.常温下铬在浓硝酸中发生钝化 |
C.可直接蒸发 溶液制备无水 溶液制备无水 |
D.已知碱性条件下,Cr(Ⅲ)可被氧化为Cr(Ⅵ),则其氧化产物为 |
您最近一年使用:0次
9 . 为探究KSCN的性质进行了如下四个实验:
①向1mL0.15mol·L-1的KSCN溶液中加入1mL0.15mol·L-1FeSO4溶液,无明显现象。
②向①中所得溶液再滴加硫酸酸化的KMnO4溶液,溶液先变红后褪色。
③向1mL 0.15mol·L-1的KSCN溶液中加入1mL 0.05mol·L-1Fe2(SO4)3溶液,溶液变红。
④向③中所得溶液再滴加0.5mL 0.5mol·L-1FeSO4溶液,溶液颜色明显变浅。
下列说法错误的是
①向1mL0.15mol·L-1的KSCN溶液中加入1mL0.15mol·L-1FeSO4溶液,无明显现象。
②向①中所得溶液再滴加硫酸酸化的KMnO4溶液,溶液先变红后褪色。
③向1mL 0.15mol·L-1的KSCN溶液中加入1mL 0.05mol·L-1Fe2(SO4)3溶液,溶液变红。
④向③中所得溶液再滴加0.5mL 0.5mol·L-1FeSO4溶液,溶液颜色明显变浅。
下列说法错误的是
| A.由①和③可得出溶液颜色变红的原因为Fe3+与SCN-生成红色物质 |
| B.由②和③的现象可说明还原性:Fe2+>SCN- |
| C.④中溶液颜色变浅的原因可能是Fe2+也可以与SCN-络合 |
| D.将③中所得溶液分为两等份,分别加入0.5mLH2O、0.5mL 0.5mol·L-1FeSO4溶液,对比二者颜色变化即可确定④中颜色变浅的原因 |
您最近一年使用:0次
名校
10 . 在热带海域中,珊瑚虫在浅海区域分泌石灰石骨骼,与藻类共生形成美丽的珊瑚。下列说法错误的是
A.珊瑚形成的反应为Ca2+ (aq)+2HCO (aq)⇌ CaCO3(s)+ H2O(l)+CO2(aq) (aq)⇌ CaCO3(s)+ H2O(l)+CO2(aq) |
| B.与温带海域相比,热带海域水温较高是利于形成珊瑚的原因之一 |
| C.与深海区域相比,浅海区阳光强烈,藻类光合作用强,更有利于珊瑚形成 |
D.大气中CO2浓度增加,会导致海水中CO 浓度增大,有利于珊瑚形成 浓度增大,有利于珊瑚形成 |
您最近一年使用:0次
2022-01-13更新
|
521次组卷
|
7卷引用:山东省济南市2021-2022学年上学期高三上学期1月学情检测化学试题
山东省济南市2021-2022学年上学期高三上学期1月学情检测化学试题(已下线)一轮巩固卷1-【赢在高考·黄金20卷】备战2022年高考化学模拟卷(广东专用)山东省枣庄市2022-2023学年高二上学期期末考试化学试题2024届内蒙古自治区包头市高三下学期三模理科综合试题-高中化学四川省宜宾市叙州区第一中学校2023-2024学年高二上学期10月月考化学试题(已下线)选择题11-15辽宁省六校协作体2023-2024学年高二上学期12月月考化学试题



