11-12高二上·江苏南通·阶段练习
1 . 在450℃并有催化剂存在下,于一容积恒定的密闭容器内进行下列反应:
2SO2(g)+O2(g) 2SO3(g) △H=―190 kJ·mol—1
2SO3(g) △H=―190 kJ·mol—1
⑴该反应500℃时的平衡常数________ 450℃时的平衡常数(填“>”、“<”或“=”)。
⑵判断该反应达到平衡状态的标志是_______________ 。(填字母)
a.SO2和SO3浓度相等 b.SO2百分含量保持不变
c.容器中气体的压强不变 d.v(O2)正=2v(SO3)逆
e.容器中混合气体的密度保持不变
⑶欲提高SO2的转化率,下列措施可行的是_______________ 。(填字母)
a.向装置中再充入N2 b.向装置中再充入O2
c.改变反应的催化剂 d.升高温度
⑷在一个固定容积为5 L的密闭容器中充入0.20 mol SO2和0.10 mol O2,半分钟后达到平衡,测得容器中含SO30.18 mol;若继续通入0.20 mol SO2和0.10 mol O2,则平衡____________ 移动(填“向正反应方向”、“向逆反应方向”或“不”),再次达到平衡后,______ mol<n(SO3)<______ mol。
2SO2(g)+O2(g)
 2SO3(g) △H=―190 kJ·mol—1
2SO3(g) △H=―190 kJ·mol—1⑴该反应500℃时的平衡常数
⑵判断该反应达到平衡状态的标志是
a.SO2和SO3浓度相等 b.SO2百分含量保持不变
c.容器中气体的压强不变 d.v(O2)正=2v(SO3)逆
e.容器中混合气体的密度保持不变
⑶欲提高SO2的转化率,下列措施可行的是
a.向装置中再充入N2 b.向装置中再充入O2
c.改变反应的催化剂 d.升高温度
⑷在一个固定容积为5 L的密闭容器中充入0.20 mol SO2和0.10 mol O2,半分钟后达到平衡,测得容器中含SO30.18 mol;若继续通入0.20 mol SO2和0.10 mol O2,则平衡
您最近一年使用:0次
10-11高二上·江西九江·阶段练习
2 . 在密闭容器中达到平衡的化学反应N2O4(g) 2NO2(g) △H>0,改变条件,下列说法不正确的是
2NO2(g) △H>0,改变条件,下列说法不正确的是
 2NO2(g) △H>0,改变条件,下列说法不正确的是
2NO2(g) △H>0,改变条件,下列说法不正确的是| A.温度不变体积减小,反应速率增大,再次平衡时混合气颜色变浅 |
| B.温度和体积不变,加入少许NO2,再次平衡时混合气中NO2的百分含量减少 |
| C.体积不变时加入少许N2O4,再度平衡时颜色变深 |
| D.体积不变时升高温度,再次平衡时混合气颜色变深 |
您最近一年使用:0次
11-12高二上·黑龙江·期中
3 . 已建立化学平衡的可逆反应,改变条件使化学平衡向正反应方向移动,下列叙述中正确的是( )
| A.生成物的产量一定增大 | B.生成物的百分含量一定增大 |
| C.反应物的浓度一定降低 | D.每种反应物的转化率一定增大 |
您最近一年使用:0次
2016-12-09更新
|
342次组卷
|
3卷引用:2011-2012年黑龙江哈三中高二上学期期中考试化学(理)试卷
(已下线)2011-2012年黑龙江哈三中高二上学期期中考试化学(理)试卷甘肃省武威第五中学2016-2017学年高二下学期第二次月考化学试题湖南省邵阳市第十一中学2020-2021学年高二上学期期中考试化学试题
2014·重庆·一模
解题方法
4 . 还原沉淀法是处理含铬(含Cr2O72-和CrO42-)工业废水的常用方法,过程如下: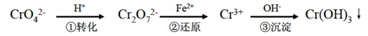
已知转化过程中的反应为2CrO42﹣(aq)+2H+(aq) Cr2O72﹣(aq)+H2O(l)。转化后所得溶液中铬元素的含量为28.6 g/L,CrO42-有10/11转化为Cr2O72-,下列说法不正确的是
Cr2O72﹣(aq)+H2O(l)。转化后所得溶液中铬元素的含量为28.6 g/L,CrO42-有10/11转化为Cr2O72-,下列说法不正确的是
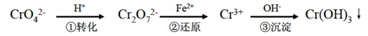
已知转化过程中的反应为2CrO42﹣(aq)+2H+(aq)
 Cr2O72﹣(aq)+H2O(l)。转化后所得溶液中铬元素的含量为28.6 g/L,CrO42-有10/11转化为Cr2O72-,下列说法不正确的是
Cr2O72﹣(aq)+H2O(l)。转化后所得溶液中铬元素的含量为28.6 g/L,CrO42-有10/11转化为Cr2O72-,下列说法不正确的是| A.溶液颜色保持不变,说明上述可逆反应达到平衡状态 |
| B.若用绿矾(FeSO4·7H2O)作还原剂,处理1L废水,至少需要917.4 g |
| C.常温下转化反应的平衡常数K=l×1014.则转化后所得溶液的pH=6 |
| D.常温下Ksp[Cr(OH)3]=1×10-32,要使处理后废水中的c(Cr3+)降至1×10-5mol/L,应调溶液的pH=5 |
您最近一年使用:0次
2016-12-09更新
|
305次组卷
|
12卷引用:2014届重庆南开中学高三二诊模拟考理综化学试卷
(已下线)2014届重庆南开中学高三二诊模拟考理综化学试卷(已下线)2013-2014重庆南开中学高三二诊模拟考理综化学试卷(已下线)2014届重庆南开中学高三二诊模拟考理综化学试卷 2015届黑龙江省哈尔滨六中高三上学期期末化学试卷2015届河北省衡水中学高三下学期三调考试化学试卷2015届山东省济宁市泗水县第一中学高三4月模拟化学试卷辽宁省六校协作体2017-2018学年高二上学期期中考试化学试题2017.11辽宁省六校协作体高二期中化学试卷成都经开区实验中学2017-2018学年度2015级12月月考理科综合(化学)试题2019年秋高三化学复习强化练习—— 与浓度积的相关计算(强化练)夯基提能2020届高三化学选择题对题专练——选修4化学反应原理—— 沉淀溶解平衡及其影响因素 (提升练习)2020届高三化学化学二轮复习——常考题型:浓度积及浓度积常数【精编24题】
10-11高三上·云南昆明·阶段练习
解题方法
5 . X、Y、Z为周期表中前20号主族元素,原子序数递增,X、Y原子的最外层电子数是其电子层数的2倍,Z是人体中含量最高的金属元素。
(1)下列含氧酸根化学式书写不正确的是__________ (填序号)。
a.XO3- b.XO32- c.YO32- d.Y2O32-
(2)X、Y的原子可构成只含极性键的非极性分子,它的电子式是______________ ,空间构型是___________ 。
(3)Y的最高价含氧酸是重要的化工产品。
①已知YO2被空气氧化,每生成1mol气态YO3,放出98.3kJ热量。该反应的热化学方程式是______________ 。
②实验测得相同条件下一定量的Y单质分别在空气和在氧气中充分燃烧后产物的成分(体积分数)如表。Y在纯氧中燃烧的产物中YO3含量比空气中少,试分析其原因_____________ 。
(1)下列含氧酸根化学式书写不正确的是
a.XO3- b.XO32- c.YO32- d.Y2O32-
(2)X、Y的原子可构成只含极性键的非极性分子,它的电子式是
(3)Y的最高价含氧酸是重要的化工产品。
①已知YO2被空气氧化,每生成1mol气态YO3,放出98.3kJ热量。该反应的热化学方程式是
②实验测得相同条件下一定量的Y单质分别在空气和在氧气中充分燃烧后产物的成分(体积分数)如表。Y在纯氧中燃烧的产物中YO3含量比空气中少,试分析其原因
| YO2 | YO3 | |
| 空气 | 94%—95% | 5%—6% |
| 氧气 | 97%—98% | 2%—3% |
您最近一年使用:0次
14-15高三上·上海杨浦·期末
解题方法
6 . 下列事实不能用平衡移动原理解释的是
| 2SO2+O2⇌2SO3的平衡体系中,加入由18O构成的氧气,则SO2中的18O的含量会增加 |  I2(g)+H2(g)⇌2HI(g)加压后颜色加深 | 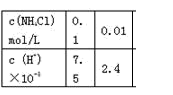 | 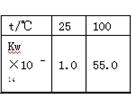 |
| A | B | C | D |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2014-02-28更新
|
403次组卷
|
3卷引用:2014届上海市杨浦区高三上学期期末学业质量调研化学试卷
11-12高二上·河南驻马店·期中
7 . 已经建立化学平衡的某可逆反应,当条件改变时化学平衡向正反应方向移动,下列叙述正确的是①生成物的质量分数一定增加 ②生成物的产量一定增加 ③反应物的转化率一定增加 ④反应物的浓度一定减小 ⑤正反应速率一定比逆反应速率大
| A.①②③④⑤ | B.②④⑤ | C.②⑤ | D.⑤ |
您最近一年使用:0次



