1 . 5 mL 0.1mol·L−1KI溶液与10 mL 0.1 mol·L−1FeCl3溶液发生反应:2Fe3+(aq)+2I−(aq) 2Fe2+(aq)+I2(aq),达到平衡。下别说法不正确的是
2Fe2+(aq)+I2(aq),达到平衡。下别说法不正确的是
 2Fe2+(aq)+I2(aq),达到平衡。下别说法不正确的是
2Fe2+(aq)+I2(aq),达到平衡。下别说法不正确的是| A.加入一定量铁粉,平衡逆向移动 |
| B.向该水溶液中加入CCl4,振荡,平衡正向移动 |
| C.经过CCl4多次萃取分离后,向水溶液中滴加KSCN溶液,若溶液出现血红色,证明该化学反应存在限度 |
D.该反应的平衡常数K= |
您最近一年使用:0次
名校
2 . 为探究浓度对化学平衡的影响,某同学进行如下实验:下列说法不正确 的是
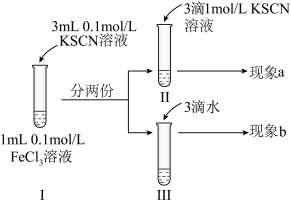

| A.该实验通过观察颜色变化以判断生成物浓度的变化 |
| B.观察到现象a比现象b中红色更深,即可证明增加反应物浓度,平衡正向移动 |
| C.进行II、III对比实验的主要目的是防止由于溶液体积变化引起各离子浓度变化而干扰实验结论得出 |
| D.若I中加入KSCN溶液的体积改为2mL也可以达到实验目的 |
您最近一年使用:0次
2020-07-09更新
|
269次组卷
|
7卷引用:北京市延庆区2019-2020学年高二下学期期末考试化学试题
北京市延庆区2019-2020学年高二下学期期末考试化学试题(已下线)第19讲 化学平衡 (练) — 2022年高考化学一轮复习讲练测(新教材新高考)湖南省长沙市长郡中学2021-2022学年高二上学期第一次月考化学试题(已下线)考向22 化学平衡状态 化学平衡的移动-备战2022年高考化学一轮复习考点微专题(已下线)第19讲 化学平衡(练)-2023年高考化学一轮复习讲练测(新教材新高考)河南省商丘名校联盟2022-2023学年高二上学期期中考试化学试题河南省兰考县第一高级中学2022-2023学年高二上学期期中考试化学试题
名校
3 . 将5 mL 0.005 mol/L FeCl3溶液和5 mL 0.015 mol/L KSCN溶液混合,达到平衡后呈红色。再将混合液分为5份,分别进行如下实验:

下列说法不正确的是

下列说法不正确的是
| A.对比实验①和②,为了证明增加反应物浓度,平衡发生正向移动 |
| B.对比实验①和③,为了证明增加反应物浓度,平衡发生逆向移动 |
| C.对比实验①和④,为了证明增加反应物浓度,平衡发生正向移动 |
| D.对比实验①和⑤,为了证明减少反应物浓度,平衡发生逆向移动 |
您最近一年使用:0次
2018-11-13更新
|
244次组卷
|
7卷引用:【区级联考】北京市海淀区2019届高三第一学期期中考试化学试题
【区级联考】北京市海淀区2019届高三第一学期期中考试化学试题四川省广安市邻水实验学校2018-2019学年高二上学期第三次月考化学试题【校级联考】甘肃省民乐一中、张掖二中2019届高三上学期第一次调研考试(12月)理科综合化学试题福建省南安第一中学2019-2020学年高二上学期第一次阶段考试化学试题四川省邻水市实验中学2019-2020学年高二12月月考化学试题(已下线)2019年12月25日《每日一题》人教版(选修4)—— 影响化学平衡的因素(已下线)2.3.1 浓度对化学平衡的影响(重点练)——2020-2021学年高二化学上学期十分钟同步课堂专练(苏教版选修4)
名校
4 . 新制氢氧化铜存在平衡:Cu(OH)2 +2OH-⇌ (深蓝色)。某同学进行下列实验:
(深蓝色)。某同学进行下列实验:
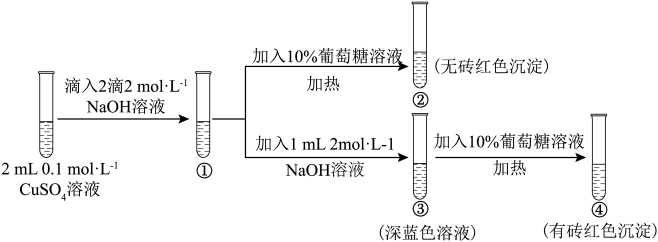
下列说法不正确 的是
 (深蓝色)。某同学进行下列实验:
(深蓝色)。某同学进行下列实验:
下列说法
| A.①中出现蓝色沉淀 |
B.③中现象是Cu(OH)2 +2OH-⇌ 正向移动的结果 正向移动的结果 |
| C.④中现象证明葡萄糖具有还原性 |
D.对比②和④可知Cu(OH)2氧化性强于 |
您最近一年使用:0次
2017-02-17更新
|
742次组卷
|
10卷引用:2017届北京市海淀区高三上学期期末化学试卷
2017届北京市海淀区高三上学期期末化学试卷【全国百强校】北京师范大学附属中学2017-2018学年高二下学期期中考试化学试题【全国百强校】北京101中学2017-2018学年高二下学期期中考试化学试题四川省双流中学2018-2019学年高二6月月考化学试题安徽省定远县育才学校2019-2020学年高二下学期期末考试化学试题(已下线)2.3.1 浓度对化学平衡的影响(基础练)——2020-2021学年高二化学上学期十分钟同步课堂专练(苏教版选修4)湖南省常德市一中2020-2021学年高二上学期期末考试化学试题北京市中央民族大学附属中学2022届高三9月月考化学试题第四章 生物大分子(已下线)考点12 金属材料(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(新高考专用)
11-12高一下·山西临汾·期中
5 . 判断下列说法是否正确。
1.一个D2O分子所含的中子数为8。_______
2.HI、HBr、HCl、HF的稳定性依次增强。_______
3.同主族元素从上到下,单质的熔点逐渐降低。_______
4.常温下Na与足量O2反应生成Na2O,随温度升高生成Na2O的速率逐渐加快。_______
5.从能量角度看,断开化学键要放热,形成化学键要吸热。一个化学反应是释放能量,还是吸收能量,取决于二者的相对大小。_______
6.将锌片和铜片用导线连接,并平行插入稀硫酸中,由于锌片是负极,所以溶液中的H+向负极迁移。_______
7.在二氧化硫与氧气的反应中,适当提高氧气浓度,可提高二氧化硫的转化率。_______
8.二氯甲烷没有同分异构体,证明甲烷分子具有正四面体结构。_______
9.用点燃或通入酸性高锰酸钾溶液中的方法均可以鉴别甲烷和乙烯。_______
10.苯不与酸性高锰酸钾溶液、溴水发生反应,证明苯不具有类似乙烯中的双键。_______
1.一个D2O分子所含的中子数为8。
2.HI、HBr、HCl、HF的稳定性依次增强。
3.同主族元素从上到下,单质的熔点逐渐降低。
4.常温下Na与足量O2反应生成Na2O,随温度升高生成Na2O的速率逐渐加快。
5.从能量角度看,断开化学键要放热,形成化学键要吸热。一个化学反应是释放能量,还是吸收能量,取决于二者的相对大小。
6.将锌片和铜片用导线连接,并平行插入稀硫酸中,由于锌片是负极,所以溶液中的H+向负极迁移。
7.在二氧化硫与氧气的反应中,适当提高氧气浓度,可提高二氧化硫的转化率。
8.二氯甲烷没有同分异构体,证明甲烷分子具有正四面体结构。
9.用点燃或通入酸性高锰酸钾溶液中的方法均可以鉴别甲烷和乙烯。
10.苯不与酸性高锰酸钾溶液、溴水发生反应,证明苯不具有类似乙烯中的双键。
您最近一年使用:0次
名校
6 . 已知重铬酸钾(K2Cr2O7)溶液中存在如下平衡: (橙色)+ H2O⇌2H++ 2
(橙色)+ H2O⇌2H++ 2 (黄色)
(黄色)
①向2 mL 0.1 mol·L-1 K2Cr2O7溶液中滴入3滴6 mol·L-1 NaOH溶液,溶液由橙色变为黄色;向所得溶液中再滴入5滴浓H2SO4,溶液由黄色变为橙色。
②向2 mL 0.1 mol·L-1 酸化的K2Cr2O7溶液中滴入适量(NH4)2Fe(SO4)2溶液,溶液由橙色变为绿色,发生反应: + 14H++ 6Fe2+=2Cr3+(绿色) + 6Fe3+ + 7H2O。
+ 14H++ 6Fe2+=2Cr3+(绿色) + 6Fe3+ + 7H2O。
下列分析正确的是
 (橙色)+ H2O⇌2H++ 2
(橙色)+ H2O⇌2H++ 2 (黄色)
(黄色)①向2 mL 0.1 mol·L-1 K2Cr2O7溶液中滴入3滴6 mol·L-1 NaOH溶液,溶液由橙色变为黄色;向所得溶液中再滴入5滴浓H2SO4,溶液由黄色变为橙色。
②向2 mL 0.1 mol·L-1 酸化的K2Cr2O7溶液中滴入适量(NH4)2Fe(SO4)2溶液,溶液由橙色变为绿色,发生反应:
 + 14H++ 6Fe2+=2Cr3+(绿色) + 6Fe3+ + 7H2O。
+ 14H++ 6Fe2+=2Cr3+(绿色) + 6Fe3+ + 7H2O。下列分析正确的是
| A.实验①和②均能证明K2Cr2O7溶液中存在上述平衡 |
B.实验②能说明氧化性: >Fe3+ >Fe3+ |
C. 和Fe2+在酸性溶液中可以大量共存 和Fe2+在酸性溶液中可以大量共存 |
| D.向K2Cr2O7溶液中加入水时,平衡不移动 |
您最近一年使用:0次
名校
解题方法
7 . 下列实验不能 达到预期实验目的是
| 实验内容 | 实验目的 | |
| A | KI淀粉溶液中滴入氯水变蓝,再通入SO2,蓝色褪去 | 证明SO2具有氧化性 |
| B | 将氯化铁晶体溶解于少量浓盐酸中,再加水稀释 | 配制氯化铁溶液 |
| C | 向5mL0.1mol·L-1的K2Cr2O7溶液两支试管中分别滴加浓H2SO4和5mol·L-1的NaOH溶液,观察并记录两支试管溶液颜色的变化 | 探究浓度对化学平衡的影响 |
| D | 其他条件相同,测定等浓度的CH3COONa和NaClO溶液的pH | 比较Ka(CH3COOH)和Ka(HClO)的大小 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
8 . 下列实验方案不能达到相应目的的是
| A | B | C | D | |
| 目的 | 探究温度对化学平衡的影响 | 研究浓度对化学平衡的影响 | 实现铜棒镀银 | 证明化学反应存在一定的限度 |
| 实验方案 | 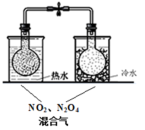 | 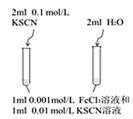 | 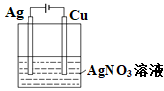 | 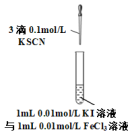 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2020-11-13更新
|
277次组卷
|
4卷引用:北京市一零一中学2020-2021学年高二上学期期中考试化学试题
名校
解题方法
9 . 为验证氧化性Cl2 > Fe3+ > SO2,某小组用下图所示装置进行实验(夹持仪器和A中加热装置已略,气密性已检验)。

实验过程:
I.打开弹簧夹K1~K4,通入一段时间N2,再将T型导管插入B中,继续通入N2,然后关闭K1、K3、K4。
Ⅱ.打开活塞a,滴加一定量的浓盐酸,给A加热。
Ⅲ.当B中溶液变黄时,停止加热,夹紧弹簧夹K2。
Ⅳ.打开活塞b,使约2mL的溶液流入D试管中,检验其中的离子。
Ⅴ.打开弹簧夹K3、活塞c,加入70%的硫酸,一段时间后夹紧弹簧夹K3。
Ⅵ.更新试管D,重复过程Ⅳ,检验B溶液中的离子。
(1)过程Ⅰ的目的是_________________________________________________ 。
(2)棉花中浸润的溶液为________________________ 。
(3)A中发生反应的化学方程式为_______________________________________ 。
(4)过程Ⅴ中,B溶液中发生反应的离子方程式是_______________________________ 。
(5)甲、乙、丙三位同学分别完成了上述实验,他们的检测结果一定能够证明氧化性Cl2 > Fe3+ >SO2的是____________________ (填“甲”“乙”“丙”)。
(6)进行实验过程Ⅴ时,B中溶液颜色由黄色逐渐变为红棕色,停止通气,放置一段时间后溶液颜色变为浅绿色。查阅资料:Fe2+(aq) +  (aq)
(aq) FeSO3(s)(墨绿色)。
FeSO3(s)(墨绿色)。
提出假设:FeCl3与 SO2的反应经历了中间产物FeSO3,溶液的红棕色是FeSO3(墨绿色)与FeCl3(黄色)的混合色。某同学设计如下实验,证实该假设成立:

①溶液E为__________________ 。
②请用化学平衡原理解释步骤3中红棕色溶液颜色变为浅绿色的原因_____________

实验过程:
I.打开弹簧夹K1~K4,通入一段时间N2,再将T型导管插入B中,继续通入N2,然后关闭K1、K3、K4。
Ⅱ.打开活塞a,滴加一定量的浓盐酸,给A加热。
Ⅲ.当B中溶液变黄时,停止加热,夹紧弹簧夹K2。
Ⅳ.打开活塞b,使约2mL的溶液流入D试管中,检验其中的离子。
Ⅴ.打开弹簧夹K3、活塞c,加入70%的硫酸,一段时间后夹紧弹簧夹K3。
Ⅵ.更新试管D,重复过程Ⅳ,检验B溶液中的离子。
(1)过程Ⅰ的目的是
(2)棉花中浸润的溶液为
(3)A中发生反应的化学方程式为
(4)过程Ⅴ中,B溶液中发生反应的离子方程式是
(5)甲、乙、丙三位同学分别完成了上述实验,他们的检测结果一定能够证明氧化性Cl2 > Fe3+ >SO2的是
| 过程ⅣB溶液中含有的离子 | 过程Ⅵ B溶液中含有的离子 | |
| 甲 | 有Fe3+无Fe2+ | 有 |
| 乙 | 既有Fe3+又有Fe2+ | 有 |
| 丙 | 有Fe3+无Fe2+ | 有Fe2+ |
 (aq)
(aq) FeSO3(s)(墨绿色)。
FeSO3(s)(墨绿色)。提出假设:FeCl3与 SO2的反应经历了中间产物FeSO3,溶液的红棕色是FeSO3(墨绿色)与FeCl3(黄色)的混合色。某同学设计如下实验,证实该假设成立:

①溶液E为
②请用化学平衡原理解释步骤3中红棕色溶液颜色变为浅绿色的原因
您最近一年使用:0次
2020-12-02更新
|
280次组卷
|
3卷引用:甘肃省白银市会宁县第四中学2021届高三上学期第三次月考化学试题
解题方法
10 . 下列实验中能达到预期实验目的的是
实验操作 | 预期实验目的 | |
A | 分别加热Fe2(SO4)3溶液和FeCl3溶液 | 得到Fe2(SO4)3和FeCl3固体 |
B | 在室温下分别向2支盛有4.0mL浓度为0.01mol/LKMnO4溶液的试管中同时加入2.0mL浓度分别为0.10mol/L和0.20mol/L的H2C2O4溶液,观察实验现象 | 探究浓度对化学反应速率的影响 |
C | 向盛有5.0mL0.005mol/LFeCl3溶液中加入5.0mL0.01mol/LKSCN溶液,再继续加入少量KCl固体 | 证明溶液中存在平衡:Fe3++3SCN-⇌Fe(SCN)3 |
D | 用玻璃棒蘸取少量0.1mol/LNaClO溶液,滴在pH试纸上 | 测定0.1mol/LNaClO溶液的pH |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次



