1 . 乙醇催化合成乙酸乙酯的新方法为: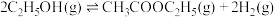 。在2L密闭容器中充入
。在2L密闭容器中充入
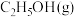 发生反应,乙醇的转化率
发生反应,乙醇的转化率 变化如图所示。下列分析正确的是
变化如图所示。下列分析正确的是
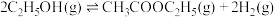 。在2L密闭容器中充入
。在2L密闭容器中充入
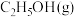 发生反应,乙醇的转化率
发生反应,乙醇的转化率 变化如图所示。下列分析正确的是
变化如图所示。下列分析正确的是
| A.降低温度,有利于提高乙醇的平衡转化率 |
B.230℃,该反应的平衡常数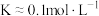 |
C.m、n两点中,乙酸乙酯的浓度均为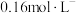 |
| D.反应在230℃、恒压容器中进行,达平衡时,乙醇的转化率小于48% |
您最近一年使用:0次
2 . 反应;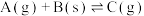
 ,在其他条件不变时,改变其中一个条件,则生成
,在其他条件不变时,改变其中一个条件,则生成 的速率(填“增大”、“不变”、“减小”):
的速率(填“增大”、“不变”、“减小”):
(1)升温_______ 。
(2)使用催化剂_______ 。
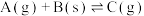
 ,在其他条件不变时,改变其中一个条件,则生成
,在其他条件不变时,改变其中一个条件,则生成 的速率(填“增大”、“不变”、“减小”):
的速率(填“增大”、“不变”、“减小”):(1)升温
(2)使用催化剂
您最近一年使用:0次
解题方法
3 . 工业上采用高温活性炭催化CO与C12合成光气(COCl2)。T℃时,向2L刚性密闭容器中充入2molCO气体、2molCl2气体和适量的活性炭,发生反应:CO(g)+Cl2(g) COCl2(g)
COCl2(g)  H<0,测得混合气中COCl2的体积分数
H<0,测得混合气中COCl2的体积分数 (COCl2)随时间t的关系如图曲线I所示。下列说法正确的是
(COCl2)随时间t的关系如图曲线I所示。下列说法正确的是
 COCl2(g)
COCl2(g)  H<0,测得混合气中COCl2的体积分数
H<0,测得混合气中COCl2的体积分数 (COCl2)随时间t的关系如图曲线I所示。下列说法正确的是
(COCl2)随时间t的关系如图曲线I所示。下列说法正确的是
A.当体系中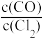 保持不变,则该反应达到化学平衡状态 保持不变,则该反应达到化学平衡状态 |
| B.曲线Ⅱ相对曲线I改变的条件可能升高温度 |
| C.A点时,向容器中加入等物质的量CO和Cl2,反应速率减小 |
| D.A点CO的转化率为60% |
您最近一年使用:0次
4 . 一定温度下,将1molA和1molB气体充入2L密闭容器,发生反应A(g)+B(g) 2C(g)+D(s),t1时达到平衡,在t2、t3时刻分别改变反应的一个条件,测得容器中气体C的浓度随时间变化如图所示,下列说法正确的是
2C(g)+D(s),t1时达到平衡,在t2、t3时刻分别改变反应的一个条件,测得容器中气体C的浓度随时间变化如图所示,下列说法正确的是
 2C(g)+D(s),t1时达到平衡,在t2、t3时刻分别改变反应的一个条件,测得容器中气体C的浓度随时间变化如图所示,下列说法正确的是
2C(g)+D(s),t1时达到平衡,在t2、t3时刻分别改变反应的一个条件,测得容器中气体C的浓度随时间变化如图所示,下列说法正确的是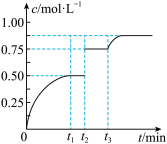
| A.若t1=2min,则v(D)=0.125mol/(L·min) |
| B.t2时刻改变的条件是增加等物质的量的A和B |
| C.t1时刻后向体系中再充入A、B、C各1mol,则v正>v逆 |
| D.若t3时刻改变的条件是升温,则该反应是放热反应 |
您最近一年使用:0次
解题方法
5 . “氢经济”是“双碳”转型中非常关键的一环。大量安全制空是关键技术之一。
方法一:甲烷-水蒸气催化重整法。其涉及的主要反应如下:
反应I:

反应Ⅱ:
(1)反应 能自发进行的条件是
能自发进行的条件是________ (填“高温”“低温”或“任何温度下”)
(2)为了提高 的平衡转化率,同时提高CO的浓度,可以采取的措施是________(填字母)。
的平衡转化率,同时提高CO的浓度,可以采取的措施是________(填字母)。
(3)恒定压强为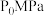 时,将
时,将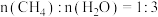 的混合气体投入反应器中发生反应I和Ⅱ,平衡时,各组分的物质的量分数与温度的关系如图所示。
的混合气体投入反应器中发生反应I和Ⅱ,平衡时,各组分的物质的量分数与温度的关系如图所示。 的物质的量分数与温度的变化曲线是
的物质的量分数与温度的变化曲线是________ (填字母)。
②系统中 的含量在700℃左右出现峰值,试从化学平衡的角度解释出现峰值的原因:
的含量在700℃左右出现峰值,试从化学平衡的角度解释出现峰值的原因:________ 。
③600℃时,计算反应Ⅱ的平衡常数
________ ( 是以分压表示的平衡常数,分压=总压
是以分压表示的平衡常数,分压=总压 物质的量分数,结果可用分数表示)。
物质的量分数,结果可用分数表示)。
方法二:甲醇催化脱空法。催化反应的部分机理如下:
历程i: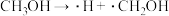 历程ii:
历程ii: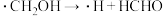
历程iii: 历程iv:
历程iv: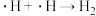
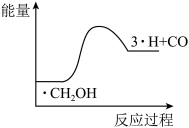
(4)在一个2L恒容密闭容器中投入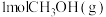 ,20min后,测得甲醇的转化率(X)与甲醛的选择性(S)分别与温度的关系如左图所示。700℃时,历程iii能量~反应过程如右图所示,在图上画出历程ii的“能量~反应过程”示意图
,20min后,测得甲醇的转化率(X)与甲醛的选择性(S)分别与温度的关系如左图所示。700℃时,历程iii能量~反应过程如右图所示,在图上画出历程ii的“能量~反应过程”示意图________ 。
方法一:甲烷-水蒸气催化重整法。其涉及的主要反应如下:
反应I:


反应Ⅱ:

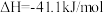
(1)反应
 能自发进行的条件是
能自发进行的条件是(2)为了提高
 的平衡转化率,同时提高CO的浓度,可以采取的措施是________(填字母)。
的平衡转化率,同时提高CO的浓度,可以采取的措施是________(填字母)。| A.使用高效催化剂 | B.升高温度 |
| C.增大压强 | D.增大 和 和 物质的量之比 物质的量之比 |
(3)恒定压强为
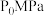 时,将
时,将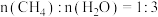 的混合气体投入反应器中发生反应I和Ⅱ,平衡时,各组分的物质的量分数与温度的关系如图所示。
的混合气体投入反应器中发生反应I和Ⅱ,平衡时,各组分的物质的量分数与温度的关系如图所示。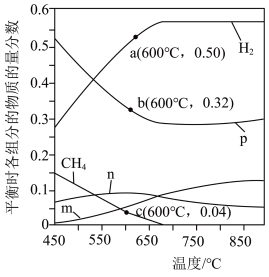
 的物质的量分数与温度的变化曲线是
的物质的量分数与温度的变化曲线是②系统中
 的含量在700℃左右出现峰值,试从化学平衡的角度解释出现峰值的原因:
的含量在700℃左右出现峰值,试从化学平衡的角度解释出现峰值的原因:③600℃时,计算反应Ⅱ的平衡常数

 是以分压表示的平衡常数,分压=总压
是以分压表示的平衡常数,分压=总压 物质的量分数,结果可用分数表示)。
物质的量分数,结果可用分数表示)。方法二:甲醇催化脱空法。催化反应的部分机理如下:
历程i:
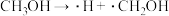 历程ii:
历程ii: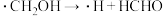
历程iii:
 历程iv:
历程iv: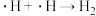
(4)在一个2L恒容密闭容器中投入
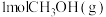 ,20min后,测得甲醇的转化率(X)与甲醛的选择性(S)分别与温度的关系如左图所示。700℃时,历程iii能量~反应过程如右图所示,在图上画出历程ii的“能量~反应过程”示意图
,20min后,测得甲醇的转化率(X)与甲醛的选择性(S)分别与温度的关系如左图所示。700℃时,历程iii能量~反应过程如右图所示,在图上画出历程ii的“能量~反应过程”示意图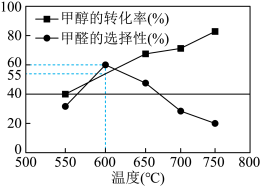
您最近一年使用:0次
6 . 下列事实中,不能用勒夏特列原理解释的是
| A.打开可乐饮料后会产生大量气泡 |
B.“ ”球浸泡在热水中,颜色变深 ”球浸泡在热水中,颜色变深 |
C.工业合成氨时采用500℃的高温(已知该反应 ) ) |
D.加水稀释 溶液,其电离程度增大 溶液,其电离程度增大 |
您最近一年使用:0次
7 . 下列说法不正确的是:
A.反应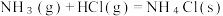 在低温下能自发进行,则该反应的△H>0 在低温下能自发进行,则该反应的△H>0 |
| B.对于2A(g)+B(g)⇌2C(g)△H>0,当温度升高时,平衡向正反应方向移动,V正和V逆均增大 |
| C.对于2A(g)+B(g)⇌2C(g)△H>0,增大A的浓度,平衡向正反应方向移动,V正和V逆均增大 |
| D.升高温度或加入催化剂能使单 |
您最近一年使用:0次
8 . 研发二氧化碳的利用技术,将二氧化碳转化为能源是减轻环境污染和解决能源问题的方案之一、回答下列问题:
(1)利用CO2合成二甲醚有两种工艺。
工艺1:
涉及以下主要反应:
反应Ⅰ.甲醇的合成:CO2(g)+3H2(g) CH3OH(g)+H2O(g) △H1=-49.0kJ/mol
CH3OH(g)+H2O(g) △H1=-49.0kJ/mol
反应Ⅱ.逆水汽变换:CO2(g)+H2(g) CO(g)+H2O(g) △H2=+41.0kJ/mol
CO(g)+H2O(g) △H2=+41.0kJ/mol
反应Ⅲ.甲醇脱水:2CH3OH(g) CH3OCH3(g)+H2O(g) △H3=-23.5kJ/mol
CH3OCH3(g)+H2O(g) △H3=-23.5kJ/mol
工艺2:反应Ⅳ.2CO2(g)+6H2(g) CH3OCH3(g)+3H2O(g) △H
CH3OCH3(g)+3H2O(g) △H
①△H=___________ kJ/mol,反应Ⅳ在___________ (填“低温”“高温”或“任意温度”)下自发进行。
②反应Ⅳ的活化能Ea(正)___________ (填“>”“<"或“=”)Ea(逆)。
③在恒温恒容的密闭容器中,下列说法能判断反应Ⅳ达到平衡的是___________ (填标号)。
A.气体物质中碳元素与氧元素的质量比不变
B.容器内CH3OCH3浓度保持不变
C.容器内气体密度不变
D.容器内气体的平均摩尔质量不变
(2)在不同压强下,按照n(CO2):n(H2)=1:3投料合成甲醇(反应Ⅰ),实验测得CO2的平衡转化率和CH3OH的平衡产率随温度的变化关系如图甲、乙所示。___________ (填标号)。
A.图甲纵坐标表示CH3OH的平衡产率
B.p1<p2<p3
C.为了同时提高CO2的平衡转化率和CH3OH的平衡产率,应选择低温、高压条件
D.一定温度、压强下,提高CO2的平衡转化率的主要方向是寻找活性更高的催化剂
②图乙中,某温度时,三条曲线几乎交于一点的原因是___________ 。
(3)在T1温度下,将3molCO2和7molH2充入2L的恒容密闭容器中发生反应Ⅰ和Ⅳ,达到平衡状态时CH3OH(g)和CH3OCH3(g)的物质的量分别为1mol和0.5mol。
①反应经过10min达到平衡,0~10min内CO2的平均反应速率v(CO2)=___________ mol/(L·min)。
②T1温度时反应Ⅰ的平衡常数K=___________ 。
(1)利用CO2合成二甲醚有两种工艺。
工艺1:
涉及以下主要反应:
反应Ⅰ.甲醇的合成:CO2(g)+3H2(g)
 CH3OH(g)+H2O(g) △H1=-49.0kJ/mol
CH3OH(g)+H2O(g) △H1=-49.0kJ/mol反应Ⅱ.逆水汽变换:CO2(g)+H2(g)
 CO(g)+H2O(g) △H2=+41.0kJ/mol
CO(g)+H2O(g) △H2=+41.0kJ/mol反应Ⅲ.甲醇脱水:2CH3OH(g)
 CH3OCH3(g)+H2O(g) △H3=-23.5kJ/mol
CH3OCH3(g)+H2O(g) △H3=-23.5kJ/mol工艺2:反应Ⅳ.2CO2(g)+6H2(g)
 CH3OCH3(g)+3H2O(g) △H
CH3OCH3(g)+3H2O(g) △H①△H=
②反应Ⅳ的活化能Ea(正)
③在恒温恒容的密闭容器中,下列说法能判断反应Ⅳ达到平衡的是
A.气体物质中碳元素与氧元素的质量比不变
B.容器内CH3OCH3浓度保持不变
C.容器内气体密度不变
D.容器内气体的平均摩尔质量不变
(2)在不同压强下,按照n(CO2):n(H2)=1:3投料合成甲醇(反应Ⅰ),实验测得CO2的平衡转化率和CH3OH的平衡产率随温度的变化关系如图甲、乙所示。
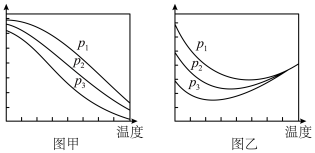
A.图甲纵坐标表示CH3OH的平衡产率
B.p1<p2<p3
C.为了同时提高CO2的平衡转化率和CH3OH的平衡产率,应选择低温、高压条件
D.一定温度、压强下,提高CO2的平衡转化率的主要方向是寻找活性更高的催化剂
②图乙中,某温度时,三条曲线几乎交于一点的原因是
(3)在T1温度下,将3molCO2和7molH2充入2L的恒容密闭容器中发生反应Ⅰ和Ⅳ,达到平衡状态时CH3OH(g)和CH3OCH3(g)的物质的量分别为1mol和0.5mol。
①反应经过10min达到平衡,0~10min内CO2的平均反应速率v(CO2)=
②T1温度时反应Ⅰ的平衡常数K=
您最近一年使用:0次
解题方法
9 . 已知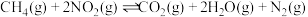
 。在
。在 时,向恒容密闭容器中充入
时,向恒容密闭容器中充入 和
和 发生上述反应,起始时测得总压强为
发生上述反应,起始时测得总压强为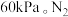 分压与时间关系如图所示。其中,
分压与时间关系如图所示。其中, 为以平衡分压代替平衡浓度表示的平衡常数,分压
为以平衡分压代替平衡浓度表示的平衡常数,分压 总压
总压 物质的量分数。下列说法中错误的是
物质的量分数。下列说法中错误的是
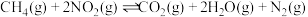
 。在
。在 时,向恒容密闭容器中充入
时,向恒容密闭容器中充入 和
和 发生上述反应,起始时测得总压强为
发生上述反应,起始时测得总压强为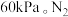 分压与时间关系如图所示。其中,
分压与时间关系如图所示。其中, 为以平衡分压代替平衡浓度表示的平衡常数,分压
为以平衡分压代替平衡浓度表示的平衡常数,分压 总压
总压 物质的量分数。下列说法中错误的是
物质的量分数。下列说法中错误的是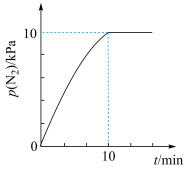
A.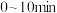 用 用 分压变化表示的速率为 分压变化表示的速率为 |
B.该温度下平衡常数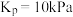 |
C.若改为绝热体系进行,则平衡后 转化率增大 转化率增大 |
D. 时,单位时间内 时,单位时间内 键断裂数目与 键断裂数目与 键形成数目相等 键形成数目相等 |
您最近一年使用:0次
10 . 科学家在 直接转化制备
直接转化制备 的研究中取得重要进展,制备原理为
的研究中取得重要进展,制备原理为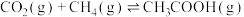 ,已知部分化学键的键能数据如下:
,已知部分化学键的键能数据如下:
下列说法错误的是
 直接转化制备
直接转化制备 的研究中取得重要进展,制备原理为
的研究中取得重要进展,制备原理为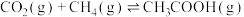 ,已知部分化学键的键能数据如下:
,已知部分化学键的键能数据如下:| 共价键 |  |  |  |  |  |
键能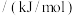 | 413 | 497 | 462 | 351 | 348 |
A.该反应的反应热: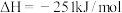 |
B.该反应原子利用率 |
| C.高温高压有利于该反应进行 |
D.若设计成原电池,则正极反应为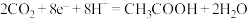 |
您最近一年使用:0次



