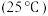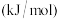1 . 在反应N2(g)+3H2(g) 2NH3(g) △H<0中,既能使反应速率加快又能增大H2转化率的是
2NH3(g) △H<0中,既能使反应速率加快又能增大H2转化率的是
①增大压强 ②升高温度③及时液化移走NH3④通入N2 ⑤通入H2⑥加入催化剂
 2NH3(g) △H<0中,既能使反应速率加快又能增大H2转化率的是
2NH3(g) △H<0中,既能使反应速率加快又能增大H2转化率的是①增大压强 ②升高温度③及时液化移走NH3④通入N2 ⑤通入H2⑥加入催化剂
| A.①②③ | B.①②④ | C.①④ | D.①②⑥ |
您最近一年使用:0次
2 . 烟气脱硫脱硝技术是环境科学研究的热点。某小组模拟O3氧化结合(NH4)2SO3溶液吸收法同时脱除SO2和NO。气体反应器中的主要反应原理及相关数据如下表。
不正确 的是
反应 | 平衡常数 | 活化能/ |
 |  | 24.6 |
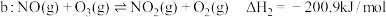 | 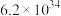 | 3.17 |
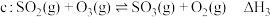 | 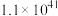 | 58.17 |
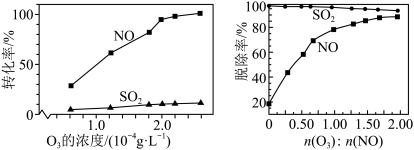
A.已知: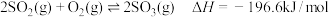 则 则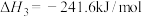 |
| B.其他条件不变,在相同时间内,SO2和NO的转化率均随温度升高而降低 |
| C.其他条件不变,在相同时间内,随O3浓度的升高,NO的转化率远远高于SO2的转化率 |
| D.其他条件不变,在相同时间内,O3的浓度很低时,SO2的脱除率远高于NO的脱除率,因为反应c速率大于反应b |
您最近一年使用:0次
3 . 不同催化剂作用下NH3还原NOx的机理与效果是研究烟气(含NOx、O2、N2等)脱硝的热点。
(1)NH3还原NO的主反应为4NH3(g)+4NO(g)+O2(g)=4N2(g)+6H2O(g)。
已知:N2(g)+O2(g)=2NO(g)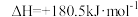 ;4NH3(g)+3O2(g)=2N2(g)+6H2O(g)
;4NH3(g)+3O2(g)=2N2(g)+6H2O(g) 
上述主反应的
____ 。
(2)在某钒催化剂中添加一定量Cu2O可加快NO的脱除效率,其可能机理如图所示(*表示物种吸附在催化剂表面,部分物种未画出)。____ 。
②烟气中若含有SO2,会生成NH4HSO4堵塞催化剂孔道。生成NH4HSO4的化学方程式为____ 。
(3)将模拟烟气(一定比例NOx、NH3、O2和N2)以一定流速通过装有Fe/Zr催化剂的反应管,测得NOx转化率随温度变化的曲线如图所示。_____ 。
②温度高于450℃时,NOx转化率已降低为负值,其可能原因是____ 。
(1)NH3还原NO的主反应为4NH3(g)+4NO(g)+O2(g)=4N2(g)+6H2O(g)。
已知:N2(g)+O2(g)=2NO(g)
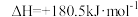 ;4NH3(g)+3O2(g)=2N2(g)+6H2O(g)
;4NH3(g)+3O2(g)=2N2(g)+6H2O(g) 
上述主反应的

(2)在某钒催化剂中添加一定量Cu2O可加快NO的脱除效率,其可能机理如图所示(*表示物种吸附在催化剂表面,部分物种未画出)。
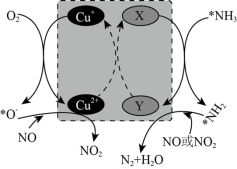
②烟气中若含有SO2,会生成NH4HSO4堵塞催化剂孔道。生成NH4HSO4的化学方程式为
(3)将模拟烟气(一定比例NOx、NH3、O2和N2)以一定流速通过装有Fe/Zr催化剂的反应管,测得NOx转化率随温度变化的曲线如图所示。
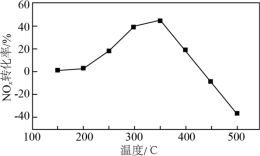
②温度高于450℃时,NOx转化率已降低为负值,其可能原因是
您最近一年使用:0次
解题方法
4 . 在一定条件下的密闭容器中发生反应: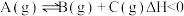 下列措施中,不能提高A的平衡转化率的是
下列措施中,不能提高A的平衡转化率的是
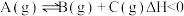 下列措施中,不能提高A的平衡转化率的是
下列措施中,不能提高A的平衡转化率的是| A.恒容条件下通入稀有气体 | B.及时分离出C |
| C.降低反应温度 | D.增大容器的体积 |
您最近一年使用:0次
名校
5 . 脱除汽车尾气中 和
和 包括以下两个反应:
包括以下两个反应:
①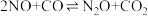
②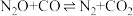
将恒定组成的 和
和 混合气通入不同温度的反应器,相同时间内检测物质浓度,结果如下。
混合气通入不同温度的反应器,相同时间内检测物质浓度,结果如下。 的脱除率
的脱除率
下列分析不正确的是
 和
和 包括以下两个反应:
包括以下两个反应:①
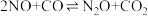
②
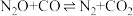
将恒定组成的
 和
和 混合气通入不同温度的反应器,相同时间内检测物质浓度,结果如下。
混合气通入不同温度的反应器,相同时间内检测物质浓度,结果如下。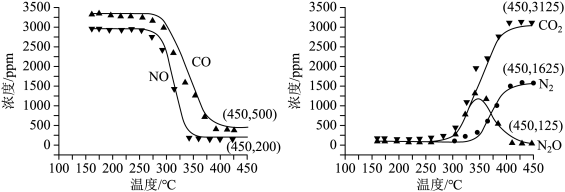
 的脱除率
的脱除率
下列分析不正确的是
A.低温不利于 和 和 的脱除 的脱除 |
B.高温下 和 和 主要脱除反应可以写为: 主要脱除反应可以写为: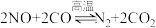 |
C.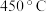 ,该时间段内 ,该时间段内 的脱除率约为 的脱除率约为 |
D.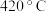 ,该时间段内几乎不发生反应①,主要发生反应② ,该时间段内几乎不发生反应①,主要发生反应② |
您最近一年使用:0次
名校
解题方法
6 . 甲基叔戊基醚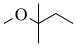 (TAME,简写为T)常用作汽油添加剂。在催化剂作用下,通过甲醇
(TAME,简写为T)常用作汽油添加剂。在催化剂作用下,通过甲醇 (简写为M)与2-甲基-2-丁烯(简写为A)的液相反应制得。通过控制条件,体系中主要发生如下反应(
(简写为M)与2-甲基-2-丁烯(简写为A)的液相反应制得。通过控制条件,体系中主要发生如下反应( 为2-甲基-1-丁烯的简写,不考虑其他副反应):
为2-甲基-1-丁烯的简写,不考虑其他副反应):
反应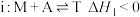
反应ii: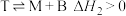
反应iii:
(1)磷钼酸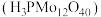 可作为制备TAME反应催化剂的浸渍试剂。已知钼元素位于第五周期第VIB族,核外电子排布与
可作为制备TAME反应催化剂的浸渍试剂。已知钼元素位于第五周期第VIB族,核外电子排布与 相似。
相似。
①基态钼原子的价层电子排布式为_______ 。
②完成化学方程式: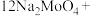
_______ 
(2)比较
_______  (填“>”、“<”或“=”)。
(填“>”、“<”或“=”)。
(3)我国学者团队对制备TAME反应的催化剂进行了研究。研究衣明:用不同浓度(13%)的磷钼酸浸渍催化剂,浓度越大催化剂催化活性越好。用浓度分别为 的磷钼酸浸渍催化剂进行了三组实验,得到
的磷钼酸浸渍催化剂进行了三组实验,得到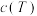 随时间
随时间 的变化曲线如图所示。
的变化曲线如图所示。
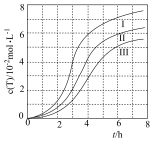
①用 的磷钼酸浸渍时,在
的磷钼酸浸渍时,在 内,
内, 的平均生成速率为
的平均生成速率为_______ 。
②下列仿关说法正确的有_______ 。
A.三组实验中,反应速率都随反应进程一直增大
B.平衡后加入惰性溶剂四氢呋喃稀释, 减小
减小
C.催化剂可加快化学反应速率,提高甲醇的平衡转化率
D.降低温度,反应 和ii的正、逆反应速率都减小
和ii的正、逆反应速率都减小
E.达到平衡后,加入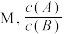 不变
不变
(4)研究团队继续研究其他条件不变时,不同醇烯比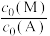 (甲醇
(甲醇 与烯烃
与烯烃 的起始物质的量浓度之比)对平衡的影响,当
的起始物质的量浓度之比)对平衡的影响,当 起始浓度
起始浓度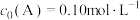 时,测得平衡时
时,测得平衡时 和
和 的
的 随
随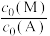 的变化曲线如图。
的变化曲线如图。
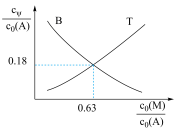
①曲线 呈现如图所示变化的原因是
呈现如图所示变化的原因是_______ 。
②当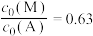 时,计算反应I的平衡常数
时,计算反应I的平衡常数_______ (写出计算过程)。
 (TAME,简写为T)常用作汽油添加剂。在催化剂作用下,通过甲醇
(TAME,简写为T)常用作汽油添加剂。在催化剂作用下,通过甲醇 (简写为M)与2-甲基-2-丁烯(简写为A)的液相反应制得。通过控制条件,体系中主要发生如下反应(
(简写为M)与2-甲基-2-丁烯(简写为A)的液相反应制得。通过控制条件,体系中主要发生如下反应( 为2-甲基-1-丁烯的简写,不考虑其他副反应):
为2-甲基-1-丁烯的简写,不考虑其他副反应):反应
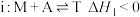
反应ii:
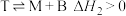
反应iii:

(1)磷钼酸
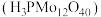 可作为制备TAME反应催化剂的浸渍试剂。已知钼元素位于第五周期第VIB族,核外电子排布与
可作为制备TAME反应催化剂的浸渍试剂。已知钼元素位于第五周期第VIB族,核外电子排布与 相似。
相似。①基态钼原子的价层电子排布式为
②完成化学方程式:
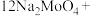

(2)比较

 (填“>”、“<”或“=”)。
(填“>”、“<”或“=”)。(3)我国学者团队对制备TAME反应的催化剂进行了研究。研究衣明:用不同浓度(13%)的磷钼酸浸渍催化剂,浓度越大催化剂催化活性越好。用浓度分别为
 的磷钼酸浸渍催化剂进行了三组实验,得到
的磷钼酸浸渍催化剂进行了三组实验,得到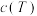 随时间
随时间 的变化曲线如图所示。
的变化曲线如图所示。
①用
 的磷钼酸浸渍时,在
的磷钼酸浸渍时,在 内,
内, 的平均生成速率为
的平均生成速率为②下列仿关说法正确的有
A.三组实验中,反应速率都随反应进程一直增大
B.平衡后加入惰性溶剂四氢呋喃稀释,
 减小
减小C.催化剂可加快化学反应速率,提高甲醇的平衡转化率
D.降低温度,反应
 和ii的正、逆反应速率都减小
和ii的正、逆反应速率都减小E.达到平衡后,加入
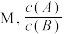 不变
不变(4)研究团队继续研究其他条件不变时,不同醇烯比
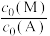 (甲醇
(甲醇 与烯烃
与烯烃 的起始物质的量浓度之比)对平衡的影响,当
的起始物质的量浓度之比)对平衡的影响,当 起始浓度
起始浓度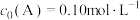 时,测得平衡时
时,测得平衡时 和
和 的
的 随
随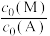 的变化曲线如图。
的变化曲线如图。
①曲线
 呈现如图所示变化的原因是
呈现如图所示变化的原因是②当
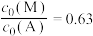 时,计算反应I的平衡常数
时,计算反应I的平衡常数
您最近一年使用:0次
2024-03-31更新
|
517次组卷
|
2卷引用:广东省广州市第六十五中学2023-2024学年高三下学期期初综合训练化学试题
名校
解题方法
7 . 工业上用乙苯催化脱氢制取苯乙烯的反应如下:
 (g)
(g)
 (g)+H2(g)。现将xmol乙苯蒸气通入体积可变的密闭容器中发生反应,维持体系总压强p总恒定。在某催化剂作用下,乙苯的平衡转化率随温度的变化如表所示。不考虑副反应,下列说法错误的是[已知:气体分压(p分)=气体总压(p总)×体积分数]
(g)+H2(g)。现将xmol乙苯蒸气通入体积可变的密闭容器中发生反应,维持体系总压强p总恒定。在某催化剂作用下,乙苯的平衡转化率随温度的变化如表所示。不考虑副反应,下列说法错误的是[已知:气体分压(p分)=气体总压(p总)×体积分数]
温度 | 400℃ | 450℃ | 500℃ | 550℃ |
平衡转化率 | 10% | 20% | 40% | 60% |
| A.400℃时,再向体系中通入水蒸气,V正、V逆均减小,且乙苯的转化率升高 |
B.500℃时,用平衡分压代替平衡浓度表示的化学平衡常数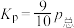 |
| C.500℃时,再向体系中通入0.2xmol乙苯,平衡时各物质的体积分数保持不变 |
| D.550℃时平衡体系中苯乙烯的体积分数是450℃时的2.25倍 |
您最近一年使用:0次
8 . 地热能的开发利用(如下图)过程中需要研究管道的腐蚀与结构问题。
资料:地热水储藏在地下数百米的高压环境中,温度高达250℃以上,其中溶解有CO2、H2S、SiO2以及Na+、Ca2+、 、Cl-等。
、Cl-等。
①输送蒸汽的钢制管道与蒸汽冷凝液接触时,主要发生_______ (填“析氢”或“吸氧”)腐蚀,负极发生的电极反应是_______ 。
②蒸汽冷凝液中有H2SO4,是由蒸汽与O2反应生成的,该反应的化学方程式是_______ 。
(2)地热水沿地热井管道上升时,随压强减小,达到某一高度(汽化位置)时剧烈汽化。由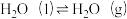 △H1>0可知,“热水”与“地热水”相比,温度会
△H1>0可知,“热水”与“地热水”相比,温度会_______ (填“升高”或“降低”)。
(3)汽化位置的管道中结垢最严重,主要成分是CaCO3,其形成与如下平衡有关。
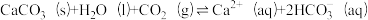 △H2
△H2
已知CaCO3溶解度与CO2压强(p)和温度(T)的关系如下图所示。_______ 0(填“>”或“<”)。
②比较p1和p2大小并说明理由:_______ 。
③汽化位置最易析出CaCO3的因素:压强减小,水剧烈汽化,导致_______ 。
(4)地热水中的SiO2以Si(OH)4形式存在,其溶解-析出过程可表示为:_______ 。
资料:地热水储藏在地下数百米的高压环境中,温度高达250℃以上,其中溶解有CO2、H2S、SiO2以及Na+、Ca2+、
 、Cl-等。
、Cl-等。
①输送蒸汽的钢制管道与蒸汽冷凝液接触时,主要发生
②蒸汽冷凝液中有H2SO4,是由蒸汽与O2反应生成的,该反应的化学方程式是
(2)地热水沿地热井管道上升时,随压强减小,达到某一高度(汽化位置)时剧烈汽化。由
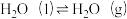 △H1>0可知,“热水”与“地热水”相比,温度会
△H1>0可知,“热水”与“地热水”相比,温度会(3)汽化位置的管道中结垢最严重,主要成分是CaCO3,其形成与如下平衡有关。
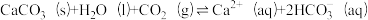 △H2
△H2已知CaCO3溶解度与CO2压强(p)和温度(T)的关系如下图所示。

②比较p1和p2大小并说明理由:
③汽化位置最易析出CaCO3的因素:压强减小,水剧烈汽化,导致
(4)地热水中的SiO2以Si(OH)4形式存在,其溶解-析出过程可表示为:

您最近一年使用:0次
2024-03-21更新
|
44次组卷
|
2卷引用:北京市第五中学2023-2024学年高二下学期开学考试化学试题
名校
解题方法
9 . 2024年2月国家工业和信息化部指出到2025年初步建立工业领域碳达峰碳中和标准体系, 有效转化是研究“碳中和”的重要方向。实现有效转化的一种常见途径是捕集
有效转化是研究“碳中和”的重要方向。实现有效转化的一种常见途径是捕集 转化为合成气(
转化为合成气( 和
和 ),再转化为烃类及含氧化合物等高附加值化学品(即费-托合成)。
),再转化为烃类及含氧化合物等高附加值化学品(即费-托合成)。
捕集 涉及下列反应:
涉及下列反应:
i.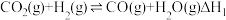
ii.
(1)有关物质能量变化如图所示,设稳定单质的焓(H)为0,则
_____________ ,利于该反应自发进行的条件是_____________ (填“高温”或“低温”)。

(2)在一定条件下,选择合适的催化剂只进行反应i: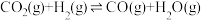 。调整
。调整 和
和 初始投料比,测得在一定投料比和一定温度下,该反应
初始投料比,测得在一定投料比和一定温度下,该反应 的平衡转化率如图所示。
的平衡转化率如图所示。
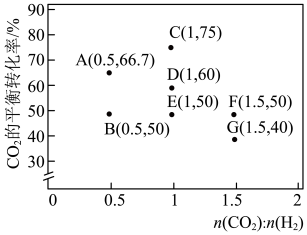
已知: 是以物质的量分数表示的化学平衡常数;对于反应
是以物质的量分数表示的化学平衡常数;对于反应 ,
,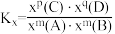 ,x为物质的量分数);反应速率
,x为物质的量分数);反应速率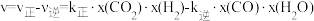 ,
, 分别为正、逆反应速率常数。
分别为正、逆反应速率常数。
①下列关于i反应说法不正确的是_____________ ;
a.催化剂参与了反应,改变了反应的活化能和
b.某温度反应达到平衡状态,升高温度,正反应速率提高的幅度更大
c.恒温恒压,混合气体密度不变可以作为反应达到平衡状态的标志
d.将 液化,及时分离,有利于提高反应物的转化率
液化,及时分离,有利于提高反应物的转化率
②B、E、F三点反应温度最高的是_____________ 点;
③计算E点所示的投料比在从起始到平衡的过程中,当 转化率达到
转化率达到 时,
时,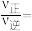
_____________ (用分数表示)。
(3)保持总压为 恒定,初始
恒定,初始 和
和 的物质的量之比
的物质的量之比 ,发生上述i、ii反应,不同温度下平衡组分物质的量分数如图。
,发生上述i、ii反应,不同温度下平衡组分物质的量分数如图。
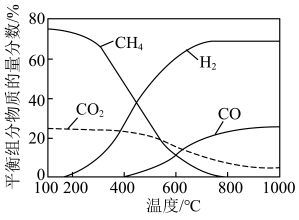
①在 以下时,
以下时, 含量高于
含量高于 的原因为
的原因为_____________ ;
②某温度下平衡体系中 和
和 的物质的量分数均为10%,此时反应i的平衡常数
的物质的量分数均为10%,此时反应i的平衡常数
_____________ (用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
 有效转化是研究“碳中和”的重要方向。实现有效转化的一种常见途径是捕集
有效转化是研究“碳中和”的重要方向。实现有效转化的一种常见途径是捕集 转化为合成气(
转化为合成气( 和
和 ),再转化为烃类及含氧化合物等高附加值化学品(即费-托合成)。
),再转化为烃类及含氧化合物等高附加值化学品(即费-托合成)。捕集
 涉及下列反应:
涉及下列反应:i.
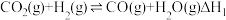
ii.

(1)有关物质能量变化如图所示,设稳定单质的焓(H)为0,则


(2)在一定条件下,选择合适的催化剂只进行反应i:
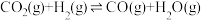 。调整
。调整 和
和 初始投料比,测得在一定投料比和一定温度下,该反应
初始投料比,测得在一定投料比和一定温度下,该反应 的平衡转化率如图所示。
的平衡转化率如图所示。
已知:
 是以物质的量分数表示的化学平衡常数;对于反应
是以物质的量分数表示的化学平衡常数;对于反应 ,
,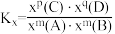 ,x为物质的量分数);反应速率
,x为物质的量分数);反应速率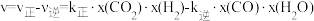 ,
, 分别为正、逆反应速率常数。
分别为正、逆反应速率常数。①下列关于i反应说法不正确的是
a.催化剂参与了反应,改变了反应的活化能和

b.某温度反应达到平衡状态,升高温度,正反应速率提高的幅度更大
c.恒温恒压,混合气体密度不变可以作为反应达到平衡状态的标志
d.将
 液化,及时分离,有利于提高反应物的转化率
液化,及时分离,有利于提高反应物的转化率②B、E、F三点反应温度最高的是
③计算E点所示的投料比在从起始到平衡的过程中,当
 转化率达到
转化率达到 时,
时,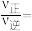
(3)保持总压为
 恒定,初始
恒定,初始 和
和 的物质的量之比
的物质的量之比 ,发生上述i、ii反应,不同温度下平衡组分物质的量分数如图。
,发生上述i、ii反应,不同温度下平衡组分物质的量分数如图。 
①在
 以下时,
以下时, 含量高于
含量高于 的原因为
的原因为②某温度下平衡体系中
 和
和 的物质的量分数均为10%,此时反应i的平衡常数
的物质的量分数均为10%,此时反应i的平衡常数
您最近一年使用:0次
名校
10 . 在恒容密闭容器中按物质的量之比 充入
充入 和
和 ,发生反应:
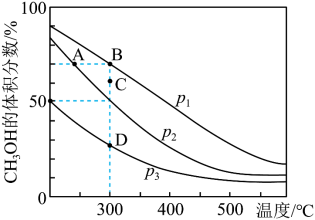
,发生反应: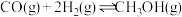 ,测得平衡混合物中
,测得平衡混合物中 的体积分数在不同压强下随温度的变化情况如图所示。下列说法正确的是
的体积分数在不同压强下随温度的变化情况如图所示。下列说法正确的是
 充入
充入 和
和 ,发生反应:
,发生反应: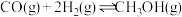 ,测得平衡混合物中
,测得平衡混合物中 的体积分数在不同压强下随温度的变化情况如图所示。下列说法正确的是
的体积分数在不同压强下随温度的变化情况如图所示。下列说法正确的是
A.该反应的 | B.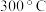 时,该反应的平衡常数 时,该反应的平衡常数 |
C.压强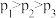 | D.压强为 、温度为 、温度为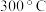 的条件下,C点 的条件下,C点 |
您最近一年使用:0次