名校
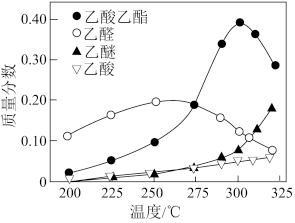
1 . 科学家研究了乙醇催化合成乙酸乙酯2C2H5OH(g) CH3COOC2H5(g)+2H2(g)的新方法。在常压下反应,冷凝收集,测得常温下液体收集物中主要产物的质量分数如图所示。下列推测合理的是
CH3COOC2H5(g)+2H2(g)的新方法。在常压下反应,冷凝收集,测得常温下液体收集物中主要产物的质量分数如图所示。下列推测合理的是
 CH3COOC2H5(g)+2H2(g)的新方法。在常压下反应,冷凝收集,测得常温下液体收集物中主要产物的质量分数如图所示。下列推测合理的是
CH3COOC2H5(g)+2H2(g)的新方法。在常压下反应,冷凝收集,测得常温下液体收集物中主要产物的质量分数如图所示。下列推测合理的是
| A.乙醛是该反应的催化剂 |
| B.加压有利于提高乙酸乙酯的产率 |
| C.提高催化剂的活性和选择性,减少乙醚等副产物是工艺的关键 |
| D.随着温度的升高,乙酸乙酯的质量分数先增大后减小,说明该反应是吸热反应 |
您最近一年使用:0次
2023-02-22更新
|
173次组卷
|
2卷引用:广东省肇庆市四会市四会中学、封开县广信中学2023-2024学年高二上学期第二次月考化学试题
名校
2 . 一定温度下,某反应达平衡,平衡常数K=c(CH3OH)·c(H2O)/[c(CO2)·c3(H2)]。保持容器容积不变,升高温度,H2浓度减小,则下列说法不正确的是
| A.该反应化学方程式为CO2(g)+3H2(g)⇌CH3OH(g)+H2O(g) |
| B.恒温恒容下,再充入CO2气体,H2浓度一定减小 |
| C.恒温恒压下,再充入惰性气体,会降低反应物的转化率 |
| D.升高温度,会使正反应速率增大,平衡常数减小 |
您最近一年使用:0次
2022-11-13更新
|
85次组卷
|
3卷引用:广东省肇庆市第一中学2022-2023学年高二上学期期中考试化学试题
名校
解题方法
3 . 有一处于平衡状态的反应:A(s)+2B(g) 3C(g),ΔH<0。为了使平衡向逆反应方向移动,可选择的条件是
3C(g),ΔH<0。为了使平衡向逆反应方向移动,可选择的条件是
①升温 ②降温 ③加压 ④减压 ⑤加催化剂
 3C(g),ΔH<0。为了使平衡向逆反应方向移动,可选择的条件是
3C(g),ΔH<0。为了使平衡向逆反应方向移动,可选择的条件是①升温 ②降温 ③加压 ④减压 ⑤加催化剂
| A.①③ | B.①③⑤ | C.①④ | D.②④⑤ |
您最近一年使用:0次
2022-11-12更新
|
216次组卷
|
3卷引用:广东省肇庆市四会中学、广信中学2022-2023学年高二上学期第一次教学质量联考化学试题
4 . 在80℃时,在甲、乙、丙三个恒容密闭容器中投入NO2和SO2混合气体,发生反应:NO2(g)+SO2(g) SO3(g)+NO(g)。起始浓度如表所示,其中甲经2min达到平衡,平衡时NO2的转化率为50%。下列判断错误的是
SO3(g)+NO(g)。起始浓度如表所示,其中甲经2min达到平衡,平衡时NO2的转化率为50%。下列判断错误的是
 SO3(g)+NO(g)。起始浓度如表所示,其中甲经2min达到平衡,平衡时NO2的转化率为50%。下列判断错误的是
SO3(g)+NO(g)。起始浓度如表所示,其中甲经2min达到平衡,平衡时NO2的转化率为50%。下列判断错误的是| 容器 | 甲 | 乙 | 丙 |
| c(NO2)/(mol•L-1) | 0.10 | 0.20 | 0.20 |
| c(SO2)/(mol•L-1) | 0.10 | 0.10 | 0.20 |
| A.平衡时,乙中SO2的转化率大于50% |
| B.平衡时,丙中c(SO2)是甲中的2倍 |
C.温度升至90℃,上述反应的平衡常数为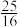 ,则正反应为放热反应 ,则正反应为放热反应 |
| D.保持温度为80℃,若起始时向容器乙中充入0.10mol•L-1NO2和0.20mol•L-1SO2,达到平衡时K=1 |
您最近一年使用:0次
名校
5 . 以下图象和叙述正确的是
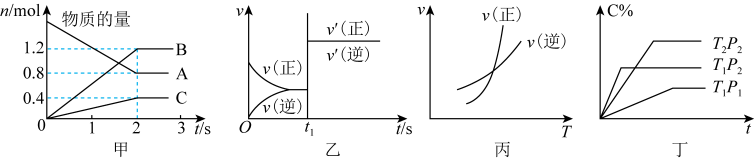

A.图甲:该图象表示的反应方程式为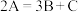 ,反应速率 ,反应速率 |
B.图乙:某温度下发生反应: , , 时刻改变的条件一定是加入催化剂 时刻改变的条件一定是加入催化剂 |
| C.图丙:对图中反应升高温度,该反应平衡常数增大 |
D.图丁:对于反应: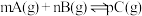 , , 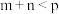 |
您最近一年使用:0次
2022-07-10更新
|
1168次组卷
|
5卷引用:广东省肇庆市封开县广信中学、四会中学2023-2024学年高二上学期第一次联考化学试题
名校
6 . 煤液化制乙醇的反应如下:2CO(g)+4H2(g)  CH3CH2OH(l)+H2O(l) ΔH<0,若利用这个反应进行乙醇(CH3CH2OH)的工业化生产,采取的措施正确的是
CH3CH2OH(l)+H2O(l) ΔH<0,若利用这个反应进行乙醇(CH3CH2OH)的工业化生产,采取的措施正确的是
 CH3CH2OH(l)+H2O(l) ΔH<0,若利用这个反应进行乙醇(CH3CH2OH)的工业化生产,采取的措施正确的是
CH3CH2OH(l)+H2O(l) ΔH<0,若利用这个反应进行乙醇(CH3CH2OH)的工业化生产,采取的措施正确的是| A.适宜温度、高压、催化剂 | B.低温、高压、催化剂 |
| C.低温、低压 | D.高温、高压 |
您最近一年使用:0次
2022-09-06更新
|
297次组卷
|
5卷引用:广东省肇庆市四会中学、广信中学2022-2023学年高二上学期第一次教学质量联考化学试题
名校
7 . 恒温下,反应aX(g)  bY(g)+cZ(g)达到平衡后,把容器体积压缩到原来的一半且达到新平衡时,X的物质的量浓度由0.1 mol·L-1增大到0.17 mol·L−1,下列判断正确的是
bY(g)+cZ(g)达到平衡后,把容器体积压缩到原来的一半且达到新平衡时,X的物质的量浓度由0.1 mol·L-1增大到0.17 mol·L−1,下列判断正确的是
 bY(g)+cZ(g)达到平衡后,把容器体积压缩到原来的一半且达到新平衡时,X的物质的量浓度由0.1 mol·L-1增大到0.17 mol·L−1,下列判断正确的是
bY(g)+cZ(g)达到平衡后,把容器体积压缩到原来的一半且达到新平衡时,X的物质的量浓度由0.1 mol·L-1增大到0.17 mol·L−1,下列判断正确的是| A.a>b+c | B.a<b+c | C.a=b+c | D.a=b=c |
您最近一年使用:0次
2022-09-06更新
|
185次组卷
|
2卷引用:广东省肇庆市四会中学、广信中学2022-2023学年高二上学期第一次教学质量联考化学试题
名校
8 . 下列事实不能用勒夏特列原理解释的是
| A.新制氯水在光照下颜色变浅 |
B.由 、 、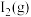 、 、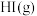 组成的平衡体系加压后颜色变深 组成的平衡体系加压后颜色变深 |
C.对于 ,及时分离出钾蒸气 ,及时分离出钾蒸气 |
D.对于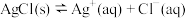 ,选择稀盐酸代替蒸馏水洗涤 ,选择稀盐酸代替蒸馏水洗涤 沉淀 沉淀 |
您最近一年使用:0次
2022-01-23更新
|
183次组卷
|
2卷引用:广东省肇庆市2021-2022学年高二上学期期末考试化学试题
名校
解题方法
9 . 一定温度下,将 和
和 充入
充入 密闭容器中发生反应:
密闭容器中发生反应: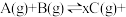
 ,在
,在 时达到平衡。在
时达到平衡。在 、
、 时分别改变反应的一个条件,测得容器中
时分别改变反应的一个条件,测得容器中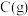 的浓度随时间变化情况如图所示。
的浓度随时间变化情况如图所示。
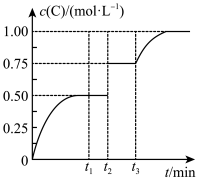
下列有关说法正确的是
 和
和 充入
充入 密闭容器中发生反应:
密闭容器中发生反应: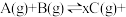
 ,在
,在 时达到平衡。在
时达到平衡。在 、
、 时分别改变反应的一个条件,测得容器中
时分别改变反应的一个条件,测得容器中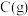 的浓度随时间变化情况如图所示。
的浓度随时间变化情况如图所示。
下列有关说法正确的是
A. |
B.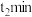 时改变的条件是使用催化剂 时改变的条件是使用催化剂 |
C. 时改变的条件是只增大生成物C的浓度 时改变的条件是只增大生成物C的浓度 |
D. 、 、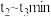 阶段反应的平衡常数均为4 阶段反应的平衡常数均为4 |
您最近一年使用:0次
2022-01-19更新
|
82次组卷
|
3卷引用:广东省肇庆市第一中学2022-2023学年高二上学期期中考试化学试题
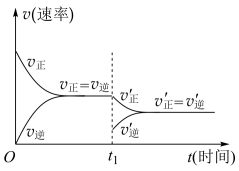
10 . 在N2(g)+3H2(g)  2NH3(g)(正反应为放热反应)的平衡体系中,在t1时刻只改变某一条件,其反应速率随时间变化的曲线如图,根据图象能得出的结论是
2NH3(g)(正反应为放热反应)的平衡体系中,在t1时刻只改变某一条件,其反应速率随时间变化的曲线如图,根据图象能得出的结论是
 2NH3(g)(正反应为放热反应)的平衡体系中,在t1时刻只改变某一条件,其反应速率随时间变化的曲线如图,根据图象能得出的结论是
2NH3(g)(正反应为放热反应)的平衡体系中,在t1时刻只改变某一条件,其反应速率随时间变化的曲线如图,根据图象能得出的结论是
| A.改变条件,平衡向逆反应方向移动 |
| B.t1时刻,改变的条件是减少了NH3的浓度 |
| C.t1时刻,改变的条件是增大了体系的压强 |
| D.达新平衡时,正反应速率增大,逆反应速率减小 |
您最近一年使用:0次



