1 . 在密闭容器中发生如下反应
 ;达到平衡后,改变下列条件,判断平衡移动的方向(向正反应方向、向逆反应方向、不移动)
;达到平衡后,改变下列条件,判断平衡移动的方向(向正反应方向、向逆反应方向、不移动)
(1)升高温度,平衡_______ 移动;
(2)增大压强,平衡_______ 移动:
(3)增大H2(g)浓度,平衡_______ 移动:加入C,平衡_______ 移动;
(4)加入催化剂,平衡_______ 移动。

 ;达到平衡后,改变下列条件,判断平衡移动的方向(向正反应方向、向逆反应方向、不移动)
;达到平衡后,改变下列条件,判断平衡移动的方向(向正反应方向、向逆反应方向、不移动)(1)升高温度,平衡
(2)增大压强,平衡
(3)增大H2(g)浓度,平衡
(4)加入催化剂,平衡
您最近一年使用:0次
2021-05-04更新
|
855次组卷
|
4卷引用:新疆喀什巴楚县第一中学2020-2021学年高二下学期期中考试化学试题
新疆喀什巴楚县第一中学2020-2021学年高二下学期期中考试化学试题课前-2.4 化学反应的调控-课前、课中、课后(人教版2019选择性必修1)(已下线)2.2.3 浓度、压强对化学平衡的影响-【帮课堂】2022-2023学年高二化学同步精品讲义(沪科版2020选择性必修第一册)(已下线)第10讲 影响化学平衡的因素(word讲义)-【帮课堂】2022-2023学年高二化学同步精品讲义(人教2019选择性必修1)
解题方法
2 . 甲烷自热重整是先进的制氢方法,包含甲烷氧化和水蒸气重整两个过程。
(1)甲烷自热重整时向反应系统同时通入甲烷、氧气和水蒸气,发生的主要化学反应如下:
①请用有关理论分析以上四个反应中反应Ⅰ速率最快的原因___ 。
②以上四个反应中,正向反应限度最大的是__ 。
a.反应Ⅰ b.反应Ⅱ c.反应Ⅲ d.反应Ⅳ
(2)甲烷水蒸气催化重整分为两阶段制备甲醇:
(ⅰ)制备合成气:CH4(g)+H2O(g) CO(g)+3H2(g)△H1=206.2kJ·mol-1
CO(g)+3H2(g)△H1=206.2kJ·mol-1
(ii)合成甲醇:CO(g)+2H2(g) CH3OH(g)△H2
CH3OH(g)△H2
制备合成气:将1.0molCH4和2.0molH2O(g)通入反应室(容积为100L),在一定条件下发生反应(ⅰ);CH4的平衡转化率与温度、压强的关系如图所示。
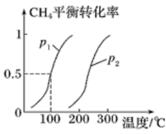
①已知100℃时达到平衡的时间为5min,则从反应开始到平衡,用氢气表示的平均反应速率为:v(H2)=___ mol·L-1·min-1。
②图中p1___ p2(填“<”、“>”或“=”)。
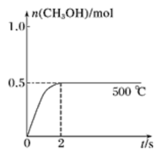
合成甲醇:在Cu2O/ZnO作催化剂的条件下,向2L的密闭容器中通入1molCO(g)和2molH2(g),发生反应(ⅱ),反应过程中CH3OH(g)的物质的量(n)与时间(t)及温度的关系如图所示。
③据研究,反应过程中起催化作用的为Cu2O。实际生产中随反应进行,Cu2O的量会减少,导致催化效率降低。若在反应体系中充入少量CO2,有利于保持Cu2O的催化效率不降低,原因是___ 。
④在500℃恒压条件下,请在图中画出反应体系中n(CH3OH)随时间t变化的总趋势图___ 。
(1)甲烷自热重整时向反应系统同时通入甲烷、氧气和水蒸气,发生的主要化学反应如下:
| 反应过程 | 反应序号 | 化学方程式 | △H/kJ·mol-1 | 活化能Ea/kJ·mol-1 |
| 甲烷氧化 | Ⅰ | CH4(g)+2O2(g)→CO2(g)+2H2O(g) | -802.6 | 125.6 |
| Ⅱ | CH4(g)+O2(g)→CO2(g)+2H2(g) | -322.0 | 172.5 | |
| 水蒸气重整 | Ⅲ | CH4(g)+H2O(g)→CO(g)+3H2(g) | +206.2 | 240.1 |
| Ⅳ | CH4(g)+2H2O(g)→CO2(g)+4H2(g) | +158.6 | 243.9 |
①请用有关理论分析以上四个反应中反应Ⅰ速率最快的原因
②以上四个反应中,正向反应限度最大的是
a.反应Ⅰ b.反应Ⅱ c.反应Ⅲ d.反应Ⅳ
(2)甲烷水蒸气催化重整分为两阶段制备甲醇:
(ⅰ)制备合成气:CH4(g)+H2O(g)
 CO(g)+3H2(g)△H1=206.2kJ·mol-1
CO(g)+3H2(g)△H1=206.2kJ·mol-1(ii)合成甲醇:CO(g)+2H2(g)
 CH3OH(g)△H2
CH3OH(g)△H2制备合成气:将1.0molCH4和2.0molH2O(g)通入反应室(容积为100L),在一定条件下发生反应(ⅰ);CH4的平衡转化率与温度、压强的关系如图所示。

①已知100℃时达到平衡的时间为5min,则从反应开始到平衡,用氢气表示的平均反应速率为:v(H2)=
②图中p1
合成甲醇:在Cu2O/ZnO作催化剂的条件下,向2L的密闭容器中通入1molCO(g)和2molH2(g),发生反应(ⅱ),反应过程中CH3OH(g)的物质的量(n)与时间(t)及温度的关系如图所示。
③据研究,反应过程中起催化作用的为Cu2O。实际生产中随反应进行,Cu2O的量会减少,导致催化效率降低。若在反应体系中充入少量CO2,有利于保持Cu2O的催化效率不降低,原因是
④在500℃恒压条件下,请在图中画出反应体系中n(CH3OH)随时间t变化的总趋势图

您最近一年使用:0次
名校
3 . 现有反应mA(g)+nB(g)  pC(g),达到平衡后,当升高温度时,B的转化率变大;当减小压强时,混合体系中C的质量分数减小,则:
pC(g),达到平衡后,当升高温度时,B的转化率变大;当减小压强时,混合体系中C的质量分数减小,则:
(1)m+n___________ p(填“>”、“<”或“=”)。
(2)减压时,A的质量分数___________ (填“增大”、“减小”或“不变”,下同)。
(3)若加入B(容器体积不变),则A的转化率___________ ,B的转化率___________ 。
(4)若升高温度,则平衡时,B、C的浓度之比将___________ 。
(5)若加入催化剂,平衡时气体混合物的总物质的量___________ 。
(6)若B是有色物质,A、C均为无色物质,则加入C(体积不变)时混合物的颜色___________ (填“变浅”、“变深”或“不变”,下同),而维持容器内气体的压强不变充入氖气时,混合物的颜色___________ 。
 pC(g),达到平衡后,当升高温度时,B的转化率变大;当减小压强时,混合体系中C的质量分数减小,则:
pC(g),达到平衡后,当升高温度时,B的转化率变大;当减小压强时,混合体系中C的质量分数减小,则:(1)m+n
(2)减压时,A的质量分数
(3)若加入B(容器体积不变),则A的转化率
(4)若升高温度,则平衡时,B、C的浓度之比将
(5)若加入催化剂,平衡时气体混合物的总物质的量
(6)若B是有色物质,A、C均为无色物质,则加入C(体积不变)时混合物的颜色
您最近一年使用:0次
名校
解题方法
4 . 不同温度、压强下,在合成氨平衡体系中N2(g)+3H2(g) 2NH3(g),NH3的物质的量分数见表(N2和H2起始物质的量之比为1:3):
2NH3(g),NH3的物质的量分数见表(N2和H2起始物质的量之比为1:3):
(1)N原子最外层电子排布式为___ ,氮气能在大气中稳定存在的原因是___ 。
(2)已知该反应在2L密闭容器中进行,5min内氨的质量增加了1.7g,则此段时间内H2的平均反应速率为___ mol/(L·min)。
(3)该反应的平衡常数表达式___ ,升高温度,K值___ (选填“增大”、“减小”或“不变”)。T℃(K=3.6)的某一时刻下,c(N2)=1mol/L,c(H2)=3mol/L,c(NH3)=9mol/L,在这种情况下该反应是否处于平衡状态___ (选填“是”、“否”),此时反应速率是v正___ v逆(选填“>”、“<”或“=”)。
(4)合成氨是生产条件一般为压强在20MPa~50MPa,温度为500℃左右,选用该条件的主要原因是___ 。
(5)从表中数据可知,在该条件下氨的平衡含量并不高,为提高原料利用率,工业生产中采取的措施是___ 。
(6)工业上用氨水吸收SO2尾气,最终得到化肥(NH4)2SO4。(NH4)2SO4溶液中离子浓度由大到小的顺序是___ 。
 2NH3(g),NH3的物质的量分数见表(N2和H2起始物质的量之比为1:3):
2NH3(g),NH3的物质的量分数见表(N2和H2起始物质的量之比为1:3):| 温度/氨的平衡含量(%)/压强(MPa) | 20 | 30 | 60 | 100 |
| 200 | 86.4 | 89.9 | 95.4 | 98.8 |
| 300 | 64.2 | 71.0 | 84.2 | 92.6 |
| 400 | 38.2 | 47.0 | 65.2 | 79.8 |
| 500 | 19.1 | 26.4 | 42.2 | 57.5 |
(1)N原子最外层电子排布式为
(2)已知该反应在2L密闭容器中进行,5min内氨的质量增加了1.7g,则此段时间内H2的平均反应速率为
(3)该反应的平衡常数表达式
(4)合成氨是生产条件一般为压强在20MPa~50MPa,温度为500℃左右,选用该条件的主要原因是
(5)从表中数据可知,在该条件下氨的平衡含量并不高,为提高原料利用率,工业生产中采取的措施是
(6)工业上用氨水吸收SO2尾气,最终得到化肥(NH4)2SO4。(NH4)2SO4溶液中离子浓度由大到小的顺序是
您最近一年使用:0次
名校
5 . 在密闭容器中发生如下反应C (s)+H2O(g ) CO(g)+H2(g)△H>0;达到平衡后,改变下列条件,判断平衡移动的方向(正反应方向、逆反应方向、不移动)
CO(g)+H2(g)△H>0;达到平衡后,改变下列条件,判断平衡移动的方向(正反应方向、逆反应方向、不移动)
(1)升高温度,平衡___________ 移动;
(2)增大压强,平衡___________ 移动;
(3)增大H2(g)浓度,平衡___________ 移动;加入C,平衡___________ 移动;
(4)加入催化剂,平衡___________ 移动。
(5)若要提高H2O(g)的转化率和化学反应速率可采取的措施___________ 。
 CO(g)+H2(g)△H>0;达到平衡后,改变下列条件,判断平衡移动的方向(正反应方向、逆反应方向、不移动)
CO(g)+H2(g)△H>0;达到平衡后,改变下列条件,判断平衡移动的方向(正反应方向、逆反应方向、不移动)(1)升高温度,平衡
(2)增大压强,平衡
(3)增大H2(g)浓度,平衡
(4)加入催化剂,平衡
(5)若要提高H2O(g)的转化率和化学反应速率可采取的措施
您最近一年使用:0次
2021-01-12更新
|
607次组卷
|
2卷引用:陕西省宝鸡市渭滨中学2020-2021学年度高二上学期期中考试化学试题
名校
6 . 在一定条件下,xA+yB⇌zC的反应达到平衡.
(1)已知A、B、C都是气体,在减压后平衡向逆反应方向移动,则x、y、z之间的关系是___ 。
(2)已知C是气体,且x+y=z,在增大压强时,如果平衡发生移动,则向____ 移动.(填“正向”、“逆向”、“无法判断”)
(3)已知B、C是气体,当其他条件不变,增大A的物质的量时,平衡不移动,则A是_____ 态.(填“气”、“液”、“固”)
(4)加热后C的质量分数减少,则正反应是_____ 热反应。
(1)已知A、B、C都是气体,在减压后平衡向逆反应方向移动,则x、y、z之间的关系是
(2)已知C是气体,且x+y=z,在增大压强时,如果平衡发生移动,则向
(3)已知B、C是气体,当其他条件不变,增大A的物质的量时,平衡不移动,则A是
(4)加热后C的质量分数减少,则正反应是
您最近一年使用:0次
2021-01-09更新
|
146次组卷
|
5卷引用:2015-2016学年广东省清远市第一中学高二上学期10月月考化学试卷
7 . 合成氨反应N2(g)+3H2(g) 2NH3(g),若在恒温、恒压条件下向平衡体系中通入氩气,平衡
2NH3(g),若在恒温、恒压条件下向平衡体系中通入氩气,平衡_____ 移动(填“向左”“向右”或“不”);使用催化剂平衡_____ 移动(同上),反应的△H______ (填“增大”“减小”或“不改变”)。
 2NH3(g),若在恒温、恒压条件下向平衡体系中通入氩气,平衡
2NH3(g),若在恒温、恒压条件下向平衡体系中通入氩气,平衡
您最近一年使用:0次
8 . 在密闭容器中进行下列反应:CO2(g)+C(s) 2CO(g) ΔH>0,起始通入2molCO,达到平衡后,改变下列条件,则指定物质的浓度、百分含量(填“不变”“增大”“减小”)及平衡如何变化(填“正移”“逆移”“不移动”):
2CO(g) ΔH>0,起始通入2molCO,达到平衡后,改变下列条件,则指定物质的浓度、百分含量(填“不变”“增大”“减小”)及平衡如何变化(填“正移”“逆移”“不移动”):
(1)增加C,平衡________ ,c(CO)________ 。
(2)减小密闭容器的体积,保持温度不变,则平衡___________ ,c(CO2)________ 。
(3)通入N2,保持密闭容器的体积和温度不变,则平衡________ ,c(CO2)________ 。
(4)保持密闭容器的体积不变,升高温度,则平衡___________ ,c(CO)_______ 。
(5)恒压通入N2,CO2的百分含量_________ 。
(6)保持密闭容器的体积和温度不变,加入催化剂,CO2的百分含量________ 。
 2CO(g) ΔH>0,起始通入2molCO,达到平衡后,改变下列条件,则指定物质的浓度、百分含量(填“不变”“增大”“减小”)及平衡如何变化(填“正移”“逆移”“不移动”):
2CO(g) ΔH>0,起始通入2molCO,达到平衡后,改变下列条件,则指定物质的浓度、百分含量(填“不变”“增大”“减小”)及平衡如何变化(填“正移”“逆移”“不移动”):(1)增加C,平衡
(2)减小密闭容器的体积,保持温度不变,则平衡
(3)通入N2,保持密闭容器的体积和温度不变,则平衡
(4)保持密闭容器的体积不变,升高温度,则平衡
(5)恒压通入N2,CO2的百分含量
(6)保持密闭容器的体积和温度不变,加入催化剂,CO2的百分含量
您最近一年使用:0次
2020-11-01更新
|
139次组卷
|
2卷引用:山西省新绛县第二中学2019-2020学年高二上学期第一次考试化学试题
9 . 化学平衡移动原理:
(1)增大反应物浓度或减少生成物浓度,平衡___________ 移动;
(2)升高温度,平衡_________ 移动;
(3)增大压强,平衡______ 移动;
(4)使用催化剂,平衡_________ 移动。
(1)增大反应物浓度或减少生成物浓度,平衡
(2)升高温度,平衡
(3)增大压强,平衡
(4)使用催化剂,平衡
您最近一年使用:0次
10 . 在密闭容器内使3molH2和1molN2混合发生下列反应:3H2+N2 2NH3 △H<0(下列空格选填“向正反应方向”“向逆反应方向”“不”)
2NH3 △H<0(下列空格选填“向正反应方向”“向逆反应方向”“不”)
(1)当达到平衡时,保持体积不变,升高温度,平衡将_______ 移动。
(2)当达到平衡时,充入Ar气,并保持体积不变,平衡将_______ 移动。
(3)当达到平衡时,充入Ar气,并保持压强不变,平衡将______ 移动。
(4)当达到平衡时,充入N2并保持体积不变,平衡将________ 移动。
 2NH3 △H<0(下列空格选填“向正反应方向”“向逆反应方向”“不”)
2NH3 △H<0(下列空格选填“向正反应方向”“向逆反应方向”“不”)(1)当达到平衡时,保持体积不变,升高温度,平衡将
(2)当达到平衡时,充入Ar气,并保持体积不变,平衡将
(3)当达到平衡时,充入Ar气,并保持压强不变,平衡将
(4)当达到平衡时,充入N2并保持体积不变,平衡将
您最近一年使用:0次



