在密闭容器中发生如下反应C (s)+H2O(g ) CO(g)+H2(g)△H>0;达到平衡后,改变下列条件,判断平衡移动的方向(正反应方向、逆反应方向、不移动)
CO(g)+H2(g)△H>0;达到平衡后,改变下列条件,判断平衡移动的方向(正反应方向、逆反应方向、不移动)
(1)升高温度,平衡___________ 移动;
(2)增大压强,平衡___________ 移动;
(3)增大H2(g)浓度,平衡___________ 移动;加入C,平衡___________ 移动;
(4)加入催化剂,平衡___________ 移动。
(5)若要提高H2O(g)的转化率和化学反应速率可采取的措施___________ 。
 CO(g)+H2(g)△H>0;达到平衡后,改变下列条件,判断平衡移动的方向(正反应方向、逆反应方向、不移动)
CO(g)+H2(g)△H>0;达到平衡后,改变下列条件,判断平衡移动的方向(正反应方向、逆反应方向、不移动)(1)升高温度,平衡
(2)增大压强,平衡
(3)增大H2(g)浓度,平衡
(4)加入催化剂,平衡
(5)若要提高H2O(g)的转化率和化学反应速率可采取的措施
更新时间:2021-01-12 00:05:41
|
相似题推荐
填空题
|
容易
(0.94)
解题方法
【推荐1】化学平衡移动的概念
从一个平衡状态变为另一个平衡状态,称为化学平衡的移动。化学平衡的移动,就是改变___________ ,破坏原有的平衡状态,建立起新的平衡状态的过程。
从一个平衡状态变为另一个平衡状态,称为化学平衡的移动。化学平衡的移动,就是改变
您最近一年使用:0次
填空题
|
容易
(0.94)
解题方法
【推荐2】甲烷和二氧化碳都是温室气体。随着石油资源日益枯竭,储量丰富的甲烷(天然气、页岩气、可燃冰的主要成分)及二氧化碳的高效利用已成为科学研究的热点。在催化剂作用下,将甲烷部分氧化制备合成气(CO和H2)的反应为CH4(g)+ O2(g)=CO(g)+2H2(g)。欲提高甲烷的平衡转化率,可采取的两条措施是
O2(g)=CO(g)+2H2(g)。欲提高甲烷的平衡转化率,可采取的两条措施是_____ 。
 O2(g)=CO(g)+2H2(g)。欲提高甲烷的平衡转化率,可采取的两条措施是
O2(g)=CO(g)+2H2(g)。欲提高甲烷的平衡转化率,可采取的两条措施是
您最近一年使用:0次
填空题
|
容易
(0.94)
【推荐3】一定量的CO2与足量的C在恒压密闭容器中发生反应:C(s)+CO2(g)=2CO(g) ΔH=+173 kJ·mol-1,若压强为p kPa,平衡时体系中气体体积分数与温度的关系如图所示,回答下列问题:

(1)650 ℃时CO2的平衡转化率为___________ 。
(2)t1 ℃时平衡常数Kp=___________ (用平衡分压代替平衡浓度计算,分压=总压×物质的量分数);该温度下达平衡后若再充入等物质的量的CO和CO2气体,则平衡___________ (填“正向”“逆向”或“不”)移动,原因是___________ 。

(1)650 ℃时CO2的平衡转化率为
(2)t1 ℃时平衡常数Kp=
您最近一年使用:0次
填空题
|
容易
(0.94)
【推荐1】H2O由液态变为气态的过程可以用下式来表示:H2O(l)⇌ H2O(g)。我们也可以用平衡移动原理来解释这一变化中的一些问题,如:H2O的汽化是吸热过程,所以温度升高,平衡向生成更多的H2O(g)的方向移动。请回答下面两个问题:减小压强,平衡向______ 移动。所以高山上由于空气稀薄,水的沸点比平地上______ (填高或低)。高压锅中水的沸点比普通锅中水的沸点______ (填高或低)。
您最近一年使用:0次
填空题
|
容易
(0.94)
【推荐2】化学反应达到平衡后,改变温度平衡是否一定发生移动________ ?
您最近一年使用:0次
填空题
|
容易
(0.94)
解题方法
【推荐1】压强变化对化学平衡的影响规律
增大压强,平衡向___________ 的方向移动;
减小压强,平衡向___________ 的方向移动。
对于反应前后气体分子数目不变的反应,增大压强时,改变反应体系的压强,平衡___________ 移动。
增大压强,平衡向
减小压强,平衡向
对于反应前后气体分子数目不变的反应,增大压强时,改变反应体系的压强,平衡
您最近一年使用:0次
填空题
|
容易
(0.94)
【推荐2】在其他条件不变的情况下,压强对化学平衡的影响规律
Δvg=(化学方程式中气态反应产物化学式前系数之和)-(化学方程式中气态反应物化学式前系数之和)。
(1)Δvg=0:改变压强,化学平衡___________ ;
(2)Δvg≠0:改变压强,化学平衡向___________ 方向移动。
Δvg=(化学方程式中气态反应产物化学式前系数之和)-(化学方程式中气态反应物化学式前系数之和)。
(1)Δvg=0:改变压强,化学平衡
(2)Δvg≠0:改变压强,化学平衡向
您最近一年使用:0次
填空题
|
容易
(0.94)
名校
解题方法
【推荐3】对于已达平衡的下列反应
2HI(g)⇌H2(g)+I2(g) ①
2NO2⇌N2O4 ②
2NH3(g)⇌N2(g)+3H2(g) ③
(1)保持容器容积不变,再通入一定量的反应物,反应①反应物的转化率_______ 反应②的转化率_______ (填增大、减小、不变,下同)。
(2)保持压强不变,通入一定量的N2O4,反应②生成物的百分含量_______
(3)保持容器容积不变,通入一定量氖气,则达到平衡时反应②NO2转化率_______
(4)保持压强不变,通入氖气使体系的容积增大一倍,则达到平衡时反应③NH3百分含量_____ 。
2HI(g)⇌H2(g)+I2(g) ①
2NO2⇌N2O4 ②
2NH3(g)⇌N2(g)+3H2(g) ③
(1)保持容器容积不变,再通入一定量的反应物,反应①反应物的转化率
(2)保持压强不变,通入一定量的N2O4,反应②生成物的百分含量
(3)保持容器容积不变,通入一定量氖气,则达到平衡时反应②NO2转化率
(4)保持压强不变,通入氖气使体系的容积增大一倍,则达到平衡时反应③NH3百分含量
您最近一年使用:0次
填空题
|
容易
(0.94)
【推荐1】一定条件下,某可逆反应在密闭容器中建立化学平衡,在 时刻改变某一个条件,建立新的平衡,其
时刻改变某一个条件,建立新的平衡,其 图像如下:
图像如下:
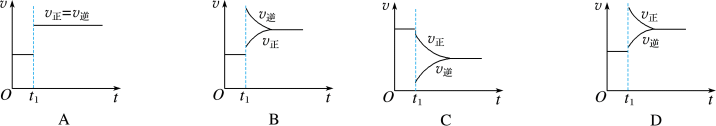
(1)对于反应 ,
, 时刻缩小容器体积,其图像为
时刻缩小容器体积,其图像为___________ (填字母),平衡___________ (填“向正反应方向”、“向逆反应方向”或“不”)移动。
(2)对于反应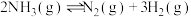 ,
, 时刻增大容器体积,其图像为
时刻增大容器体积,其图像为___________ (填字母),平衡___________ (填“向正反应方向”、“向逆反应方向”或“不”)移动。
(3)对于反应 ,
, 时刻缩小容器体积,其图像为
时刻缩小容器体积,其图像为___________ (填字母),平衡___________ (填“向正反应方向”、“向逆反应方向”或“不”)移动。
 时刻改变某一个条件,建立新的平衡,其
时刻改变某一个条件,建立新的平衡,其 图像如下:
图像如下:
(1)对于反应
 ,
, 时刻缩小容器体积,其图像为
时刻缩小容器体积,其图像为(2)对于反应
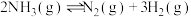 ,
, 时刻增大容器体积,其图像为
时刻增大容器体积,其图像为(3)对于反应
 ,
, 时刻缩小容器体积,其图像为
时刻缩小容器体积,其图像为
您最近一年使用:0次
填空题
|
容易
(0.94)
【推荐2】内容
在封闭体系中,如果改变平衡体系的一个条件(如浓度、温度或压强),平衡将向___________ 这个改变的方向移动。
在封闭体系中,如果改变平衡体系的一个条件(如浓度、温度或压强),平衡将向
您最近一年使用:0次

 2HI(g)
2HI(g)

