1 . 目前生产钛的方法之一是先将TiO2转化为TiCl4,再进一步还原得到钛。以下是碳氯化法制备TiCl4:TiO2(s)+2Cl2(g)+2C(s) TiCl4(g)+2CO(g) ∆H
TiCl4(g)+2CO(g) ∆H kJ·mol−1。
kJ·mol−1。
(1)对于该反应:增大压强,平衡___________ 移动(填“正向”“不”或“逆向”);温度升高,平衡转化率___________ (填“增大”“减小”或“不变”)。
(2)恒温恒容时,下列叙述一定能说明该反应达到平衡状态的是______。
(3)在某温度下,该恒容体系已经达到平衡,若向其中加入少量碳,TiCl4的体积分数将___________ (填选项);若加入少量氯气,TiCl4的体积分数将___________ (填选项)。
A.减小 B.不变 C.增大
 TiCl4(g)+2CO(g) ∆H
TiCl4(g)+2CO(g) ∆H kJ·mol−1。
kJ·mol−1。(1)对于该反应:增大压强,平衡
(2)恒温恒容时,下列叙述一定能说明该反应达到平衡状态的是______。
| A.混合气体的压强保持不变 | B.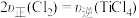 |
| C.混合气体的密度保持不变 | D.Cl2和CO物质的量相等 |
A.减小 B.不变 C.增大
您最近半年使用:0次
名校
2 . 我国提出2060年达“碳中和”目标,将CO2转化为高附加值产品是实现该目标的一种方式,如:CH3OH、HCOOH等。回答下列问题:
(1)下列措施有利于“碳中和”的是_____。
CO2和H2在催化剂作用下发生反应可合成清洁能源甲醇:
(2)已知该反应的正反应率 (k为正反应的速率常数),某温度时测得数据如表中所示。则此温度下表中a=
(k为正反应的速率常数),某温度时测得数据如表中所示。则此温度下表中a=_____ 。
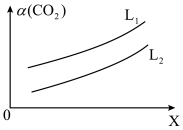
(3)在一定条件下,体系中CO2的平衡转化率(α)与L和X的关系如图所示,该反应为放热反应,L和X分别表示温度或压强。X表示的物理量是_____ (填“温度”或“压强”),L1_____ L2(填“>”或“<”)。
(1)下列措施有利于“碳中和”的是_____。
| A.植树造林,发展绿色经济 | B.通过裂化将重油转化为汽油 |
| C.在燃煤中添加CaO或CaCO3 | D.大力开采和使用可燃冰 |
CO2和H2在催化剂作用下发生反应可合成清洁能源甲醇:

(2)已知该反应的正反应率
 (k为正反应的速率常数),某温度时测得数据如表中所示。则此温度下表中a=
(k为正反应的速率常数),某温度时测得数据如表中所示。则此温度下表中a=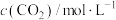 | 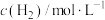 |  | |
| 1 | 0.02 | 0.01 | 2.0×10-4 |
| 2 | 0.04 | 0.01 | a |
(3)在一定条件下,体系中CO2的平衡转化率(α)与L和X的关系如图所示,该反应为放热反应,L和X分别表示温度或压强。X表示的物理量是

您最近半年使用:0次
名校
解题方法
3 . 通常在乙苯蒸汽中掺混水蒸气,控制温度600℃,并保持总压为常压。不同温度下,乙苯的平衡转化率和某催化剂作用下苯乙烯的选择性(指除 以外的产物中苯乙烯的物质的量分数)如图:
以外的产物中苯乙烯的物质的量分数)如图:
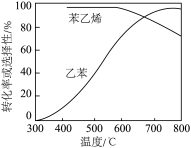
(1)掺入水蒸气能提高乙苯的平衡转化率,解释说明该事实_____ 。
(2)控制反应温度为600℃的理由是_____ 。
(3)某机构用 代替水蒸气开发了乙苯-二氧化碳催化脱氢制苯乙烯。保持常压和原料气比例不变,与掺水蒸气工艺相比,在相同的生产效率下,可降低操作温度;该工艺中还能够发生反应:CO2+H2=CO+H2O,CO2+C=2CO。新工艺的特点有
代替水蒸气开发了乙苯-二氧化碳催化脱氢制苯乙烯。保持常压和原料气比例不变,与掺水蒸气工艺相比,在相同的生产效率下,可降低操作温度;该工艺中还能够发生反应:CO2+H2=CO+H2O,CO2+C=2CO。新工艺的特点有_____
①CO2与H2反应,使乙苯脱氢反应的化学平衡右移
②不用高温水蒸气,可降低能量消耗
③有利于减少积炭
④有利用CO2资源利用
 以外的产物中苯乙烯的物质的量分数)如图:
以外的产物中苯乙烯的物质的量分数)如图:
(1)掺入水蒸气能提高乙苯的平衡转化率,解释说明该事实
(2)控制反应温度为600℃的理由是
(3)某机构用
 代替水蒸气开发了乙苯-二氧化碳催化脱氢制苯乙烯。保持常压和原料气比例不变,与掺水蒸气工艺相比,在相同的生产效率下,可降低操作温度;该工艺中还能够发生反应:CO2+H2=CO+H2O,CO2+C=2CO。新工艺的特点有
代替水蒸气开发了乙苯-二氧化碳催化脱氢制苯乙烯。保持常压和原料气比例不变,与掺水蒸气工艺相比,在相同的生产效率下,可降低操作温度;该工艺中还能够发生反应:CO2+H2=CO+H2O,CO2+C=2CO。新工艺的特点有①CO2与H2反应,使乙苯脱氢反应的化学平衡右移
②不用高温水蒸气,可降低能量消耗
③有利于减少积炭
④有利用CO2资源利用
您最近半年使用:0次
4 . 完成下列问题
(1)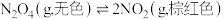 的平衡体系,降低温度,气体颜色变浅,则正反应是
的平衡体系,降低温度,气体颜色变浅,则正反应是___________ 热反应;若增大压强,平衡向___________ 移动(填“正反应方向”、“逆反应方向”或“不”),正反应速率___________ (填“增大”或“减小”)。
(2)某温度下,纯水的 为
为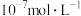 ,则此时
,则此时 为
为___________  ,若温度不变,滴入稀
,若温度不变,滴入稀 使
使 ,则由水电离出的
,则由水电离出的 为
为___________  ,某温度(T0℃)时,水的
,某温度(T0℃)时,水的 ,则该温度
,则该温度___________ (填“高于”、“低于”或“等于”)25℃其理由是___________ 。碳酸氢钠溶液显___________ 性,水解方程式表示为___________ 。
(1)
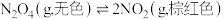 的平衡体系,降低温度,气体颜色变浅,则正反应是
的平衡体系,降低温度,气体颜色变浅,则正反应是(2)某温度下,纯水的
 为
为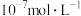 ,则此时
,则此时 为
为 ,若温度不变,滴入稀
,若温度不变,滴入稀 使
使 ,则由水电离出的
,则由水电离出的 为
为 ,某温度(T0℃)时,水的
,某温度(T0℃)时,水的 ,则该温度
,则该温度
您最近半年使用:0次
5 . 卤素化合物在生产生活中应用广泛,回答下列问题
(1)研究表明 气体中存在单体和环状六聚体的平衡:
气体中存在单体和环状六聚体的平衡: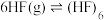 ,HF形成环状六聚体的作用力是
,HF形成环状六聚体的作用力是____________ ;在测定 相对分子质量的实验中,
相对分子质量的实验中,____________ (填“低压”或“高压”)有利于测定的准确性.
(2) 气体是高效绿色消毒剂,但其性质不稳定,浓度大时会发生爆炸.可用草酸
气体是高效绿色消毒剂,但其性质不稳定,浓度大时会发生爆炸.可用草酸 和氯酸钾
和氯酸钾 在酸性条件下制备
在酸性条件下制备 ,离子方程式为
,离子方程式为__________ ;产物中的另一种气体可以起到的作用是________________ .
(3) 与
与 以共价键形成
以共价键形成 ,其中
,其中________ 显负电性, 与水反应的方程式是
与水反应的方程式是____________ .
(4)利用 和浓磷酸制备
和浓磷酸制备 的原理是:
的原理是: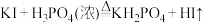 ,该反应中利用了浓磷酸的什么性质:
,该反应中利用了浓磷酸的什么性质:________ (“强酸性”“强氧化性”“高沸点”).
(1)研究表明
 气体中存在单体和环状六聚体的平衡:
气体中存在单体和环状六聚体的平衡: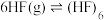 ,HF形成环状六聚体的作用力是
,HF形成环状六聚体的作用力是 相对分子质量的实验中,
相对分子质量的实验中,(2)
 气体是高效绿色消毒剂,但其性质不稳定,浓度大时会发生爆炸.可用草酸
气体是高效绿色消毒剂,但其性质不稳定,浓度大时会发生爆炸.可用草酸 和氯酸钾
和氯酸钾 在酸性条件下制备
在酸性条件下制备 ,离子方程式为
,离子方程式为(3)
 与
与 以共价键形成
以共价键形成 ,其中
,其中 与水反应的方程式是
与水反应的方程式是(4)利用
 和浓磷酸制备
和浓磷酸制备 的原理是:
的原理是: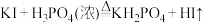 ,该反应中利用了浓磷酸的什么性质:
,该反应中利用了浓磷酸的什么性质:
您最近半年使用:0次
6 . 汽车尾气是造成空气污染的原因之一。其中涉及的反应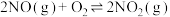 在其他条件不变达平衡时,分别测得NO 的平衡转化率在不同压强(p1、p2) 和温度下变化的曲线(如图):
在其他条件不变达平衡时,分别测得NO 的平衡转化率在不同压强(p1、p2) 和温度下变化的曲线(如图):

比较p1、p2的大小关系:___________ (填“>”“<”或“=”)。
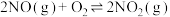 在其他条件不变达平衡时,分别测得NO 的平衡转化率在不同压强(p1、p2) 和温度下变化的曲线(如图):
在其他条件不变达平衡时,分别测得NO 的平衡转化率在不同压强(p1、p2) 和温度下变化的曲线(如图):
比较p1、p2的大小关系:
您最近半年使用:0次
7 . 在密闭容器中,使2molN2和6molH2混合发生下列反应:  。
。
(1)当反应达到平衡时,N2和H2的浓度比是_____ ;N2和H2的转化率比是_____ 。
(2)升高平衡体系的温度(保持体积不变),混合气体的平均相对分子质量_____ ;密度_____ 。(填“变大”、“变小”或“不变”)
(3)当达到平衡时,将c(N2)、c(H2)、c(NH3)同时增加一倍,平衡将_____ 。(填“正移”“逆移”或“不移动”,下同)
(4)当达到平衡时,充入氩气,并保持压强不变,平衡将_____ 。
 。
。(1)当反应达到平衡时,N2和H2的浓度比是
(2)升高平衡体系的温度(保持体积不变),混合气体的平均相对分子质量
(3)当达到平衡时,将c(N2)、c(H2)、c(NH3)同时增加一倍,平衡将
(4)当达到平衡时,充入氩气,并保持压强不变,平衡将
您最近半年使用:0次
解题方法
8 . A:一定条件下,某可逆反应在密闭容器中建立化学平衡,在 时刻改变某一个条件,建立新的平衡,其
时刻改变某一个条件,建立新的平衡,其 图像如下:
图像如下:
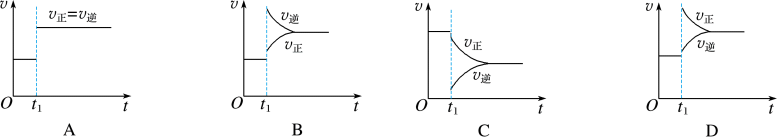
(1)对于反应: ,
, 时刻缩小容器体积,其图像为
时刻缩小容器体积,其图像为___________ (填字母,下同),平衡___________ (填“向正反应方向”“向逆反应方向”或“不”,下同)移动。
(2)对于反应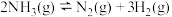 ,
, 时刻增大容器体积,其图像为
时刻增大容器体积,其图像为___________ ,平衡___________ 移动。
(3)对于反应 ,
, 时刻缩小容器体积,其图像为
时刻缩小容器体积,其图像为___________ ,平衡___________ 移动。
B:可逆反应 在不同温度(和)及压强(和)下,产生Z的物质的量n和反应时间t的关系如图所示,根据图像回答下列问题:
在不同温度(和)及压强(和)下,产生Z的物质的量n和反应时间t的关系如图所示,根据图像回答下列问题:
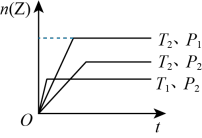
(4)温度 和
和 的关系为
的关系为
___________ (填“>”、“<”或“=”,下同) ,压强
,压强 和
和 的关系为
的关系为
___________  。
。
(5)a___________ 1。
(6)该反应的正反应为___________ (填“吸热”或“放热”反应)。
 时刻改变某一个条件,建立新的平衡,其
时刻改变某一个条件,建立新的平衡,其 图像如下:
图像如下:
(1)对于反应:
 ,
, 时刻缩小容器体积,其图像为
时刻缩小容器体积,其图像为(2)对于反应
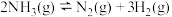 ,
, 时刻增大容器体积,其图像为
时刻增大容器体积,其图像为(3)对于反应
 ,
, 时刻缩小容器体积,其图像为
时刻缩小容器体积,其图像为B:可逆反应
 在不同温度(和)及压强(和)下,产生Z的物质的量n和反应时间t的关系如图所示,根据图像回答下列问题:
在不同温度(和)及压强(和)下,产生Z的物质的量n和反应时间t的关系如图所示,根据图像回答下列问题: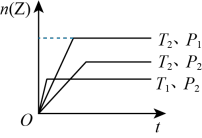
(4)温度
 和
和 的关系为
的关系为
 ,压强
,压强 和
和 的关系为
的关系为
 。
。(5)a
(6)该反应的正反应为
您最近半年使用:0次
解题方法
9 .  时,A、B、C三种气体在恒容密闭容器中反应时,浓度的变化情况如图,回答下列问题。
时,A、B、C三种气体在恒容密闭容器中反应时,浓度的变化情况如图,回答下列问题。
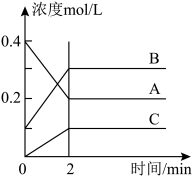
(1)写出该反应的方程式:___________ 。
(2)前 ,A的分解速率为
,A的分解速率为___________ 。
(3)达到平衡后,若增大压强,平衡向___________ 方向移动(填“正”或“逆”或“不移动)。
(4)该反应的平衡常数
___________ 。
(5) 反应达平衡,容器内混合气体的平均相对分子质量比起始时
反应达平衡,容器内混合气体的平均相对分子质量比起始时___________ (填“大”,“小”或“相等”,下同),混合气体密度比起始时___________
(6)在某一时刻采取下列措施能使该反应速率减小的是___________。
 时,A、B、C三种气体在恒容密闭容器中反应时,浓度的变化情况如图,回答下列问题。
时,A、B、C三种气体在恒容密闭容器中反应时,浓度的变化情况如图,回答下列问题。
(1)写出该反应的方程式:
(2)前
 ,A的分解速率为
,A的分解速率为(3)达到平衡后,若增大压强,平衡向
(4)该反应的平衡常数

(5)
 反应达平衡,容器内混合气体的平均相对分子质量比起始时
反应达平衡,容器内混合气体的平均相对分子质量比起始时(6)在某一时刻采取下列措施能使该反应速率减小的是___________。
| A.加催化剂 | B.降低温度 |
| C.容积不变,充入A | D.容积不变,从容器中分离出A |
您最近半年使用:0次
10 . 可逆反应mA(g)+nB(g)⇌pC(g)+qD(g)的相关物质体积分数的变化图像如下,请回答下列问题:

(1)温度T1_______ T2(填“>”、“<”或“=”,下同)。
(2)压强p1_______ p2。
(3)m+n_______ p+q。
(4)正反应为_______ (填“放热”或“吸热”)反应。

(1)温度T1
(2)压强p1
(3)m+n
(4)正反应为
您最近半年使用:0次



