2022高三·全国·专题练习
名校
解题方法
1 . 氨气中氢含量高,是一种优良的小分子储氢载体,且安全、易储运,可通过下面两种方法由氨气得到氢气。某兴趣小组对该反应进行了实验探究。在一定温度和催化剂的条件下,将0.1mol NH3通入3L的密闭容器中进行反应(此时容器内总压为200kPa),各物质的分压随时间的变化曲线如图所示。

(1)若保持容器容积不变,t1时反应达到平衡,用H2的浓度变化表示0~t1时间内的反应速率v(H2)=_______ mol·L-1·min-1(用含t1的代数式表示);
(2)t2时将容器容积迅速缩小至原来的一半并保持不变,图中能正确表示压缩后N2分压变化趋势的曲线是___________ (用图中a、b、c、d表示),理由是___________
(3)在该温度下,反应的标准平衡常数Kθ=____ 。[已知:分压=总压×该组分物质的量分数,对于反应dD(g)+eE(g)⇌gG(g)+hH(g) Kθ= ,其中pθ=100kPa,pG、pH、pD、pE为各组分的平衡分压]。
,其中pθ=100kPa,pG、pH、pD、pE为各组分的平衡分压]。

(1)若保持容器容积不变,t1时反应达到平衡,用H2的浓度变化表示0~t1时间内的反应速率v(H2)=
(2)t2时将容器容积迅速缩小至原来的一半并保持不变,图中能正确表示压缩后N2分压变化趋势的曲线是
(3)在该温度下,反应的标准平衡常数Kθ=
 ,其中pθ=100kPa,pG、pH、pD、pE为各组分的平衡分压]。
,其中pθ=100kPa,pG、pH、pD、pE为各组分的平衡分压]。
您最近半年使用:0次
名校
2 . 二氧化碳一甲烷重整反应制备合成气(H2+CO)是一种生产高附加值化学品的低碳过程。该过程存在如下化学反应:
①

②
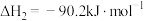
③
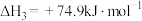
④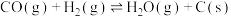
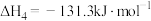
回答下列问题:
(1)
_______ ,反应①_______ 正向自发进行(填标号)。
A.低温下能 B.高温下能 C.任何温度下都能 D.任何温度下都不能
(2)反应体系总压强分别为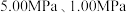 和
和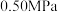 时,
时, 平衡转化率随反应温度变化如图所示,则代表反应体系总压强为
平衡转化率随反应温度变化如图所示,则代表反应体系总压强为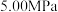 的曲线是
的曲线是_______ (填“Ⅰ”“Ⅱ”或“Ⅲ”),判断依据是_______ 。 时,平衡时部分组分的物质的量随反应温度变化如图所示。随反应温度的升高,
时,平衡时部分组分的物质的量随反应温度变化如图所示。随反应温度的升高, 的物质的量先增加后减少,主要原因是
的物质的量先增加后减少,主要原因是_______ 。 和
和 ,达到平衡时
,达到平衡时 的转化率为
的转化率为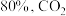 的转化率为
的转化率为 ,碳单质的物质的量为
,碳单质的物质的量为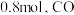 的物质的量为
的物质的量为_______  ,反应①用摩尔分数表示的平衡常数
,反应①用摩尔分数表示的平衡常数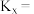
_______ (结果保留两位小数)。
上述平衡时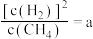 ,向体系通入
,向体系通入 气,重新达到平衡时,
气,重新达到平衡时,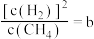 ,则a
,则a_______ b(填“>”“<”或“=”)。(已知反应 的
的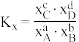 ,物质
,物质 的摩尔分数
的摩尔分数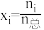 )
)
①


②

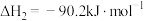
③

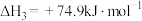
④
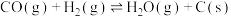
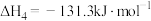
回答下列问题:
(1)

A.低温下能 B.高温下能 C.任何温度下都能 D.任何温度下都不能
(2)反应体系总压强分别为
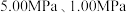 和
和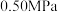 时,
时, 平衡转化率随反应温度变化如图所示,则代表反应体系总压强为
平衡转化率随反应温度变化如图所示,则代表反应体系总压强为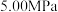 的曲线是
的曲线是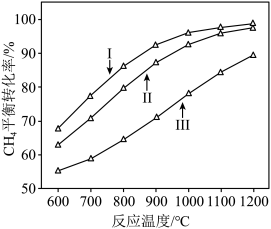
 时,平衡时部分组分的物质的量随反应温度变化如图所示。随反应温度的升高,
时,平衡时部分组分的物质的量随反应温度变化如图所示。随反应温度的升高, 的物质的量先增加后减少,主要原因是
的物质的量先增加后减少,主要原因是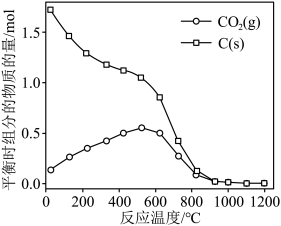
 和
和 ,达到平衡时
,达到平衡时 的转化率为
的转化率为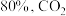 的转化率为
的转化率为 ,碳单质的物质的量为
,碳单质的物质的量为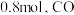 的物质的量为
的物质的量为 ,反应①用摩尔分数表示的平衡常数
,反应①用摩尔分数表示的平衡常数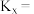
上述平衡时
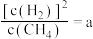 ,向体系通入
,向体系通入 气,重新达到平衡时,
气,重新达到平衡时,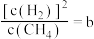 ,则a
,则a 的
的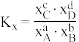 ,物质
,物质 的摩尔分数
的摩尔分数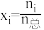 )
)
您最近半年使用:0次
2024-01-20更新
|
1061次组卷
|
4卷引用:2024年1月河南普通高等学校招生考试适应性测试化学试题
2024年1月河南普通高等学校招生考试适应性测试化学试题(已下线)T29-原理综合题(已下线)2024年1月“九省联考”河南卷真题完全解读与考后提升湖南省长沙市雅礼中学2023-2024学年高三下学期月考(八)化学试题
22-23高二上·全国·课时练习
3 . 可逆反应2X(g)+aY(g) 3Z(g)在不同温度(T1和T2)及压强(p1和p2)下,产生Z的物质的量n和反应时间t的关系如图所示,根据图象回答下列问题:
3Z(g)在不同温度(T1和T2)及压强(p1和p2)下,产生Z的物质的量n和反应时间t的关系如图所示,根据图象回答下列问题:

(1)温度T1和T2的关系为T1____ (填“>”、“<”或“=”,下同)T2,压强p1和p2的关系为p1____ p2。
(2)a____ 1。
(3)该反应的正反应为____ (填“吸热”或“放热”反应)。
 3Z(g)在不同温度(T1和T2)及压强(p1和p2)下,产生Z的物质的量n和反应时间t的关系如图所示,根据图象回答下列问题:
3Z(g)在不同温度(T1和T2)及压强(p1和p2)下,产生Z的物质的量n和反应时间t的关系如图所示,根据图象回答下列问题:
(1)温度T1和T2的关系为T1
(2)a
(3)该反应的正反应为
您最近半年使用:0次
解题方法
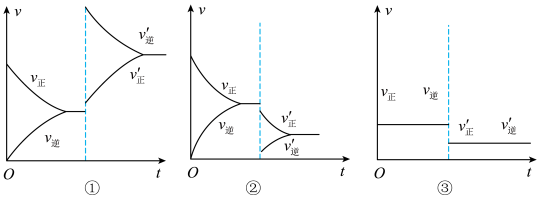
4 . 已知反应mA(g)+nB(g)⇌pC(g)+qD(g),当反应达到平衡后,改变压强,其反应速率的变化曲线分别如图所示。
回答下列问题:
(1)①表示改变压强的方式是________ (填“增大”或“减小”,下同)压强,化学平衡________ (填“正向”“逆向”或“不”,下同)移动,m+n__________ (填“>”“<”或“=”,下同)p+q。
(2)②表示改变压强的方式是___________ 压强,化学平衡___________ 移动,m+n___________ p+q。
(3)③表示改变压强的方式是___________ 压强,化学平衡___________ 移动,m+n___________ p+q。

回答下列问题:
(1)①表示改变压强的方式是
(2)②表示改变压强的方式是
(3)③表示改变压强的方式是
您最近半年使用:0次
5 . 一定条件下,某可逆反应在密闭容器中建立化学平衡,在 时刻改变某一个条件,建立新的平衡,其
时刻改变某一个条件,建立新的平衡,其 图像如下:
图像如下:
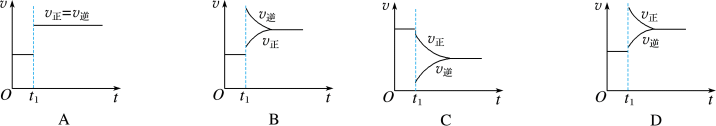
(1)对于反应 ,
, 时刻缩小容器体积,其图像为
时刻缩小容器体积,其图像为___________ (填字母),平衡___________ (填“向正反应方向”、“向逆反应方向”或“不”)移动。
(2)对于反应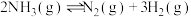 ,
, 时刻增大容器体积,其图像为
时刻增大容器体积,其图像为___________ (填字母),平衡___________ (填“向正反应方向”、“向逆反应方向”或“不”)移动。
(3)对于反应 ,
, 时刻缩小容器体积,其图像为
时刻缩小容器体积,其图像为___________ (填字母),平衡___________ (填“向正反应方向”、“向逆反应方向”或“不”)移动。
 时刻改变某一个条件,建立新的平衡,其
时刻改变某一个条件,建立新的平衡,其 图像如下:
图像如下:
(1)对于反应
 ,
, 时刻缩小容器体积,其图像为
时刻缩小容器体积,其图像为(2)对于反应
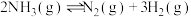 ,
, 时刻增大容器体积,其图像为
时刻增大容器体积,其图像为(3)对于反应
 ,
, 时刻缩小容器体积,其图像为
时刻缩小容器体积,其图像为
您最近半年使用:0次
2023-08-30更新
|
650次组卷
|
2卷引用:第二章 化学反应速率与化学平衡 第二节 化学平衡 第3课时 影响化学平衡的因素
6 . 甲醇既是重要的化工原料,又可作为燃料。利用合成气(主要成分为CO、CO2和H2)在催化剂作用下合成甲醇。发生的主要反应如下:
①CO(g)+2H2(g) CH3OH(g) ΔH1=-99 kJ·mol-1
CH3OH(g) ΔH1=-99 kJ·mol-1
②CO2(g)+3H2(g) CH3OH(g)+H2O(g) ΔH2=-58 kJ·mol-1
CH3OH(g)+H2O(g) ΔH2=-58 kJ·mol-1
③CO2(g)+H2(g) CO(g)+H2O(g) ΔH3=+41 kJ·mol-1
CO(g)+H2O(g) ΔH3=+41 kJ·mol-1
回答下列问题:
(1)反应①的化学平衡常数K的表达式为___________ ;图1中能正确反映平衡常数K随温度变化关系的曲线为___________ (填曲线标记字母),其判断理由是___________ 。

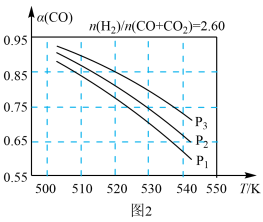
(2)合成气组成 =2.60时,体系中的CO平衡转化率(α)与温度和压强的关系如图2所示。α(CO)值随温度升高而
=2.60时,体系中的CO平衡转化率(α)与温度和压强的关系如图2所示。α(CO)值随温度升高而___________ (填“增大”或“减小”),其原因是___________ ;图2中的压强由大到小为___________ ,其判断理由是___________ 。
①CO(g)+2H2(g)
 CH3OH(g) ΔH1=-99 kJ·mol-1
CH3OH(g) ΔH1=-99 kJ·mol-1②CO2(g)+3H2(g)
 CH3OH(g)+H2O(g) ΔH2=-58 kJ·mol-1
CH3OH(g)+H2O(g) ΔH2=-58 kJ·mol-1③CO2(g)+H2(g)
 CO(g)+H2O(g) ΔH3=+41 kJ·mol-1
CO(g)+H2O(g) ΔH3=+41 kJ·mol-1回答下列问题:
(1)反应①的化学平衡常数K的表达式为

(2)合成气组成
 =2.60时,体系中的CO平衡转化率(α)与温度和压强的关系如图2所示。α(CO)值随温度升高而
=2.60时,体系中的CO平衡转化率(α)与温度和压强的关系如图2所示。α(CO)值随温度升高而
您最近半年使用:0次
解题方法
7 . 美国Bay工厂使用石油热裂解的副产物甲烷来制取氢气,其过程分两步进行;
第一步:CH4(g)+H2O(g) CO(g)+3H2(g) △H>0
CO(g)+3H2(g) △H>0
第二步:CO(g)+H2O(g) H2(g)+CO2(g)
H2(g)+CO2(g)
(1)其他条件相同时、第Ⅰ步反应中CH4的平衡转化率随压强和温度的变化如图所示。
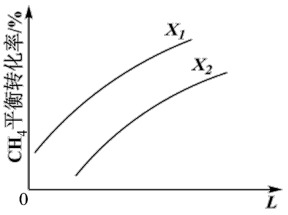
图中L表示____ (填“温度”或“压强”)。其另外一个物理量X1____ X2(填“>”或“<”)。
(2)反应CO(g)+H2O(g) H2(g)+CO2(g)的平衡常数K随湿度的变化如表所示。
H2(g)+CO2(g)的平衡常数K随湿度的变化如表所示。
①从表中数据可以推断,此反应的正反应为____ (填“吸热”或“放热”)反应。
②500℃时,向恒容密闭容器中充入CO(g)和H2O(g)各3mol,达到平衡后CO(g)的转化率为____ ;若该反应在绝热容器(与外界环境没有热交换)中进行,达到平衡后CO(g)的转化率将____ (填“增大”、“减小”或“不变”)。
③在830℃时,向恒容密闭容器中充入2molCO(g),5molH2O(g),4molH2(g)和3molCO2(g),此时v正____ v逆(填“>”、“<”或“=”)。
第一步:CH4(g)+H2O(g)
 CO(g)+3H2(g) △H>0
CO(g)+3H2(g) △H>0第二步:CO(g)+H2O(g)
 H2(g)+CO2(g)
H2(g)+CO2(g)(1)其他条件相同时、第Ⅰ步反应中CH4的平衡转化率随压强和温度的变化如图所示。

图中L表示
(2)反应CO(g)+H2O(g)
 H2(g)+CO2(g)的平衡常数K随湿度的变化如表所示。
H2(g)+CO2(g)的平衡常数K随湿度的变化如表所示。| 温度/℃ | 400 | 500 | 830 | 1000 |
| 平衡常数K | 10 | 9 | 1 | 0.6 |
①从表中数据可以推断,此反应的正反应为
②500℃时,向恒容密闭容器中充入CO(g)和H2O(g)各3mol,达到平衡后CO(g)的转化率为
③在830℃时,向恒容密闭容器中充入2molCO(g),5molH2O(g),4molH2(g)和3molCO2(g),此时v正
您最近半年使用:0次
2023高三·全国·专题练习
8 . 现代制备乙烯常用乙烷氧化裂解法,主反应为C2H6(g)+ O2(g)
O2(g) C2H4(g)+H2O(g) ΔH=−110kJ·mol-1,反应时还会生成CH4、CO、CO2等副产物(副反应均为放热反应),如图所示为温度对乙烷氧化裂解反应的影响。[乙烯选择性=
C2H4(g)+H2O(g) ΔH=−110kJ·mol-1,反应时还会生成CH4、CO、CO2等副产物(副反应均为放热反应),如图所示为温度对乙烷氧化裂解反应的影响。[乙烯选择性= ×100%;乙烯收率=乙烷转化率×乙烯选择性]
×100%;乙烯收率=乙烷转化率×乙烯选择性]________ ,反应的最佳温度为_________ 。
A.650℃ B.700℃ C.775℃ D.850℃
(2)工业上,保持体系总压强恒定在100kPa下进行该反应,且通常在乙烷和氧气的混合气体中掺入惰性气体(惰性气体的体积分数为70%),掺入惰性气体的目的是___________ 。
 O2(g)
O2(g) C2H4(g)+H2O(g) ΔH=−110kJ·mol-1,反应时还会生成CH4、CO、CO2等副产物(副反应均为放热反应),如图所示为温度对乙烷氧化裂解反应的影响。[乙烯选择性=
C2H4(g)+H2O(g) ΔH=−110kJ·mol-1,反应时还会生成CH4、CO、CO2等副产物(副反应均为放热反应),如图所示为温度对乙烷氧化裂解反应的影响。[乙烯选择性= ×100%;乙烯收率=乙烷转化率×乙烯选择性]
×100%;乙烯收率=乙烷转化率×乙烯选择性]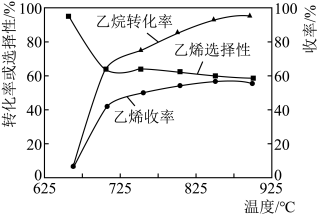
A.650℃ B.700℃ C.775℃ D.850℃
(2)工业上,保持体系总压强恒定在100kPa下进行该反应,且通常在乙烷和氧气的混合气体中掺入惰性气体(惰性气体的体积分数为70%),掺入惰性气体的目的是
您最近半年使用:0次
9 . (一)一种工业制硝酸的方法经历下列几个步骤:
 △H1<0
△H1<0
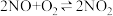 △H2<0
△H2<0
 △H3<0
△H3<0
已知:NO在1000℃以上会发生分解反应。
(1)工业生产中未直接在一个设备中将NH3催化氧化至NO2,而设计了两步氧化,中间经过热交换器降温,这样做的目的除了节约能源,还有_______________ 目的;
(2)实验发现,单位时间内NH3的氧化率[ ]会随着温度的升高先增大后减小(如图所示),分析1000℃后NH3的氧化率减小的可能原因
]会随着温度的升高先增大后减小(如图所示),分析1000℃后NH3的氧化率减小的可能原因________________ 。

(3) 的反应历程如下:
的反应历程如下:
反应Ⅰ: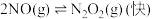 △H1<0
△H1<0

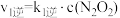
反应Ⅱ: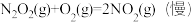 △H2<0
△H2<0
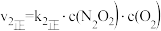
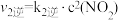
①一定条件下,反应 达到平衡状态,平衡常数K=
达到平衡状态,平衡常数K=________________ 。(用含k1正、k1逆、k2正、k2逆的代数式表示);
②已知反应速率常数k随温度升高而增大,则升高温度后k2正增大的倍数________________ k2逆增大的倍数(填“大于”“小于”或“等于”)。
(二)工业上也可以直接由N2O4合成HNO3,其中最关键的步骤为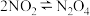 ,利用现代手持技术传感器可以探究压强对该平衡的影响。
,利用现代手持技术传感器可以探究压强对该平衡的影响。
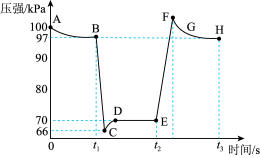
在恒定温度和标准压强条件下,往针筒中充入一定体积的NO2气体后密封并保持活塞位置不变。分别在t1、t2时迅速移动活塞后并保持活塞位置不变,测定针筒内气体压强变化如图所示。
(4)有关该过程说法正确的是_______________ 。
a.E、H两点对应的NO2的体积分数较大的为E点
b.B向里快速推注射器活塞,E向外快速拉注射器活塞
c.B、C、D三点正反应速率最大的是B点
d.C点时体系的颜色比D点深
(5)求D点Kp=_______________ (不必化成小数);
(6)图像中C、E两点气体平均摩尔质量最大的点为_______________ (填代号)。
 △H1<0
△H1<0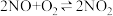 △H2<0
△H2<0 △H3<0
△H3<0已知:NO在1000℃以上会发生分解反应。
(1)工业生产中未直接在一个设备中将NH3催化氧化至NO2,而设计了两步氧化,中间经过热交换器降温,这样做的目的除了节约能源,还有
(2)实验发现,单位时间内NH3的氧化率[
 ]会随着温度的升高先增大后减小(如图所示),分析1000℃后NH3的氧化率减小的可能原因
]会随着温度的升高先增大后减小(如图所示),分析1000℃后NH3的氧化率减小的可能原因
(3)
 的反应历程如下:
的反应历程如下:反应Ⅰ:
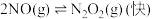 △H1<0
△H1<0 
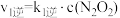
反应Ⅱ:
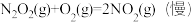 △H2<0
△H2<0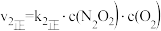
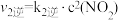
①一定条件下,反应
 达到平衡状态,平衡常数K=
达到平衡状态,平衡常数K=②已知反应速率常数k随温度升高而增大,则升高温度后k2正增大的倍数
(二)工业上也可以直接由N2O4合成HNO3,其中最关键的步骤为
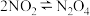 ,利用现代手持技术传感器可以探究压强对该平衡的影响。
,利用现代手持技术传感器可以探究压强对该平衡的影响。
在恒定温度和标准压强条件下,往针筒中充入一定体积的NO2气体后密封并保持活塞位置不变。分别在t1、t2时迅速移动活塞后并保持活塞位置不变,测定针筒内气体压强变化如图所示。
(4)有关该过程说法正确的是
a.E、H两点对应的NO2的体积分数较大的为E点
b.B向里快速推注射器活塞,E向外快速拉注射器活塞
c.B、C、D三点正反应速率最大的是B点
d.C点时体系的颜色比D点深
(5)求D点Kp=
(6)图像中C、E两点气体平均摩尔质量最大的点为
您最近半年使用:0次
10 . 一定条件下,某可逆反应在密闭容器中建立化学平衡,在t1时刻改变某一个条件,建立新的平衡,其v-t图像如下:

(1)对于反应:2SO2(g)+O2(g) 2SO3(g),t1时刻缩小容器体积,其图像为
2SO3(g),t1时刻缩小容器体积,其图像为________ (填字母,下同),平衡_________ (填“向正反应方向”“向逆反应方向”或“不”,下同)移动。
(2)对于反应2NH3(g) N2(g)+3H2(g),t1时刻增大容器体积,其图像为
N2(g)+3H2(g),t1时刻增大容器体积,其图像为________ ,平衡__________________ 移动。
(3)对于反应H2(g)+I2(g) 2HI(g),t1时刻缩小容器体积,其图像为
2HI(g),t1时刻缩小容器体积,其图像为________ ,平衡________ 移动。

(1)对于反应:2SO2(g)+O2(g)
 2SO3(g),t1时刻缩小容器体积,其图像为
2SO3(g),t1时刻缩小容器体积,其图像为(2)对于反应2NH3(g)
 N2(g)+3H2(g),t1时刻增大容器体积,其图像为
N2(g)+3H2(g),t1时刻增大容器体积,其图像为(3)对于反应H2(g)+I2(g)
 2HI(g),t1时刻缩小容器体积,其图像为
2HI(g),t1时刻缩小容器体积,其图像为
您最近半年使用:0次
2022-09-27更新
|
985次组卷
|
4卷引用:云南省砚山县第二高级中学2021-2022学年高二下学期期中(4月)考试化学试题



