1 . 可逆反应mA(g)+nB(g)⇌pC(g)+qD(g)的相关物质体积分数的变化图像如下,请回答下列问题:

(1)温度T1_______ T2(填“>”、“<”或“=”,下同)。
(2)压强p1_______ p2。
(3)m+n_______ p+q。
(4)正反应为_______ (填“放热”或“吸热”)反应。

(1)温度T1
(2)压强p1
(3)m+n
(4)正反应为
您最近半年使用:0次
名校
2 . 氮的化合物在生产、生活中广泛存在。回答下列问题:
(1)用焦炭还原NO的反应为2NO(g)+C(s) N2(g)+CO2(g),向容积均为1L的甲、乙、丙三个恒容、恒温(反应温度分别为400°C、400°C、T°C)容器中分别加入足量的焦炭和一定量的NO,测得各容器中n(NO)随反应时间t的变化情况如下表所示:
N2(g)+CO2(g),向容积均为1L的甲、乙、丙三个恒容、恒温(反应温度分别为400°C、400°C、T°C)容器中分别加入足量的焦炭和一定量的NO,测得各容器中n(NO)随反应时间t的变化情况如下表所示:
①该反应为___________ (填“放热”或“吸热”)反应,该反应的平衡常数的表达式为K=___________ 。
②乙容器在200min达到平衡状态,则0~200min内用NO的浓度变化表示的平均反应速率v(NO)=___________ 。
(2)用焦炭还原NO2的反应为2NO2(g)+2C(s) N2(g)+2CO2(g)。在恒温(T°C)条件下,1molNO2和足量的焦炭发生该反应,测得平衡时NO2和CO2的物质的量浓度与平衡总压的关系如图所示。
N2(g)+2CO2(g)。在恒温(T°C)条件下,1molNO2和足量的焦炭发生该反应,测得平衡时NO2和CO2的物质的量浓度与平衡总压的关系如图所示。
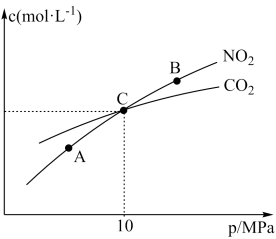
①A、B两点的浓度平衡常数关系为Kc(A)___________ Kc(B)(填“<”“>”或“=”)。A、B、C三点中,NO2的平衡转化率最高的是___________ 点(填“A”“B”或“C”)。
②该温度(T°C)下,反应的压强平衡常数Kp=___________ MPa(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
(1)用焦炭还原NO的反应为2NO(g)+C(s)
 N2(g)+CO2(g),向容积均为1L的甲、乙、丙三个恒容、恒温(反应温度分别为400°C、400°C、T°C)容器中分别加入足量的焦炭和一定量的NO,测得各容器中n(NO)随反应时间t的变化情况如下表所示:
N2(g)+CO2(g),向容积均为1L的甲、乙、丙三个恒容、恒温(反应温度分别为400°C、400°C、T°C)容器中分别加入足量的焦炭和一定量的NO,测得各容器中n(NO)随反应时间t的变化情况如下表所示:| t/min | 0 | 40 | 80 | 120 | 160 |
| n(NO)(甲容器)/mol | 2.00 | 1.50 | 1.10 | 0.80 | 0.80 |
| n(NO)(乙容器)/mol | 1.00 | 0.80 | 0.65 | 0.53 | 0.45 |
| n(NO)(丙容器)/mol | 2.00 | 1.45 | 1.00 | 1.00 | 1.00 |
②乙容器在200min达到平衡状态,则0~200min内用NO的浓度变化表示的平均反应速率v(NO)=
(2)用焦炭还原NO2的反应为2NO2(g)+2C(s)
 N2(g)+2CO2(g)。在恒温(T°C)条件下,1molNO2和足量的焦炭发生该反应,测得平衡时NO2和CO2的物质的量浓度与平衡总压的关系如图所示。
N2(g)+2CO2(g)。在恒温(T°C)条件下,1molNO2和足量的焦炭发生该反应,测得平衡时NO2和CO2的物质的量浓度与平衡总压的关系如图所示。
①A、B两点的浓度平衡常数关系为Kc(A)
②该温度(T°C)下,反应的压强平衡常数Kp=
您最近半年使用:0次
名校
3 . 在一定条件下,xA+yB⇌zC的反应达到平衡.
(1)已知A、B、C都是气体,在减压后平衡向逆反应方向移动,则x、y、z之间的关系是___ 。
(2)已知C是气体,且x+y=z,在增大压强时,如果平衡发生移动,则向____ 移动.(填“正向”、“逆向”、“无法判断”)
(3)已知B、C是气体,当其他条件不变,增大A的物质的量时,平衡不移动,则A是_____ 态.(填“气”、“液”、“固”)
(4)加热后C的质量分数减少,则正反应是_____ 热反应。
(1)已知A、B、C都是气体,在减压后平衡向逆反应方向移动,则x、y、z之间的关系是
(2)已知C是气体,且x+y=z,在增大压强时,如果平衡发生移动,则向
(3)已知B、C是气体,当其他条件不变,增大A的物质的量时,平衡不移动,则A是
(4)加热后C的质量分数减少,则正反应是
您最近半年使用:0次
2021-01-09更新
|
146次组卷
|
5卷引用:广西柳州市城中区第二中学2016-2017学年高一下学期期末考试化学试题
4 . 化学平衡移动原理:
(1)增大反应物浓度或减少生成物浓度,平衡___________ 移动;
(2)升高温度,平衡_________ 移动;
(3)增大压强,平衡______ 移动;
(4)使用催化剂,平衡_________ 移动。
(1)增大反应物浓度或减少生成物浓度,平衡
(2)升高温度,平衡
(3)增大压强,平衡
(4)使用催化剂,平衡
您最近半年使用:0次
5 . 在密闭容器内使3molH2和1molN2混合发生下列反应:3H2+N2 2NH3 △H<0(下列空格选填“向正反应方向”“向逆反应方向”“不”)
2NH3 △H<0(下列空格选填“向正反应方向”“向逆反应方向”“不”)
(1)当达到平衡时,保持体积不变,升高温度,平衡将_______ 移动。
(2)当达到平衡时,充入Ar气,并保持体积不变,平衡将_______ 移动。
(3)当达到平衡时,充入Ar气,并保持压强不变,平衡将______ 移动。
(4)当达到平衡时,充入N2并保持体积不变,平衡将________ 移动。
 2NH3 △H<0(下列空格选填“向正反应方向”“向逆反应方向”“不”)
2NH3 △H<0(下列空格选填“向正反应方向”“向逆反应方向”“不”)(1)当达到平衡时,保持体积不变,升高温度,平衡将
(2)当达到平衡时,充入Ar气,并保持体积不变,平衡将
(3)当达到平衡时,充入Ar气,并保持压强不变,平衡将
(4)当达到平衡时,充入N2并保持体积不变,平衡将
您最近半年使用:0次
名校
解题方法
6 . (1)反应A(g)+3B(g) 2C(g)+2D(g)在四种不同情况下的反应速率分别为①VA=0.15mol/(L ·S) ②VB=0.6 mol/(L ·S) ③VC=0.4 mol/(L ·S) ④VD=0.45 mol/(L ·S),则所表示的反应快慢顺序为
2C(g)+2D(g)在四种不同情况下的反应速率分别为①VA=0.15mol/(L ·S) ②VB=0.6 mol/(L ·S) ③VC=0.4 mol/(L ·S) ④VD=0.45 mol/(L ·S),则所表示的反应快慢顺序为_________________________ (填序号)。
(2)密闭容积可变容器中存在2NO2(g) N2O4(g)转化关系,保持温度不变,则压缩容器体积引起的加压,平衡向
N2O4(g)转化关系,保持温度不变,则压缩容器体积引起的加压,平衡向________ 移动(填“左”或“右”),气体颜色变________ (填“深”或“浅”);扩大容器体积,平衡向________ 移动(填“左”或“右”),气体颜色变________ (填“深”或“浅”),平衡常数K___________ (填“变大”、“变小”或“不变”)。
(3)已知反应A(s)+3B(g) 2C(g)+2D(g)在一定温度下达平衡,则该反应的平衡常数表达式为
2C(g)+2D(g)在一定温度下达平衡,则该反应的平衡常数表达式为__________________ ,此反应△S_____ 0(填“>”、“<”或“=”)。
 2C(g)+2D(g)在四种不同情况下的反应速率分别为①VA=0.15mol/(L ·S) ②VB=0.6 mol/(L ·S) ③VC=0.4 mol/(L ·S) ④VD=0.45 mol/(L ·S),则所表示的反应快慢顺序为
2C(g)+2D(g)在四种不同情况下的反应速率分别为①VA=0.15mol/(L ·S) ②VB=0.6 mol/(L ·S) ③VC=0.4 mol/(L ·S) ④VD=0.45 mol/(L ·S),则所表示的反应快慢顺序为(2)密闭容积可变容器中存在2NO2(g)
 N2O4(g)转化关系,保持温度不变,则压缩容器体积引起的加压,平衡向
N2O4(g)转化关系,保持温度不变,则压缩容器体积引起的加压,平衡向(3)已知反应A(s)+3B(g)
 2C(g)+2D(g)在一定温度下达平衡,则该反应的平衡常数表达式为
2C(g)+2D(g)在一定温度下达平衡,则该反应的平衡常数表达式为
您最近半年使用:0次
7 . T℃时,将3molA和2molB气体通入体积为2L的密闭容器中(容积不变),发生如下反应:3A(气)+B(气)  xC(气),2min时反应达到平衡状态(温度不变),剩余1.8molB,并测得C的浓度为O.4mol/L,请填写下列空白:
xC(气),2min时反应达到平衡状态(温度不变),剩余1.8molB,并测得C的浓度为O.4mol/L,请填写下列空白:
(1)反应达到平衡时,A、B两反应物的转化率之比为α(A):α(B)=___________ 。
(2)若继续向原平衡混合物的容器中通入少量氦气(氦气和A、B、C都不反应)后,下列说法中正确的是__ (填写字母序号)。
A.化学平衡向正反应方向移动 B.化学平衡向逆反应方向移动
C.化学平衡不会发生移动 D.正、逆反应的化学反应速率保持不变
(3)在T℃时,若向原平衡混合物的容器中再充入amolC,欲使达到新的平衡时,各物质的物质的量分数与原平衡相同,则至少应再充入__________ (填A或B)________ mol(用a表示)。
 xC(气),2min时反应达到平衡状态(温度不变),剩余1.8molB,并测得C的浓度为O.4mol/L,请填写下列空白:
xC(气),2min时反应达到平衡状态(温度不变),剩余1.8molB,并测得C的浓度为O.4mol/L,请填写下列空白:(1)反应达到平衡时,A、B两反应物的转化率之比为α(A):α(B)=
(2)若继续向原平衡混合物的容器中通入少量氦气(氦气和A、B、C都不反应)后,下列说法中正确的是
A.化学平衡向正反应方向移动 B.化学平衡向逆反应方向移动
C.化学平衡不会发生移动 D.正、逆反应的化学反应速率保持不变
(3)在T℃时,若向原平衡混合物的容器中再充入amolC,欲使达到新的平衡时,各物质的物质的量分数与原平衡相同,则至少应再充入
您最近半年使用:0次
8 . 炎热的夏天暴雨之前,空气中水蒸气含量大,气压低,鱼因缺氧出现翻塘死鱼现象,若不及时人工增氧会使鱼大量死亡,造成经济损失,请说明鱼塘翻塘缺氧的原因。____________
您最近半年使用:0次
名校
解题方法
9 . 现有下列可逆反应:A(g)+B(g)  xC(g),在不同条件下生成物C在反应混合物中的质量分数(C%)和反应时间(t)的关系如下图:
xC(g),在不同条件下生成物C在反应混合物中的质量分数(C%)和反应时间(t)的关系如下图:
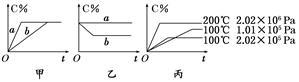
请根据图象回答下列问题:
(1)若甲图中两条曲线分别表示有催化剂和无催化剂的情况,则_______ 曲线表示无催化剂时的情况(填字母,下同);
(2)若乙图表示反应达到平衡后分别在恒温恒压条件下和恒温恒容条件下向平衡混合气体中充入惰性(与反应体系中任一物质均不反应)气体后的情况,则_______ 曲线表示恒温恒容的情况;
(3)根据丙图可以判断该可逆反应的正反应是_______ 热反应(填“吸”或“放”);
(4)化学计量数x的值_______ (填取值范围);判断的依据是________________ 。
 xC(g),在不同条件下生成物C在反应混合物中的质量分数(C%)和反应时间(t)的关系如下图:
xC(g),在不同条件下生成物C在反应混合物中的质量分数(C%)和反应时间(t)的关系如下图:
请根据图象回答下列问题:
(1)若甲图中两条曲线分别表示有催化剂和无催化剂的情况,则
(2)若乙图表示反应达到平衡后分别在恒温恒压条件下和恒温恒容条件下向平衡混合气体中充入惰性(与反应体系中任一物质均不反应)气体后的情况,则
(3)根据丙图可以判断该可逆反应的正反应是
(4)化学计量数x的值
您最近半年使用:0次
2016-12-09更新
|
1191次组卷
|
3卷引用:广西浦北中学2021-2022学年高二上学期第一次月考化学试题
广西浦北中学2021-2022学年高二上学期第一次月考化学试题(已下线)2014年高中化学人教版选修四第二章 化学反应速率与化学平衡练习卷【全国百强校】甘肃省天水一中2018-2019学年高二下学期寒假作业检测化学试题
11-12高二上·广西北海·期中
10 . 在密闭容器中进行可逆反应:CO (g)+NO2(g)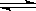 CO2(g)+NO (g)(正反应为放热反应),达到平衡后,只改变其中一个条件,对平衡的影响是:(填“向左”、“向右”、“不移动”或颜色“变深”、“变浅”或“不变化”)
CO2(g)+NO (g)(正反应为放热反应),达到平衡后,只改变其中一个条件,对平衡的影响是:(填“向左”、“向右”、“不移动”或颜色“变深”、“变浅”或“不变化”)
(1)增大容器的体积,平衡____________ ,反应混合物的颜色____________ ;
(2)通入CO2气体,平衡____________ ,反应混合物颜色_______________ ;
(3)升高温度,平衡_______________ ,反应混合物的颜色____________ ;
(4)加入一定量的N2,平衡____________ ,反应混合物的颜色___________ ;
(5)加入催化剂,平衡________________ 。
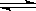 CO2(g)+NO (g)(正反应为放热反应),达到平衡后,只改变其中一个条件,对平衡的影响是:(填“向左”、“向右”、“不移动”或颜色“变深”、“变浅”或“不变化”)
CO2(g)+NO (g)(正反应为放热反应),达到平衡后,只改变其中一个条件,对平衡的影响是:(填“向左”、“向右”、“不移动”或颜色“变深”、“变浅”或“不变化”)(1)增大容器的体积,平衡
(2)通入CO2气体,平衡
(3)升高温度,平衡
(4)加入一定量的N2,平衡
(5)加入催化剂,平衡
您最近半年使用:0次



