名校
1 . 某温度下的密闭容器中:
①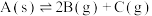 ;
;
②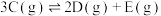
以上2个反应同时发生,10S后达平衡时, ,
,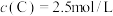 。
。
(1)加压时反应②的平衡___________ 移动。
A.向正反应方向 B.向逆反应方向 C.不移动
(2)该温度下反应①的平衡常数数值为___________ 。
①
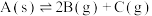 ;
;②
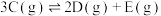
以上2个反应同时发生,10S后达平衡时,
 ,
,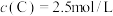 。
。(1)加压时反应②的平衡
A.向正反应方向 B.向逆反应方向 C.不移动
(2)该温度下反应①的平衡常数数值为
您最近半年使用:0次
名校
2 . I.一定温度下,某容器中加入足量的碳酸钙发生反应: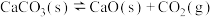 △H>0;一段时间后达到平衡。
△H>0;一段时间后达到平衡。
(1)该反应的化学平衡常数表达式为K=___________ ,为了提高CO2的生成率,可采取的措施___________ 。
A.减压 B.升温 C.增加碳酸钙的量 D.转移出CO2
(2)对于该反应,下列说法正确的是___________ 。
A.将体积缩小为原来的一半,当体系再次达到平衡时,CO2的浓度不变
B.将容器缩小为原来的一半,平衡不移动
C.将容器扩大为原来的两倍,平衡发生移动,再次平衡后,气体密度不变
D.增大压强,平衡逆向移动,K值减小
E.将体积增大为原来的2倍,再次达到平衡时,体系内压强不变
F.保持容器体积不变,充入He,平衡不移动
Ⅱ.
(3)在恒温恒压密闭容器中通入CO和H2O各1 发生反应
发生反应 ,当反应达到平衡后,维持温度与压强不变,
,当反应达到平衡后,维持温度与压强不变, 时再通入各1
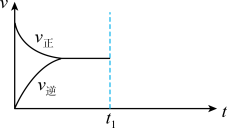
时再通入各1 的CO和H2O的混合气体,请在下图中画出正反应和逆反应速率在
的CO和H2O的混合气体,请在下图中画出正反应和逆反应速率在 后随时间t变化的曲线图
后随时间t变化的曲线图___________ 。
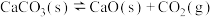 △H>0;一段时间后达到平衡。
△H>0;一段时间后达到平衡。(1)该反应的化学平衡常数表达式为K=
A.减压 B.升温 C.增加碳酸钙的量 D.转移出CO2
(2)对于该反应,下列说法正确的是
A.将体积缩小为原来的一半,当体系再次达到平衡时,CO2的浓度不变
B.将容器缩小为原来的一半,平衡不移动
C.将容器扩大为原来的两倍,平衡发生移动,再次平衡后,气体密度不变
D.增大压强,平衡逆向移动,K值减小
E.将体积增大为原来的2倍,再次达到平衡时,体系内压强不变
F.保持容器体积不变,充入He,平衡不移动
Ⅱ.
(3)在恒温恒压密闭容器中通入CO和H2O各1
 发生反应
发生反应 ,当反应达到平衡后,维持温度与压强不变,
,当反应达到平衡后,维持温度与压强不变, 时再通入各1
时再通入各1 的CO和H2O的混合气体,请在下图中画出正反应和逆反应速率在
的CO和H2O的混合气体,请在下图中画出正反应和逆反应速率在 后随时间t变化的曲线图
后随时间t变化的曲线图
您最近半年使用:0次
名校
3 . 合成氨工艺是人工固氮最重要的途径。请回答:
(1)合成氨时压强越大,原料的转化率越高,我国合成氨厂采用的压强为10Mpa-30Mpa,没有采用过大的压强的原因是___________ 。
(2)当温度、压强一定时,在原料气( 和
和 的比例不变)中添加少量惰性气体,
的比例不变)中添加少量惰性气体,_______ 利于提高平衡转化率(填“是”或“不”)。
(3)合成氨的原料气 可以通过天然气和二氧化碳转化制备,已知
可以通过天然气和二氧化碳转化制备,已知 、
、 和CO的燃烧热(△H)分别为
和CO的燃烧热(△H)分别为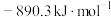 、
、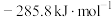 、
、 。则制备
。则制备 的热化学反应方程式为
的热化学反应方程式为___________________ ;合成氨前,原料气必须经过净化处理,以防止___________ 和安全事故发生。
(4)若将2.0mol 和6.0mol
和6.0mol  通入体积为1L的密闭容器中,分别在
通入体积为1L的密闭容器中,分别在 和
和 温度下进行反应。曲线A表示
温度下进行反应。曲线A表示 温度下
温度下 的变化,曲线B表示
的变化,曲线B表示 温度下
温度下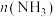 的变化,
的变化, 温度下反应到a点恰好达到平衡。
温度下反应到a点恰好达到平衡。

①温度
___________ (填“>”“<”或“=”下同) 。
。 温度下曲线B上的点
温度下曲线B上的点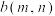 为恰好平衡时的点,则m
为恰好平衡时的点,则m___________ 12,n___________ 2;
② 温度下,若某时刻容器内气体的压强为起始时的80%,则此时v(正)
温度下,若某时刻容器内气体的压强为起始时的80%,则此时v(正)___________ (填“>”“<”或“=”)v(逆)。
(1)合成氨时压强越大,原料的转化率越高,我国合成氨厂采用的压强为10Mpa-30Mpa,没有采用过大的压强的原因是
(2)当温度、压强一定时,在原料气(
 和
和 的比例不变)中添加少量惰性气体,
的比例不变)中添加少量惰性气体,(3)合成氨的原料气
 可以通过天然气和二氧化碳转化制备,已知
可以通过天然气和二氧化碳转化制备,已知 、
、 和CO的燃烧热(△H)分别为
和CO的燃烧热(△H)分别为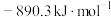 、
、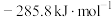 、
、 。则制备
。则制备 的热化学反应方程式为
的热化学反应方程式为(4)若将2.0mol
 和6.0mol
和6.0mol  通入体积为1L的密闭容器中,分别在
通入体积为1L的密闭容器中,分别在 和
和 温度下进行反应。曲线A表示
温度下进行反应。曲线A表示 温度下
温度下 的变化,曲线B表示
的变化,曲线B表示 温度下
温度下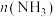 的变化,
的变化, 温度下反应到a点恰好达到平衡。
温度下反应到a点恰好达到平衡。
①温度

 。
。 温度下曲线B上的点
温度下曲线B上的点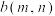 为恰好平衡时的点,则m
为恰好平衡时的点,则m②
 温度下,若某时刻容器内气体的压强为起始时的80%,则此时v(正)
温度下,若某时刻容器内气体的压强为起始时的80%,则此时v(正)
您最近半年使用:0次
2023-10-23更新
|
189次组卷
|
2卷引用:辽宁省实验中学2023-2024学年高二上学期10月月考化学试题
4 . (一)一种工业制硝酸的方法经历下列几个步骤:
 △H1<0
△H1<0
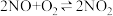 △H2<0
△H2<0
 △H3<0
△H3<0
已知:NO在1000℃以上会发生分解反应。
(1)工业生产中未直接在一个设备中将NH3催化氧化至NO2,而设计了两步氧化,中间经过热交换器降温,这样做的目的除了节约能源,还有_______________ 目的;
(2)实验发现,单位时间内NH3的氧化率[ ]会随着温度的升高先增大后减小(如图所示),分析1000℃后NH3的氧化率减小的可能原因
]会随着温度的升高先增大后减小(如图所示),分析1000℃后NH3的氧化率减小的可能原因________________ 。

(3) 的反应历程如下:
的反应历程如下:
反应Ⅰ: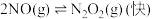 △H1<0
△H1<0

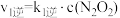
反应Ⅱ: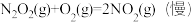 △H2<0
△H2<0
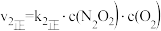
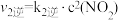
①一定条件下,反应 达到平衡状态,平衡常数K=
达到平衡状态,平衡常数K=________________ 。(用含k1正、k1逆、k2正、k2逆的代数式表示);
②已知反应速率常数k随温度升高而增大,则升高温度后k2正增大的倍数________________ k2逆增大的倍数(填“大于”“小于”或“等于”)。
(二)工业上也可以直接由N2O4合成HNO3,其中最关键的步骤为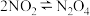 ,利用现代手持技术传感器可以探究压强对该平衡的影响。
,利用现代手持技术传感器可以探究压强对该平衡的影响。
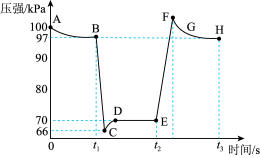
在恒定温度和标准压强条件下,往针筒中充入一定体积的NO2气体后密封并保持活塞位置不变。分别在t1、t2时迅速移动活塞后并保持活塞位置不变,测定针筒内气体压强变化如图所示。
(4)有关该过程说法正确的是_______________ 。
a.E、H两点对应的NO2的体积分数较大的为E点
b.B向里快速推注射器活塞,E向外快速拉注射器活塞
c.B、C、D三点正反应速率最大的是B点
d.C点时体系的颜色比D点深
(5)求D点Kp=_______________ (不必化成小数);
(6)图像中C、E两点气体平均摩尔质量最大的点为_______________ (填代号)。
 △H1<0
△H1<0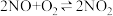 △H2<0
△H2<0 △H3<0
△H3<0已知:NO在1000℃以上会发生分解反应。
(1)工业生产中未直接在一个设备中将NH3催化氧化至NO2,而设计了两步氧化,中间经过热交换器降温,这样做的目的除了节约能源,还有
(2)实验发现,单位时间内NH3的氧化率[
 ]会随着温度的升高先增大后减小(如图所示),分析1000℃后NH3的氧化率减小的可能原因
]会随着温度的升高先增大后减小(如图所示),分析1000℃后NH3的氧化率减小的可能原因
(3)
 的反应历程如下:
的反应历程如下:反应Ⅰ:
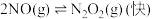 △H1<0
△H1<0 
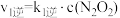
反应Ⅱ:
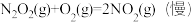 △H2<0
△H2<0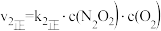
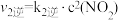
①一定条件下,反应
 达到平衡状态,平衡常数K=
达到平衡状态,平衡常数K=②已知反应速率常数k随温度升高而增大,则升高温度后k2正增大的倍数
(二)工业上也可以直接由N2O4合成HNO3,其中最关键的步骤为
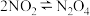 ,利用现代手持技术传感器可以探究压强对该平衡的影响。
,利用现代手持技术传感器可以探究压强对该平衡的影响。
在恒定温度和标准压强条件下,往针筒中充入一定体积的NO2气体后密封并保持活塞位置不变。分别在t1、t2时迅速移动活塞后并保持活塞位置不变,测定针筒内气体压强变化如图所示。
(4)有关该过程说法正确的是
a.E、H两点对应的NO2的体积分数较大的为E点
b.B向里快速推注射器活塞,E向外快速拉注射器活塞
c.B、C、D三点正反应速率最大的是B点
d.C点时体系的颜色比D点深
(5)求D点Kp=
(6)图像中C、E两点气体平均摩尔质量最大的点为
您最近半年使用:0次
5 . 已知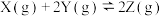
 。为了探究反应条件对该反应的影响,分别向四个密闭容器中充入一定量的反应物,反应条件及达到平衡时的有关数据如表所示,请回答下列问题:
。为了探究反应条件对该反应的影响,分别向四个密闭容器中充入一定量的反应物,反应条件及达到平衡时的有关数据如表所示,请回答下列问题:
(1)设计实验1、3的目的是探究_____ 对反应的影响,实验_____ 是为了探究压强对反应的影响。
(2)
_____ (填“>”、“<”或“=”)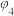 。
。
(3) 、
、 、
、 由大到小的顺序为
由大到小的顺序为_____ 。
(4) 、
、 、
、 、
、 的大小关系为
的大小关系为_____ 。
(5)若实验1、2、3、4中Z(g)的物质的量随时间的变化关系如图中曲线所示,实验1对应曲线b,则实验2、3分别对应曲线_____ 、_____ 。(填字母)
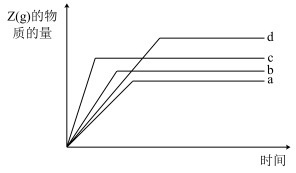
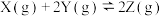
 。为了探究反应条件对该反应的影响,分别向四个密闭容器中充入一定量的反应物,反应条件及达到平衡时的有关数据如表所示,请回答下列问题:
。为了探究反应条件对该反应的影响,分别向四个密闭容器中充入一定量的反应物,反应条件及达到平衡时的有关数据如表所示,请回答下列问题:| 实验编号 | 1 | 2 | 3 | 4 |
| 反应物投入量 | 1molX(g)、2molY(g) | 1molX(g)、3molY(g) | 1molX(g)、2molY(g) | 1molX(g)、2molY(g) |
| 反应温度/℃ | 500 | 500 | 400 | 500 |
| 压强 | 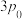 | 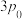 | 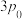 |  |
| 平衡时Z(g)的体积分数 |  | 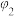 |  | 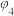 |
| Y(g)的平衡转化率 |  |  |  | 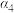 |
| 化学平衡常数 |  |  |  |  |
(2)

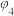 。
。(3)
 、
、 、
、 由大到小的顺序为
由大到小的顺序为(4)
 、
、 、
、 、
、 的大小关系为
的大小关系为(5)若实验1、2、3、4中Z(g)的物质的量随时间的变化关系如图中曲线所示,实验1对应曲线b,则实验2、3分别对应曲线

您最近半年使用:0次
2023-07-23更新
|
131次组卷
|
2卷引用:辽宁省葫芦岛市协作校2022-2023学年高二上学期期中考试化学试题
名校
6 . 肼( )是一种应用广泛的化工原料。工业上先合成氨气:
)是一种应用广泛的化工原料。工业上先合成氨气:
 ,再进一步制备肼。完成下列填空:
,再进一步制备肼。完成下列填空:
(1)合成氨需要选择合适的催化剂,分别选用A、B、C三种催化剂进行试验,所得结果如图所示(其他条件相同),则生产中适宜选择的催化剂是_______ (填“A”或“B”或“C”)

(2)一定条件下,对在密闭容器中进行的合成氨反应达平衡后,其他条件不变时,若同时压缩容器的体积和升高温度达新平衡后,与原平衡相比,请将有关物理量的变化的情况填入下表中(填“增大”、“减小”或“无法确定”)
(3)通常把拆开1mol某化学键所吸收的能量看成该化学键的键能。已知部分化学键的键能如下:
发射神舟飞船的长征火箭用了肼( ,气态)为燃料,若它在氧气(气态)中燃烧,生成
,气态)为燃料,若它在氧气(气态)中燃烧,生成 (气态)和
(气态)和 (气态)。该反应的热化学方程式为:
(气态)。该反应的热化学方程式为:_______ 。
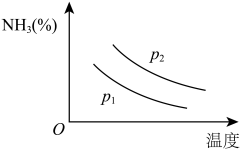
(4)氨主要用于生产化肥和硝酸。“十三五”期间,预计我国合成氨产量将保持稳中略增。下图是不同温度和不同压强下,反应达到平衡后,混合物中 含量(体积%)的变化情况,已知初始时
含量(体积%)的变化情况,已知初始时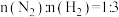 。判断
。判断 、
、 压强的大小关系,
压强的大小关系,
_______  (选填“>”、“<”或“=”)。
(选填“>”、“<”或“=”)。
(5)通过 传感器可监测
传感器可监测 的含量,其工作原理如图。
的含量,其工作原理如图。
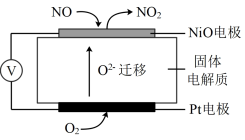
①Pt电极是电源的_______ (填“正”或“负”)极上发生的是_______ 反应(填“氧化”或“还原”)。
②写出NiO电极上的电极反应式:_______ 。
 )是一种应用广泛的化工原料。工业上先合成氨气:
)是一种应用广泛的化工原料。工业上先合成氨气:
 ,再进一步制备肼。完成下列填空:
,再进一步制备肼。完成下列填空:(1)合成氨需要选择合适的催化剂,分别选用A、B、C三种催化剂进行试验,所得结果如图所示(其他条件相同),则生产中适宜选择的催化剂是

(2)一定条件下,对在密闭容器中进行的合成氨反应达平衡后,其他条件不变时,若同时压缩容器的体积和升高温度达新平衡后,与原平衡相比,请将有关物理量的变化的情况填入下表中(填“增大”、“减小”或“无法确定”)
| 反应速率 | 平衡常数K | |
| 变化情况 |
| 化学键 | N—H | N—N | O=O | N≡N | O—H |
| 键能(kJ/mol) | 386 | 167 | 498 | 946 | 460 |
 ,气态)为燃料,若它在氧气(气态)中燃烧,生成
,气态)为燃料,若它在氧气(气态)中燃烧,生成 (气态)和
(气态)和 (气态)。该反应的热化学方程式为:
(气态)。该反应的热化学方程式为:(4)氨主要用于生产化肥和硝酸。“十三五”期间,预计我国合成氨产量将保持稳中略增。下图是不同温度和不同压强下,反应达到平衡后,混合物中
 含量(体积%)的变化情况,已知初始时
含量(体积%)的变化情况,已知初始时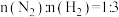 。判断
。判断 、
、 压强的大小关系,
压强的大小关系,
 (选填“>”、“<”或“=”)。
(选填“>”、“<”或“=”)。
(5)通过
 传感器可监测
传感器可监测 的含量,其工作原理如图。
的含量,其工作原理如图。
①Pt电极是电源的
②写出NiO电极上的电极反应式:
您最近半年使用:0次
7 . 在1L的密闭容器中,加入0.5molCaCO3,发生反应:CaCO3(s)⇌CaO(s)+CO2(g),图中A表示CO2的平衡浓度与温度的关系曲线。

(1)该反应正反应方向为_______ 热反应(填“吸”或“放”),温度为T5℃时,该反应的平衡常数 _______ 。
(2)达到平衡后,保持温度不变,再次通入1molCO2,平衡移动的方向_______ (填“正方向”、“逆方向”或“不”),再次平衡后容器内的压强 _______ (填“增大”、“减小”或“不变”)。
(3)加快该化学反应速率并能增加该反应进行程度的措施:_______ 。(写一种即可)

(1)该反应正反应方向为
(2)达到平衡后,保持温度不变,再次通入1molCO2,平衡移动的方向
(3)加快该化学反应速率并能增加该反应进行程度的措施:
您最近半年使用:0次
名校
8 . 工业上,裂解正丁烷可以获得乙烯、丙烯等化工原料。
反应1: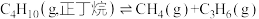

反应2: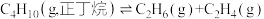

已知几种共价键的键能如下表:
(1)根据上述数据估算, =
=_______ kJ·mol-1。
(2)正丁烷和异丁烷之间转化的能量变化如图所示。
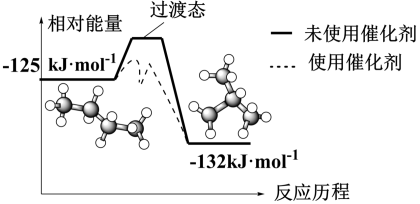
①正丁烷气体转化成异丁烷气体的热化学方程式为_______ 。
②下列有关催化剂的叙述错误的是_______ (填标号)。
A.能改变反应途径 B.能降低反应焓变
C.能加快反应速率 D.能增大平衡常数
(3)向密闭容器中投入一定量的正丁烷,发生反应1和反应2,测得正丁烷的平衡转化率(α)与压强(p)、温度(T)的关系如图所示。
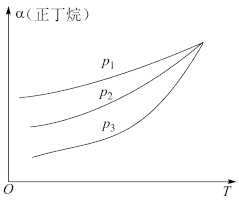
① 、
、 、
、 由小到大的顺序为
由小到大的顺序为_______ 。
②随着温度升高,三种不同压强下正丁烷的平衡转化率趋向相等,原因是_______ 。
(4)在一定温度下,向密闭容器中投入正丁烷,同时发生反应1和反应2。测得部分物质的浓度与时间的关系如图,平衡时压强为17akPa。
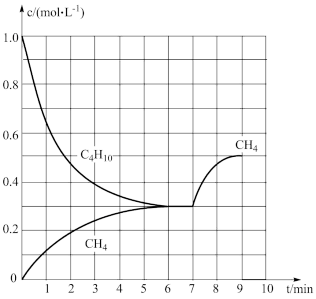
①7min时改变的条件可能是_______ (填标号)。
A.增大压强 B.增大正丁烷的浓度 C.加入催化剂
②该温度下,反应1的平衡常数
_______ kPa。(提示:组分分压=总压×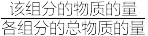 )
)
(5)以惰性材料为电极,正丁烷、空气在熔融盐(以MCO3为电解质)中构成的燃料电池的能量转化率高,通入空气的电极为_______ (填“正极”或“负极”)。
反应1:
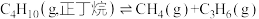

反应2:
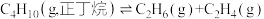

已知几种共价键的键能如下表:
| 共价键 | C—H |  | C—C |
| 键能/(kJ·mol-1) | 413 | 614 | 347 |
(1)根据上述数据估算,
 =
=(2)正丁烷和异丁烷之间转化的能量变化如图所示。

①正丁烷气体转化成异丁烷气体的热化学方程式为
②下列有关催化剂的叙述错误的是
A.能改变反应途径 B.能降低反应焓变
C.能加快反应速率 D.能增大平衡常数
(3)向密闭容器中投入一定量的正丁烷,发生反应1和反应2,测得正丁烷的平衡转化率(α)与压强(p)、温度(T)的关系如图所示。

①
 、
、 、
、 由小到大的顺序为
由小到大的顺序为②随着温度升高,三种不同压强下正丁烷的平衡转化率趋向相等,原因是
(4)在一定温度下,向密闭容器中投入正丁烷,同时发生反应1和反应2。测得部分物质的浓度与时间的关系如图,平衡时压强为17akPa。

①7min时改变的条件可能是
A.增大压强 B.增大正丁烷的浓度 C.加入催化剂
②该温度下,反应1的平衡常数

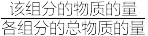 )
)(5)以惰性材料为电极,正丁烷、空气在熔融盐(以MCO3为电解质)中构成的燃料电池的能量转化率高,通入空气的电极为
您最近半年使用:0次
2021-12-03更新
|
884次组卷
|
10卷引用:辽宁省抚顺市第二中学2022届高三下学期高考预测化学试题
辽宁省抚顺市第二中学2022届高三下学期高考预测化学试题广东省2021-2022学年高三11月联考化学试题河南省名校联盟2021-2022学年高三上学期11月联考化学试题湖南省百所学校大联考2021-2022学年高三11月联考化学试题(已下线)第19周 晚练题-备战2022年高考化学周测与晚练(新高考专用)(已下线)押新高考卷17题 化学反应原理综合题-备战2022年高考化学临考题号押题(新高考通版)浙江省舟山市普陀中学2023届高三返校考试化学试题河北省保定市部分学校2021-2022学年高三上学期期中考试化学试题广东省韶关市2021-2022学年高三上学期期中考试化学试题(已下线)专题十 化学能与热能-实战高考·二轮复习核心突破
名校
解题方法
9 . 在一定条件下,可逆反应mA+nB pC达到平衡,若:
pC达到平衡,若:
(1)A、B、C都是气体,减小压强,平衡正向移动,则m+n和p的关系是___ 。
(2)A、C是气体,增加B的量,平衡不移动,则B为___ 。
(3)A、C是气体,而且m+n=p,增大压强可使平衡发生移动,则平衡移动的方向是___ 。
(4)加热后,可使 的质量增加,则正反应是
的质量增加,则正反应是___ (填“放热”或“吸热”)反应。
 pC达到平衡,若:
pC达到平衡,若:(1)A、B、C都是气体,减小压强,平衡正向移动,则m+n和p的关系是
(2)A、C是气体,增加B的量,平衡不移动,则B为
(3)A、C是气体,而且m+n=p,增大压强可使平衡发生移动,则平衡移动的方向是
(4)加热后,可使
 的质量增加,则正反应是
的质量增加,则正反应是
您最近半年使用:0次
2021-10-24更新
|
108次组卷
|
31卷引用:2014-2015学年辽宁实验分校高一下6月阶段测试化学试卷
2014-2015学年辽宁实验分校高一下6月阶段测试化学试卷(已下线)09~10年鹤岗一中高一下学期期末考试化学卷(已下线)2010年江苏省启东中学高二上学期期中考试化学卷(已下线)2010-2011学年广东省深圳高级中学高二下学期期中考试化学试卷(已下线)2010-2011学年江苏省启东中学高二上学期期中考试化学试题(理)(已下线)2011-2012年河北省南宫中学高二上学期9月份月考化学(理)试卷(已下线)2011-2012学年黑龙江省绥棱县第一中学高二上学期期末考试化学试卷(已下线)2011-2012年安徽红星中安工大附中高二下学期期中联考理科化学试卷(已下线)2011-2012学年广东始兴县风度中学高二下学期期中考试理综化学试卷(已下线)2011-2012学年广东省始兴县风度中学高二下学期期末考试理综化学卷(已下线)2012-2013学年甘肃省兰州一中高二上学期期末考试化学试卷(已下线)2012-2013学年山东省临沂市高二上学期期中考试化学试卷(已下线)2013-2014学年陕西省岐山县高二上学期期中质量检测理科化学试卷2014-2015学年天津市宝坻区四校高二11月联考化学试卷2015-2016学年陕西省西安一中高二上10月月考化学试卷2015-2016学年湖南省株洲十八中高二上学期期中(理)化学试卷2015-2016学年天津市和平区高二上学期期末考试化学试卷2015-2016学年湖南省怀化市会同三中高二上12月月考化学试卷2016-2017学年吉林省汪清六中高二上第一次月考化学试卷内蒙古阿拉善左旗高级中学2017-2018学年高二上学期期末考试化学试题甘肃省武威第五中学2017-2018学年高二下学期第二次月考化学试题甘肃省武威第五中学2018-2019学年高二上学期期末考试化学试题黑龙江省齐齐哈尔市龙江二中2019-2020学年高二12月月考化学试题湖南省湘西土家族苗族自治州花垣县边城高级中学2020-2021学年高二上学期9月月考化学试题西藏自治区拉萨市第二高级中学2019-2020学年高二上学期期末考试化学试题河北省衡水市武邑武罗学校2020-2021学年高二上学期期中考试化学试题黑龙江省绥化市望奎县第一中学2021-2022学年高二上学期第一次月考化学试题黑龙江省大兴安岭实验中学(西校区)2021-2022学年高二上学期第一次月考化学试题甘肃省兰州市西固区三校2021-2022学年高二上学期期中联考化学(理科)试题陕西省汉滨区五里高级中学2022-2023学年高二上学期期中考试化学试题河南省许昌市鄢陵县职业教育中心2021-2022学年高二上学期第一次月考化学试题
名校
10 . 肌肉中的肌红蛋白(Mb)可与O2结合生成MbO2:Mb(aq)+O2(g)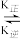 MbO2(aq)其中k正和k逆分别表示正反应和逆反应的速率常数,即v正=k正·c(Mb)·P(O2),v逆=k逆·c(MbO2)。37℃时测得肌红蛋白的结合度(α)与P(O2)的关系如下表[结合度(α)指已与O2结合的肌红蛋白占总肌红蛋白的百分比]回答下列问题:
MbO2(aq)其中k正和k逆分别表示正反应和逆反应的速率常数,即v正=k正·c(Mb)·P(O2),v逆=k逆·c(MbO2)。37℃时测得肌红蛋白的结合度(α)与P(O2)的关系如下表[结合度(α)指已与O2结合的肌红蛋白占总肌红蛋白的百分比]回答下列问题:
(1)计算37℃、P(O2)为2.00kPa时,上述反应的平衡常数K=_______ kPa﹣1。(气体和溶液中的溶质分别用分压和物质的量浓度表达)
(2)导出平衡时肌红蛋白与O2的结合度(α)与O2的压强[P(O2)]之间的关系式α=_______ (用含有k正、k逆的式子表示)。
(3)37℃时,若空气中氧气分压为20.0kPa,人正常呼吸时α的最大值为_______ %(计算结果保留小数点后两位)
(4)一般情况下,高烧患者体内MbO2的浓度会比其健康时_______ (填“高”或“低”,下同);在温度不变的条件下,游客在高山山顶时体内MbO2的浓度比其在山下时_______ 。
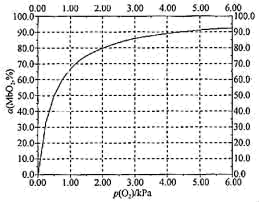
(5)37℃时,下图中坐标为(1.00,50.0)的点对应的反应状态为向_______ 进行(填“左”或“右”),此时v正:v逆=_______ (填数值)。
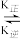 MbO2(aq)其中k正和k逆分别表示正反应和逆反应的速率常数,即v正=k正·c(Mb)·P(O2),v逆=k逆·c(MbO2)。37℃时测得肌红蛋白的结合度(α)与P(O2)的关系如下表[结合度(α)指已与O2结合的肌红蛋白占总肌红蛋白的百分比]回答下列问题:
MbO2(aq)其中k正和k逆分别表示正反应和逆反应的速率常数,即v正=k正·c(Mb)·P(O2),v逆=k逆·c(MbO2)。37℃时测得肌红蛋白的结合度(α)与P(O2)的关系如下表[结合度(α)指已与O2结合的肌红蛋白占总肌红蛋白的百分比]回答下列问题:| P(O2) | 0.50 | 1.00 | 2.00 | 3.00 | 4.00 | 5.00 | 6.00 |
| α(MbO2%) | 50.0 | 67.0 | 80.0 | 85.0 | 88.0 | 90.3 | 91.0 |
(1)计算37℃、P(O2)为2.00kPa时,上述反应的平衡常数K=
(2)导出平衡时肌红蛋白与O2的结合度(α)与O2的压强[P(O2)]之间的关系式α=
(3)37℃时,若空气中氧气分压为20.0kPa,人正常呼吸时α的最大值为
(4)一般情况下,高烧患者体内MbO2的浓度会比其健康时
(5)37℃时,下图中坐标为(1.00,50.0)的点对应的反应状态为向

您最近半年使用:0次
2021-01-09更新
|
668次组卷
|
4卷引用:辽宁省五校2021届高三上学期期末联考化学试题
辽宁省五校2021届高三上学期期末联考化学试题辽宁省实验中学2021届高三上学期期末考试化学试题(已下线)解密09 化学反应速率与平衡(分层训练)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练(已下线)解密09 化学反应速率与平衡(分层训练)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练(浙江专版)



