已知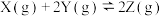
 。为了探究反应条件对该反应的影响,分别向四个密闭容器中充入一定量的反应物,反应条件及达到平衡时的有关数据如表所示,请回答下列问题:
。为了探究反应条件对该反应的影响,分别向四个密闭容器中充入一定量的反应物,反应条件及达到平衡时的有关数据如表所示,请回答下列问题:
(1)设计实验1、3的目的是探究_____ 对反应的影响,实验_____ 是为了探究压强对反应的影响。
(2)
_____ (填“>”、“<”或“=”)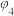 。
。
(3) 、
、 、
、 由大到小的顺序为
由大到小的顺序为_____ 。
(4) 、
、 、
、 、
、 的大小关系为
的大小关系为_____ 。
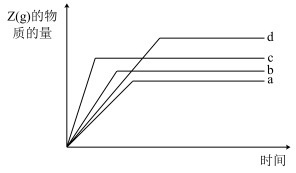
(5)若实验1、2、3、4中Z(g)的物质的量随时间的变化关系如图中曲线所示,实验1对应曲线b,则实验2、3分别对应曲线_____ 、_____ 。(填字母)
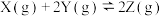
 。为了探究反应条件对该反应的影响,分别向四个密闭容器中充入一定量的反应物,反应条件及达到平衡时的有关数据如表所示,请回答下列问题:
。为了探究反应条件对该反应的影响,分别向四个密闭容器中充入一定量的反应物,反应条件及达到平衡时的有关数据如表所示,请回答下列问题:| 实验编号 | 1 | 2 | 3 | 4 |
| 反应物投入量 | 1molX(g)、2molY(g) | 1molX(g)、3molY(g) | 1molX(g)、2molY(g) | 1molX(g)、2molY(g) |
| 反应温度/℃ | 500 | 500 | 400 | 500 |
| 压强 | 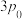 | 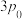 | 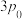 |  |
| 平衡时Z(g)的体积分数 |  | 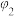 |  | 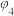 |
| Y(g)的平衡转化率 |  |  |  | 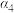 |
| 化学平衡常数 |  |  |  |  |
(2)

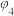 。
。(3)
 、
、 、
、 由大到小的顺序为
由大到小的顺序为(4)
 、
、 、
、 、
、 的大小关系为
的大小关系为(5)若实验1、2、3、4中Z(g)的物质的量随时间的变化关系如图中曲线所示,实验1对应曲线b,则实验2、3分别对应曲线

更新时间:2023-07-23 21:16:48
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】现有反应aA(g)+bB(g) pC(g),达到平衡后,当升高温度时,B的转化率变大;当减小压强时,混合体系中C的质量分数也减小,则
pC(g),达到平衡后,当升高温度时,B的转化率变大;当减小压强时,混合体系中C的质量分数也减小,则
(1)该反应的逆反应是____ 反应(填“吸热或放热),且a+b___ p(填“>”“<”或“=”)。
(2)减压时,A的质量分数______ (填“增大”“减小”或“不变”,下同)。
(3)若加入B(体积不变),则A的转化率________ ,B的转化率________ 。
(4)若升高温度,则平衡时,B、C的浓度之比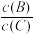 将
将________ 。
(5)若B是有色物质,A、C均为无色物质,则加入C(体积不变)时混合物的颜色________ (填“变浅”“变深”或“不变”,下同),而维持容器内气体的压强不变,充入氖气时,混合物的颜色________ 。
 pC(g),达到平衡后,当升高温度时,B的转化率变大;当减小压强时,混合体系中C的质量分数也减小,则
pC(g),达到平衡后,当升高温度时,B的转化率变大;当减小压强时,混合体系中C的质量分数也减小,则(1)该反应的逆反应是
(2)减压时,A的质量分数
(3)若加入B(体积不变),则A的转化率
(4)若升高温度,则平衡时,B、C的浓度之比
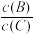 将
将(5)若B是有色物质,A、C均为无色物质,则加入C(体积不变)时混合物的颜色
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】下图中,P为可自由滑动的活塞,关闭K,V(A)=aL,V(B)=0.8aL(连通管的体积忽略不计)。在相同温度和有催化剂存在的条件下,分别向容器A、B中各充入1molN2和3molH2,发生反应N2(g)+3H2(g) 2NH3(g);ΔH=-92.4kJ/mol。达到平衡后,V(B)=0.6aL。
2NH3(g);ΔH=-92.4kJ/mol。达到平衡后,V(B)=0.6aL。
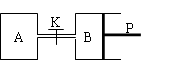
⑴B中N2的转化率是_______ 。A中N2的转化率______ (填“大于”、“等于”或“小于”)B中N2的转化率。理由是_______________________ 。
⑵打开K,一段时间后反应再次达到平衡,则B的体积为_______ 。请说明理由?
⑶A反应达到平衡时,放出akJ的热量,若向A中充入2molNH3,在相同条件下达到平衡时吸收热量为bkJ,则a和b的关系是______________ 。
⑷B中反应达到平衡后,只改变下列条件,c(NH3)不改变的是_____ (填序号)。
A. 升高温度 B. 向容器充入1molAr(g)
C. 向容器中充入2molNH3 D. 选用效果更好的催化剂
 2NH3(g);ΔH=-92.4kJ/mol。达到平衡后,V(B)=0.6aL。
2NH3(g);ΔH=-92.4kJ/mol。达到平衡后,V(B)=0.6aL。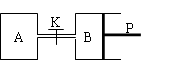
⑴B中N2的转化率是
⑵打开K,一段时间后反应再次达到平衡,则B的体积为
⑶A反应达到平衡时,放出akJ的热量,若向A中充入2molNH3,在相同条件下达到平衡时吸收热量为bkJ,则a和b的关系是
⑷B中反应达到平衡后,只改变下列条件,c(NH3)不改变的是
A. 升高温度 B. 向容器充入1molAr(g)
C. 向容器中充入2molNH3 D. 选用效果更好的催化剂
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】(1)在一体积为10L的容器中,通入一定量的CO和H2O,在850℃时发生如下反应:CO(g)十H2O(g) CO2(g)十H2(g) △H<0。CO和H2O浓度变化如下图,则0~4min的平均反应速率υ(CO)=
CO2(g)十H2(g) △H<0。CO和H2O浓度变化如下图,则0~4min的平均反应速率υ(CO)=_______ mol/(L·min),此时该反应的平衡常数为_______ 。

(2)T ℃(高于850℃)时,在相同容器中发生上述反应,容器内各物质的浓度变化如上表。
①表中3min~4min之间反应处于_____ 状态;c1_____ 0.08 (填 “>”、“<”或“=”)。
②反应在4min~5min间,平衡向逆方向移动,可能的原因是_______ (填序号,下同),表中5min~6min之间数值发生变化,可能的原因是_______ 。
a.增加了水蒸气的量 b.降低温度
c.使用催化剂 d.增加氢气的浓度
 CO2(g)十H2(g) △H<0。CO和H2O浓度变化如下图,则0~4min的平均反应速率υ(CO)=
CO2(g)十H2(g) △H<0。CO和H2O浓度变化如下图,则0~4min的平均反应速率υ(CO)=
(2)T ℃(高于850℃)时,在相同容器中发生上述反应,容器内各物质的浓度变化如上表。
①表中3min~4min之间反应处于
②反应在4min~5min间,平衡向逆方向移动,可能的原因是
a.增加了水蒸气的量 b.降低温度
c.使用催化剂 d.增加氢气的浓度
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】如图所示(a中活塞的质量与筒壁的摩擦力不计;与K相连的细管的体积也忽略不计)。在标准状况下:
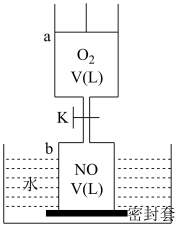
(1)b中气体与水不接触,打开K足够长时间后,a中气体体积减少(ΔV)的范围是:_______ 。
(2)在上述(1)之后,快速推a中活塞至a中气体全部进入b中,观察到的现象是_______ ,原因是_______ 。
(3)若固定a中活塞如图所示,打开K,移走b的密封套,足够长时间后,观察到液面上升,其中涉及的化学反应方程式为_______ 。

(1)b中气体与水不接触,打开K足够长时间后,a中气体体积减少(ΔV)的范围是:
(2)在上述(1)之后,快速推a中活塞至a中气体全部进入b中,观察到的现象是
(3)若固定a中活塞如图所示,打开K,移走b的密封套,足够长时间后,观察到液面上升,其中涉及的化学反应方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】工业上用CO和H2反应制备二甲醚(CH3OCH3)的条件是压强2.0~10.0 MPa,温度300 ℃。设备中进行如下反应。
①CO(g)+2H2(g) CH3OH(g) ΔH=-90.7 kJ/mol
CH3OH(g) ΔH=-90.7 kJ/mol
②2CH3OH(g) CH3OCH3(g)+H2O(g) ΔH=-23.5 kJ/mol
CH3OCH3(g)+H2O(g) ΔH=-23.5 kJ/mol
③CO(g)+H2O(g) CO2(g)+H2(g) ΔH=-41.2 kJ/mol
CO2(g)+H2(g) ΔH=-41.2 kJ/mol
请回答下列问题:
(1)在温度和容器容积不变的条件下发生反应①,能说明该反应达到平衡状态的依据是_______ 。
a.容器中压强保持不变
b. 混合气体中c(CO)不变
c.混合气体的平均相对分子质量不变
d.v正(CO)=v逆(H2)
(2)在容积为2 L的恒温密闭容器中加入a mol CH3OH(g)发生反应②,达到平衡后若再加入a mol CH3OH(g)重新达到平衡时,CH3OH的转化率_______ (填“增大”“减小”或“不变”)。
(3)850 ℃时在一容积为10 L的密闭容器中通入一定量的CO和H2O(g)发生反应③,CO和H2O(g)浓度变化如图所示。
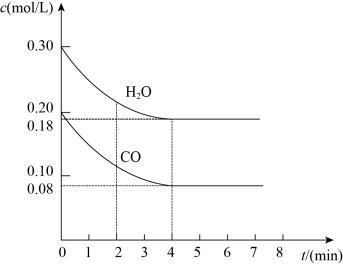
①0~4 min的平均反应速率v(CO)=_______ 。
②若温度不变,向该容器中加入4 mol CO(g)、2 mol H2O(g)、3 mol CO2(g)和3 mol H2(g),起始时v正(CO)_______ v逆(H2)(填“<”“>”或“=”),请结合必要的计算过程说明理由: _______ 。
①CO(g)+2H2(g)
 CH3OH(g) ΔH=-90.7 kJ/mol
CH3OH(g) ΔH=-90.7 kJ/mol②2CH3OH(g)
 CH3OCH3(g)+H2O(g) ΔH=-23.5 kJ/mol
CH3OCH3(g)+H2O(g) ΔH=-23.5 kJ/mol③CO(g)+H2O(g)
 CO2(g)+H2(g) ΔH=-41.2 kJ/mol
CO2(g)+H2(g) ΔH=-41.2 kJ/mol请回答下列问题:
(1)在温度和容器容积不变的条件下发生反应①,能说明该反应达到平衡状态的依据是
a.容器中压强保持不变
b. 混合气体中c(CO)不变
c.混合气体的平均相对分子质量不变
d.v正(CO)=v逆(H2)
(2)在容积为2 L的恒温密闭容器中加入a mol CH3OH(g)发生反应②,达到平衡后若再加入a mol CH3OH(g)重新达到平衡时,CH3OH的转化率
(3)850 ℃时在一容积为10 L的密闭容器中通入一定量的CO和H2O(g)发生反应③,CO和H2O(g)浓度变化如图所示。

①0~4 min的平均反应速率v(CO)=
②若温度不变,向该容器中加入4 mol CO(g)、2 mol H2O(g)、3 mol CO2(g)和3 mol H2(g),起始时v正(CO)
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】在密闭容器中,使2molN2和6molH2混合发生下列反应:N2(g)+3H2(g) NH3(g) △H<0。
NH3(g) △H<0。
(1)当反应达到平衡时,N2和H2的浓度比是___ ;N2和H2的转化率比是___ 。反应的化学平衡常数K表达式为___ 。
(2)升高平衡体系的温度(保持体积不变),混合气体的平均相对分子质量___ ,密度___ 。(填“变大”“变小”或“不变”)
(3)当达到平衡时,充入氩气,并保持压强不变,平衡将___ (填“正向”“逆向”或“不”)移动。
(4)若容器恒容、绝热,加热使容器内温度迅速升至原来的2倍,平衡将___ (填“向左移动”“向右移动”或“不移动”)。达到新平衡后,容器内温度____ (填“大于”“小于”或“等于”)原来的2倍。
(5)10s后的某一时刻(t1)改变了外界条件,其速率随时间的变化图象如图所示:则下列说法符合该图象的是____ 。

A.t1时刻,增大了N2的浓度 B.t1时刻,升高了体系温度
C.t1时刻,缩小了容器体积 D.t1时刻,使用了催化剂
 NH3(g) △H<0。
NH3(g) △H<0。(1)当反应达到平衡时,N2和H2的浓度比是
(2)升高平衡体系的温度(保持体积不变),混合气体的平均相对分子质量
(3)当达到平衡时,充入氩气,并保持压强不变,平衡将
(4)若容器恒容、绝热,加热使容器内温度迅速升至原来的2倍,平衡将
(5)10s后的某一时刻(t1)改变了外界条件,其速率随时间的变化图象如图所示:则下列说法符合该图象的是

A.t1时刻,增大了N2的浓度 B.t1时刻,升高了体系温度
C.t1时刻,缩小了容器体积 D.t1时刻,使用了催化剂
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】氢气是一种理想的绿色能源。利用生物质发酵得到的乙醇制取氢气,具有良好的应用前景。乙醇水蒸气重整制氢的部分反应过程如下图所示:
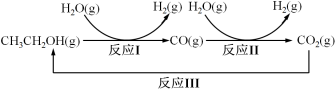
已知:反应I和反应II的平衡常数随温度变化曲线如图所示。
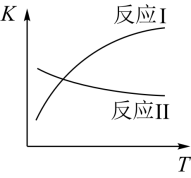
(1)反应I中,1 mol CH3CH2OH(g)参与反应后的热量变化是256 kJ。
①H2O的电子式是_______ 。
②反应I的热化学方程式是_______ 。
(2)反应II,在进气比[n(CO): n(H2O)]不同时,测得相应的CO的平衡转化率见下图(各点对应的反应温度可能相同,也可能不同)。
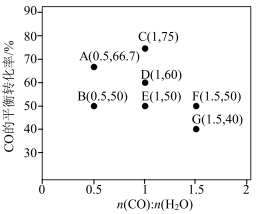
①图中D、E两点对应的反应温度分别为TD和TE.判断:TD_______ TE(填“<” “=”或“>”)。
②经分析,A、E和G三点对应的反应温度相同,其原因是A、E和G三点对应的_______ 相同。
③当不同的进气比达到相同的CO平衡转化率时,对应的反应温度和进气比的关系是_______ 。

已知:反应I和反应II的平衡常数随温度变化曲线如图所示。

(1)反应I中,1 mol CH3CH2OH(g)参与反应后的热量变化是256 kJ。
①H2O的电子式是
②反应I的热化学方程式是
(2)反应II,在进气比[n(CO): n(H2O)]不同时,测得相应的CO的平衡转化率见下图(各点对应的反应温度可能相同,也可能不同)。

①图中D、E两点对应的反应温度分别为TD和TE.判断:TD
②经分析,A、E和G三点对应的反应温度相同,其原因是A、E和G三点对应的
③当不同的进气比达到相同的CO平衡转化率时,对应的反应温度和进气比的关系是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】已知化学反应,回答下列问题:
① ,其化学平衡常数为
,其化学平衡常数为 ;
;
② ,其化学平衡常数为
,其化学平衡常数为
在温度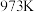 和
和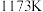 的情况下,
的情况下,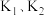 的值分别如图:
的值分别如图:
(1)书写反应①的化学平衡常数表达式_______ 。
(2)通过表格中的数值推断:反应②是_______ (填“吸热”或“放热”)反应。
(3)现有反应③: ,反应③是
,反应③是_______ (填“吸热”或“放热”)反应,说明理由:_______ 。
①
 ,其化学平衡常数为
,其化学平衡常数为 ;
;②
 ,其化学平衡常数为
,其化学平衡常数为
在温度
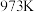 和
和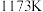 的情况下,
的情况下,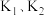 的值分别如图:
的值分别如图:| 温度 |  |  |
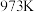 | 1.47 | 2.38 |
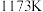 | 2.15 | 1.67 |
(2)通过表格中的数值推断:反应②是
(3)现有反应③:
 ,反应③是
,反应③是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】石油气“芳构化”是由石油气生产高辛烷值汽油的一种有效生产工艺。测得反应2C4H10 C8H10(g)+5H2在不同温度下的平衡常数变化如下:
C8H10(g)+5H2在不同温度下的平衡常数变化如下:
(1)该反应的正反应是________ (填“吸热”或“放热”)反应。
(2)向2 L密闭定容容器中充入2 mol C4H10,反应10 s后测得H2浓度为1 mol·L-1,此10 s内,以C8H10表示的平均速率为____________________ 。
(3)能表示该反应在恒温恒容密闭容器中t1时刻后已经达平衡状态的图示是__________ 。


(4)下图表示某温度时将一定量的C4H10(含少量H2)充入容器中反应期间物质浓度随时间的变化(容器容积可变),实线代表C8H10,虚线代表C4H10。请用实线补充画出t1~t4间C8H10的浓度变化曲线。_____________

 C8H10(g)+5H2在不同温度下的平衡常数变化如下:
C8H10(g)+5H2在不同温度下的平衡常数变化如下:温度(℃) | 400 | 450 | 500 |
平衡常数K | a | 6a | 40a |
(1)该反应的正反应是
(2)向2 L密闭定容容器中充入2 mol C4H10,反应10 s后测得H2浓度为1 mol·L-1,此10 s内,以C8H10表示的平均速率为
(3)能表示该反应在恒温恒容密闭容器中t1时刻后已经达平衡状态的图示是


(4)下图表示某温度时将一定量的C4H10(含少量H2)充入容器中反应期间物质浓度随时间的变化(容器容积可变),实线代表C8H10,虚线代表C4H10。请用实线补充画出t1~t4间C8H10的浓度变化曲线。

您最近一年使用:0次



