名校
1 . 氢能作为一种清洁、高效、安全、可持续的新能源,被视为21世纪最具发展潜力的清洁能源,是人类的战略能源发展方向。目前,制备氢气有多种途径:途径一:甲醇产生氢气的反应为:
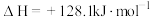
(1)已知相关物质的标准熵数值如下表:
该反应能自发进行的最低温度为___________ K。(保留小数点后1位)
途径二:乙酸制氢的反应为:
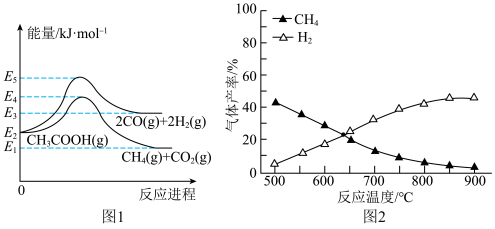
反应I: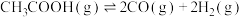
反应Ⅱ: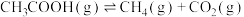
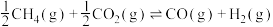

①由图1可得,
___________ kJ·mol-1;
②恒温恒容下发生上述反应,下列说法正确的是___________ 。
A.混合气体密度不变时,反应达到平衡
B.充入CO2,可提高CH4的转化率
C.加入催化剂,可提高H2的平衡产率
D.充入Ar,对H2的产率不产生影响
(3)一定条件下,在密闭容器中加入一定量的乙酸,只发生反应I和反应Ⅱ。
①在相同时间,测得温度与气体产率的关系如上图2所示。约650℃之前,氢气产率低于甲烷的可能原因是___________ 。
②设达到平衡时,体系总压强为p,乙酸体积分数为20%,反应I消耗的乙酸占投入量的20%,则反应Ⅱ的平衡常数 为
为___________ 。(用平衡分压代替平衡浓度计算)
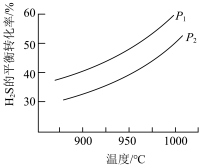
途径三:热分解H2S制氢的反应为: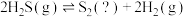
(4)不同温度和压强下,H2S的平衡转化率变化如图。生成物S2的状态为___________ (填“气态”或“非气态”),P1___________ P2(填“>”或“<”)。

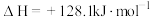
(1)已知相关物质的标准熵数值如下表:
| 化学式 |  |  |  |
标准熵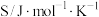 | 126.8 | 130.7 | 197.7 |
途径二:乙酸制氢的反应为:
反应I:
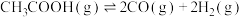
反应Ⅱ:
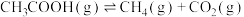
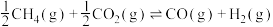

①由图1可得,

②恒温恒容下发生上述反应,下列说法正确的是
A.混合气体密度不变时,反应达到平衡
B.充入CO2,可提高CH4的转化率
C.加入催化剂,可提高H2的平衡产率
D.充入Ar,对H2的产率不产生影响
(3)一定条件下,在密闭容器中加入一定量的乙酸,只发生反应I和反应Ⅱ。
①在相同时间,测得温度与气体产率的关系如上图2所示。约650℃之前,氢气产率低于甲烷的可能原因是
②设达到平衡时,体系总压强为p,乙酸体积分数为20%,反应I消耗的乙酸占投入量的20%,则反应Ⅱ的平衡常数
 为
为途径三:热分解H2S制氢的反应为:
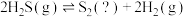
(4)不同温度和压强下,H2S的平衡转化率变化如图。生成物S2的状态为
您最近半年使用:0次
2024-04-21更新
|
116次组卷
|
2卷引用:东北三省四城市联考暨沈阳市高三下学期质量监测(二)化学试题
2 . 用来表示可逆反应: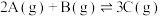
 的正确图像是
的正确图像是
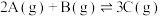
 的正确图像是
的正确图像是A.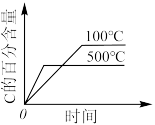 | B.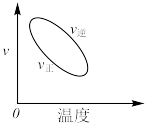 |
C.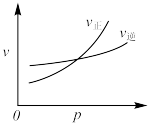 | D. |
您最近半年使用:0次
3 . 某密闭容器中。发生反应COCl2(g) CO(g)+Cl2(g) ∆H>0。当该反应达到平衡时,保持温度和容积不变,向该容器中充入少量的稀有气体,下列图像正确的是
CO(g)+Cl2(g) ∆H>0。当该反应达到平衡时,保持温度和容积不变,向该容器中充入少量的稀有气体,下列图像正确的是
 CO(g)+Cl2(g) ∆H>0。当该反应达到平衡时,保持温度和容积不变,向该容器中充入少量的稀有气体,下列图像正确的是
CO(g)+Cl2(g) ∆H>0。当该反应达到平衡时,保持温度和容积不变,向该容器中充入少量的稀有气体,下列图像正确的是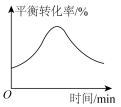 | 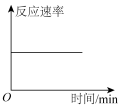 | 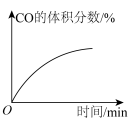 | 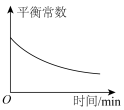 |
| A | B | C | D |
| A.A | B.B | C.C | D.d |
您最近半年使用:0次
2024-02-01更新
|
149次组卷
|
2卷引用:辽宁省抚顺市六校协作体2023-2024学年高二上学期期末考试化学试题
名校
解题方法
4 . 一定条件下发生反应: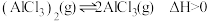 ,平衡时该体系的气体平均摩尔质量(M)在不同温度(T)下随压强(p)的变化曲线如图所示。下列说法正确的是
,平衡时该体系的气体平均摩尔质量(M)在不同温度(T)下随压强(p)的变化曲线如图所示。下列说法正确的是
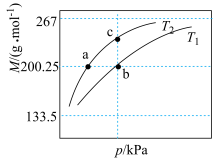
 ,平衡时该体系的气体平均摩尔质量(M)在不同温度(T)下随压强(p)的变化曲线如图所示。下列说法正确的是
,平衡时该体系的气体平均摩尔质量(M)在不同温度(T)下随压强(p)的变化曲线如图所示。下列说法正确的是
A.温度: | B.a、b两点M相同,平衡常数也相同 |
C.反应速率: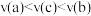 | D. 的物质的量浓度: 的物质的量浓度: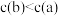 |
您最近半年使用:0次
2024-01-22更新
|
207次组卷
|
2卷引用:辽宁省朝阳市建平县2023-2024学年高三上学期1月期末化学试题
解题方法
5 . 在一定温度和催化剂的条件下,将(0.1mol NH3通入3L的恒容密闭容器中进行反应2NH3(g)=N2(g)+3H2(g)(初始容器内总压为200kPa),各物质的分压随时间的变化曲线如下图所示。下列说法错误的是


A.用H2的浓度变化表示0~t1时间内的反应速率v(H2)=0.02/t1mol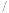 (L·min) (L·min) |
| B.混合气体的平均相对分子质量不再改变时,反应达平衡 |
| C.在该温度下的压强平衡常数为4800(kPa)2 |
| D.若t2时将容器体积迅速缩小至原来的一半,N2分压变化趋势的曲线是a |
您最近半年使用:0次
6 . 下列说法正确的是
A.将装有 气体的注射器压缩至原体积的一半,压缩后的气体颜色比压缩前深,则说明增大压强, 气体的注射器压缩至原体积的一半,压缩后的气体颜色比压缩前深,则说明增大压强, 平衡向逆反应方向移动 平衡向逆反应方向移动 |
B.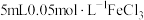 溶液中滴入几滴KSCN溶液,溶液呈红色,再加入少量KCl固体,溶液红色变浅,则说明增大生成物浓度,平衡向逆反应方向移动 溶液中滴入几滴KSCN溶液,溶液呈红色,再加入少量KCl固体,溶液红色变浅,则说明增大生成物浓度,平衡向逆反应方向移动 |
C.加热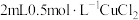 溶液,溶液变为黄绿色,则说明 溶液,溶液变为黄绿色,则说明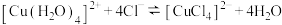 的 的 |
D.对 的平衡体系压缩体积,体系颜色变深,则说明增大压强,平衡向逆反应方向移动 的平衡体系压缩体积,体系颜色变深,则说明增大压强,平衡向逆反应方向移动 |
您最近半年使用:0次
名校
解题方法
7 . 在一容积可变的密闭容器中加入一定量的X、Y,发生反应mX(g)⇌nY(g) ∆H=QkJ/mol。反应达到平衡时,Y的物质的量浓度与温度、气体体积的关系如表所示:
下列说法正确 的是
| 温度(℃) | c(Y)/(mol/L) | ||
| 1L | 2L | 4L | |
| 100 | 1.00 | 0.75 | 0.53 |
| 200 | 1.20 | 0.90 | 0.63 |
| 300 | 1.30 | 1.00 | 0.70 |
| A.m>n |
| B.Q<0 |
| C.体积不变,温度升高,平衡向逆反应方向移动 |
| D.温度不变,压强增大,Y的质量分数减少 |
您最近半年使用:0次
2024-01-18更新
|
24次组卷
|
22卷引用:辽宁省大连市第二十四中学2017-2018学年高二上学期期中考试化学试题
辽宁省大连市第二十四中学2017-2018学年高二上学期期中考试化学试题(已下线)2011-2012学年江西省上高二中高二上学期第三次月考化学试卷(已下线)2011-2012学年湖南省望城县第一中学高二上学期期末质量检测化学试卷(已下线)2012-2013学年河北省邢台一中高一下学期第三次月考化学试卷(已下线)2013-2014学年黑龙江省哈师大附中高二上学期期中化学试卷(已下线)2013-2014学年安徽省屯溪一中高二上学期期中考试化学试卷(已下线)2014年高二化学人教版选修四 8化学平衡移动练习卷(已下线)2015届黑龙江省双鸭山市第一中学高三9月月考化学试卷(已下线)2014-2015湖南省新化一中高二上学期期中化学试卷2014-2015学年内蒙古包头市第一中学高一下学期期末考试化学试卷2015-2016浙江宁波效实中学高二上期中考试化学试题卷2015-2016学年云南省昆明三中高二下期中化学试卷2016-2017学年四川省成都开发区实验中学高二10月月考化学卷黑龙江省孙吴县第一中学2017-2018学年高二上学期期中考试化学试题步步为赢 高二化学暑假作业:作业九 化学反应速率和化学平衡吉林省白城市第一中学2018-2019学年高一下学期期末考试化学试题福建省三明市三地三校2020-2021学年高二上学期期中联考化学试题吉林省延边朝鲜族自治州汪清县第四中学2020-2021学年高二上学期期末考试化学试题黑龙江省鹤岗市第一中学2021-2022学年高二上学期期中考试化学试题湖南师范大学附属中学2021-2022学年高一下学期期末考试化学试题湖南省常德市第一中学2023-2024学年高二上学期12月月考化学试题海南省琼海市嘉积中学2023-2024学年高二上学期期末考试化学试题A卷
名校
8 . 下列实验装置能够达到实验目的的是
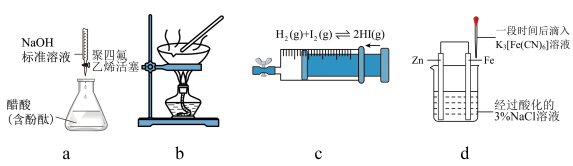

| A.图a测定醋酸的浓度 | B.图b由 溶液制取无水 溶液制取无水 |
| C.图c探究压强对平衡的影响 | D.图d验证 保护了 保护了 |
您最近半年使用:0次
2024-01-13更新
|
1295次组卷
|
7卷引用:辽宁省沈阳市部分高中2023-2024学年高三上学期教学质量监测(一)化学试题
辽宁省沈阳市部分高中2023-2024学年高三上学期教学质量监测(一)化学试题2024届辽宁省沈阳市高三教学质量检测(一模)化学试题辽宁省沈阳市2024届高三一模化学试题吉林省通化市梅河口市第五中学2023-2024学年高三上学期1月期末化学试题(已下线)热点07 常见化学实验仪器与基本操作(已下线)专题03 化学实验基础-【好题汇编】2024年高考化学一模试题分类汇编(全国通用)江西省宜春市丰城市第九中学2023-2024学年高三上学期期末考试化学试题
名校
解题方法
9 . 完成下列问题。
(1)氨基甲酸铵是合成尿素的一种中间产物。将体积比为2∶1的 和
和 混合气体充入一个容积不变的真空密闭容器中,在恒定温度下使其发生下列反应并达到平衡:
混合气体充入一个容积不变的真空密闭容器中,在恒定温度下使其发生下列反应并达到平衡: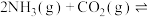
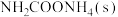
 ,反应过程中氨气质量与时间关系如图所示:
,反应过程中氨气质量与时间关系如图所示:
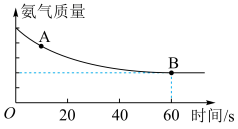
A点正反应速率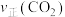
___________ B点逆反应速率 (填“>”、“<”或“=”),上述反应达平衡状态后降低体系温度,新平衡体系中
(填“>”、“<”或“=”),上述反应达平衡状态后降低体系温度,新平衡体系中 的体积分数与原平衡相比
的体积分数与原平衡相比___________ (填“下降”、“不变”或“升高”)
(2)温度为T℃,向体积不等的恒容密闭容器中分别加入足量活性炭和1mol ,发生反应:
,发生反应: ,反应相同时间,测得各容器中
,反应相同时间,测得各容器中 的转化率与容器体积的关系如下图所示。
的转化率与容器体积的关系如下图所示。
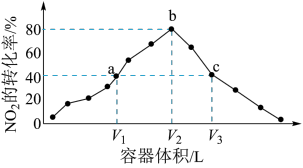
下列说法正确的是___________ 。
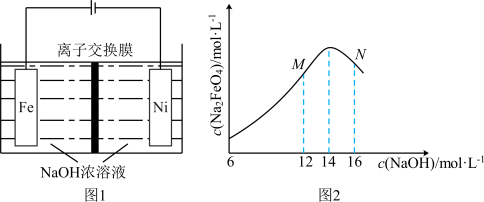
A.容器内的压强: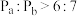
B.图中c点所示条件下,
C.向a点平衡体系中充入一定量的 ,达到平衡时,
,达到平衡时, 的转化率比原平衡大
的转化率比原平衡大
(3)电解法制取 ,同时可获得氢气:
,同时可获得氢气: ,工作原理如图1所示。已知:若NaOH溶液浓度过高,铁电极区会产生红褐色物质:
,工作原理如图1所示。已知:若NaOH溶液浓度过高,铁电极区会产生红褐色物质: 只在强碱性条件下稳定。
只在强碱性条件下稳定。
①电解时,Fe电极发生的电极反应式为___________ 。
②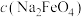 随初始
随初始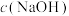 的变化如图2,则分别分析M、N点
的变化如图2,则分别分析M、N点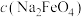 均低于最高值的可能的原因:M点
均低于最高值的可能的原因:M点___________ ;N点___________ 。
(4)甲醚( )是重要的化工原料,制取原理如下:
)是重要的化工原料,制取原理如下:
主反应①: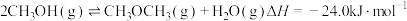 。
。
副反应②: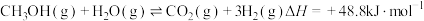 。
。
选择合适的催化剂。在不同温度和5MPa压强下,测得甲醚的选择性如下图所示。 的选择性=(2×
的选择性=(2× 的物质的量/反应的
的物质的量/反应的 的物质的量)×100%
的物质的量)×100%
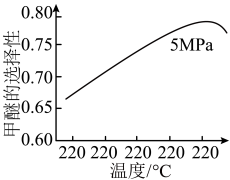
图中,温度高于265℃后甲醚选择性降低,从平衡的角度分析,其可能的原因是___________ 。
(1)氨基甲酸铵是合成尿素的一种中间产物。将体积比为2∶1的
 和
和 混合气体充入一个容积不变的真空密闭容器中,在恒定温度下使其发生下列反应并达到平衡:
混合气体充入一个容积不变的真空密闭容器中,在恒定温度下使其发生下列反应并达到平衡: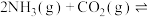
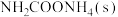
 ,反应过程中氨气质量与时间关系如图所示:
,反应过程中氨气质量与时间关系如图所示:
A点正反应速率
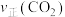
 (填“>”、“<”或“=”),上述反应达平衡状态后降低体系温度,新平衡体系中
(填“>”、“<”或“=”),上述反应达平衡状态后降低体系温度,新平衡体系中 的体积分数与原平衡相比
的体积分数与原平衡相比(2)温度为T℃,向体积不等的恒容密闭容器中分别加入足量活性炭和1mol
 ,发生反应:
,发生反应: ,反应相同时间,测得各容器中
,反应相同时间,测得各容器中 的转化率与容器体积的关系如下图所示。
的转化率与容器体积的关系如下图所示。
下列说法正确的是
A.容器内的压强:
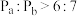
B.图中c点所示条件下,

C.向a点平衡体系中充入一定量的
 ,达到平衡时,
,达到平衡时, 的转化率比原平衡大
的转化率比原平衡大(3)电解法制取
 ,同时可获得氢气:
,同时可获得氢气: ,工作原理如图1所示。已知:若NaOH溶液浓度过高,铁电极区会产生红褐色物质:
,工作原理如图1所示。已知:若NaOH溶液浓度过高,铁电极区会产生红褐色物质: 只在强碱性条件下稳定。
只在强碱性条件下稳定。
①电解时,Fe电极发生的电极反应式为
②
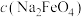 随初始
随初始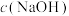 的变化如图2,则分别分析M、N点
的变化如图2,则分别分析M、N点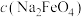 均低于最高值的可能的原因:M点
均低于最高值的可能的原因:M点(4)甲醚(
 )是重要的化工原料,制取原理如下:
)是重要的化工原料,制取原理如下:主反应①:
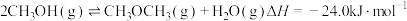 。
。副反应②:
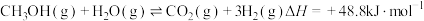 。
。选择合适的催化剂。在不同温度和5MPa压强下,测得甲醚的选择性如下图所示。
 的选择性=(2×
的选择性=(2× 的物质的量/反应的
的物质的量/反应的 的物质的量)×100%
的物质的量)×100%
图中,温度高于265℃后甲醚选择性降低,从平衡的角度分析,其可能的原因是
您最近半年使用:0次
名校
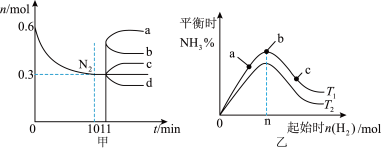
10 . 一定条件下,关于工业合成氨的反应, ,图甲表示1L密闭容器中
,图甲表示1L密闭容器中 随时间的变化曲线,图乙表示在恒温恒容下,初始投料0.6mol
随时间的变化曲线,图乙表示在恒温恒容下,初始投料0.6mol ,改变起始时
,改变起始时 对该平衡的影响。下列说法正确的是
对该平衡的影响。下列说法正确的是
 ,图甲表示1L密闭容器中
,图甲表示1L密闭容器中 随时间的变化曲线,图乙表示在恒温恒容下,初始投料0.6mol
随时间的变化曲线,图乙表示在恒温恒容下,初始投料0.6mol ,改变起始时
,改变起始时 对该平衡的影响。下列说法正确的是
对该平衡的影响。下列说法正确的是
A.甲:10min内该反应的平均速率 |
B.甲:从11min起其他条件不变,压缩容器体积,则 的变化曲线为b 的变化曲线为b |
C.乙:a、b、c三点所处的平衡状态中,b点 的转化率最高 的转化率最高 |
D.乙: |
您最近半年使用:0次



