名校
解题方法
1 . 完成下列问题。
(1)氨基甲酸铵是合成尿素的一种中间产物。将体积比为2∶1的 和
和 混合气体充入一个容积不变的真空密闭容器中,在恒定温度下使其发生下列反应并达到平衡:
混合气体充入一个容积不变的真空密闭容器中,在恒定温度下使其发生下列反应并达到平衡: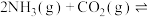
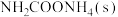
 ,反应过程中氨气质量与时间关系如图所示:
,反应过程中氨气质量与时间关系如图所示:
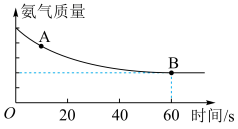
A点正反应速率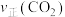
___________ B点逆反应速率 (填“>”、“<”或“=”),上述反应达平衡状态后降低体系温度,新平衡体系中
(填“>”、“<”或“=”),上述反应达平衡状态后降低体系温度,新平衡体系中 的体积分数与原平衡相比
的体积分数与原平衡相比___________ (填“下降”、“不变”或“升高”)
(2)温度为T℃,向体积不等的恒容密闭容器中分别加入足量活性炭和1mol ,发生反应:
,发生反应: ,反应相同时间,测得各容器中
,反应相同时间,测得各容器中 的转化率与容器体积的关系如下图所示。
的转化率与容器体积的关系如下图所示。
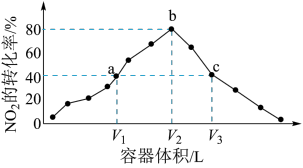
下列说法正确的是___________ 。
A.容器内的压强: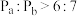
B.图中c点所示条件下,
C.向a点平衡体系中充入一定量的 ,达到平衡时,
,达到平衡时, 的转化率比原平衡大
的转化率比原平衡大
(3)电解法制取 ,同时可获得氢气:
,同时可获得氢气: ,工作原理如图1所示。已知:若NaOH溶液浓度过高,铁电极区会产生红褐色物质:
,工作原理如图1所示。已知:若NaOH溶液浓度过高,铁电极区会产生红褐色物质: 只在强碱性条件下稳定。
只在强碱性条件下稳定。
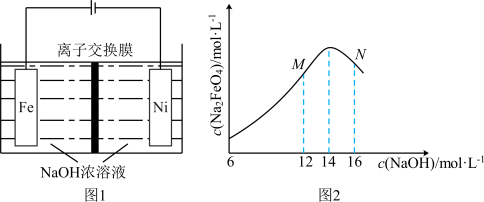
①电解时,Fe电极发生的电极反应式为___________ 。
②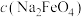 随初始
随初始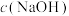 的变化如图2,则分别分析M、N点
的变化如图2,则分别分析M、N点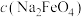 均低于最高值的可能的原因:M点
均低于最高值的可能的原因:M点___________ ;N点___________ 。
(4)甲醚( )是重要的化工原料,制取原理如下:
)是重要的化工原料,制取原理如下:
主反应①: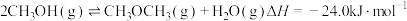 。
。
副反应②: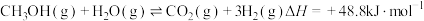 。
。
选择合适的催化剂。在不同温度和5MPa压强下,测得甲醚的选择性如下图所示。 的选择性=(2×
的选择性=(2× 的物质的量/反应的
的物质的量/反应的 的物质的量)×100%
的物质的量)×100%
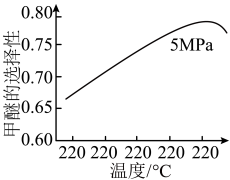
图中,温度高于265℃后甲醚选择性降低,从平衡的角度分析,其可能的原因是___________ 。
(1)氨基甲酸铵是合成尿素的一种中间产物。将体积比为2∶1的
 和
和 混合气体充入一个容积不变的真空密闭容器中,在恒定温度下使其发生下列反应并达到平衡:
混合气体充入一个容积不变的真空密闭容器中,在恒定温度下使其发生下列反应并达到平衡: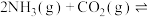
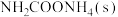
 ,反应过程中氨气质量与时间关系如图所示:
,反应过程中氨气质量与时间关系如图所示:
A点正反应速率
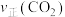
 (填“>”、“<”或“=”),上述反应达平衡状态后降低体系温度,新平衡体系中
(填“>”、“<”或“=”),上述反应达平衡状态后降低体系温度,新平衡体系中 的体积分数与原平衡相比
的体积分数与原平衡相比(2)温度为T℃,向体积不等的恒容密闭容器中分别加入足量活性炭和1mol
 ,发生反应:
,发生反应: ,反应相同时间,测得各容器中
,反应相同时间,测得各容器中 的转化率与容器体积的关系如下图所示。
的转化率与容器体积的关系如下图所示。
下列说法正确的是
A.容器内的压强:
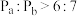
B.图中c点所示条件下,

C.向a点平衡体系中充入一定量的
 ,达到平衡时,
,达到平衡时, 的转化率比原平衡大
的转化率比原平衡大(3)电解法制取
 ,同时可获得氢气:
,同时可获得氢气: ,工作原理如图1所示。已知:若NaOH溶液浓度过高,铁电极区会产生红褐色物质:
,工作原理如图1所示。已知:若NaOH溶液浓度过高,铁电极区会产生红褐色物质: 只在强碱性条件下稳定。
只在强碱性条件下稳定。
①电解时,Fe电极发生的电极反应式为
②
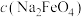 随初始
随初始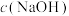 的变化如图2,则分别分析M、N点
的变化如图2,则分别分析M、N点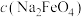 均低于最高值的可能的原因:M点
均低于最高值的可能的原因:M点(4)甲醚(
 )是重要的化工原料,制取原理如下:
)是重要的化工原料,制取原理如下:主反应①:
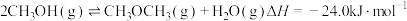 。
。副反应②:
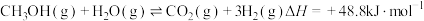 。
。选择合适的催化剂。在不同温度和5MPa压强下,测得甲醚的选择性如下图所示。
 的选择性=(2×
的选择性=(2× 的物质的量/反应的
的物质的量/反应的 的物质的量)×100%
的物质的量)×100%
图中,温度高于265℃后甲醚选择性降低,从平衡的角度分析,其可能的原因是
您最近半年使用:0次
名校
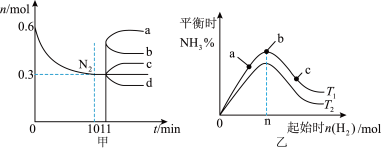
2 . 一定条件下,关于工业合成氨的反应, ,图甲表示1L密闭容器中
,图甲表示1L密闭容器中 随时间的变化曲线,图乙表示在恒温恒容下,初始投料0.6mol
随时间的变化曲线,图乙表示在恒温恒容下,初始投料0.6mol ,改变起始时
,改变起始时 对该平衡的影响。下列说法正确的是
对该平衡的影响。下列说法正确的是
 ,图甲表示1L密闭容器中
,图甲表示1L密闭容器中 随时间的变化曲线,图乙表示在恒温恒容下,初始投料0.6mol
随时间的变化曲线,图乙表示在恒温恒容下,初始投料0.6mol ,改变起始时
,改变起始时 对该平衡的影响。下列说法正确的是
对该平衡的影响。下列说法正确的是
A.甲:10min内该反应的平均速率 |
B.甲:从11min起其他条件不变,压缩容器体积,则 的变化曲线为b 的变化曲线为b |
C.乙:a、b、c三点所处的平衡状态中,b点 的转化率最高 的转化率最高 |
D.乙: |
您最近半年使用:0次
名校
解题方法
3 . Ⅰ.25℃时,制备亚硝酰氯所涉及的热化学方程式和平衡常数如下表。
(1)则该温度下,
___________  ;K3=
;K3=___________ (用 和
和 表示)。
表示)。
Ⅱ.完成下列问题
(2)25℃时,在体积为2L的恒容密闭容器中通入0.08molNO和0.04mol 发生上述反应③,若反应开始与结束时温度相同,数字压强仪显示反应过程中压强(p)随时间(t)的变化如图Ⅰ实线所示,则
发生上述反应③,若反应开始与结束时温度相同,数字压强仪显示反应过程中压强(p)随时间(t)的变化如图Ⅰ实线所示,则
___________ (填“>”“<”或“=”)0;
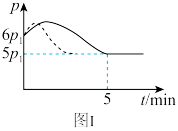
(3)若其他条件相同,仅改变某一条件,测得其压强随时间的变化如图Ⅰ虚线所示,则改变的条件是___________ ;
(4)5min时,再充入0.08molNO和0.04mol ,则达平衡后NO的体积分数将
,则达平衡后NO的体积分数将___________ (填“增大”“减小”或“不变”)。
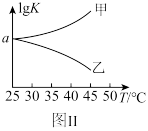
(5)图Ⅱ是甲、乙两同学描绘上述反应③的平衡常数的对数值(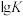 )与温度的变化关系图,其中正确的曲线是
)与温度的变化关系图,其中正确的曲线是___________ (填“甲”或“乙”)。
Ⅲ.在300℃下,将 和
和 按物质的量之比为1:3通入一恒容密闭容器中,容器压强为8MPa,发生反应
按物质的量之比为1:3通入一恒容密闭容器中,容器压强为8MPa,发生反应 ,达到平衡时,测得
,达到平衡时,测得 的平衡转化率为50%,
的平衡转化率为50%,
(6)该反应条件下的平衡常数为
___________ (用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
| 热化学方程式 | 平衡常数 | |
| ① | 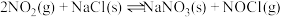 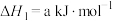 |  |
| ② | 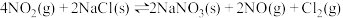 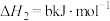 |  |
| ③ |  |  |
(1)则该温度下,

 ;K3=
;K3= 和
和 表示)。
表示)。Ⅱ.完成下列问题
(2)25℃时,在体积为2L的恒容密闭容器中通入0.08molNO和0.04mol
 发生上述反应③,若反应开始与结束时温度相同,数字压强仪显示反应过程中压强(p)随时间(t)的变化如图Ⅰ实线所示,则
发生上述反应③,若反应开始与结束时温度相同,数字压强仪显示反应过程中压强(p)随时间(t)的变化如图Ⅰ实线所示,则

(3)若其他条件相同,仅改变某一条件,测得其压强随时间的变化如图Ⅰ虚线所示,则改变的条件是
(4)5min时,再充入0.08molNO和0.04mol
 ,则达平衡后NO的体积分数将
,则达平衡后NO的体积分数将(5)图Ⅱ是甲、乙两同学描绘上述反应③的平衡常数的对数值(
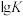 )与温度的变化关系图,其中正确的曲线是
)与温度的变化关系图,其中正确的曲线是
Ⅲ.在300℃下,将
 和
和 按物质的量之比为1:3通入一恒容密闭容器中,容器压强为8MPa,发生反应
按物质的量之比为1:3通入一恒容密闭容器中,容器压强为8MPa,发生反应 ,达到平衡时,测得
,达到平衡时,测得 的平衡转化率为50%,
的平衡转化率为50%,(6)该反应条件下的平衡常数为

您最近半年使用:0次
4 . 填空。
(1)下列事实不能用勒夏特列原理来解释的是___________ 。
A.高压有利于氢气与氮气合成氨
B.实验室中常用排饱和食盐水的方法收集Cl2
C.工业上生产硫酸时,充入过量的空气以提高SO2的转化率
D.H2、I2、HI平衡混合气体加压后颜色加深
E.压缩NO2与N2O4混合气,气体颜色变深
F.500℃左右比常况下更有利于合成氨
G.开启啤酒后,瓶中马上泛起大量泡沫
(2)某化学科研小组研究在其他条件不变时,改变某一条件对反应 的化学平衡状态的影响,得到如图所示的变化规律(图中T表示温度,n表示物质的量)
的化学平衡状态的影响,得到如图所示的变化规律(图中T表示温度,n表示物质的量)

根据图像得出的结论,若正反应吸热,则T1___________ T2(填“>”“<”或“=”)。对于a、b、c三点:AB3的物质的量由大到小为___________ ,A2的平衡转化率由大到小为___________ ,B2的平衡转化率由大到小为___________ 。
(3)根据以下3个热化学方程式:
 △H1
△H1
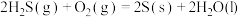 △H2
△H2
 △H3
△H3
△H1、△H2、△H3三者由大到小的顺序是___________ 。
(4)已知(NH4)2CO3捕碳的反应: 。将一定量的(NH4)2CO3溶液置于密闭容器中,并充入一定量的CO2气体,保持其它初始实验条件不变,分别在不同温度下,经过相同时间测得CO2气体浓度,得到趋势图。
。将一定量的(NH4)2CO3溶液置于密闭容器中,并充入一定量的CO2气体,保持其它初始实验条件不变,分别在不同温度下,经过相同时间测得CO2气体浓度,得到趋势图。

I.c点的逆反应速率和d点的正反应速率的大小关系为
___________  。(填“>”“=”或“<”)。
。(填“>”“=”或“<”)。
Ⅱ.b、c、d三点的平衡常数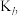 、
、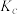 、
、 从大到小的顺序为
从大到小的顺序为___________ (填“>”、“=”或“<”)。
(1)下列事实不能用勒夏特列原理来解释的是
A.高压有利于氢气与氮气合成氨
B.实验室中常用排饱和食盐水的方法收集Cl2
C.工业上生产硫酸时,充入过量的空气以提高SO2的转化率
D.H2、I2、HI平衡混合气体加压后颜色加深

E.压缩NO2与N2O4混合气,气体颜色变深
F.500℃左右比常况下更有利于合成氨
G.开启啤酒后,瓶中马上泛起大量泡沫
(2)某化学科研小组研究在其他条件不变时,改变某一条件对反应
 的化学平衡状态的影响,得到如图所示的变化规律(图中T表示温度,n表示物质的量)
的化学平衡状态的影响,得到如图所示的变化规律(图中T表示温度,n表示物质的量)
根据图像得出的结论,若正反应吸热,则T1
(3)根据以下3个热化学方程式:
 △H1
△H1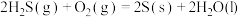 △H2
△H2 △H3
△H3△H1、△H2、△H3三者由大到小的顺序是
(4)已知(NH4)2CO3捕碳的反应:
 。将一定量的(NH4)2CO3溶液置于密闭容器中,并充入一定量的CO2气体,保持其它初始实验条件不变,分别在不同温度下,经过相同时间测得CO2气体浓度,得到趋势图。
。将一定量的(NH4)2CO3溶液置于密闭容器中,并充入一定量的CO2气体,保持其它初始实验条件不变,分别在不同温度下,经过相同时间测得CO2气体浓度,得到趋势图。
I.c点的逆反应速率和d点的正反应速率的大小关系为

 。(填“>”“=”或“<”)。
。(填“>”“=”或“<”)。Ⅱ.b、c、d三点的平衡常数
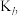 、
、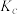 、
、 从大到小的顺序为
从大到小的顺序为
您最近半年使用:0次
名校
5 . 某温度下的密闭容器中:
①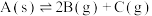 ;
;
②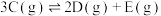
以上2个反应同时发生,10S后达平衡时, ,
,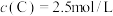 。
。
(1)加压时反应②的平衡___________ 移动。
A.向正反应方向 B.向逆反应方向 C.不移动
(2)该温度下反应①的平衡常数数值为___________ 。
①
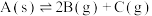 ;
;②
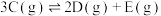
以上2个反应同时发生,10S后达平衡时,
 ,
,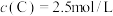 。
。(1)加压时反应②的平衡
A.向正反应方向 B.向逆反应方向 C.不移动
(2)该温度下反应①的平衡常数数值为
您最近半年使用:0次
名校
6 . 下列实验装置中进行的相关实验或操作能达到目的的是
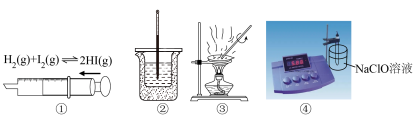

| A.①:探究压强对化学平衡的影响 | B.②:测定中和反应反应热 |
C.③:蒸发 溶液制备 溶液制备 固体 固体 | D.④:测定NaClO溶液的pH |
您最近半年使用:0次
2023-12-06更新
|
213次组卷
|
3卷引用:辽宁省葫芦岛市协作校2023-2024学年高三上学期第二次考试化学试题
名校
7 . I.一定温度下,某容器中加入足量的碳酸钙发生反应: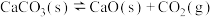 △H>0;一段时间后达到平衡。
△H>0;一段时间后达到平衡。
(1)该反应的化学平衡常数表达式为K=___________ ,为了提高CO2的生成率,可采取的措施___________ 。
A.减压 B.升温 C.增加碳酸钙的量 D.转移出CO2
(2)对于该反应,下列说法正确的是___________ 。
A.将体积缩小为原来的一半,当体系再次达到平衡时,CO2的浓度不变
B.将容器缩小为原来的一半,平衡不移动
C.将容器扩大为原来的两倍,平衡发生移动,再次平衡后,气体密度不变
D.增大压强,平衡逆向移动,K值减小
E.将体积增大为原来的2倍,再次达到平衡时,体系内压强不变
F.保持容器体积不变,充入He,平衡不移动
Ⅱ.
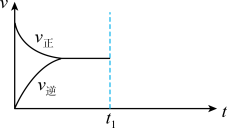
(3)在恒温恒压密闭容器中通入CO和H2O各1 发生反应
发生反应 ,当反应达到平衡后,维持温度与压强不变,
,当反应达到平衡后,维持温度与压强不变, 时再通入各1
时再通入各1 的CO和H2O的混合气体,请在下图中画出正反应和逆反应速率在
的CO和H2O的混合气体,请在下图中画出正反应和逆反应速率在 后随时间t变化的曲线图
后随时间t变化的曲线图___________ 。
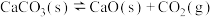 △H>0;一段时间后达到平衡。
△H>0;一段时间后达到平衡。(1)该反应的化学平衡常数表达式为K=
A.减压 B.升温 C.增加碳酸钙的量 D.转移出CO2
(2)对于该反应,下列说法正确的是
A.将体积缩小为原来的一半,当体系再次达到平衡时,CO2的浓度不变
B.将容器缩小为原来的一半,平衡不移动
C.将容器扩大为原来的两倍,平衡发生移动,再次平衡后,气体密度不变
D.增大压强,平衡逆向移动,K值减小
E.将体积增大为原来的2倍,再次达到平衡时,体系内压强不变
F.保持容器体积不变,充入He,平衡不移动
Ⅱ.
(3)在恒温恒压密闭容器中通入CO和H2O各1
 发生反应
发生反应 ,当反应达到平衡后,维持温度与压强不变,
,当反应达到平衡后,维持温度与压强不变, 时再通入各1
时再通入各1 的CO和H2O的混合气体,请在下图中画出正反应和逆反应速率在
的CO和H2O的混合气体,请在下图中画出正反应和逆反应速率在 后随时间t变化的曲线图
后随时间t变化的曲线图
您最近半年使用:0次
名校
解题方法
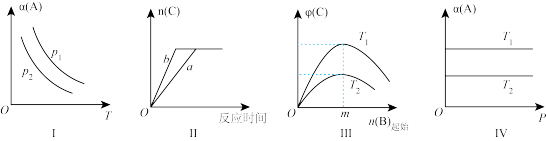
8 . 在其他条件不变时,改变某一外界条件对反应 化学平衡的影响,得到如图所示的图像(p表示压强,T表示温度,n表示物质的量,
化学平衡的影响,得到如图所示的图像(p表示压强,T表示温度,n表示物质的量, 表示平衡转化率,
表示平衡转化率, 表示体积分数),下列说法不正确的是
表示体积分数),下列说法不正确的是
 化学平衡的影响,得到如图所示的图像(p表示压强,T表示温度,n表示物质的量,
化学平衡的影响,得到如图所示的图像(p表示压强,T表示温度,n表示物质的量, 表示平衡转化率,
表示平衡转化率, 表示体积分数),下列说法不正确的是
表示体积分数),下列说法不正确的是
A.在Ⅰ中,若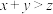 ,则 ,则 |
| B.在Ⅱ中,若实现a→b只能加入合适的催化剂 |
C.在Ⅲ中,随着B的起始物质的量的增加,在m点时,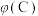 达到最大值,则m点反应物A与B的投料量比为 达到最大值,则m点反应物A与B的投料量比为 |
D.在Ⅳ中,若 ,则该反应的平衡常数 ,则该反应的平衡常数 |
您最近半年使用:0次
名校
9 . 一定条件下,某密闭容器内存在下列平衡:
 。则下列有关说法正确的是
。则下列有关说法正确的是

 。则下列有关说法正确的是
。则下列有关说法正确的是| A.缩小反应容器的体积,使压强增大,平衡不移动,混合气体颜色深浅不变 |
| B.保持容积不变,改变体系温度,体系颜色一定发生变化 |
| C.保持容积不变,继续充入HI气体,则HI的转化率将减小 |
D.保持其他条件不变,升高温度, 增大, 增大, 减小 减小 |
您最近半年使用:0次
2023-11-11更新
|
64次组卷
|
2卷引用:辽宁省瓦房店市高级中学2023-2024学年高二上学期10月联考化学试题
名校
10 . 下列事实不能用勒夏特列原理解释的是
| A.在合成氨实际生产中,使气态氨变成液氨后及时从平衡混合物中分离出去,以提高原料的利用率 |
B. 、 、 、 、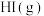 组成的平衡体系,加压后体系颜色变深 组成的平衡体系,加压后体系颜色变深 |
C.向重铬酸钾( )溶液中滴加少量NaOH溶液,溶液颜色由橙色变为黄色 )溶液中滴加少量NaOH溶液,溶液颜色由橙色变为黄色 |
| D.实验室中常用排饱和食盐水的方法收集氯气 |
您最近半年使用:0次
2023-11-04更新
|
361次组卷
|
2卷引用:辽宁省辽东南协作校2023-2024学年高二上学期12月月考化学(A卷)试题



