1 . 用来表示可逆反应: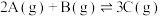
 的正确图像是
的正确图像是
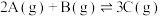
 的正确图像是
的正确图像是A.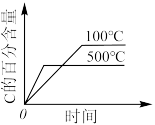 | B.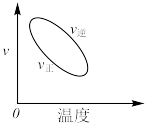 |
C.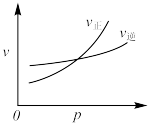 | D. |
您最近半年使用:0次
名校
解题方法
2 . 反应 ,在温度为
,在温度为 时,平衡体系中
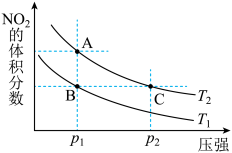
时,平衡体系中 的体积分数随压强变化曲线如图所示。下列说法正确的是
的体积分数随压强变化曲线如图所示。下列说法正确的是
 ,在温度为
,在温度为 时,平衡体系中
时,平衡体系中 的体积分数随压强变化曲线如图所示。下列说法正确的是
的体积分数随压强变化曲线如图所示。下列说法正确的是
A.A、C两点的反应速率: |
| B.A、C两点气体的颜色:A深,C浅 |
C.由状态 到状态 到状态 ,可以用加热的方法 ,可以用加热的方法 |
D.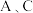 两点气体的平均相对分子质量: 两点气体的平均相对分子质量: |
您最近半年使用:0次
2023-08-11更新
|
1241次组卷
|
26卷引用:辽宁省朝阳市建平县建平县实验中学2023-2024学年高二上学期开学考试化学试题
辽宁省朝阳市建平县建平县实验中学2023-2024学年高二上学期开学考试化学试题辽宁省大连市普兰店第二中学2020-2021学年高二上学期期中考试化学试题内蒙古通辽市科左后旗甘旗卡第二高级中学2020-2021学年高二下学期开学考试化学试题辽宁省鞍山市普通高中2022-2023学年高二上学期第一次月考化学试题广东省东莞市二中2020-2021学年上学期高二10月考试化学试题四川省成都市实验外国语学校(西区)2019-2020 学年高二上学期期中考试化学试题江西省名校2021-2022学年高二上学期第一次月考化学试题安徽省淮北市树人高级中学2021-2022学年高二上学期第一次月考化学试题浙江省绍兴鲁迅中学2021-2022学年高二上学期第一次限时训练化学试题江西省新余市第四中学2021-2022学年高二上学期第一次月考化学试题(已下线)必考点03 化学平衡-【对点变式题】2021-2022学年高二化学上学期期中期末必考题精准练(人教版)安徽省亳州市第二中学2021-2022学年高二上学期期中考试化学试题广东省佛山市第一中学2021-2022学年高二上学期第一次段考化学试题 吉林省松原市长岭县第三中学2021-2022学年高二上学期第三次考试化学试题湖北省宜城市第三高级中学2021-2022学年高二上学期期中考试化学试卷题安徽省怀宁县第二中学2021-2022学年高二上学期期中考试化学试题大庆市肇州县肇州中学2021-2022学年高二上学期第二次月考化学试题广东省江门市第一中学2022-2023学年高二上学期第一次月考化学试题河南省平顶山市汝州第一高级中学2022-2023学年高二10月月考化学试题湖南省邵阳市武冈市2022-2023学年高二上学期期中考试化学试题(已下线)第06讲 化学反应速率与化学平衡的图像-【暑假自学课】2023年新高二化学暑假精品课(人教版2019选择性必修1)湖南师范大学附属中学2022-2023学年高一下学期期末考试化学试题山东学情2023-2024学年高二上学期10月质量检测(人教版)化学试题四川省仁寿第一中学校南校区2023-2024学年高二上学期10月月考化学试题浙江省湖州市吴兴高级中学2023-2024学年高二上学期10月阶段性测试化学试题天津市第四十七中学2023-2024学年高二上学期11月期中考试化学试题
名校
3 . 对于可逆反应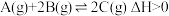 ,下列图像中正确的是
,下列图像中正确的是
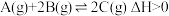 ,下列图像中正确的是
,下列图像中正确的是A.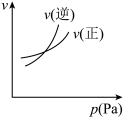 | B.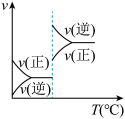 | C.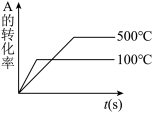 | D.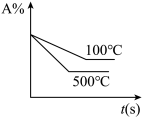 |
您最近半年使用:0次
2022-11-13更新
|
144次组卷
|
76卷引用:辽宁省庄河市高级中学2017-2018学年高二上学期开学考试化学试题
辽宁省庄河市高级中学2017-2018学年高二上学期开学考试化学试题2015-2016学年宁夏吴忠中学高二下开学考试化学试卷吉林省长春外国语学校2017-2018学年高一上学期开学测试化学试题河北省邢台市第二中学2019-2020学年高二下学期开学考试化学试题新疆维吾尔自治区呼图壁县第一中学2020-2021学年高二下学期期初考试化学试题(已下线)2010-2011学年云南省昆明一中高二下学期期中考试化学试卷(已下线)2011-2012学年湖北省襄阳市四校高二上学期期中考试化学试卷(已下线)2011-2012学年四川省金堂中学高二下学期期中考试化学试卷 (已下线)2012-2013学年广东东莞第七高级中学高二上期中考试化学试卷(已下线)2013-2014学年广东省肇庆市高二上学期末考试化学试卷(已下线)2013-2014北京市房山区下学期高二期末测验化学试卷(已下线)2014-2015学年云南省玉溪市第一中学高二上学期期中考试化学试卷(已下线)2014-2015学年吉林省汪清县第六中学高二上学期期中考试化学试卷2014-2015学年重庆复旦中学高二上学期期中化学试卷2014-2015黑龙江省鸡西市龙东南四校高二上学期期末联考化学试卷2015-2016学年河南省鄢陵高级中学高二上学期第二次月考化学试卷2015-2016北京大学附中宇华教育集团高二12月化学卷2015-2016北京大学附中宇华教育集团高一12月化学卷2015-2016学年安徽省钱桥中学、泥河中学高二上12月联考化学试卷2015-2016学年安徽省六安一中高二上第一阶段测化学试卷2015-2016学年贵州省大方一中高二上学期期末化学试卷2015-2016学年河北省邢台一中高一下期中化学试卷2015-2016学年广西南宁市二十六中高二下学期期中化学试卷2015-2016学年云南省云天化中学高二下期中理综化学试卷2016-2017学年浙江省温州中学高二上10月月考化学试卷2016-2017学年贵州省思南中学高二上半期考试化学卷2016-2017学年河南郸城高级中学高二上第二次考试化学卷2016-2017学年西藏山南二中高二上学期期中化学试卷浙江省2018版考前特训(2017年10月)学考70快练:化学反应速率及反应限度贵州省思南中学2017-2018学年高二上学期第一次月考化学试题甘肃省武威市第六中学2017-2018学年高二上学期第一次学段考试化学试题云南省德宏州芒市第一中学2017-2018学年高二上学期期中考试化学试题陕西省渭南市尚德中学2017-2018学年高二上学期期中考试化学试卷山东省枣庄市第三中学2017-2018学年高二第六学段学情调查(1月)化学试题贵州省毕节市实验高级中学2017-2018学年高二上学期期末考试化学试题安徽省滁州市民办高中2017-2018学年高一下学期第二次月考化学试题【全国百强校】内蒙古集宁一中(东校区)2017-2018学年高一下学期期末考试化学试题云南省腾冲市第八中学2017-2018学年高二下学期期末考试化学试题广东省蓝精灵中学2018-2019学年高二上学期联考化学试题2017-2018学年鲁科版高二化学选修4第二章第一节化学反应的方向作业题【全国百强校】安徽省铜陵市第一中学2018-2019学年高二上学期10月月考化学试题西藏自治区日喀则市南木林高级中学2018-2019学年高二上学期期中考试化学试题新疆维吾尔自治区伊宁市生产建设兵团四师一中2018-2019学年高二上学期期中考试化学试题吉林省长春市九台区师范高级中学2018-2019学年高二上学期期中考试化学试题江苏省邗江中学2018-2019学年高二下学期期中考试化学试题甘肃省张掖市山丹县第一中学2017—2018学年高二上学期期末质量检测化学试题安徽省芜湖市城南实验中学2019-2020学年高二上学期期中考试化学试题湖南省常德市石门县第二中学2019-2020学年高二上学期第二次月考化学试题贵州省金沙中学2019年普通高中学生学业基础水平测试化学试题(已下线)【南昌新东方】江西省九江一中2014-2015学年高二上学期期中化学试卷(已下线)专题讲座(七) 常考速率、平衡图像题解题策略(精练)-2021年高考化学一轮复习讲练测河南省安阳县第三高级中学2020-2021学年高二上学期第一次阶段考试化学试题广东省佛山市第一中学2020-2021学年高二上学期第一次段考化学(选考)试题黑龙江省伊春市伊美区第二中学2018-2019学年高二上学期阶段考试(12月)化学试题黑龙江省绥化地区肇东第四中学2020-2021学年高二上学期期末考试化学试题西藏日喀则市上海实验学校2019-2020学年高二上学期期末考试化学试题江苏省宿迁市沭阳县潼阳中学2020-2021学年高二下学期第一次月考化学试题福建省南安市柳城中学2020-2021学年高二上学期第二次月考化学试题青海省海南州贵德高级中学2020-2021学年高二下学期期中化学试题新疆乌鲁木齐市第二十中学2020-2021学年高二上学期段考(期中)化学试题吉林省延边第二中学2020-2021学年高二上学期第一次考试月考化学试题黑龙江省双鸭山市第一中学2021-2022学年高二上学期第一次月考化学试题广东省广州市北师大附中为明学校2021-2022学年高二10月月考化学试题河南省平顶山九校联盟2021-2022学年高二上学期期中考试化学试题广东省珠海市第二中学2021-2022学年高二上学期期中考试化学试题黑龙江省绥化市第一中学2021-2022学年高二上学期期末考试化学试题黑龙江省饶河县高级中学2021-2022学年上学期期末考试化学试题湖北省部分高中联考协作体2022-2023学年高二上学期期中考试化学试题(已下线)第七章 化学反应速率与化学平衡 第44练 化学反应速率、平衡的常规图像河南省南阳市2022-2023学年高二下学期期末考试化学试题(已下线)第4讲 化学反应速率及平衡图像江西省南昌市第一中学2023-2024学年高二上学期10月月考化学试题浙江省湖州市吴兴高级中学2023-2024学年高二上学期10月阶段性测试化学试题浙江省杭州东方中学2023-2024学年高二上学期期中考试化学试题河南省郑州学森实验学校2023-2024学年高二上学期期中考试 化学试题广西防城港市实验高级中学2023-2024学年高二下学期期中考试化学试题
名校
4 . 下列事实不能用勒夏特列原理解释的是
| A.光照新制的氯水时,溶液的pH逐渐减小 |
| B.合成氨工厂采用增大压强以提高原料的利用率 |
| C.实验室用排饱和食盐水法收集氯气 |
| D.由H2、I2(g)、HI气体组成的平衡加压后颜色变深 |
您最近半年使用:0次
名校
5 . 在某容积一定的密闭容器中,可逆反应:A(g)+B(g) xC(g),有图Ⅰ所示的反应曲线,试判断对图Ⅱ的说法中正确的是(T表示温度,p表示压强,C%表示C的体积分数)
xC(g),有图Ⅰ所示的反应曲线,试判断对图Ⅱ的说法中正确的是(T表示温度,p表示压强,C%表示C的体积分数)
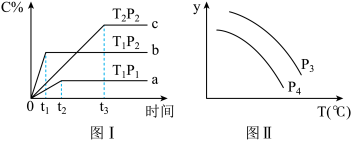
 xC(g),有图Ⅰ所示的反应曲线,试判断对图Ⅱ的说法中正确的是(T表示温度,p表示压强,C%表示C的体积分数)
xC(g),有图Ⅰ所示的反应曲线,试判断对图Ⅱ的说法中正确的是(T表示温度,p表示压强,C%表示C的体积分数)
| A.p3>p4,y轴表示A的物质的量 |
| B.p3<p4,y轴表示C的体积分数 |
| C.p3<p4,y轴表示混合气体的密度 |
| D.p3>p4,y轴表示混合气体的平均相对分子质量 |
您最近半年使用:0次
2022-09-17更新
|
503次组卷
|
8卷引用:辽宁省沈阳实验中学2022-2023学年高二上学期开学考试化学试题
名校
6 . 如图所示,三个烧瓶中分别充满NO2气体并分别装在盛有水的三个烧杯中,在①烧杯中加入CaO,在②烧杯中不加其他任何物质,在③烧杯中加入NH4Cl晶体,发现①中红棕色变深,③中红棕色变浅。已知:2NO2(红棕色) N2O4(无色),下列叙述正确的是
N2O4(无色),下列叙述正确的是
 N2O4(无色),下列叙述正确的是
N2O4(无色),下列叙述正确的是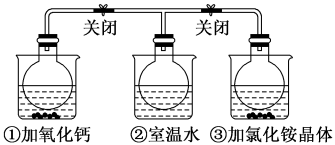
A.2NO2 N2O4是吸热反应 N2O4是吸热反应 |
| B.NH4Cl溶于水时吸收热量 |
| C.①烧瓶中平衡时混合气体的平均相对分子质量增大 |
| D.③烧瓶中气体的压强增大 |
您最近半年使用:0次
2022-08-28更新
|
1126次组卷
|
23卷引用:【全国百强校】辽宁省鞍山市第一中学2018-2019学年高二下学期开学考试化学试题
【全国百强校】辽宁省鞍山市第一中学2018-2019学年高二下学期开学考试化学试题江西省赣州市第一中学2020-2021学年高二下学期开学测试化学试题河南省信阳高级中学2020-2021学年高二下学期回顾测试化学试题(已下线)2010年北京市八一中学高二第二学期期末考试化学试卷2018版化学(苏教版)高考总复习专题七课时跟踪训练--化学平衡的移动新疆生产建设兵团第二中学2017-2018学年高二上学期第四次月考(期末)化学试题新疆自治区生产建设兵团第二中学2018-2019学年高二第一次月考化学试题陕西省延安市第一中学2019-2020学年高二上学期期中考试化学试题(已下线)专题7.2 化学平衡状态 化学平衡移动(练)-《2020年高考一轮复习讲练测》云南省普洱市江城县第一中学2019—2020学年高二上学期期末考试化学试题四川省泸州市泸县第二中学2019-2020学年高二下学期第一次在线月考化学试题黑龙江省大庆市第四中学2019-2020学年高二上学期第一次检测化学试题(已下线)2.3.2+影响化学平衡状态的因素-2020-2021学年高二化学同步课堂帮帮帮(人教版选修4)安徽省蚌埠田家炳中学2020-2021学年高二10月月考化学试题江西省上饶市2020-2021学年高二上学期期末教学质量测试化学试题福建省三明第一中学2021-2022学年高二上学期第一次月考化学试题福建省莆田市擢英中学2021-2022学年高二上学期第一次月考化学试卷(已下线)2.2.2 浓度商、温度对化学平衡的影响-【帮课堂】2022-2023学年高二化学同步精品讲义(沪科版2020选择性必修第一册)黑龙江省伊春市伊美区第二中学2021-2022学年高二上学期期中考试化学试题广东省深圳市宝安区宝安中学2022-2023学年高一上学期期中考试化学试题新疆奇台县第一中学2022-2023学年高二上学期期中考试化学试题山东省淄博市部分学校联考2022-2023学年高一下学期4月期中考试化学试题(已下线)选择题11-15
名校
7 . 下列事实能用勒夏特列原理来解释的是
A.实验室采用排饱和食盐水的方法收集氯气Cl2+H2O H++Cl-+HClO H++Cl-+HClO |
B.工业上合成氨反应N2(g)+3H2(g) 2NH3(g) △H<0选择500℃ 2NH3(g) △H<0选择500℃ |
C.H2、I2、HI平衡混合气体加压后颜色加深H2(g)+I2(g) 2HI(g) 2HI(g) |
D.SO2氧化成SO3,往往需要使用催化剂2SO2(g)+O2(g) 2SO3(g) 2SO3(g) |
您最近半年使用:0次
2022-08-25更新
|
414次组卷
|
10卷引用:辽宁省辽河油田第二高级中学2021-2022学年高二上学期开学考试化学试题
辽宁省辽河油田第二高级中学2021-2022学年高二上学期开学考试化学试题重庆市九校联盟2017-2018学年高二上学期期中考试化学试题【区级联考】天津市武清区2018-2019学年高二上学期期中质量调查化学试题湖南省永州市双牌县第二中学2019-2020学年高二上学期期中考试化学试题(选考)吉林省洮南市第一中学2021-2022学年高二上学期第一次月考化学试题吉林省长春市第二十中学2021-2022学年高二上学期第一次质量检测化学试题新疆昌吉州2021-2022学年高二上学期期中质量检测化学试题江西省宜春市万载中学2021-2022学年高二上学期第二次月考化学试题上海市奉贤中学2022-2023学年高二上学期10月阶段测试化学试题重庆市渝东六校共同体2022-2023学年高二上学期联合诊断考试化学试题
名校
8 . 高温下,某反应达平衡,平衡常数K= ,恒容时,温度升高,B的浓度减小,下列说法正确的是
,恒容时,温度升高,B的浓度减小,下列说法正确的是
①该反应的焓变为正值
②恒温恒容下,增大压强B浓度一定增大
③升高温度,平衡常数K值减小
④该反应化学方程式为C(g)+D(g) A(g)+B(g)
A(g)+B(g)
⑤增加A的量,A的转化率减小
⑥加入催化剂,平衡不移动,V(正)、V(逆)都不变
 ,恒容时,温度升高,B的浓度减小,下列说法正确的是
,恒容时,温度升高,B的浓度减小,下列说法正确的是①该反应的焓变为正值
②恒温恒容下,增大压强B浓度一定增大
③升高温度,平衡常数K值减小
④该反应化学方程式为C(g)+D(g)
 A(g)+B(g)
A(g)+B(g)⑤增加A的量,A的转化率减小
⑥加入催化剂,平衡不移动,V(正)、V(逆)都不变
| A.①③⑥ | B.①⑤ | C.①④⑤ | D.①②⑤ |
您最近半年使用:0次
9 . 我国在应对气候变化工作中取得显著成效,并向国际社会承诺2030年实现“碳达峰”,2060年实现“碳中和”。因此将CO2转化为高附加值化学品成为科学家研究的重要课题。异丁烯[CH2=C(CH3)2]作为汽油添加剂的主要成分,可利用异丁烷与CO2反应来制备。
反应I:CH3CH(CH3)CH3(g)+CO2(g) CH2=C(CH3)2(g)+H2O(g)+CO(g) ΔH1
CH2=C(CH3)2(g)+H2O(g)+CO(g) ΔH1
反应II:CH3CH(CH3)CH3(g) CH2=C(CH3)2(g)+H2(g) ΔH2=+124 kJ∙mol−1
CH2=C(CH3)2(g)+H2(g) ΔH2=+124 kJ∙mol−1
回答下列问题:
(1)已知:CO(g)+H2O(g) CO2(g)+H2(g) ΔH=−41.2 kJ∙mol−1,则ΔH1=
CO2(g)+H2(g) ΔH=−41.2 kJ∙mol−1,则ΔH1=___________ 。
(2)向1.0L恒容密闭容器中加入0.1molCH3CH(CH3)CH3(g)和0.1molCO2(g),利用反应I制备异丁烯。已知正反应速率可表示为v正=k正c[CH3CH(CH3)CH3]∙c(CO2),逆反应速率可表示为,v逆=k逆c[CH2=C(CH3)2]∙c(H2O)∙c(CO),其中k正、k逆为速率常数。
①图1中能够代表k逆的曲线为___________ (填“L1”“L2”、或“L3”“L4”)。
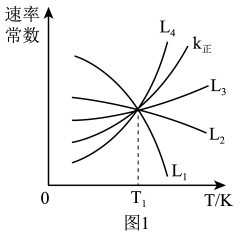
②温度为T1时,该反应的化学平衡常数K=___________ ;
(3)利用M催化CO2,加氢制CH3OH的反应历程如图2所示,其中吸附在催化剂表面的物种用*表示,Ea表示活化能,单位为eV。
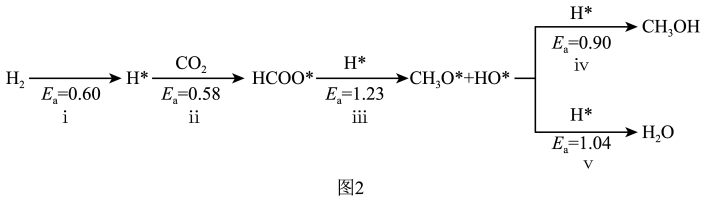
 转化为
转化为 的化学方程式为
的化学方程式为___________ 。
(4)工业上在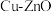 催化下利用CO2发生如下反应I生产甲醇,同时伴有反应II发生。
催化下利用CO2发生如下反应I生产甲醇,同时伴有反应II发生。
I.CO2(g)+3H2(g) CH3OH (g)+ H2O(g) ΔH= −49.4 kJ∙mol−1
CH3OH (g)+ H2O(g) ΔH= −49.4 kJ∙mol−1
II.CO2(g)+ H2(g) CO (g)+ H2O(g) ΔH=+41.2 kJ∙mol−1
CO (g)+ H2O(g) ΔH=+41.2 kJ∙mol−1
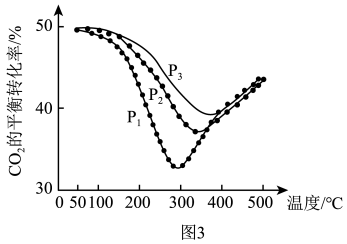
不同条件下,按照n(CO2):n(H2)=1:3投料,CO2的平衡转化率如图3所示。压强p1、p2、p3由大到小的顺序是___________ 。压强为p1时,温度高于300℃之后,随着温度升高CO2平衡转化率增大的原因___________ 。
(5)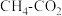 重整技术是实现“碳中和”的一种理想的CO2利用技术,反应为:CO2(g)+CH4(g)
重整技术是实现“碳中和”的一种理想的CO2利用技术,反应为:CO2(g)+CH4(g) 2CO (g)+2H2(g)。某温度下,向一恒容密闭容器中充入CO2和CH4发生此反应,初始时CO2和CH4的分压分别为15kPa、20kPa,一段时间达到平衡后,测得体系压强增加了10kPa,则该反应的平衡常数Kp=
2CO (g)+2H2(g)。某温度下,向一恒容密闭容器中充入CO2和CH4发生此反应,初始时CO2和CH4的分压分别为15kPa、20kPa,一段时间达到平衡后,测得体系压强增加了10kPa,则该反应的平衡常数Kp=___________ (kPa)2(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
反应I:CH3CH(CH3)CH3(g)+CO2(g)
 CH2=C(CH3)2(g)+H2O(g)+CO(g) ΔH1
CH2=C(CH3)2(g)+H2O(g)+CO(g) ΔH1反应II:CH3CH(CH3)CH3(g)
 CH2=C(CH3)2(g)+H2(g) ΔH2=+124 kJ∙mol−1
CH2=C(CH3)2(g)+H2(g) ΔH2=+124 kJ∙mol−1回答下列问题:
(1)已知:CO(g)+H2O(g)
 CO2(g)+H2(g) ΔH=−41.2 kJ∙mol−1,则ΔH1=
CO2(g)+H2(g) ΔH=−41.2 kJ∙mol−1,则ΔH1=(2)向1.0L恒容密闭容器中加入0.1molCH3CH(CH3)CH3(g)和0.1molCO2(g),利用反应I制备异丁烯。已知正反应速率可表示为v正=k正c[CH3CH(CH3)CH3]∙c(CO2),逆反应速率可表示为,v逆=k逆c[CH2=C(CH3)2]∙c(H2O)∙c(CO),其中k正、k逆为速率常数。
①图1中能够代表k逆的曲线为

②温度为T1时,该反应的化学平衡常数K=
(3)利用M催化CO2,加氢制CH3OH的反应历程如图2所示,其中吸附在催化剂表面的物种用*表示,Ea表示活化能,单位为eV。

 转化为
转化为 的化学方程式为
的化学方程式为(4)工业上在
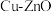 催化下利用CO2发生如下反应I生产甲醇,同时伴有反应II发生。
催化下利用CO2发生如下反应I生产甲醇,同时伴有反应II发生。I.CO2(g)+3H2(g)
 CH3OH (g)+ H2O(g) ΔH= −49.4 kJ∙mol−1
CH3OH (g)+ H2O(g) ΔH= −49.4 kJ∙mol−1II.CO2(g)+ H2(g)
 CO (g)+ H2O(g) ΔH=+41.2 kJ∙mol−1
CO (g)+ H2O(g) ΔH=+41.2 kJ∙mol−1不同条件下,按照n(CO2):n(H2)=1:3投料,CO2的平衡转化率如图3所示。压强p1、p2、p3由大到小的顺序是

(5)
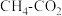 重整技术是实现“碳中和”的一种理想的CO2利用技术,反应为:CO2(g)+CH4(g)
重整技术是实现“碳中和”的一种理想的CO2利用技术,反应为:CO2(g)+CH4(g) 2CO (g)+2H2(g)。某温度下,向一恒容密闭容器中充入CO2和CH4发生此反应,初始时CO2和CH4的分压分别为15kPa、20kPa,一段时间达到平衡后,测得体系压强增加了10kPa,则该反应的平衡常数Kp=
2CO (g)+2H2(g)。某温度下,向一恒容密闭容器中充入CO2和CH4发生此反应,初始时CO2和CH4的分压分别为15kPa、20kPa,一段时间达到平衡后,测得体系压强增加了10kPa,则该反应的平衡常数Kp=
您最近半年使用:0次
名校
10 . 某温度下,在恒容密闭容器中加入一定量X,发生反应2X(s) Y (s)+Z(g),一段时间后达到平衡。下列说法错误的是
Y (s)+Z(g),一段时间后达到平衡。下列说法错误的是
 Y (s)+Z(g),一段时间后达到平衡。下列说法错误的是
Y (s)+Z(g),一段时间后达到平衡。下列说法错误的是| A.升高温度,若c(Z)增大,则△H>0 |
| B.加入一定量Z,达新平衡后m(Y)减小 |
| C.加入一定量X,达新平衡后c(Z)增大 |
| D.加入一定量氩气,平衡不移动 |
您最近半年使用:0次
2021-10-21更新
|
952次组卷
|
7卷引用:辽宁省沈阳市第八十三中学2022-2023学年高二上学期开学考试化学试题
辽宁省沈阳市第八十三中学2022-2023学年高二上学期开学考试化学试题四川省仁寿县四校联考2021-2022学年高二上学期10月月考化学试题(已下线)必考点03 化学平衡-【对点变式题】2021-2022学年高二化学上学期期中期末必考题精准练(人教版)黑龙江省密山市第四中学2021-2022学年高二上学期期中考试化学(理)试题江苏省连云港市赣榆智贤中学2022-2023学年高二上学期第一次学情检测化学试题广东省惠州市实验中学2022-2023学年高二上学期期中考试化学试题河北省衡水市枣强中学2023-2024学年高二下学期第一次调研考试化学试题



