名校
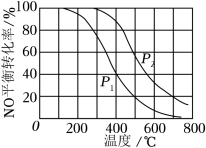
1 . 一定条件下,将NO(g)和O2(g)按物质的量之比2:1充入反应容器,发生反应:2NO(g)+O2(g) 2NO2(g)。其他条件相同时,分别测得NO的平衡转化率在不同压强(p1、p2)下随温度变化的曲线如图所示。下列说法正确的是
2NO2(g)。其他条件相同时,分别测得NO的平衡转化率在不同压强(p1、p2)下随温度变化的曲线如图所示。下列说法正确的是
 2NO2(g)。其他条件相同时,分别测得NO的平衡转化率在不同压强(p1、p2)下随温度变化的曲线如图所示。下列说法正确的是
2NO2(g)。其他条件相同时,分别测得NO的平衡转化率在不同压强(p1、p2)下随温度变化的曲线如图所示。下列说法正确的是
| A.p1>p2 |
| B.其他条件不变,温度升高,该反应的反应限度减小 |
| C.400℃、p1条件下,O2的平衡转化率为20% |
D.400℃时,该反应的化学平衡常数的数值为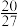 |
您最近半年使用:0次
2024-03-13更新
|
51次组卷
|
2卷引用:湖南省岳阳市岳阳县第一中学2023-2024学年高二下学期开学化学试题
名校
2 . 当今世界多国相继规划了碳达峰、碳中和的时间节点。因此,研发二氧化碳利用技术,降低空气中二氧化碳含量成为研究热点。其中用 、
、 为原料合成甲醇(
为原料合成甲醇( )过程主要涉及以下反应:
)过程主要涉及以下反应:
反应Ⅰ:

反应Ⅱ:

反应Ⅲ:
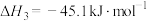
(1)根据盖斯定律,反应Ⅰ的
_______ 。
(2)我国学者结合实验与计算机模拟结果,研究了 与
与 在
在 /Cu催化剂表面生成
/Cu催化剂表面生成 和
和 的部分反应历程,如图所示,其中吸附在催化剂表面的物种用*标注。
的部分反应历程,如图所示,其中吸附在催化剂表面的物种用*标注。
_______ eV。并写出该历程的化学方程式_______ 。
(3)上述反应体系在一定条件下建立平衡后,下列说法正确的有_______(填字母)。
(4)加压,甲醇产率将_______ (填“升高”“不变”“降低”或“无法确定”);若原料二氧化碳中掺混一氧化碳,随一氧化碳含量的增加,甲醇产率将_______ (填“升高”“不变”“降低”或“无法确定”)。
(5)加入新催化剂使1mol 和3mol
和3mol  在1L密闭容器中只发生反应Ⅰ、Ⅱ,
在1L密闭容器中只发生反应Ⅰ、Ⅱ, 平衡转化率和甲醇选择率(甲醇选择率是指转化生成甲醇的
平衡转化率和甲醇选择率(甲醇选择率是指转化生成甲醇的 物质的量分数)与温度的变化趋势如图所示。
物质的量分数)与温度的变化趋势如图所示。_______ (填“473K”“513K”或“553K”)。
②553K时,若反应后体系的总压为p,反应Ⅰ的
_______ (列出计算式)。( 为压强平衡常数,其表达式写法:在浓度平衡常数表达式中用气体分压代替浓度,气体的分压等于总压乘以物质的量分数。)
为压强平衡常数,其表达式写法:在浓度平衡常数表达式中用气体分压代替浓度,气体的分压等于总压乘以物质的量分数。)
 、
、 为原料合成甲醇(
为原料合成甲醇( )过程主要涉及以下反应:
)过程主要涉及以下反应:反应Ⅰ:


反应Ⅱ:


反应Ⅲ:

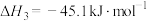
(1)根据盖斯定律,反应Ⅰ的

(2)我国学者结合实验与计算机模拟结果,研究了
 与
与 在
在 /Cu催化剂表面生成
/Cu催化剂表面生成 和
和 的部分反应历程,如图所示,其中吸附在催化剂表面的物种用*标注。
的部分反应历程,如图所示,其中吸附在催化剂表面的物种用*标注。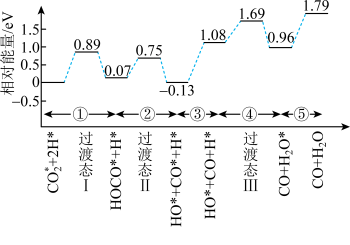

(3)上述反应体系在一定条件下建立平衡后,下列说法正确的有_______(填字母)。
| A.升高温度,反应Ⅱ正向移动,反应Ⅲ逆向移动 |
| B.加入反应Ⅰ的催化剂,可以降低反应的活化能及反应热 |
C.增大 的浓度,有利于提高 的浓度,有利于提高 的平衡转化率 的平衡转化率 |
D.及时分离出 ,可以使得反应Ⅰ的正反应速率增大 ,可以使得反应Ⅰ的正反应速率增大 |
(4)加压,甲醇产率将
(5)加入新催化剂使1mol
 和3mol
和3mol  在1L密闭容器中只发生反应Ⅰ、Ⅱ,
在1L密闭容器中只发生反应Ⅰ、Ⅱ, 平衡转化率和甲醇选择率(甲醇选择率是指转化生成甲醇的
平衡转化率和甲醇选择率(甲醇选择率是指转化生成甲醇的 物质的量分数)与温度的变化趋势如图所示。
物质的量分数)与温度的变化趋势如图所示。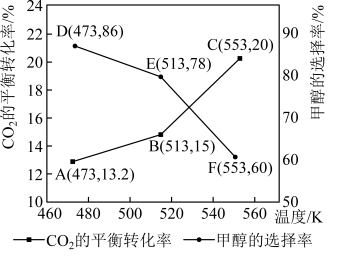
②553K时,若反应后体系的总压为p,反应Ⅰ的

 为压强平衡常数,其表达式写法:在浓度平衡常数表达式中用气体分压代替浓度,气体的分压等于总压乘以物质的量分数。)
为压强平衡常数,其表达式写法:在浓度平衡常数表达式中用气体分压代替浓度,气体的分压等于总压乘以物质的量分数。)
您最近半年使用:0次
2023-09-30更新
|
254次组卷
|
5卷引用:湖南省平江县颐华高级中学2023-2024学年高三下学期入学考试化学试题
名校
解题方法
3 . 在催化剂作用下, 氧化
氧化 可获得
可获得 。其主要化学反应如下:
。其主要化学反应如下:
反应Ⅰ.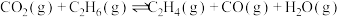

反应Ⅱ.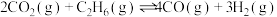

压强分别为 、
、 时,将
时,将
 和
和
 的混合气体置于密闭容器中反应,不同温度下体系中乙烷的平衡转化率、乙烯的选择性[
的混合气体置于密闭容器中反应,不同温度下体系中乙烷的平衡转化率、乙烯的选择性[ ]如图所示。下列说法正确的是
]如图所示。下列说法正确的是
 氧化
氧化 可获得
可获得 。其主要化学反应如下:
。其主要化学反应如下:反应Ⅰ.
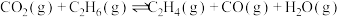

反应Ⅱ.
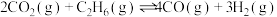

压强分别为
 、
、 时,将
时,将
 和
和
 的混合气体置于密闭容器中反应,不同温度下体系中乙烷的平衡转化率、乙烯的选择性[
的混合气体置于密闭容器中反应,不同温度下体系中乙烷的平衡转化率、乙烯的选择性[ ]如图所示。下列说法正确的是
]如图所示。下列说法正确的是
A. |
B.压强为 、温度为210℃时,反应达平衡时, 、温度为210℃时,反应达平衡时, |
C. 的选择性下降的原因可能是随着温度的升高,反应Ⅱ中生成的 的选择性下降的原因可能是随着温度的升高,反应Ⅱ中生成的 抑制了反应Ⅰ的进行 抑制了反应Ⅰ的进行 |
D.研发低温下 转化率高和 转化率高和 选择性高的催化剂,可以提高平衡时 选择性高的催化剂,可以提高平衡时 产率 产率 |
您最近半年使用:0次
2023-09-22更新
|
204次组卷
|
11卷引用:湖南省平江县颐华高级中学2023-2024学年高三下学期入学考试化学试题
湖南省平江县颐华高级中学2023-2024学年高三下学期入学考试化学试题湖南省长沙市雅礼中学2024届高三上学期月考试卷(一)化学试题湖南省常德市第一中学2023-2024学年高三上学期第六次月考化学试题湖南省常德市第一中学2023-2024学年高三上学期第六次月考化学试题江苏省无锡市2022-2023学年高三上学期期末调研测试化学试题(已下线)素养卷04 化学反应速率与平衡图像题-【小题小卷】冲刺2023年高考化学小题限时集训(新高考专用)(已下线)选择题11-13江苏省常州市联盟学校2022-2023学年高二下学期期中学情调研化学试题江苏省南京市第九中学2023-2024学年高二上学期期末化学试卷江苏省南京市六校联合体2023-2024学年高二下学期四月联考化学试卷江苏省盐城市三校联考2023-2024学年高二下学期4月期中考试化学试题
名校
4 . 实验是学习化学的基础。下列有关化学实验的叙述正确的是
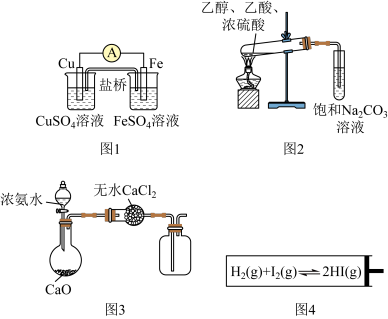
| A.用图1装置比较Cu和Fe的活泼性强弱 |
| B.用图2装置制取乙酸乙酯 |
| C.用图3装置制取并收集干燥的氨气 |
D.缩小图4中容器体积,H2(g)+I2(g) 2HI(g)平衡逆向移动,气体颜色加深 2HI(g)平衡逆向移动,气体颜色加深 |
您最近半年使用:0次
2023-04-21更新
|
866次组卷
|
8卷引用:湖南省衡阳市衡阳县第二中学2023-2024学年高三下学期开学摸底考试化学试卷
湖南省衡阳市衡阳县第二中学2023-2024学年高三下学期开学摸底考试化学试卷(已下线)2023年普通高中学业水平选择性考试化学押题卷(四)(已下线)山东省枣庄市2022-2023学年高三下学期二模考试化学试题变式题(选择题1-5)(已下线)化学-2023年高考押题预测卷03(辽宁卷)(含考试版、全解全析、参考答案、答题卡)(已下线)专题05 化学实验基础-2023年高考化学真题题源解密(全国通用)福建省永春第一中学2023届高三下学期适应性考试(五)化学试题福建省莆田第二十五中学2023-2024学年高三上学期月考四化学试题福建省莆田五中2023-2024学年高二上学期第三次月考化学试卷
名校
解题方法
5 . 已知:反应反应2NH3(g) N2(g)+3H2(g) △H=+akJ•mol﹣1(a>0)。某兴趣小组在一定温度和催化剂的条件下,将1molNH3通入2L的密闭容器中进行反应(此时容器内总压强为200kPa),各物质的分压随时间的变化曲线如图所示。下列有关说法正确的是
N2(g)+3H2(g) △H=+akJ•mol﹣1(a>0)。某兴趣小组在一定温度和催化剂的条件下,将1molNH3通入2L的密闭容器中进行反应(此时容器内总压强为200kPa),各物质的分压随时间的变化曲线如图所示。下列有关说法正确的是

 N2(g)+3H2(g) △H=+akJ•mol﹣1(a>0)。某兴趣小组在一定温度和催化剂的条件下,将1molNH3通入2L的密闭容器中进行反应(此时容器内总压强为200kPa),各物质的分压随时间的变化曲线如图所示。下列有关说法正确的是
N2(g)+3H2(g) △H=+akJ•mol﹣1(a>0)。某兴趣小组在一定温度和催化剂的条件下,将1molNH3通入2L的密闭容器中进行反应(此时容器内总压强为200kPa),各物质的分压随时间的变化曲线如图所示。下列有关说法正确的是
A.若保持容器体积不变,0~t1min内,N2的平均反应速率为 mol•L﹣1•min﹣1 mol•L﹣1•min﹣1 |
| B.若保持容器体积不变,该温度下,当N2和H2的分压比保持不变时,表明反应已达平衡 |
| C.若保持容器体积不变,t1min时,反应放出0.2akJ的热量 |
| D.t2min时,将容器体积迅速缩小一半并保持不变,N2的分压变化如图中曲线b所示 |
您最近半年使用:0次
名校
6 . 向 容器中充入
容器中充入 和
和 ,发生反应
,发生反应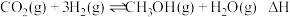 ,测得反应在不同压强、不同温度下,平衡混合物中
,测得反应在不同压强、不同温度下,平衡混合物中 体积分数如图Ⅰ所示,测得反应时逆反应速率与容器中
体积分数如图Ⅰ所示,测得反应时逆反应速率与容器中 关系如图Ⅱ所示。下列说法正确的是
关系如图Ⅱ所示。下列说法正确的是
 容器中充入
容器中充入 和
和 ,发生反应
,发生反应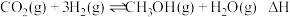 ,测得反应在不同压强、不同温度下,平衡混合物中
,测得反应在不同压强、不同温度下,平衡混合物中 体积分数如图Ⅰ所示,测得反应时逆反应速率与容器中
体积分数如图Ⅰ所示,测得反应时逆反应速率与容器中 关系如图Ⅱ所示。下列说法正确的是
关系如图Ⅱ所示。下列说法正确的是
A. |
B.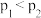 |
C.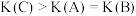 |
| D.图Ⅱ中当x点平衡体系升高至某一温度时,反应可重新达平衡状态,新平衡点可能是d |
您最近半年使用:0次
2023-02-11更新
|
953次组卷
|
5卷引用:湖南省部分学校2022-2023学年高三下学期开学考试化学试题
名校
7 . 利用CO生产甲醇的反应为2H2(g)+CO(g)=CH3OH(g),在密闭容器中按物质的量之比为2:1充入H2和CO,测得平衡混合物中CH3OH的体积分数在不同压强下随温度的变化情况如图所示。下列相关说法错误的是
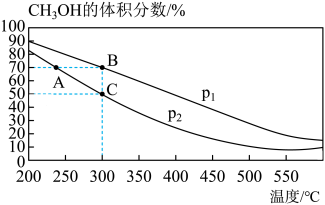

| A.该反应的△H<0,且P1>P2 |
| B.B点与C点的平衡常数关系为KB=KC |
C.C点对应的平衡常数Kp= |
| D.在恒温恒压条件下,平衡后再向容器中加入1molCH3OH(g),再达平衡时CH3OH(g)的转化率降低 |
您最近半年使用:0次
2022-12-08更新
|
433次组卷
|
5卷引用:湖南省岳阳县第一中学2022-2023学年高二下学期开学考试化学试题
8 . 一定温度下,在三个容积均为1.0 L的恒容密闭容器中仅发生反应:CH3OH(g)+CO(g) CH3COOH(g) △H<0。下列说法正确的是
CH3COOH(g) △H<0。下列说法正确的是
 CH3COOH(g) △H<0。下列说法正确的是
CH3COOH(g) △H<0。下列说法正确的是| 容器编号 | 温度/K | 物质的起始浓度/mol·L-1 | 物质的平衡浓度/mol·L-1 | ||
| c(CH3OH) | c(CO) | c(CH3COOH) | c(CH3COOH) | ||
| I | 530 | 0.50 | 0.50 | 0 | 0.40 |
| II | 530 | 0.20 | 0.20 | 0.40 | |
| III | 510 | 0 | 0 | 0.50 | |
| A.容器I中反应达到平衡所需时间比容器III中的长 |
| B.达到平衡时,容器I中的CH3OH体积分数比容器II中的小 |
| C.达平衡时,容器I中CH3OH转化率与容器III中CH3COOH转化率之和小于1 |
| D.若起始时向容器I中充入2.0 mol CH3OH(g)、0.10 mol CO(g)和8.0 mol CH3COOH(g),则反应将向逆反应方向进行 |
您最近半年使用:0次
名校
解题方法
9 . 一定条件下,CH4与H2O(g)发生反应:CH4(g)+H2O(g)  CO(g)+3H2(g),设起始n(H2O)/n(CH4)=Z,在恒压条件下,平衡时CH4的体积分数φ(CH4)与Z和温度T的关系如图所示,下列说法正确的是
CO(g)+3H2(g),设起始n(H2O)/n(CH4)=Z,在恒压条件下,平衡时CH4的体积分数φ(CH4)与Z和温度T的关系如图所示,下列说法正确的是

 CO(g)+3H2(g),设起始n(H2O)/n(CH4)=Z,在恒压条件下,平衡时CH4的体积分数φ(CH4)与Z和温度T的关系如图所示,下列说法正确的是
CO(g)+3H2(g),设起始n(H2O)/n(CH4)=Z,在恒压条件下,平衡时CH4的体积分数φ(CH4)与Z和温度T的关系如图所示,下列说法正确的是
| A.图中X点对应的平衡混合物中n(H2O)/n(CH4)=3 |
| B.图中Z的大小关系为a>3>b |
| C.该反应的焓变ΔH>0 |
| D.温度不变时,增大X点对应的平衡体系的压强后,φ(CH4)减小 |
您最近半年使用:0次
2022-08-28更新
|
504次组卷
|
5卷引用:湖南省长沙市南雅中学2020-2021学年度高二上学期入学考试化学试题
湖南省长沙市南雅中学2020-2021学年度高二上学期入学考试化学试题广东省广州真光中学2021-2022学年高二上学期12月月考化学试题(已下线)2.2.3 浓度、压强对化学平衡的影响-【帮课堂】2022-2023学年高二化学同步精品讲义(沪科版2020选择性必修第一册)(已下线)第10讲 影响化学平衡的因素(word讲义)-【帮课堂】2022-2023学年高二化学同步精品讲义(人教2019选择性必修1)广东省广州市真光中学2022-2023学年高二上学期期中考试化学试题
名校
10 . 下列实验事实不能 用勒夏特列原理解释的是
| A.打开啤酒瓶盖,喷出大量泡沫 |
| B.新制的氯水在光照下颜色逐渐变浅 |
| C.实验室用排饱和食盐水而不用排水法收集氯气 |
| D.H2、I2、HI平衡混合气加压后颜色变深 |
您最近半年使用:0次
2022-02-28更新
|
129次组卷
|
3卷引用:湖南省常德市汉寿县第一中学2023-2024学年高二下学期开学化学试题



