名校
解题方法
1 . 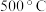 ,将
,将 和
和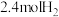 充入体积为
充入体积为 的已装有催化剂的恒容密闭容器中发生合成氨反应
的已装有催化剂的恒容密闭容器中发生合成氨反应 ,“此反应放热,下列说法正确的是
,“此反应放热,下列说法正确的是
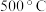 ,将
,将 和
和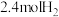 充入体积为
充入体积为 的已装有催化剂的恒容密闭容器中发生合成氨反应
的已装有催化剂的恒容密闭容器中发生合成氨反应 ,“此反应放热,下列说法正确的是
,“此反应放热,下列说法正确的是A.平衡时, 的浓度可能为 的浓度可能为 |
| B.容器内气体的密度不再随时间改变说明该反应已达到平衡状态 |
C.若已知生成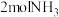 放出 放出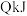 的热量,则该反应达平衡时放出的热量小于 的热量,则该反应达平衡时放出的热量小于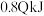 |
D.反应平衡后,向容器中充入一定体积的氨气,使容器中气体总压强增大,则 、 、 均增大 均增大 |
您最近半年使用:0次
解题方法
2 .  通过不同方式转化为高附加值化学品有利于实现“双碳目标”,其中
通过不同方式转化为高附加值化学品有利于实现“双碳目标”,其中 加氢转化为二甲醚(
加氢转化为二甲醚( )是常见的一种方式,其反应过程如下:
)是常见的一种方式,其反应过程如下:
Ⅰ.
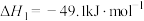
Ⅱ.

Ⅲ.
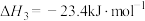
回答下列问题:
(1) 加氢制
加氢制 反应的热化学方程式为
反应的热化学方程式为___________ 。
(2)进料比 时,不同压强下
时,不同压强下 平衡转化率随温度的变化关系如图所示。①四条曲线对应压强
平衡转化率随温度的变化关系如图所示。①四条曲线对应压强 、
、 、
、 和
和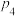 由大到小的顺序为
由大到小的顺序为___________ ,判断依据是___________ 。②压强为 时,
时, 平衡转化率随温度升高先减小后增大,原因是
平衡转化率随温度升高先减小后增大,原因是___________ 。___________ 。
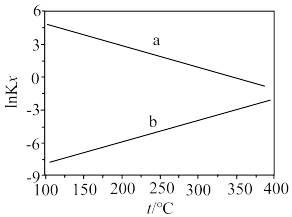
(4)反应Ⅱ和反应Ⅲ的平衡常数(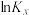 )随温度变化关系如图2所示,表示反应Ⅱ的曲线为
)随温度变化关系如图2所示,表示反应Ⅱ的曲线为___________ (填“a”或“b”)。恒温恒压条件下,向体系中通入 和
和 ,达到平衡时
,达到平衡时 转化率为50%,
转化率为50%, 为0.07mol,该条件下生成的CO可以忽略不计,则
为0.07mol,该条件下生成的CO可以忽略不计,则 的物质的量为
的物质的量为___________ mol, 加氢制
加氢制 的反应用摩尔分数表示的平衡常数
的反应用摩尔分数表示的平衡常数
___________ (列出计算式)。(已知反应 的
的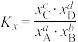 ,物质i的摩尔分数
,物质i的摩尔分数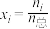 。)
。)
 通过不同方式转化为高附加值化学品有利于实现“双碳目标”,其中
通过不同方式转化为高附加值化学品有利于实现“双碳目标”,其中 加氢转化为二甲醚(
加氢转化为二甲醚( )是常见的一种方式,其反应过程如下:
)是常见的一种方式,其反应过程如下:Ⅰ.

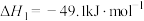
Ⅱ.


Ⅲ.

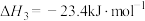
回答下列问题:
(1)
 加氢制
加氢制 反应的热化学方程式为
反应的热化学方程式为(2)进料比
 时,不同压强下
时,不同压强下 平衡转化率随温度的变化关系如图所示。①四条曲线对应压强
平衡转化率随温度的变化关系如图所示。①四条曲线对应压强 、
、 、
、 和
和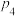 由大到小的顺序为
由大到小的顺序为 时,
时, 平衡转化率随温度升高先减小后增大,原因是
平衡转化率随温度升高先减小后增大,原因是
(4)反应Ⅱ和反应Ⅲ的平衡常数(
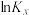 )随温度变化关系如图2所示,表示反应Ⅱ的曲线为
)随温度变化关系如图2所示,表示反应Ⅱ的曲线为 和
和 ,达到平衡时
,达到平衡时 转化率为50%,
转化率为50%, 为0.07mol,该条件下生成的CO可以忽略不计,则
为0.07mol,该条件下生成的CO可以忽略不计,则 的物质的量为
的物质的量为 加氢制
加氢制 的反应用摩尔分数表示的平衡常数
的反应用摩尔分数表示的平衡常数
 的
的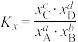 ,物质i的摩尔分数
,物质i的摩尔分数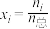 。)
。)
您最近半年使用:0次
昨日更新
|
367次组卷
|
3卷引用:河南省周口市2024届高三二模理综-化学试题
3 . 一定条件下,银催化剂表面上存在反应: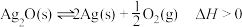 ,起始状态Ⅰ中有
,起始状态Ⅰ中有 、
、 和
和 ,经下列过程达到各平衡状态(已知状态Ⅰ和Ⅲ的固体质量相等),下列叙述正确的是
,经下列过程达到各平衡状态(已知状态Ⅰ和Ⅲ的固体质量相等),下列叙述正确的是

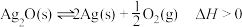 ,起始状态Ⅰ中有
,起始状态Ⅰ中有 、
、 和
和 ,经下列过程达到各平衡状态(已知状态Ⅰ和Ⅲ的固体质量相等),下列叙述正确的是
,经下列过程达到各平衡状态(已知状态Ⅰ和Ⅲ的固体质量相等),下列叙述正确的是
A.从Ⅰ到Ⅱ的过程 |
B.反应的平衡压强: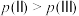 |
C.平衡常数: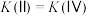 |
D.若体积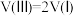 ,则 ,则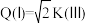 |
您最近半年使用:0次
解题方法
4 . 将0.40molN2O4气体充入2L固定容积的密闭容器中发生如下反应: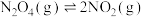
 。在温度为T3、T4时,平衡体系中NO2的体积分数随压强变化的曲线如图所示。下列说法正确的是
。在温度为T3、T4时,平衡体系中NO2的体积分数随压强变化的曲线如图所示。下列说法正确的是

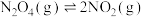
 。在温度为T3、T4时,平衡体系中NO2的体积分数随压强变化的曲线如图所示。下列说法正确的是
。在温度为T3、T4时,平衡体系中NO2的体积分数随压强变化的曲线如图所示。下列说法正确的是
| A.a、c两点的反应速率:a>c | B.a、b两点N2O4的转化率:a>b |
| C.a、c两点气体的颜色:a浅,c深 | D.由a点到b点,可以用加热的方法 |
您最近半年使用:0次
解题方法
5 . 已知: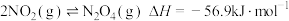 ,反应速率表达式为
,反应速率表达式为
 是反应速率常数,只与温度有关)。下列说法正确的是
是反应速率常数,只与温度有关)。下列说法正确的是
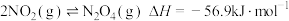 ,反应速率表达式为
,反应速率表达式为
 是反应速率常数,只与温度有关)。下列说法正确的是
是反应速率常数,只与温度有关)。下列说法正确的是| A.达到平衡后,充入NO2,v正增大,v逆减小 |
| B.达到平衡后,加入催化剂,v正和v逆都增大 |
| C.达到平衡后,升高温度,k正增大、k逆减小 |
| D.若恒温恒压条件下充入NO,则平衡不移动 |
您最近半年使用:0次
6 . 温度为T℃,向体积不等的恒容密闭容器中分别加入足量活性炭和1molNO2,发生反应:2C(s)+2NO2(g) N2(g)+2CO2(g)。反应相同时间后,测得各容器中NO2的转化率与容器体积的关系如图所示,下列说法正确的是
N2(g)+2CO2(g)。反应相同时间后,测得各容器中NO2的转化率与容器体积的关系如图所示,下列说法正确的是
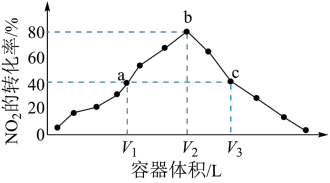
 N2(g)+2CO2(g)。反应相同时间后,测得各容器中NO2的转化率与容器体积的关系如图所示,下列说法正确的是
N2(g)+2CO2(g)。反应相同时间后,测得各容器中NO2的转化率与容器体积的关系如图所示,下列说法正确的是
| A.T℃时,a、b两点平衡常数Ka<Kb |
B.图中c点所示条件下, (正)= (正)= (逆) (逆) |
| C.容器内的压强:Pa∶Pb>6∶7 |
| D.图中b点所示条件下,再向体系中充入一定量的NO2,达到平衡时,NO2的转化率比原平衡大 |
您最近半年使用:0次
2024-02-21更新
|
85次组卷
|
6卷引用:河南省焦作市博爱县第一中学2023-2024学年高二上学期10月月考化学试题
名校
7 . 一定温度下,将1molA(g)和1molB(g)充入2L密闭容器中发生反应:A(g)+B(g) xC(g)+D(s) ΔH<0在t1时达到平衡。在t2、t3时刻分别改变反应的一个条件,测得容器中C(g)的浓度随时间变化如图所示。下列有关说法正确的是
xC(g)+D(s) ΔH<0在t1时达到平衡。在t2、t3时刻分别改变反应的一个条件,测得容器中C(g)的浓度随时间变化如图所示。下列有关说法正确的是

 xC(g)+D(s) ΔH<0在t1时达到平衡。在t2、t3时刻分别改变反应的一个条件,测得容器中C(g)的浓度随时间变化如图所示。下列有关说法正确的是
xC(g)+D(s) ΔH<0在t1时达到平衡。在t2、t3时刻分别改变反应的一个条件,测得容器中C(g)的浓度随时间变化如图所示。下列有关说法正确的是
| A.x=1 |
| B.t2时刻改变的条件是使用催化剂 |
| C.t3时刻改变的条件是增大反应物的浓度或降温 |
| D.t1~t2、t2~t3平衡常数相等,且K=4 |
您最近半年使用:0次
名校
8 .  催化加氢可合成二甲醚,发生的主要反应有:
催化加氢可合成二甲醚,发生的主要反应有:
反应I:
反应II: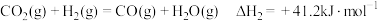
向恒压的容器中充入 和
和 ,若仅考虑上述反应,平衡时
,若仅考虑上述反应,平衡时 和
和 的选择性及
的选择性及 的转化率随温度的变化如图中实线所示。
的转化率随温度的变化如图中实线所示。 的选择性
的选择性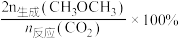 。
。
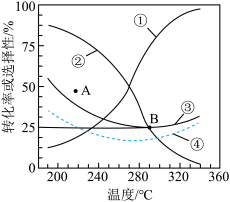
(1)图中曲线___________ 表示平衡时 的选择性,在
的选择性,在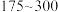 ℃范围内,随着温度的升高,平衡时
℃范围内,随着温度的升高,平衡时 的选择性变化的原因是
的选择性变化的原因是___________ 。
(2)平衡时 的转化率随温度的变化
的转化率随温度的变化___________ (填“可能”或“不可能”)如图中虚线④所示。若达到平衡后,再充入 和
和 ,重新达到平衡时
,重新达到平衡时 的体积分数
的体积分数___________ (填“增大”“减小”或“不变”)。
(3)①220℃时,在催化剂作用下 与
与 反应一段时间后,测得
反应一段时间后,测得 的选择性为
的选择性为 (图中A点)。不改变反应时间和温度,一定能提高
(图中A点)。不改变反应时间和温度,一定能提高 选择性的措施有
选择性的措施有___________ (答一点即可)。反应状态达B点时,容器中 为
为___________ mol(用最简分数表示)。
②关于合成二甲醚工艺的理解,下列说法正确的是___________
A.合成二甲醚的反应在A点和B点时的化学平衡常数 (A)小于
(A)小于 (B)
(B)
B.当温度、压强一定时,在原料气(比例不变)中添加少量情性气体,有利于提高平衡转化率
C.其他条件不变,改为恒容条件,CO平衡选择性比恒压条件下的平衡选择性高
D.由图像可知,CO2加氢合成二甲醚应该使用较低温下具有良好活性的催化剂
(4)经实践,合成甲醚的适宜温度为260℃,原因是___________ 。
 催化加氢可合成二甲醚,发生的主要反应有:
催化加氢可合成二甲醚,发生的主要反应有:反应I:

反应II:
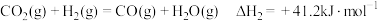
向恒压的容器中充入
 和
和 ,若仅考虑上述反应,平衡时
,若仅考虑上述反应,平衡时 和
和 的选择性及
的选择性及 的转化率随温度的变化如图中实线所示。
的转化率随温度的变化如图中实线所示。 的选择性
的选择性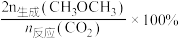 。
。
(1)图中曲线
 的选择性,在
的选择性,在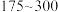 ℃范围内,随着温度的升高,平衡时
℃范围内,随着温度的升高,平衡时 的选择性变化的原因是
的选择性变化的原因是(2)平衡时
 的转化率随温度的变化
的转化率随温度的变化 和
和 ,重新达到平衡时
,重新达到平衡时 的体积分数
的体积分数(3)①220℃时,在催化剂作用下
 与
与 反应一段时间后,测得
反应一段时间后,测得 的选择性为
的选择性为 (图中A点)。不改变反应时间和温度,一定能提高
(图中A点)。不改变反应时间和温度,一定能提高 选择性的措施有
选择性的措施有 为
为②关于合成二甲醚工艺的理解,下列说法正确的是
A.合成二甲醚的反应在A点和B点时的化学平衡常数
 (A)小于
(A)小于 (B)
(B)B.当温度、压强一定时,在原料气(比例不变)中添加少量情性气体,有利于提高平衡转化率
C.其他条件不变,改为恒容条件,CO平衡选择性比恒压条件下的平衡选择性高
D.由图像可知,CO2加氢合成二甲醚应该使用较低温下具有良好活性的催化剂
(4)经实践,合成甲醚的适宜温度为260℃,原因是
您最近半年使用:0次
名校
9 . 合成氨反应为:N2(g)+3H2(g)  2NH3(g) ΔH= -92.4kJ·mol-1,下列说法正确的是
2NH3(g) ΔH= -92.4kJ·mol-1,下列说法正确的是
 2NH3(g) ΔH= -92.4kJ·mol-1,下列说法正确的是
2NH3(g) ΔH= -92.4kJ·mol-1,下列说法正确的是| A.合成氨反应在任何温度下都能自发 | B.将混合气体进行循环利用符合绿色化学思想 |
| C.合成氨实际生产中选择高压和低温 | D.将氨液化分离,可促进平衡正移,加快反应速率 |
您最近半年使用:0次
名校
10 . Ⅰ.甲醇是一种重要的化工原料,具有开发和应用的广阔前景。工业上使用水煤气(CO与H2的混合气体)转化成甲醇,反应为CO(g)+2H2(g) CH3OH(g)。CO的平衡转化率与温度、压强的关系如图所示。
CH3OH(g)。CO的平衡转化率与温度、压强的关系如图所示。
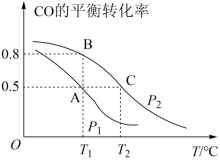
(1)在T2℃、p2压强时,往一容积为2L的密闭容器内,充入0.3molCO与0.4molH2发生反应。平衡时H2的体积分数是___________ ;平衡常数K=___________ 。平衡后再加入1.0molCO后重新到达平衡,则CO的转化率___________ (填“增大”、“不变”成“减小”),CO与CH3OH的浓度比
___________ (填“增大”、“不变”或“减小”)。
(2)若以不同比例投料,测得某时刻各物质的物质的量如下,CO:0.1mol、H2:0.2mol、CH3OH:0.2mol,此时v(正)___________ v(逆)(填“>”、“<”或“=”)。
(3)若p2压强恒定为p,则平衡常数Kp=___________ (Kp用气体平衡分压代替气体平衡浓度计算,分压=总压×气体的物质的量分数,整理出含p的最简表达式)。
Ⅱ.在真空1L密闭容器内加入amolPH4I固体,在一定温度下发生如下反应:
①PH4I(s) PH3(g)+HI(g)
PH3(g)+HI(g)
②4PH3(g) P4(g)+6H2(g)
P4(g)+6H2(g)
③2HI(g) H2(g)+I2(g)
H2(g)+I2(g)
以上三个反应建立平衡后,测得HI为bmol,I2为cmol,H2为dmol。
(4)平衡后,增大压强,容器内n(I2)将___________ (填“增加”、“减小”或“不变”)。
(5)平衡后容器内P4(g)的物质的量___________ 。
(6)求反应①的K___________ 。
 CH3OH(g)。CO的平衡转化率与温度、压强的关系如图所示。
CH3OH(g)。CO的平衡转化率与温度、压强的关系如图所示。
(1)在T2℃、p2压强时,往一容积为2L的密闭容器内,充入0.3molCO与0.4molH2发生反应。平衡时H2的体积分数是

(2)若以不同比例投料,测得某时刻各物质的物质的量如下,CO:0.1mol、H2:0.2mol、CH3OH:0.2mol,此时v(正)
(3)若p2压强恒定为p,则平衡常数Kp=
Ⅱ.在真空1L密闭容器内加入amolPH4I固体,在一定温度下发生如下反应:
①PH4I(s)
 PH3(g)+HI(g)
PH3(g)+HI(g) ②4PH3(g)
 P4(g)+6H2(g)
P4(g)+6H2(g) ③2HI(g)
 H2(g)+I2(g)
H2(g)+I2(g)以上三个反应建立平衡后,测得HI为bmol,I2为cmol,H2为dmol。
(4)平衡后,增大压强,容器内n(I2)将
(5)平衡后容器内P4(g)的物质的量
(6)求反应①的K
您最近半年使用:0次



