Ⅰ.甲醇是一种重要的化工原料,具有开发和应用的广阔前景。工业上使用水煤气(CO与H2的混合气体)转化成甲醇,反应为CO(g)+2H2(g) CH3OH(g)。CO的平衡转化率与温度、压强的关系如图所示。
CH3OH(g)。CO的平衡转化率与温度、压强的关系如图所示。
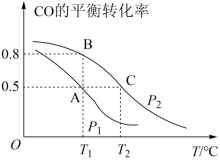
(1)在T2℃、p2压强时,往一容积为2L的密闭容器内,充入0.3molCO与0.4molH2发生反应。平衡时H2的体积分数是___________ ;平衡常数K=___________ 。平衡后再加入1.0molCO后重新到达平衡,则CO的转化率___________ (填“增大”、“不变”成“减小”),CO与CH3OH的浓度比
___________ (填“增大”、“不变”或“减小”)。
(2)若以不同比例投料,测得某时刻各物质的物质的量如下,CO:0.1mol、H2:0.2mol、CH3OH:0.2mol,此时v(正)___________ v(逆)(填“>”、“<”或“=”)。
(3)若p2压强恒定为p,则平衡常数Kp=___________ (Kp用气体平衡分压代替气体平衡浓度计算,分压=总压×气体的物质的量分数,整理出含p的最简表达式)。
Ⅱ.在真空1L密闭容器内加入amolPH4I固体,在一定温度下发生如下反应:
①PH4I(s) PH3(g)+HI(g)
PH3(g)+HI(g)
②4PH3(g) P4(g)+6H2(g)
P4(g)+6H2(g)
③2HI(g) H2(g)+I2(g)
H2(g)+I2(g)
以上三个反应建立平衡后,测得HI为bmol,I2为cmol,H2为dmol。
(4)平衡后,增大压强,容器内n(I2)将___________ (填“增加”、“减小”或“不变”)。
(5)平衡后容器内P4(g)的物质的量___________ 。
(6)求反应①的K___________ 。
 CH3OH(g)。CO的平衡转化率与温度、压强的关系如图所示。
CH3OH(g)。CO的平衡转化率与温度、压强的关系如图所示。
(1)在T2℃、p2压强时,往一容积为2L的密闭容器内,充入0.3molCO与0.4molH2发生反应。平衡时H2的体积分数是

(2)若以不同比例投料,测得某时刻各物质的物质的量如下,CO:0.1mol、H2:0.2mol、CH3OH:0.2mol,此时v(正)
(3)若p2压强恒定为p,则平衡常数Kp=
Ⅱ.在真空1L密闭容器内加入amolPH4I固体,在一定温度下发生如下反应:
①PH4I(s)
 PH3(g)+HI(g)
PH3(g)+HI(g) ②4PH3(g)
 P4(g)+6H2(g)
P4(g)+6H2(g) ③2HI(g)
 H2(g)+I2(g)
H2(g)+I2(g)以上三个反应建立平衡后,测得HI为bmol,I2为cmol,H2为dmol。
(4)平衡后,增大压强,容器内n(I2)将
(5)平衡后容器内P4(g)的物质的量
(6)求反应①的K
更新时间:2024-02-12 18:01:18
|
相似题推荐
【推荐1】降低大气中CO2的含量及有效地开发利用CO2,已引起了全世界的普遍重视
(1)CO2加氢合成DME(二甲醚)是解决能源危机的研究方向之一。
①2CO2(g) + 6H2(g) CH3OCH3(g) + 3H2O(g) △H= -122.4kJ·mol-1
CH3OCH3(g) + 3H2O(g) △H= -122.4kJ·mol-1
某温度下,将2.0 mol CO2(g) 和6.0 mol H2(g)充入容积为2 L的密闭容器中,反应到达平衡时,改变压强和温度,平衡体系中 CH3OCH3(g) 的物质分数变化情况如图所示,则P1_______ P2(填“>”“<”或“=”,下同)。若T1、P1,T3、P3时平衡常数分别为K1、K3,则K1________ K3,T1、P1时H2的平衡转化率为______________ 。
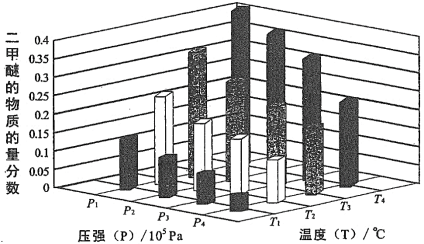
②在恒容密闭容器里按体积比为1∶3充入二氧化碳和氢气,一定条件下反应达到平衡状态。当改变反应的某一个条件后,下列能说明平衡一定向逆反应方向移动的是______ (填序号)。
A.反应物的浓度增大 B.混合气体的密度减小
C.正反应速率小于逆反应速率 D.氢气的转化率减小
(2)将一定量的CO2气体通入氢氧化钠的溶液中,向所得溶液中边滴加稀盐酸边振荡至过量、产生的气体与加入盐酸物质的量的关系如图(忽略气体的溶解和HCl的挥发)。请回答:当加入HCl 的物质的量为1 mol时,溶液中所含溶质的化学式__________ ,a点溶液中各离子浓度由大到小的关系式为____________________________________ 。
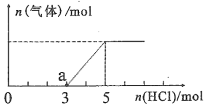
(3)CO2在自然界循环时可与CaCO3反应,CaCO3是一种难溶物质,其Ksp = 2.8×10-9。CaCl2溶液与Na2CO3溶液混合可形成CaCO3沉淀,现将等体积的CaCl2溶液与Na2CO3溶液混合,若混合前Na2CO3溶液的浓度为2×10-4 mol·L-1,则生成沉淀加入CaCl2溶液的最小浓度为___________ mol·L-1。
(1)CO2加氢合成DME(二甲醚)是解决能源危机的研究方向之一。
①2CO2(g) + 6H2(g)
 CH3OCH3(g) + 3H2O(g) △H= -122.4kJ·mol-1
CH3OCH3(g) + 3H2O(g) △H= -122.4kJ·mol-1某温度下,将2.0 mol CO2(g) 和6.0 mol H2(g)充入容积为2 L的密闭容器中,反应到达平衡时,改变压强和温度,平衡体系中 CH3OCH3(g) 的物质分数变化情况如图所示,则P1

②在恒容密闭容器里按体积比为1∶3充入二氧化碳和氢气,一定条件下反应达到平衡状态。当改变反应的某一个条件后,下列能说明平衡一定向逆反应方向移动的是
A.反应物的浓度增大 B.混合气体的密度减小
C.正反应速率小于逆反应速率 D.氢气的转化率减小
(2)将一定量的CO2气体通入氢氧化钠的溶液中,向所得溶液中边滴加稀盐酸边振荡至过量、产生的气体与加入盐酸物质的量的关系如图(忽略气体的溶解和HCl的挥发)。请回答:当加入HCl 的物质的量为1 mol时,溶液中所含溶质的化学式

(3)CO2在自然界循环时可与CaCO3反应,CaCO3是一种难溶物质,其Ksp = 2.8×10-9。CaCl2溶液与Na2CO3溶液混合可形成CaCO3沉淀,现将等体积的CaCl2溶液与Na2CO3溶液混合,若混合前Na2CO3溶液的浓度为2×10-4 mol·L-1,则生成沉淀加入CaCl2溶液的最小浓度为
您最近半年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】氮化铝(AlN)广泛应用于集成电路,其制备原理是将氧化铝与碳粉混合均匀,在持续流动的氮气流中加热至1750℃,发生如下反应:
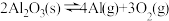
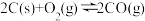
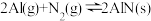
(1)断开N2分子内的共价键要_____ 热量(填“吸收”或“放出”)
(2)分析反应②对①、③平衡移动的影响_____ 。
(3)Al2O3、C、N2合成AlN的平衡常数表达式K=___________ 。
(4)用蒸馏法测定产品中AlN的含量,装置如下(加热及夹持装置略):
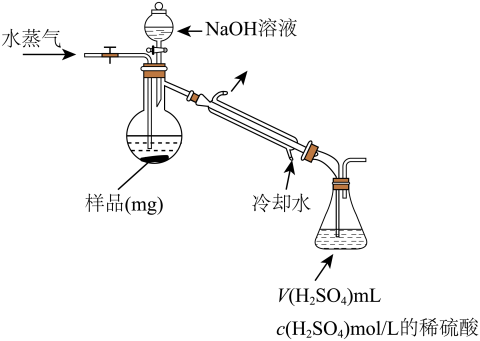
①AlN与NaOH溶液反应产生NH3的化学方程式是____________ 。
②锥形瓶内吸收NH3的离子方程式是____________ 。
③检验NH3是否完全蒸出的方法是:另取少量蒸馏出的溶液,_____ (将检验过程补充完整)。
④NH3完全吸收后,向锥形瓶中加入指示剂,用浓度为c((N aOH)mol/L的NaOH标准溶液滴定过量的H2SO4,终点时用去标准溶液的体积为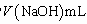 。下面有关计算正确的是
。下面有关计算正确的是_____ 。A.样品中AlN的质量: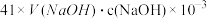
B.AlN的质量分数:
C.锥形瓶吸收NH3的物质的量: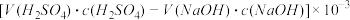
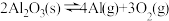
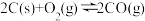
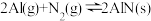
(1)断开N2分子内的共价键要
(2)分析反应②对①、③平衡移动的影响
(3)Al2O3、C、N2合成AlN的平衡常数表达式K=
(4)用蒸馏法测定产品中AlN的含量,装置如下(加热及夹持装置略):

①AlN与NaOH溶液反应产生NH3的化学方程式是
②锥形瓶内吸收NH3的离子方程式是
③检验NH3是否完全蒸出的方法是:另取少量蒸馏出的溶液,
④NH3完全吸收后,向锥形瓶中加入指示剂,用浓度为c((N aOH)mol/L的NaOH标准溶液滴定过量的H2SO4,终点时用去标准溶液的体积为
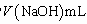 。下面有关计算正确的是
。下面有关计算正确的是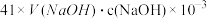
B.AlN的质量分数:

C.锥形瓶吸收NH3的物质的量:
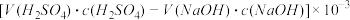
您最近半年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐3】重铬酸铵[(NH4)2Cr2O7]用作分析试剂、催化剂及媒染剂等。某化学兴趣小组对重铬酸铵的一些性质及组成进行探究。已知: (橙色)
(橙色) (黄色)
(黄色) 。回答下列问题:
。回答下列问题:
(1)在试管中加入少量重铬酸铵样品,滴加足量6 mol/LNaOH溶液,振荡、微热。产生的现象是_______ ,写出该反应的化学方程式:_______ 。
(2)为探究重铬酸铵的分解产物,按下图连接好装置,在A中加入2.520 g重铬酸铵样品进行实验。
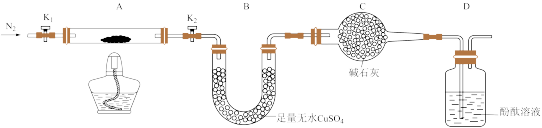
①实验过程中通入N2的主要目的是_______ 。
②加热A至恒重,观察到B中固体由白变蓝,D中酚酞溶液不变色,同时测得A、B中质量变化分别为1.00 g、0.720 g,则重铬酸铵受热分解的化学方程式为_______ 。
(3)实验室常利用甲醛法测定重铬酸铵样品中氮的质量分数,其反应原理为2Ba2++ +H2O=2BaCrO4↓+2H+,4
+H2O=2BaCrO4↓+2H+,4 +6HCHO=3H++6H2O+(CH2)6N4H+,滴定时1 mol(CH2)6N4H+与1 mol H+相当],然后用NaOH标准溶液滴定反应生成的酸。(不考虑甲醛与硝酸的反应)
+6HCHO=3H++6H2O+(CH2)6N4H+,滴定时1 mol(CH2)6N4H+与1 mol H+相当],然后用NaOH标准溶液滴定反应生成的酸。(不考虑甲醛与硝酸的反应)
实验步骤:称取样品2.600 g,配成250 mL溶液,移取25.00 mL样品溶液于锥形瓶中,加入硝酸钡溶液使 完全沉淀后,加入10 mL 20%的中性甲醛溶液,摇匀,静置5 min后,加入1~2滴酚酞溶液,用0.200 mol/LNaOH标准溶液滴定至终点,重复上述操作3次。
完全沉淀后,加入10 mL 20%的中性甲醛溶液,摇匀,静置5 min后,加入1~2滴酚酞溶液,用0.200 mol/LNaOH标准溶液滴定至终点,重复上述操作3次。
①碱式滳定管用蒸馏水洗涤后,直接加入NaOH标准溶液进行滴定,则测得样品中氮的质量分数_______ (填“偏大”“偏小”或“无影响”);滴定时边滴边摇动锥形㼛,眼睛应观察_______ 。
②滳定结果如下表所示:
该样品中氮的质量分数为_______ (结果保留两位小数)。
 (橙色)
(橙色) (黄色)
(黄色) 。回答下列问题:
。回答下列问题:(1)在试管中加入少量重铬酸铵样品,滴加足量6 mol/LNaOH溶液,振荡、微热。产生的现象是
(2)为探究重铬酸铵的分解产物,按下图连接好装置,在A中加入2.520 g重铬酸铵样品进行实验。

①实验过程中通入N2的主要目的是
②加热A至恒重,观察到B中固体由白变蓝,D中酚酞溶液不变色,同时测得A、B中质量变化分别为1.00 g、0.720 g,则重铬酸铵受热分解的化学方程式为
(3)实验室常利用甲醛法测定重铬酸铵样品中氮的质量分数,其反应原理为2Ba2++
 +H2O=2BaCrO4↓+2H+,4
+H2O=2BaCrO4↓+2H+,4 +6HCHO=3H++6H2O+(CH2)6N4H+,滴定时1 mol(CH2)6N4H+与1 mol H+相当],然后用NaOH标准溶液滴定反应生成的酸。(不考虑甲醛与硝酸的反应)
+6HCHO=3H++6H2O+(CH2)6N4H+,滴定时1 mol(CH2)6N4H+与1 mol H+相当],然后用NaOH标准溶液滴定反应生成的酸。(不考虑甲醛与硝酸的反应)实验步骤:称取样品2.600 g,配成250 mL溶液,移取25.00 mL样品溶液于锥形瓶中,加入硝酸钡溶液使
 完全沉淀后,加入10 mL 20%的中性甲醛溶液,摇匀,静置5 min后,加入1~2滴酚酞溶液,用0.200 mol/LNaOH标准溶液滴定至终点,重复上述操作3次。
完全沉淀后,加入10 mL 20%的中性甲醛溶液,摇匀,静置5 min后,加入1~2滴酚酞溶液,用0.200 mol/LNaOH标准溶液滴定至终点,重复上述操作3次。①碱式滳定管用蒸馏水洗涤后,直接加入NaOH标准溶液进行滴定,则测得样品中氮的质量分数
②滳定结果如下表所示:
| 滴定次数 | 待测溶液的体积/mL | 标准溶液的体积 | |
| 滴定前刻度/mL | 滴定后刻度/mL | ||
| 1 | 25.00 | 1.05 | 21.06 |
| 2 | 25.00 | 1.98 | 21.97 |
| 3 | 25.00 | 0.20 | 21.20 |
| 4 | 25.00 | 0.45 | 20.45 |
您最近半年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐1】开发清洁能源是当今化工研究的一个热点问题。二甲醚(CH3OCH3)在未来可能替代柴油和液化气作为洁净液体燃料使用,工业上以CO和H2为原料生产CH3OCH3。工业制备二甲醚在催化反应室中(压力2.0~10.0Mpa,温度230~280℃)进行下列反应:
①CO(g)+2H2(g)⇌CH3OH(g) ΔH1=-99kJ·mol−1
②2CH3OH(g)⇌CH3OCH3(g)+H2O(g) ΔH2=-23.5kJ·mol−1
③CO(g)+H2O(g)⇌CO2(g)+H2(g) ΔH3=-41.2kJ·mol−1
(1)催化反应室中的总反应3CO(g)+3H2(g)⇌CH3OCH3(g)+CO2(g),计算ΔH=_______ 。反应来自煤的气化。已知该反应的平衡常数表达式为K=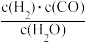 ,每生成1mol H2需要吸收131.3kJ的热量。写出该反应的热化学方程式
,每生成1mol H2需要吸收131.3kJ的热量。写出该反应的热化学方程式____________ 。
(2)在该条件下,若反应①的起始浓度分别为:c(CO)=0.6mol·L−1,c(H2)=1.4mol·L−1,8min后达到平衡,CO的转化率为50%,则8min内H2的平均反应速率为__________ 。
(3)在t℃时,反应②的平衡常数为400,此温度下,在1L的密闭容器中加入一定的甲醇,反应到某时刻测得各组分的物质的量浓度如下:
此时刻v正___ v逆(填“>”“<”或“=”),平衡时c(CH3OCH3)的物质的量浓度是___ 。
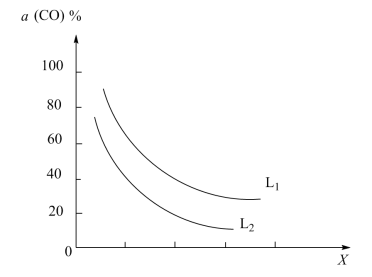
(4)在(1)小题中催化反应室的总反应3CO(g)+3H2(g)⇌CH3OCH3(g)+CO2(g),CO的平衡转化率a(CO)与温度、压强的关系如图所示,图中X代表___ (填“温度”或“压强”),且L1___ L2(填“>”“<”或“=”)。
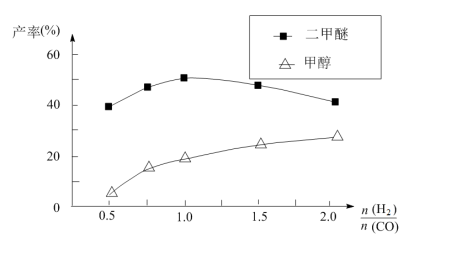
(5)在催化剂的作用下同时进行三个反应,发现随着起始投料比 的改变,二甲醚和甲醇的产率(产物中的碳原子占起始CO中碳原子的百分率)呈现如图的变化趋势。试解释投料比大于1.0之后二甲醚产率和甲醇产率变化的原因:
的改变,二甲醚和甲醇的产率(产物中的碳原子占起始CO中碳原子的百分率)呈现如图的变化趋势。试解释投料比大于1.0之后二甲醚产率和甲醇产率变化的原因:_____ 。
①CO(g)+2H2(g)⇌CH3OH(g) ΔH1=-99kJ·mol−1
②2CH3OH(g)⇌CH3OCH3(g)+H2O(g) ΔH2=-23.5kJ·mol−1
③CO(g)+H2O(g)⇌CO2(g)+H2(g) ΔH3=-41.2kJ·mol−1
(1)催化反应室中的总反应3CO(g)+3H2(g)⇌CH3OCH3(g)+CO2(g),计算ΔH=
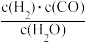 ,每生成1mol H2需要吸收131.3kJ的热量。写出该反应的热化学方程式
,每生成1mol H2需要吸收131.3kJ的热量。写出该反应的热化学方程式(2)在该条件下,若反应①的起始浓度分别为:c(CO)=0.6mol·L−1,c(H2)=1.4mol·L−1,8min后达到平衡,CO的转化率为50%,则8min内H2的平均反应速率为
(3)在t℃时,反应②的平衡常数为400,此温度下,在1L的密闭容器中加入一定的甲醇,反应到某时刻测得各组分的物质的量浓度如下:
| 物质 | CH3OH | CH3OCH3 | H2O |
| c(mol·L−1) | 0.46 | 1.0 | 1.0 |
(4)在(1)小题中催化反应室的总反应3CO(g)+3H2(g)⇌CH3OCH3(g)+CO2(g),CO的平衡转化率a(CO)与温度、压强的关系如图所示,图中X代表

(5)在催化剂的作用下同时进行三个反应,发现随着起始投料比
 的改变,二甲醚和甲醇的产率(产物中的碳原子占起始CO中碳原子的百分率)呈现如图的变化趋势。试解释投料比大于1.0之后二甲醚产率和甲醇产率变化的原因:
的改变,二甲醚和甲醇的产率(产物中的碳原子占起始CO中碳原子的百分率)呈现如图的变化趋势。试解释投料比大于1.0之后二甲醚产率和甲醇产率变化的原因:
您最近半年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐2】合成氨工业对国民经济和社会发展具有重要的意义。其原理为:N2(g)+3H2(g) 2NH3(g)△H,据此回答以下问题:
2NH3(g)△H,据此回答以下问题:
(1)已知每破坏l mol有关化学键需要的能量如下表:
则△H=_______________ 。
(2)在不同温度、压强和相同催化剂条件下,初始时N2、H2分别为0.1mol、0.3mol时,平衡后混合物中氨的体积分数(p)如图所示:
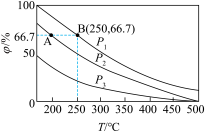
①其中,p1、p2和p3由大到小的顺序是________ ,其原因是__________ 。
②若分别用vA(N2)和vB(N2)表示从反应开始至达平衡状态A、B时的化学反应速率,则vA(N2)___________ vB(N2) (填“>”、“<"或”“=")。
③若在250℃、pl条件下,反应达到平衡时容器的体积为1 L,则该条件下合成氨的平衡常数K=_________ (列出计算式即可)。
(3)合成氨反应在催化剂作用下的反应历程为(*表示吸附态):
第一步N2(g) →2N*;H2(g)一2H* (慢反应)
第二步N*+H*= NH*;NH*+H*= NH2*;NH2*+H*= NH3* (快反应)
第三步NH3*= NH3(g) (快反应)
比较第一步反应的活化能E1与第二步反应的活化能E2的大小:E1_______ E2(填“>”“<"或“=")。
(4) H2NCOONH4是工业由氨气合成尿素的中间产物。在一定温度下、体积不变的密闭容器中发生反应:H2NCOONH4(s) 2NH3(g)+CO2(g),能说明该反应达到平衡状态的是
2NH3(g)+CO2(g),能说明该反应达到平衡状态的是___________ (填字号)。
①混合气体的压强不变
②混合气体的密度不变
③混合气体的总物质的量不变
④混合气体的平均相对分子质量不变
⑤NH3的体积分数不变
 2NH3(g)△H,据此回答以下问题:
2NH3(g)△H,据此回答以下问题:(1)已知每破坏l mol有关化学键需要的能量如下表:
| H-H | N-H | N-N | N≡N |
| 436 kJ | 391kJ | 193kJ | 946kJ |
则△H=
(2)在不同温度、压强和相同催化剂条件下,初始时N2、H2分别为0.1mol、0.3mol时,平衡后混合物中氨的体积分数(p)如图所示:

①其中,p1、p2和p3由大到小的顺序是
②若分别用vA(N2)和vB(N2)表示从反应开始至达平衡状态A、B时的化学反应速率,则vA(N2)
③若在250℃、pl条件下,反应达到平衡时容器的体积为1 L,则该条件下合成氨的平衡常数K=
(3)合成氨反应在催化剂作用下的反应历程为(*表示吸附态):
第一步N2(g) →2N*;H2(g)一2H* (慢反应)
第二步N*+H*= NH*;NH*+H*= NH2*;NH2*+H*= NH3* (快反应)
第三步NH3*= NH3(g) (快反应)
比较第一步反应的活化能E1与第二步反应的活化能E2的大小:E1
(4) H2NCOONH4是工业由氨气合成尿素的中间产物。在一定温度下、体积不变的密闭容器中发生反应:H2NCOONH4(s)
 2NH3(g)+CO2(g),能说明该反应达到平衡状态的是
2NH3(g)+CO2(g),能说明该反应达到平衡状态的是①混合气体的压强不变
②混合气体的密度不变
③混合气体的总物质的量不变
④混合气体的平均相对分子质量不变
⑤NH3的体积分数不变
您最近半年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐3】氮的化合物在生产生活中广泛存在。
(1)①氯胺(NH2Cl)的电子式为___________ 。可通过反应NH3(g)+Cl2(g)=NH2Cl(g)+HCl(g)制备氯胺,已知部分化学键的键能如表所示,则上述反应的ΔH_________ kJ/mol。
②NH2Cl与水反应生成强氧化性的物质,可作长效缓释消毒剂,该反应的化学方程式为___________ 。
(2)用焦炭还原NO的反应为:2NO(g)+C(s) N2(g)+CO2(g),向容积均为1L的甲、乙、丙三个恒容恒温(反应温度分别为400℃、400℃、T℃)容器中分别加入足量的焦炭和一定量的NO,测得各容器中n(NO)随反应时间t的变化情况如下表所示:
N2(g)+CO2(g),向容积均为1L的甲、乙、丙三个恒容恒温(反应温度分别为400℃、400℃、T℃)容器中分别加入足量的焦炭和一定量的NO,测得各容器中n(NO)随反应时间t的变化情况如下表所示:
①该正反应为______ (填“放热”或“吸热”)反应。
②乙容器在200min达到平衡状态,则0~200min内用NO的浓度变化表示的平均反应速率v(NO)=_________ mol/(L·min)。
(3)用焦炭还原NO2的反应为2NO2(g)+2C(s) N2(g)+2CO2(g),在恒温条件下,1molNO2和足量C(s)发生该反应,测得平衡时NO2和CO2的物质的量浓度与平衡总压的关系如图所示:
N2(g)+2CO2(g),在恒温条件下,1molNO2和足量C(s)发生该反应,测得平衡时NO2和CO2的物质的量浓度与平衡总压的关系如图所示:
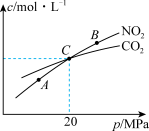
①A、B两点的浓度平衡常数关系:KA_______ KB(填“<”或“>”或“=”)。
②A、B、C三点中NO2的转化率最低的是___________ (填“A”或“B”或“C”)点。
③计算C点时该反应的压强平衡常数Kp=_________ MPa(Kp是用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
(1)①氯胺(NH2Cl)的电子式为
| 键能/(kJ·mol-1) | 391 | 243 | 191 | 431 |
| 化学键 | N-H | Cl-Cl | N-Cl | H-Cl |
(2)用焦炭还原NO的反应为:2NO(g)+C(s)
 N2(g)+CO2(g),向容积均为1L的甲、乙、丙三个恒容恒温(反应温度分别为400℃、400℃、T℃)容器中分别加入足量的焦炭和一定量的NO,测得各容器中n(NO)随反应时间t的变化情况如下表所示:
N2(g)+CO2(g),向容积均为1L的甲、乙、丙三个恒容恒温(反应温度分别为400℃、400℃、T℃)容器中分别加入足量的焦炭和一定量的NO,测得各容器中n(NO)随反应时间t的变化情况如下表所示:| t/min | 0 | 40 | 80 | 120 | 160 |
| n(NO)(甲容器,400℃)/mol | 2.00 | 1.50 | 1.10 | 0.80 | 0.80 |
| n(NO)‘(乙容器,400℃)/mol | 1.00 | 0.80 | 0.65 | 0.53 | 0.45 |
| n(NO)(丙容器,T℃)/mol | 2.00 | 1.45 | 1.00 | 1.00 | 1.00 |
②乙容器在200min达到平衡状态,则0~200min内用NO的浓度变化表示的平均反应速率v(NO)=
(3)用焦炭还原NO2的反应为2NO2(g)+2C(s)
 N2(g)+2CO2(g),在恒温条件下,1molNO2和足量C(s)发生该反应,测得平衡时NO2和CO2的物质的量浓度与平衡总压的关系如图所示:
N2(g)+2CO2(g),在恒温条件下,1molNO2和足量C(s)发生该反应,测得平衡时NO2和CO2的物质的量浓度与平衡总压的关系如图所示:
①A、B两点的浓度平衡常数关系:KA
②A、B、C三点中NO2的转化率最低的是
③计算C点时该反应的压强平衡常数Kp=
您最近半年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐1】丙烯是重要的有机合成原料.由丙烷制备丙烯是近年来研究的热点,主要涉及如下反应:
反应甲2C3H8(g)+O2(g) 2C3H6(g)+2H2O(g) △H1=-225kJ•mol-1
2C3H6(g)+2H2O(g) △H1=-225kJ•mol-1
反应乙2C3H8(g)+7O2(g) 6CO(g)+8H2O(g) △H2=-2742kJ•mol-1
6CO(g)+8H2O(g) △H2=-2742kJ•mol-1
回答下列问题:
(1)反应C3H6(g)+3O2(g) 3CO(g)+3H2O(g) △H=
3CO(g)+3H2O(g) △H=_____ kJ•mol-1。
(2)在恒容绝热密闭容器中发生反应甲,下列能说明反应甲已达到平衡状态的有_____ (填标号)。
(3)在压强恒定为200kPa条件下,按起始投料n(C3H8):n(O2)=2:1充入装有催化剂的反应器中发生反应甲和反应乙,不同温度下,反应相同时间丙烷和氧气的转化率如图。
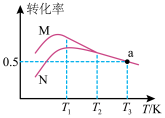
①曲线_____ (填“M”或“N”)表示O2的转化率。
②由图知,当温度高于T2时,可判断反应_____ (填“甲”或“乙”)不再发生,已知a点为平衡点,该点丙烷的分压p(C3H8)=_____ kPa(保留3位有效数字,下同),发生的反应在T3时的平衡常数Kp=_____ kPa(用平衡分压代替平衡浓度计算,分压=总压×体积分数)。
反应甲2C3H8(g)+O2(g)
 2C3H6(g)+2H2O(g) △H1=-225kJ•mol-1
2C3H6(g)+2H2O(g) △H1=-225kJ•mol-1反应乙2C3H8(g)+7O2(g)
 6CO(g)+8H2O(g) △H2=-2742kJ•mol-1
6CO(g)+8H2O(g) △H2=-2742kJ•mol-1回答下列问题:
(1)反应C3H6(g)+3O2(g)
 3CO(g)+3H2O(g) △H=
3CO(g)+3H2O(g) △H=(2)在恒容绝热密闭容器中发生反应甲,下列能说明反应甲已达到平衡状态的有
| A.容器内温度不再变化 | B.v正(O2)=2v逆(C3H6) |
| C.混合气体的密度不再变化 | D.容器内压强不再变化 |
(3)在压强恒定为200kPa条件下,按起始投料n(C3H8):n(O2)=2:1充入装有催化剂的反应器中发生反应甲和反应乙,不同温度下,反应相同时间丙烷和氧气的转化率如图。

①曲线
②由图知,当温度高于T2时,可判断反应
您最近半年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐2】CH4-CO2催化重整不仅可以得到合成气(CO和H2),还对温室气体的减排具有重要意义。回答下列问题:
(1)CH4-CO2催化重整反应为:CH4(g)+ CO2(g)=2CO(g)+2H2(g)。
已知:C(s)+2H2(g)=CH4 (g) ΔH =-75 kJ·mol−1
C(s)+O2(g)=CO2(g) ΔH =-394 kJ·mol−1
C(s)+1/2O2 (g)=CO(g) ΔH =-111 kJ·mol−1
①该催化重整反应的ΔH =_______ kJ·mol−1,有利于提高CH4平衡转化率的条件是_______ (填标号)。
A高温低压 B.低温高压 C.高温高压 D.低温低压
②某温度下,在体积为2 L的容器中加入2 mol CH4、1 mol CO2以及催化剂进行重整反应,达到平衡时CO2的转化率是50%,其平衡常数为_______ mol-2·L−2。
(2)反应中催化剂活性会因积碳反应而降低,同时存在的消碳反应则使积碳量减少。相关数据如下表:
①由上表判断,催化剂Y_______ X(填“优于”或“劣于”),理由_______ 。在反应进料气组成、压强及反应时间相同的情况下,某催化剂表面的积碳量随温度的变化关系如图所示。升高温度时,下列关于积碳反应、消碳反应的平衡常数(K)和速率(v)的叙述正确的是_______ (填标号)。 积减小,
积减小, 消增加
消增加
C.K积减小,K消增加 D. 消增加的倍数比
消增加的倍数比 积增加的倍数大
积增加的倍数大
②在一定温度下,测得某催化剂上沉积碳的生成速率方程v =k·p(CH4)·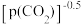 (k为速率常数)。在p(CH4)一定时,不同p(CO2)下积碳量随时间的变化趋势如图所示,则pa(CO2)、pb(CO2)、pc(CO2)从小到大的顺序为
(k为速率常数)。在p(CH4)一定时,不同p(CO2)下积碳量随时间的变化趋势如图所示,则pa(CO2)、pb(CO2)、pc(CO2)从小到大的顺序为_______ 。
(1)CH4-CO2催化重整反应为:CH4(g)+ CO2(g)=2CO(g)+2H2(g)。
已知:C(s)+2H2(g)=CH4 (g) ΔH =-75 kJ·mol−1
C(s)+O2(g)=CO2(g) ΔH =-394 kJ·mol−1
C(s)+1/2O2 (g)=CO(g) ΔH =-111 kJ·mol−1
①该催化重整反应的ΔH =
A高温低压 B.低温高压 C.高温高压 D.低温低压
②某温度下,在体积为2 L的容器中加入2 mol CH4、1 mol CO2以及催化剂进行重整反应,达到平衡时CO2的转化率是50%,其平衡常数为
(2)反应中催化剂活性会因积碳反应而降低,同时存在的消碳反应则使积碳量减少。相关数据如下表:
| 积碳反应CH4(g)= C(s)+2H2(g) | 消碳反应CO2(g)+ C(s)= 2CO(g) | ||
| ΔH/(kJ·mol−1) | +75 | +172 | |
| 活化能 (kJ·mol−1) | 催化剂X | 33 | 91 |
| 催化剂Y | 43 | 72 | |

 积减小,
积减小, 消增加
消增加 C.K积减小,K消增加 D.
 消增加的倍数比
消增加的倍数比 积增加的倍数大
积增加的倍数大②在一定温度下,测得某催化剂上沉积碳的生成速率方程v =k·p(CH4)·
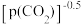 (k为速率常数)。在p(CH4)一定时,不同p(CO2)下积碳量随时间的变化趋势如图所示,则pa(CO2)、pb(CO2)、pc(CO2)从小到大的顺序为
(k为速率常数)。在p(CH4)一定时,不同p(CO2)下积碳量随时间的变化趋势如图所示,则pa(CO2)、pb(CO2)、pc(CO2)从小到大的顺序为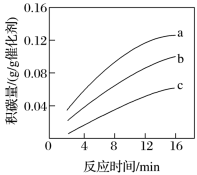
您最近半年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐3】氢能是重要的新能源。储氢作为氢能利用的关键技术,是当前关注的热点之一。
(1)氢气是清洁能源,其燃烧产物为__________ 。
(2)NaBH4是一种重要的储氢载体,能与水反应生成NaBO2,且反应前后B的化合价不变,该反应的化学方程式为___________ ,反应消耗1mol NaBH4时转移的电子数目为__________ 。
(3)储氢还可借助有机物,如利用环己烷和苯之间的可逆反应来实现脱氢和加氢:
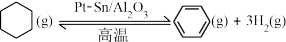 。
。
某温度下,向恒容密闭容器中加入环己烷,起始浓度为a mol/L,平衡时苯的浓度为bmol/L,该反应的平衡常数K=________________ 。
(4)一定条件下,图示装置可实现有机物的电化学储氢(忽略其它有机物)。
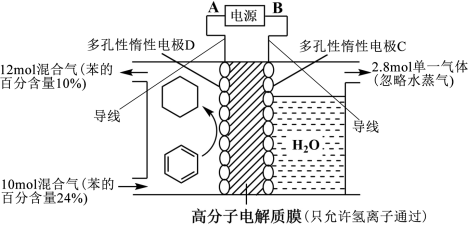
①导线中电子移动方向为_____ →_____ 。(用A、B、C、D填空)
②生成目标产物的电极反应式为_______________________________________ 。
③该储氢装置的电流效率 =
=______________ 。(
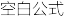 ,计算结果保留小数点后1位)
,计算结果保留小数点后1位)
(1)氢气是清洁能源,其燃烧产物为
(2)NaBH4是一种重要的储氢载体,能与水反应生成NaBO2,且反应前后B的化合价不变,该反应的化学方程式为
(3)储氢还可借助有机物,如利用环己烷和苯之间的可逆反应来实现脱氢和加氢:
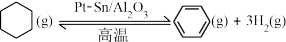 。
。某温度下,向恒容密闭容器中加入环己烷,起始浓度为a mol/L,平衡时苯的浓度为bmol/L,该反应的平衡常数K=
(4)一定条件下,图示装置可实现有机物的电化学储氢(忽略其它有机物)。

①导线中电子移动方向为
②生成目标产物的电极反应式为
③该储氢装置的电流效率
 =
=
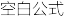 ,计算结果保留小数点后1位)
,计算结果保留小数点后1位)
您最近半年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐1】在“碳达峰、碳中和”的目标引领下,对减少 排放的相关技术研究正成为世界各国的前沿发展方向。
排放的相关技术研究正成为世界各国的前沿发展方向。
(1)300℃时,向2L的恒容密闭容器中,充入2mol 和2mol
和2mol 使之发生反应
使之发生反应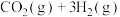
 ,测得各物质的物质的量浓度变化如图1所示:
,测得各物质的物质的量浓度变化如图1所示:
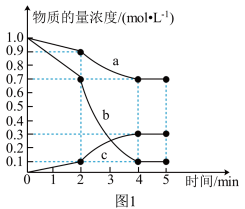
①由图可知, 的浓度随时间的变化为曲线
的浓度随时间的变化为曲线___________ (填“a”“b”或“c”);0~2min内的平均反应速率 为
为___________ 。
②已知:反应至2min时,改变了某一反应条件。由图可知,0~2min内 的生成速率
的生成速率___________ (填“大于”“小于”或“等于”)2~4min内 的生成速率。据图判断,2min时改变的反应条件可能是
的生成速率。据图判断,2min时改变的反应条件可能是___________ (填字母)。
A.加入催化剂 B.升高温度 C.降低温度 D.增加 的物质的量
的物质的量
③5min时, 的转化率(反应时消耗
的转化率(反应时消耗 的物质的量占起始投入
的物质的量占起始投入 的物质的量的百分比)为
的物质的量的百分比)为___________ ,此时容器内气体总压强与反应前容器内气体总压强之比为___________ 。
(2)一种室温下“可呼吸”的 电池装置如图2所示,电池的总反应为
电池装置如图2所示,电池的总反应为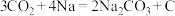 。
。
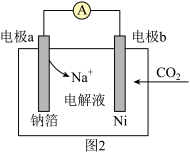
①电极a为___________ 极(填“正”或“负”)。
②电极b上发生的反应类型为___________ (填“氧化反应”或“还原反应”)。
 排放的相关技术研究正成为世界各国的前沿发展方向。
排放的相关技术研究正成为世界各国的前沿发展方向。(1)300℃时,向2L的恒容密闭容器中,充入2mol
 和2mol
和2mol 使之发生反应
使之发生反应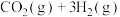
 ,测得各物质的物质的量浓度变化如图1所示:
,测得各物质的物质的量浓度变化如图1所示:
①由图可知,
 的浓度随时间的变化为曲线
的浓度随时间的变化为曲线 为
为②已知:反应至2min时,改变了某一反应条件。由图可知,0~2min内
 的生成速率
的生成速率 的生成速率。据图判断,2min时改变的反应条件可能是
的生成速率。据图判断,2min时改变的反应条件可能是A.加入催化剂 B.升高温度 C.降低温度 D.增加
 的物质的量
的物质的量③5min时,
 的转化率(反应时消耗
的转化率(反应时消耗 的物质的量占起始投入
的物质的量占起始投入 的物质的量的百分比)为
的物质的量的百分比)为(2)一种室温下“可呼吸”的
 电池装置如图2所示,电池的总反应为
电池装置如图2所示,电池的总反应为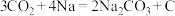 。
。
①电极a为
②电极b上发生的反应类型为
您最近半年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐2】含氨废气的排放对人类健康和生态环境有十分严重的影响,其利用和处理意义重大。2-氰基吡啶( )是生产农药、香料等的重要原料,氨氧化合成法制备原理为:2
)是生产农药、香料等的重要原料,氨氧化合成法制备原理为:2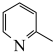
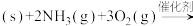 2
2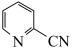
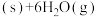
 。
。
回答下列问题:
(1)在V-Ti-O-Mo催化剂作用下,2-甲基吡啶(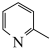 )的氨氧化过程可能有如下两条路径:
)的氨氧化过程可能有如下两条路径:
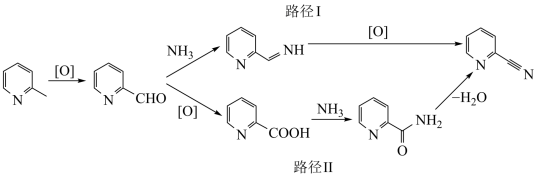
实验测得,反应按路径Ⅱ进行,从反应活化能的角度分析,原因:___________ 。
(2)路径Ⅱ中温度过高会导致2-羧基吡啶(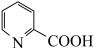 )脱羧生成吡啶(
)脱羧生成吡啶(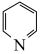 )。为探究催化剂V-Ti-O-Mo在不同温度下对反应的影响,在10L容器中加入2-甲基吡啶、氨、氧气的物质的量分别为10mol、60 mol和40 mol,在340~400℃下用时1h分别进行了多组实验,实验结果如表所示。已知:收率=转化率×选择性。
)。为探究催化剂V-Ti-O-Mo在不同温度下对反应的影响,在10L容器中加入2-甲基吡啶、氨、氧气的物质的量分别为10mol、60 mol和40 mol,在340~400℃下用时1h分别进行了多组实验,实验结果如表所示。已知:收率=转化率×选择性。
①分析上表,催化剂V-Ti-O-Mo的最佳催化温度范围是:___________ 。
②上表中a=___________ (保留一位小数);有人认为360℃时,2-甲基吡啶转化率80.7%不是该反应的平衡转化率,其理由是___________ 。
③400℃时,1h内,v(NH3)=___________ 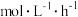 (保留三位小数)。
(保留三位小数)。
(3)钌配合物可以作为一种新型氨氧化阳极催化剂,反应过程如下。
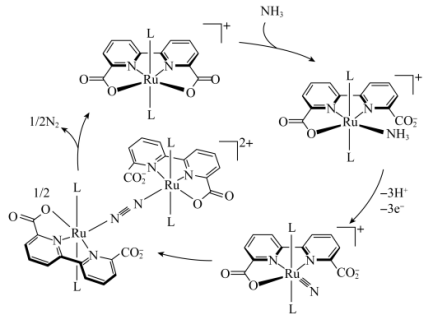
催化过程中共产生了___________ 种含钌中间产物。该电极上氨氧化的电极反应方程式为:___________ 。
 )是生产农药、香料等的重要原料,氨氧化合成法制备原理为:2
)是生产农药、香料等的重要原料,氨氧化合成法制备原理为:2
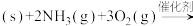 2
2
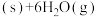
 。
。回答下列问题:
(1)在V-Ti-O-Mo催化剂作用下,2-甲基吡啶(
 )的氨氧化过程可能有如下两条路径:
)的氨氧化过程可能有如下两条路径:
实验测得,反应按路径Ⅱ进行,从反应活化能的角度分析,原因:
(2)路径Ⅱ中温度过高会导致2-羧基吡啶(
 )脱羧生成吡啶(
)脱羧生成吡啶( )。为探究催化剂V-Ti-O-Mo在不同温度下对反应的影响,在10L容器中加入2-甲基吡啶、氨、氧气的物质的量分别为10mol、60 mol和40 mol,在340~400℃下用时1h分别进行了多组实验,实验结果如表所示。已知:收率=转化率×选择性。
)。为探究催化剂V-Ti-O-Mo在不同温度下对反应的影响,在10L容器中加入2-甲基吡啶、氨、氧气的物质的量分别为10mol、60 mol和40 mol,在340~400℃下用时1h分别进行了多组实验,实验结果如表所示。已知:收率=转化率×选择性。| 反应温度/℃ | 2—甲基吡啶转化率/% | 选择性/% | 收率/% |
| 340 | 46.1 | 93.1 | 42.9 |
| 350 | 66.2 | 96.6 | a |
| 360 | 80.7 | 94.9 | 76.6 |
| 370 | 86.5 | 95.5 | 82.6 |
| 380 | 91.1 | 93.5 | 85.2 |
| 390 | 95.4 | 80.1 | 76.4 |
| 400 | 97.7 | 58.1 | 56.8 |
②上表中a=
③400℃时,1h内,v(NH3)=
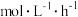 (保留三位小数)。
(保留三位小数)。(3)钌配合物可以作为一种新型氨氧化阳极催化剂,反应过程如下。

催化过程中共产生了
您最近半年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐3】汽车尾气中含有 、
、 ,排气管内的催化转化器可实现将污染性气体转化为
,排气管内的催化转化器可实现将污染性气体转化为 和
和 。
。
(1)已知:①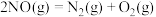
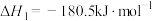
②
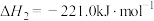
③
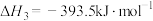
则 与
与 反应生成
反应生成 和
和 的热化学方程式为
的热化学方程式为___________ 。该反应在___________ (填“高温”或“低温”)下可自发进行。
(2) 的反应历程如图(图中所有物质均为气态)。
的反应历程如图(图中所有物质均为气态)。
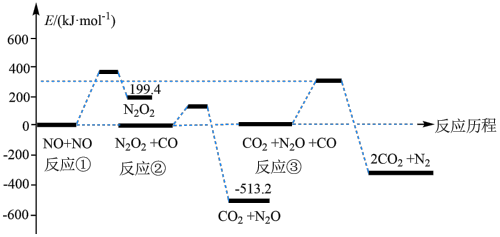
该反应的决速步骤是反应___________ (填对应序号);总反应的中间产物的化学式为___________ 。
(3)一定温度下,起始时向2L的恒容密闭容器中充入
 、
、
 ,仅发生反应
,仅发生反应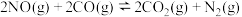 ,起始气体总压强为180kPa,20min时反应达到平衡,此时气体总压强为起始压强的
,起始气体总压强为180kPa,20min时反应达到平衡,此时气体总压强为起始压强的 ,
,
①0~20min内,
___________ ,NO转化率为___________ (保留三位有效数字)。
②此温度下,该反应的平衡常数
___________ 。
 、
、 ,排气管内的催化转化器可实现将污染性气体转化为
,排气管内的催化转化器可实现将污染性气体转化为 和
和 。
。(1)已知:①
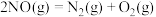
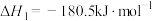
②

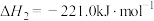
③

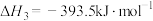
则
 与
与 反应生成
反应生成 和
和 的热化学方程式为
的热化学方程式为(2)
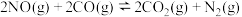 的反应历程如图(图中所有物质均为气态)。
的反应历程如图(图中所有物质均为气态)。
该反应的决速步骤是反应
(3)一定温度下,起始时向2L的恒容密闭容器中充入

 、
、
 ,仅发生反应
,仅发生反应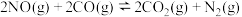 ,起始气体总压强为180kPa,20min时反应达到平衡,此时气体总压强为起始压强的
,起始气体总压强为180kPa,20min时反应达到平衡,此时气体总压强为起始压强的 ,
,①0~20min内,

②此温度下,该反应的平衡常数

您最近半年使用:0次



