合成氨工业对国民经济和社会发展具有重要的意义。其原理为:N2(g)+3H2(g) 2NH3(g)△H,据此回答以下问题:
2NH3(g)△H,据此回答以下问题:
(1)已知每破坏l mol有关化学键需要的能量如下表:
则△H=_______________ 。
(2)在不同温度、压强和相同催化剂条件下,初始时N2、H2分别为0.1mol、0.3mol时,平衡后混合物中氨的体积分数(p)如图所示:
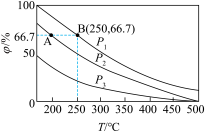
①其中,p1、p2和p3由大到小的顺序是________ ,其原因是__________ 。
②若分别用vA(N2)和vB(N2)表示从反应开始至达平衡状态A、B时的化学反应速率,则vA(N2)___________ vB(N2) (填“>”、“<"或”“=")。
③若在250℃、pl条件下,反应达到平衡时容器的体积为1 L,则该条件下合成氨的平衡常数K=_________ (列出计算式即可)。
(3)合成氨反应在催化剂作用下的反应历程为(*表示吸附态):
第一步N2(g) →2N*;H2(g)一2H* (慢反应)
第二步N*+H*= NH*;NH*+H*= NH2*;NH2*+H*= NH3* (快反应)
第三步NH3*= NH3(g) (快反应)
比较第一步反应的活化能E1与第二步反应的活化能E2的大小:E1_______ E2(填“>”“<"或“=")。
(4) H2NCOONH4是工业由氨气合成尿素的中间产物。在一定温度下、体积不变的密闭容器中发生反应:H2NCOONH4(s) 2NH3(g)+CO2(g),能说明该反应达到平衡状态的是
2NH3(g)+CO2(g),能说明该反应达到平衡状态的是___________ (填字号)。
①混合气体的压强不变
②混合气体的密度不变
③混合气体的总物质的量不变
④混合气体的平均相对分子质量不变
⑤NH3的体积分数不变
 2NH3(g)△H,据此回答以下问题:
2NH3(g)△H,据此回答以下问题:(1)已知每破坏l mol有关化学键需要的能量如下表:
| H-H | N-H | N-N | N≡N |
| 436 kJ | 391kJ | 193kJ | 946kJ |
则△H=
(2)在不同温度、压强和相同催化剂条件下,初始时N2、H2分别为0.1mol、0.3mol时,平衡后混合物中氨的体积分数(p)如图所示:

①其中,p1、p2和p3由大到小的顺序是
②若分别用vA(N2)和vB(N2)表示从反应开始至达平衡状态A、B时的化学反应速率,则vA(N2)
③若在250℃、pl条件下,反应达到平衡时容器的体积为1 L,则该条件下合成氨的平衡常数K=
(3)合成氨反应在催化剂作用下的反应历程为(*表示吸附态):
第一步N2(g) →2N*;H2(g)一2H* (慢反应)
第二步N*+H*= NH*;NH*+H*= NH2*;NH2*+H*= NH3* (快反应)
第三步NH3*= NH3(g) (快反应)
比较第一步反应的活化能E1与第二步反应的活化能E2的大小:E1
(4) H2NCOONH4是工业由氨气合成尿素的中间产物。在一定温度下、体积不变的密闭容器中发生反应:H2NCOONH4(s)
 2NH3(g)+CO2(g),能说明该反应达到平衡状态的是
2NH3(g)+CO2(g),能说明该反应达到平衡状态的是①混合气体的压强不变
②混合气体的密度不变
③混合气体的总物质的量不变
④混合气体的平均相对分子质量不变
⑤NH3的体积分数不变
更新时间:2020-09-12 22:25:08
|
相似题推荐
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐1】二氧化碳加氢合成甲醇是化学固碳的一种有效途径,不仅可以有效减少空气中的CO2排放.还可以制备出甲醇清洁能源。在CO2转化为甲醇过程中,伴随有副反应发生,因此常使用催化剂调节控制反应。科学研究者结合实验与计算机模拟,研究了CO2与H2分别在Zn/Cu、ZnO/Cu催化剂表面生成CH3OH和H2O的部分反应历程(如图1所示),其中ts-n表示过渡态。
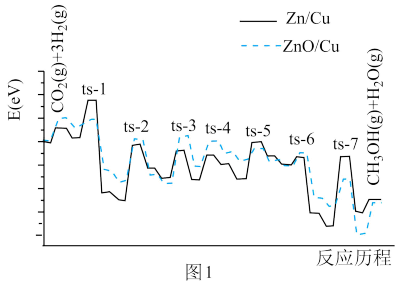
回答下列问题:
(1)①图1表示的反应中,若每生成1mol甲醇,反应物与生成物总能量差为58kJ,则反应的热化学方程式为_____ ,从反应原理分析,下列更利于该反应进行的条件是_____ (填标号)。
a.高压、高温 b.高压低温 c.低压、高温 d.低压低温
②已知CO2和H2可发生副反应:CO2(g)+H2(g) CO(g)+H2O(g) ΔH=+41kJ•mol-1部分相关化学键的键能数据如表:
CO(g)+H2O(g) ΔH=+41kJ•mol-1部分相关化学键的键能数据如表:
由此计算E(C=O)=______ kJ•mol-1。
(2)在图1给出的反应历程中,若选择Zn/Cu作为催化剂则正反应最大的活化能发生在______ (用“ts-n”具体数字表示)。图示结果显示,选择ZnO/Cu作为催化剂更优于Zn/Cu,其主要原因是______ 。
(3)图2为使用Zn/Cu催化剂、分别在525K和550K条件下(其它条件相同),CO2和H2按投料比1:9进行反应生成CH3OH的过程中,CO2的转化率随时间变化图示。
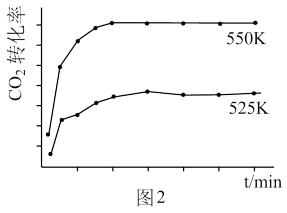
①温度略为升高(从525K→550K),CO2的转化率明显增大的可能原因是______ 。
②工业生产中,对于气相的反应体系,还可用反应体系中各组分的分压来表示化学平衡常数(Kp)。如反应:aA(g)+bB(g) dD(g)+eE(g)达到平衡时,Kp=
dD(g)+eE(g)达到平衡时,Kp=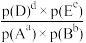 ,组分分压p(A)=P总×
,组分分压p(A)=P总×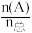 。现保持550K、pkPa条件,CO2和H2按投料比(物质的量)1:9进行生成CH3OH反应,达到平衡时,CO2的转化率为α,则反应的化学平衡常数Kp=
。现保持550K、pkPa条件,CO2和H2按投料比(物质的量)1:9进行生成CH3OH反应,达到平衡时,CO2的转化率为α,则反应的化学平衡常数Kp=______ (列出含α、p计算式)。

回答下列问题:
(1)①图1表示的反应中,若每生成1mol甲醇,反应物与生成物总能量差为58kJ,则反应的热化学方程式为
a.高压、高温 b.高压低温 c.低压、高温 d.低压低温
②已知CO2和H2可发生副反应:CO2(g)+H2(g)
 CO(g)+H2O(g) ΔH=+41kJ•mol-1部分相关化学键的键能数据如表:
CO(g)+H2O(g) ΔH=+41kJ•mol-1部分相关化学键的键能数据如表:| 化学键 | H-H | C-O | H-O | C-H | C≡O |
| E/(kJ•mol-1) | 436 | 326 | 464 | 414 | 1061 |
(2)在图1给出的反应历程中,若选择Zn/Cu作为催化剂则正反应最大的活化能发生在
(3)图2为使用Zn/Cu催化剂、分别在525K和550K条件下(其它条件相同),CO2和H2按投料比1:9进行反应生成CH3OH的过程中,CO2的转化率随时间变化图示。

①温度略为升高(从525K→550K),CO2的转化率明显增大的可能原因是
②工业生产中,对于气相的反应体系,还可用反应体系中各组分的分压来表示化学平衡常数(Kp)。如反应:aA(g)+bB(g)
 dD(g)+eE(g)达到平衡时,Kp=
dD(g)+eE(g)达到平衡时,Kp=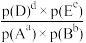 ,组分分压p(A)=P总×
,组分分压p(A)=P总×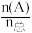 。现保持550K、pkPa条件,CO2和H2按投料比(物质的量)1:9进行生成CH3OH反应,达到平衡时,CO2的转化率为α,则反应的化学平衡常数Kp=
。现保持550K、pkPa条件,CO2和H2按投料比(物质的量)1:9进行生成CH3OH反应,达到平衡时,CO2的转化率为α,则反应的化学平衡常数Kp=
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐2】雾霾成因有多种,其中燃煤过程中产生的二氧化硫、氮氧化物以及可吸入颗粒物是山西冬季雾霾的主要组成。治霾迫在眉睫,利在千秋。
I.脱氮
已知: ①2CO(g)+O2(g)===2CO2(g) ΔH1=-566.0 kJ·mol-1
②2NO(g)+O2===2NO2(g) ΔH2=-116.5kJ·mol-1
③N2(g)+O2(g)===2NO(g) ΔH3=+180.5kJ·mol-1
(1)则燃煤所产生的废气中NO2 与CO 转化成无污染气体的热化学方程式为:________________________________ 。
(2)若1molN2(g)1molO2(g)分子中化学键断裂时分别吸收946kJ、498KJ的能量,则1molNO(g) 分子中化学键断裂时需要吸收的能量为_____________________ KJ。
Ⅱ.脱硫的反应原理2CO(g) +SO2(g) 2CO2(g) +S(1) ΔH=-QkJ·mol-1(Q>0)
2CO2(g) +S(1) ΔH=-QkJ·mol-1(Q>0)
(1)若在一定温度下,将总物质的量为3 mol的CO(g)和SO2(g) 以不同比例充入2 L的恒容容器中,结果如图所示。a、b分别表示SO2、CO 的平衡转化率的变化,c表示平衡体系中CO2的体积分数的变化。
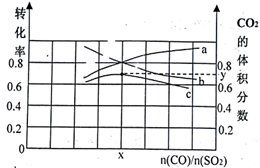
由图计算x=__________ ;CO2的体积分数y=_________ (精确到0.01),该温度下的平衡常数K=_____ 。
(2)在T1℃下,将CO与SO2按体积比为5∶4充入一恒压密闭容器中,此时容器体积为0.1V L。
①下列能判断该反应达到化学平衡状态的是_____________ 。
a.S(l)的质量不变
b.K不变
c.容器中气体的平均相对分子质量不变
d.2v正(SO2)= v正(CO2)
e.Q值不变
②压强一定的条件下,在不同温度下进行反应,测得容器的体积变化如图所示:
已知: n1≠n2
求:T1温度时,SO2的平衡转化率为_____ %;
比较大小,T1___ T2(填“>”、“<”、“=”),解释原因____________________ 。
I.脱氮
已知: ①2CO(g)+O2(g)===2CO2(g) ΔH1=-566.0 kJ·mol-1
②2NO(g)+O2===2NO2(g) ΔH2=-116.5kJ·mol-1
③N2(g)+O2(g)===2NO(g) ΔH3=+180.5kJ·mol-1
(1)则燃煤所产生的废气中NO2 与CO 转化成无污染气体的热化学方程式为:
(2)若1molN2(g)1molO2(g)分子中化学键断裂时分别吸收946kJ、498KJ的能量,则1molNO(g) 分子中化学键断裂时需要吸收的能量为
Ⅱ.脱硫的反应原理2CO(g) +SO2(g)
 2CO2(g) +S(1) ΔH=-QkJ·mol-1(Q>0)
2CO2(g) +S(1) ΔH=-QkJ·mol-1(Q>0)(1)若在一定温度下,将总物质的量为3 mol的CO(g)和SO2(g) 以不同比例充入2 L的恒容容器中,结果如图所示。a、b分别表示SO2、CO 的平衡转化率的变化,c表示平衡体系中CO2的体积分数的变化。

由图计算x=
(2)在T1℃下,将CO与SO2按体积比为5∶4充入一恒压密闭容器中,此时容器体积为0.1V L。
①下列能判断该反应达到化学平衡状态的是
a.S(l)的质量不变
b.K不变
c.容器中气体的平均相对分子质量不变
d.2v正(SO2)= v正(CO2)
e.Q值不变
②压强一定的条件下,在不同温度下进行反应,测得容器的体积变化如图所示:
已知: n1≠n2
| 温度(℃) | 初始投入总量 | 初始投料v (CO) /v (SO2) | 初始体积(L) | 平衡体积(L) |
| T1 | n1 | 5∶4 | 0.1v | 0.07v |
| T2 | n2 | 5∶4 | 0.3v | 0.22v |
比较大小,T1
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐3】图1所示的氮循环是生态系统物质循环的重要组成部分,人类活动加剧了氮循环中的物质转化。

(1)结合上图判断下列说法正确的是________ (填字母序号)。
A. 固氮过程中,N2只做氧化剂
B. 在硝化细菌作用下发生的硝化过程需要有氧化剂参与
C. 反硝化过程有助于弥补人工固氮对氮循环造成的影响
D. 同化、氨化过程中,氮元素均从无机物转移至有机物
(2)硝化过程中,NH3转化成HNO2的反应的化学方程式为_______ 。
(3)反硝化过程中,CH3OH可作为反应的还原剂,请将该反应的离子方程式补充完整:5CH3OH + 6NO3- N2↑ + 4HCO3- +□
N2↑ + 4HCO3- +□______ +□
(4)利用下表数据进行估算,写出工业合成氨反应的热化学方程式:_______ 。
(5)电解法合成氨因其原料转化率大幅度提高,有望代替传统的工业合成氨工艺。电解法合成氨的两种原理及装置如图2和图3所示。

①图2中,a电极上通入的X为_______ 。
②图3中,d电极上的电极反应式为_______ 。
③若图2和图3装置的通电时间相同、电流强度相等,电解效率分别为80%和60%,则两种装置中产生氨气的物质的量之比为_______ 。

(1)结合上图判断下列说法正确的是
A. 固氮过程中,N2只做氧化剂
B. 在硝化细菌作用下发生的硝化过程需要有氧化剂参与
C. 反硝化过程有助于弥补人工固氮对氮循环造成的影响
D. 同化、氨化过程中,氮元素均从无机物转移至有机物
(2)硝化过程中,NH3转化成HNO2的反应的化学方程式为
(3)反硝化过程中,CH3OH可作为反应的还原剂,请将该反应的离子方程式补充完整:5CH3OH + 6NO3-
 N2↑ + 4HCO3- +□
N2↑ + 4HCO3- +□(4)利用下表数据进行估算,写出工业合成氨反应的热化学方程式:
| 共价键 | N≡N | H—H | N—H |
| 断开1mol共价键所需能量(kJ) | 946 | 436 | 391 |
(5)电解法合成氨因其原料转化率大幅度提高,有望代替传统的工业合成氨工艺。电解法合成氨的两种原理及装置如图2和图3所示。

①图2中,a电极上通入的X为
②图3中,d电极上的电极反应式为
③若图2和图3装置的通电时间相同、电流强度相等,电解效率分别为80%和60%,则两种装置中产生氨气的物质的量之比为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐1】“金山银山不如绿水青山”,汽车尾气治理是我国一项重要的任务。经过化学工作者的努力,在汽车尾气系统中装置催化转化器,可有效降低NOx和CO的排放。
已知:①CO的燃烧热为283kJ·mol-1
②N2(g)+O2(g) 2NO(g) ΔH=+180.5kJ·mol-1
2NO(g) ΔH=+180.5kJ·mol-1
③2NO(g)+O2(g) 2NO2(g) ΔH=-116.5kJ·mol-1
2NO2(g) ΔH=-116.5kJ·mol-1
回答下列问题:
(1)若1molN2(g)、1molO2(g)分子中化学键断裂时分别需要吸收946kJ、498kJ的能量,则1molNO(g)分子中化学键断裂时需吸收的能量为___ kJ。
(2)利用上面提供的信息和盖斯定律,写出NO2+CO→N2+CO2的热化学方程式___ 。
(3)为了模拟反应2NO(g)+2CO(g) N2(g)+2CO2(g)在催化转化器内的工作情况,控制一定条件,让反应在恒容密闭容器中进行,用传感器测得不同时间NO和CO的浓度如下表:
N2(g)+2CO2(g)在催化转化器内的工作情况,控制一定条件,让反应在恒容密闭容器中进行,用传感器测得不同时间NO和CO的浓度如下表:
①前3s内的平均反应速率v(N2)=___ (保留两位小数),此温度下,该反应的平衡常数K=___ ;
②能说明上述反应达到平衡状态的是___ 。(填正确答案标号)
A.n(CO2)=3n(N2)
B.混合气体的平均相对分子质量不变
C.气体质量不变
D.容器内混合气体的压强不变
E.2c(CO2)=3c(N2)
③当NO与CO的浓度相等时,体系中NO的平衡转化率与温度、压强的关系如图所示,则NO的平衡转化率随温度升高而减小的原因是___ ,图中压强(p1、p2、p3)的大小顺序为___ 。

已知:①CO的燃烧热为283kJ·mol-1
②N2(g)+O2(g)
 2NO(g) ΔH=+180.5kJ·mol-1
2NO(g) ΔH=+180.5kJ·mol-1③2NO(g)+O2(g)
 2NO2(g) ΔH=-116.5kJ·mol-1
2NO2(g) ΔH=-116.5kJ·mol-1回答下列问题:
(1)若1molN2(g)、1molO2(g)分子中化学键断裂时分别需要吸收946kJ、498kJ的能量,则1molNO(g)分子中化学键断裂时需吸收的能量为
(2)利用上面提供的信息和盖斯定律,写出NO2+CO→N2+CO2的热化学方程式
(3)为了模拟反应2NO(g)+2CO(g)
 N2(g)+2CO2(g)在催化转化器内的工作情况,控制一定条件,让反应在恒容密闭容器中进行,用传感器测得不同时间NO和CO的浓度如下表:
N2(g)+2CO2(g)在催化转化器内的工作情况,控制一定条件,让反应在恒容密闭容器中进行,用传感器测得不同时间NO和CO的浓度如下表:| 时间/s | 0 | 1 | 2 | 3 | 4 | 5 |
| c(NO)/(10-4mol·L-1) | 10.00 | 4.50 | 2.50 | 1.50 | 1.00 | 1.00 |
| c(CO)/(10-3mol·L-1) | 3.60 | 3.05 | 2.85 | 2.75 | 2.70 | 2.70 |
①前3s内的平均反应速率v(N2)=
②能说明上述反应达到平衡状态的是
A.n(CO2)=3n(N2)
B.混合气体的平均相对分子质量不变
C.气体质量不变
D.容器内混合气体的压强不变
E.2c(CO2)=3c(N2)
③当NO与CO的浓度相等时,体系中NO的平衡转化率与温度、压强的关系如图所示,则NO的平衡转化率随温度升高而减小的原因是

您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐2】对甲烷和CO2的高效利用不仅能缓解大气变暖,而且对日益枯竭的石油资源也有一定的补充作用,甲烷临氧耦合CO2重整反应有:
反应(i):2CH4(g)+O2(g) 2CO(g)+4H2(g) △H=-71.4kJ•mol-1
2CO(g)+4H2(g) △H=-71.4kJ•mol-1
反应(ii):CH4(g)+CO2(g) 2CO(g)+2H2(g) △H=+247.0kJ•mol-1
2CO(g)+2H2(g) △H=+247.0kJ•mol-1
(1)写出表示CO燃烧热的热化学方程式:_____ 。
(2)在两个体积均为2L的恒容密闭容器中,起始时按表中相应的量加入物质,在相同温度下进行反应(ii):CH4(g)+CO2(g) 2CO(g)+2H2(g)(不发生其它反应),CO2的平衡转化率如下表所示:
2CO(g)+2H2(g)(不发生其它反应),CO2的平衡转化率如下表所示:
①下列能说明反应达到平衡状态是_____ 。
A.v正(CH4)=2v逆(CO)
B.容器内各物质的浓度满足c(CH4)·c(CO2)=c2(CO)·c2(H2)
C.容器内混合气体的总压强不再变化
D.容器内混合气体密度保持不变
②若容器Ⅰ内反应从开始到平衡所用的时间为tmin,则tmin内该反应的平均反应速率为:v(H2)=____ (用含t的表达式表示)。
③达到平衡时,容器Ⅰ、Ⅱ内CO的物质的量的关系满足:2n(CO)Ⅰ___ n(CO)Ⅱ(填“>”、“=”或“<”)。
(3)将CH4(g)和O2(g)以物质的量比为4:3充入盛有催化剂的恒容密闭容器内,发生上述反应(i):2CH4(g)+O2(g) 2CO(g)+4H2(g),测得CO的体积分数[ψ(CO)]与温度(T)的关系如图如示。
2CO(g)+4H2(g),测得CO的体积分数[ψ(CO)]与温度(T)的关系如图如示。
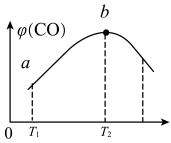
①T2℃时,CO体积分数最大的原因是____ 。
②若T2℃时,容器内起始压强为P0,平衡时CO的体积分数为20%,则反应的平衡常数KP=___ (用平衡分压强代替平衡浓度计算,分压=总压×物质的量分数)。
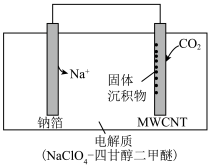
(4)2016年我国科研人员根据反应Na+CO2→Na2CO3+C(未配平)研制出一种室温“可呼吸”Na-CO2电池。放电时该电池“吸入”CO2,充电时“呼出”CO2。其放电时的工作原理如图所示,已知吸收的全部CO2中,有 转化为Na2CO3固体沉积在多壁碳纳米管(MWCNT)电极表面,写出放电时正极的电极反应式:
转化为Na2CO3固体沉积在多壁碳纳米管(MWCNT)电极表面,写出放电时正极的电极反应式:___ 。
反应(i):2CH4(g)+O2(g)
 2CO(g)+4H2(g) △H=-71.4kJ•mol-1
2CO(g)+4H2(g) △H=-71.4kJ•mol-1反应(ii):CH4(g)+CO2(g)
 2CO(g)+2H2(g) △H=+247.0kJ•mol-1
2CO(g)+2H2(g) △H=+247.0kJ•mol-1(1)写出表示CO燃烧热的热化学方程式:
(2)在两个体积均为2L的恒容密闭容器中,起始时按表中相应的量加入物质,在相同温度下进行反应(ii):CH4(g)+CO2(g)
 2CO(g)+2H2(g)(不发生其它反应),CO2的平衡转化率如下表所示:
2CO(g)+2H2(g)(不发生其它反应),CO2的平衡转化率如下表所示:| 起始物质的量(n)/mol | CO2的平衡转化率 | ||||
| CH4 | CO2 | CO | H2 | ||
| Ⅰ | 0.1 | 0.1 | 0 | 0 | 50% |
| Ⅱ | 0.1 | 0.1 | 0.2 | 0.2 | / |
①下列能说明反应达到平衡状态是
A.v正(CH4)=2v逆(CO)
B.容器内各物质的浓度满足c(CH4)·c(CO2)=c2(CO)·c2(H2)
C.容器内混合气体的总压强不再变化
D.容器内混合气体密度保持不变
②若容器Ⅰ内反应从开始到平衡所用的时间为tmin,则tmin内该反应的平均反应速率为:v(H2)=
③达到平衡时,容器Ⅰ、Ⅱ内CO的物质的量的关系满足:2n(CO)Ⅰ
(3)将CH4(g)和O2(g)以物质的量比为4:3充入盛有催化剂的恒容密闭容器内,发生上述反应(i):2CH4(g)+O2(g)
 2CO(g)+4H2(g),测得CO的体积分数[ψ(CO)]与温度(T)的关系如图如示。
2CO(g)+4H2(g),测得CO的体积分数[ψ(CO)]与温度(T)的关系如图如示。
①T2℃时,CO体积分数最大的原因是
②若T2℃时,容器内起始压强为P0,平衡时CO的体积分数为20%,则反应的平衡常数KP=
(4)2016年我国科研人员根据反应Na+CO2→Na2CO3+C(未配平)研制出一种室温“可呼吸”Na-CO2电池。放电时该电池“吸入”CO2,充电时“呼出”CO2。其放电时的工作原理如图所示,已知吸收的全部CO2中,有
 转化为Na2CO3固体沉积在多壁碳纳米管(MWCNT)电极表面,写出放电时正极的电极反应式:
转化为Na2CO3固体沉积在多壁碳纳米管(MWCNT)电极表面,写出放电时正极的电极反应式:
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐3】工业合成氨是人工固氮的一种重要方式,氨的合成实现工业化生产迄今已有100多年历史,合成氨技术是人类科学技术领域的重要突破。工业合成氨的反应如下:N2(g)+3H2(g) 2NH3(g) △H=-92.2kJ·mol-1。
2NH3(g) △H=-92.2kJ·mol-1。

(1)1molN—H键断裂吸收的能量为____ kJ。
(2)一定温度下,将N2和H2以物质的量之比为1:1充入盛有催化剂的密闭容器,下列图象t时刻一定处于平衡状态的是___ 。
a. b.
b. c.
c. d.
d.
(3)若只改变某一条件,一定可以提高合成氨平衡体系中H2的转化率,又能加快反应速率的措施是___ 。
a.升高温度 b.移走NH3 c.加入催化剂 d.再充入N2
(4)理论研究表明,在200℃,压强超过200MPa时,不使用催化剂,氨便可以顺利合成。但实际工业上合成NH3往往在温度500℃,压强20~50MPa的条件下进行,试分析采用20~50MPa的原因____ 。
(5)某小组模拟不同条件下的合成氨反应,向容器充入9.0molN2和23.0molH2,图为不同温度下平衡混合物中氨气的体积分数与总压强(P)的关系图。

①T1、T2、T3由大到小的排序为___ 。
②在T2、60MPa条件下,比较A点v正____ v逆(填“>”、“<”或“=”)。
③计算T2、60MPa平衡体系的平衡常数Kp=____ MPa-2。(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数,列出计算式即可)。
 2NH3(g) △H=-92.2kJ·mol-1。
2NH3(g) △H=-92.2kJ·mol-1。
(1)1molN—H键断裂吸收的能量为
(2)一定温度下,将N2和H2以物质的量之比为1:1充入盛有催化剂的密闭容器,下列图象t时刻一定处于平衡状态的是
a.
 b.
b. c.
c. d.
d.
(3)若只改变某一条件,一定可以提高合成氨平衡体系中H2的转化率,又能加快反应速率的措施是
a.升高温度 b.移走NH3 c.加入催化剂 d.再充入N2
(4)理论研究表明,在200℃,压强超过200MPa时,不使用催化剂,氨便可以顺利合成。但实际工业上合成NH3往往在温度500℃,压强20~50MPa的条件下进行,试分析采用20~50MPa的原因
(5)某小组模拟不同条件下的合成氨反应,向容器充入9.0molN2和23.0molH2,图为不同温度下平衡混合物中氨气的体积分数与总压强(P)的关系图。

①T1、T2、T3由大到小的排序为
②在T2、60MPa条件下,比较A点v正
③计算T2、60MPa平衡体系的平衡常数Kp=
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐1】回答下列问题。
(1)工业上用 和
和 反应合成二甲醚。已知:
反应合成二甲醚。已知:
Ⅰ.

Ⅱ.
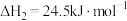
①反应I在___________ (填“高温”、“低温”或“任何温度”)下自发。
②写出 和
和 转化为
转化为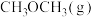 和
和 的热化学方程式
的热化学方程式___________ 。
(2)亚硝酸氨(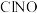 )是有机合成中的重要试剂,可由反应
)是有机合成中的重要试剂,可由反应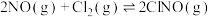 制备。在
制备。在 的密闭容器中充入
的密闭容器中充入 和
和 发生上述反应,在不同温度下测得
发生上述反应,在不同温度下测得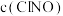 与时间的关系如图。
与时间的关系如图。
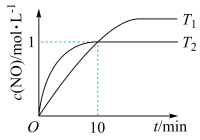
①反应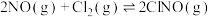 的化学平衡常数表达式为
的化学平衡常数表达式为
___________ 。
②
___________  (填“>““<”或“=”,下同),该反应的
(填“>““<”或“=”,下同),该反应的
___________ 0。
③ 时,反应从开始到
时,反应从开始到 时
时 的平均反应速率
的平均反应速率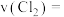
___________ 。
④写出两条能提高 平衡转化率的措施
平衡转化率的措施___________ 。
(1)工业上用
 和
和 反应合成二甲醚。已知:
反应合成二甲醚。已知:Ⅰ.


Ⅱ.

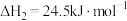
①反应I在
②写出
 和
和 转化为
转化为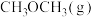 和
和 的热化学方程式
的热化学方程式(2)亚硝酸氨(
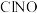 )是有机合成中的重要试剂,可由反应
)是有机合成中的重要试剂,可由反应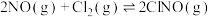 制备。在
制备。在 的密闭容器中充入
的密闭容器中充入 和
和 发生上述反应,在不同温度下测得
发生上述反应,在不同温度下测得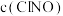 与时间的关系如图。
与时间的关系如图。
①反应
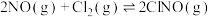 的化学平衡常数表达式为
的化学平衡常数表达式为
②

 (填“>““<”或“=”,下同),该反应的
(填“>““<”或“=”,下同),该反应的
③
 时,反应从开始到
时,反应从开始到 时
时 的平均反应速率
的平均反应速率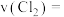
④写出两条能提高
 平衡转化率的措施
平衡转化率的措施
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐2】一氧化碳、氮的氧化物、硫的氧化物是主要的大气污染物,对这些有害气体的治理及合理利用显得尤为重要。回答下列问题:
(1)已知: 变成
变成 吸收
吸收 的能量,在一定条件下,CO与水蒸气反应可制备氢能源,反应过程中的能量变化如图所示:
的能量,在一定条件下,CO与水蒸气反应可制备氢能源,反应过程中的能量变化如图所示:

反应 为
为_______ (填“放热”或“吸热”)反应。图中虚线不可能是 的能量变化曲线,原因是
的能量变化曲线,原因是_______
(2)某工业烟气中含 ,需进行一系列处理后才能排入空气中,其中脱硝、脱硫就是重要一环,一种脱硝、脱硫的简易流程如图:
,需进行一系列处理后才能排入空气中,其中脱硝、脱硫就是重要一环,一种脱硝、脱硫的简易流程如图:
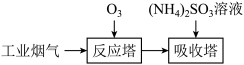
反应塔中涉及如下反应(忽略 与
与 的相互转化):
的相互转化):
Ⅰ.
Ⅱ.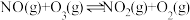
Ⅲ.
①恒温恒容条件下,反应塔中 ,反应
,反应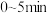 内测得
内测得 ,则
,则 末时NO的转化率为
末时NO的转化率为_______
②保持反应塔中起始浓度 ,在相同时间内,测得吸收塔中脱硝率、脱硫率与
,在相同时间内,测得吸收塔中脱硝率、脱硫率与 的关系曲线如图所示:
的关系曲线如图所示:
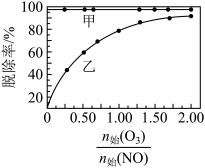
表示脱硫率的曲线是_______ (填“甲”或“乙”),理由是_______
③在某恒容密闭容器中充入一定量的 ,发生上述反应Ⅰ、Ⅱ、Ⅲ,下列说法错误的是
,发生上述反应Ⅰ、Ⅱ、Ⅲ,下列说法错误的是_______ (填序号)
a.升高温度,化学反应速率加快
b.容器中混合气体的密度不变说明反应达到平衡状态
c.容器中混合气体的压强不变说明反应达到平衡状态
d.容器中混合气体的颜色不变说明反应达到平衡状态
e.缩小容器的容积,压强增大,脱硝率和脱硫率均不变
(1)已知:
 变成
变成 吸收
吸收 的能量,在一定条件下,CO与水蒸气反应可制备氢能源,反应过程中的能量变化如图所示:
的能量,在一定条件下,CO与水蒸气反应可制备氢能源,反应过程中的能量变化如图所示:
反应
 为
为 的能量变化曲线,原因是
的能量变化曲线,原因是(2)某工业烟气中含
 ,需进行一系列处理后才能排入空气中,其中脱硝、脱硫就是重要一环,一种脱硝、脱硫的简易流程如图:
,需进行一系列处理后才能排入空气中,其中脱硝、脱硫就是重要一环,一种脱硝、脱硫的简易流程如图:
反应塔中涉及如下反应(忽略
 与
与 的相互转化):
的相互转化):Ⅰ.

Ⅱ.
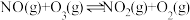
Ⅲ.

①恒温恒容条件下,反应塔中
 ,反应
,反应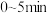 内测得
内测得 ,则
,则 末时NO的转化率为
末时NO的转化率为②保持反应塔中起始浓度
 ,在相同时间内,测得吸收塔中脱硝率、脱硫率与
,在相同时间内,测得吸收塔中脱硝率、脱硫率与 的关系曲线如图所示:
的关系曲线如图所示:
表示脱硫率的曲线是
③在某恒容密闭容器中充入一定量的
 ,发生上述反应Ⅰ、Ⅱ、Ⅲ,下列说法错误的是
,发生上述反应Ⅰ、Ⅱ、Ⅲ,下列说法错误的是a.升高温度,化学反应速率加快
b.容器中混合气体的密度不变说明反应达到平衡状态
c.容器中混合气体的压强不变说明反应达到平衡状态
d.容器中混合气体的颜色不变说明反应达到平衡状态
e.缩小容器的容积,压强增大,脱硝率和脱硫率均不变
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐1】治理汽车尾气和燃煤尾气是环境保护的重要课题.请回答下列问题:
(1)在汽车排气系统中安装三元催化转化器,可发生反应:2NO(g)+2CO(g) 2CO2(g)+N2(g).在恒容密闭容器中通入等量的CO和NO,发生上述反应时,c(CO)随温度(T)和时间(t)的变化曲线如图所示.
2CO2(g)+N2(g).在恒容密闭容器中通入等量的CO和NO,发生上述反应时,c(CO)随温度(T)和时间(t)的变化曲线如图所示.
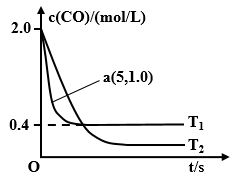
①据此判断该反应的正反应为____ (填“放热”或“吸热”)反应.
②温度T1时,该反应的平衡常数K=_____ ;反应速率v=v(正)-v(逆)=k正c2(NO)c2(CO)- k逆c2(CO2)c(N2),k正、k逆分别为正、逆反应速率常数,计算a处v(正):v(逆)=________ .
(2)下图流程是一种新型的除去尾气中氮氧化物的技术,一般采用氨气或尿素作还原剂
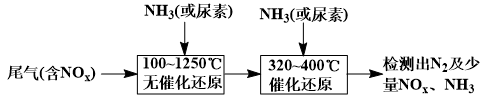
该技术中用尿素[CO(NH2)2]作还原剂还原NO2的主要反应为:4CO(NH2)2+6NO2 4CO2+7N2+8H2O ,则用NH3作还原剂还原尾气中NO(NH3、NO的物质的量之比为1:1)的化学方程式为:
4CO2+7N2+8H2O ,则用NH3作还原剂还原尾气中NO(NH3、NO的物质的量之比为1:1)的化学方程式为:______ .
(3)哈伯法合成氨的流程图如图,下列五个流程中为提高原料利用率而采取的措施________ (填序号)
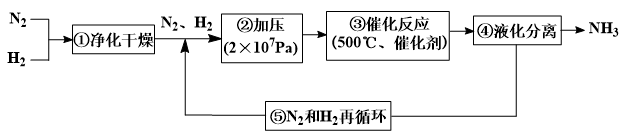
(4)一种电化学制备NH3的装置如图所示,图中陶瓷在高温时可以传输H+.下列叙述正确的是______________ (填选项)

A.Pd电极b为阴极 B.阴极的反应式为N2+6H++6e-=2NH3
C.H+由阳极向阴极迁移 D.陶瓷可以隔离N2和H2
(5)也可用CH4催化还原NOx法消除烟气中氮氧化物的污染.已知:
①CH4(g)+ 2NO2(g)= N2(g)+CO2(g)+2H2O(g) △H=-867.0kJ/mol;
②N2(g)+2O2(g)= 2NO2(g) △H=+67.0 kJ/mol;
③N2(g)+O2(g)=2NO(g) △H=+89.0 kJ/mol
则CH4催化还原NO的热化学方程式为__________________________________ .
(1)在汽车排气系统中安装三元催化转化器,可发生反应:2NO(g)+2CO(g)
 2CO2(g)+N2(g).在恒容密闭容器中通入等量的CO和NO,发生上述反应时,c(CO)随温度(T)和时间(t)的变化曲线如图所示.
2CO2(g)+N2(g).在恒容密闭容器中通入等量的CO和NO,发生上述反应时,c(CO)随温度(T)和时间(t)的变化曲线如图所示.
①据此判断该反应的正反应为
②温度T1时,该反应的平衡常数K=
(2)下图流程是一种新型的除去尾气中氮氧化物的技术,一般采用氨气或尿素作还原剂

该技术中用尿素[CO(NH2)2]作还原剂还原NO2的主要反应为:4CO(NH2)2+6NO2
 4CO2+7N2+8H2O ,则用NH3作还原剂还原尾气中NO(NH3、NO的物质的量之比为1:1)的化学方程式为:
4CO2+7N2+8H2O ,则用NH3作还原剂还原尾气中NO(NH3、NO的物质的量之比为1:1)的化学方程式为:(3)哈伯法合成氨的流程图如图,下列五个流程中为提高原料利用率而采取的措施

(4)一种电化学制备NH3的装置如图所示,图中陶瓷在高温时可以传输H+.下列叙述正确的是

A.Pd电极b为阴极 B.阴极的反应式为N2+6H++6e-=2NH3
C.H+由阳极向阴极迁移 D.陶瓷可以隔离N2和H2
(5)也可用CH4催化还原NOx法消除烟气中氮氧化物的污染.已知:
①CH4(g)+ 2NO2(g)= N2(g)+CO2(g)+2H2O(g) △H=-867.0kJ/mol;
②N2(g)+2O2(g)= 2NO2(g) △H=+67.0 kJ/mol;
③N2(g)+O2(g)=2NO(g) △H=+89.0 kJ/mol
则CH4催化还原NO的热化学方程式为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐2】CO、CO2是火力发电厂释放出的主要尾气,为减少对环境造成的影响,发电厂试图采用以下方法将其资源化利用,重新获得燃料或重要工业产品。
(1)CO与Cl2在催化剂的作用下合成光气(COCl2)。某温度下,向2L的密闭容器中投入一定量的CO和Cl2,在催化剂的作用下发生反应:CO(g)+Cl2(g) COCl2(g) ΔH =a kJ/mol反应过程中测定的部分数据如下表:
COCl2(g) ΔH =a kJ/mol反应过程中测定的部分数据如下表:
①反应0~2min末的平均速率v(COCl2)=_______ mol/(L·min)。
②在2min~4min间,v(Cl2)正______ v(Cl2)逆 (填“>”、“=”或“<”), 该温度下K =_______ L/ mol。
③已知X、L可分别代表温度或压强,如图表示L一定时,CO的转化率随X的变化关系。
X代表的物理量是__________ ;a_________ 0 (填“>”,“=”,“<”)。

(2)在催化剂作用下NO和CO转化为无毒气体:
2CO(g)+2NO(g) 2CO2(g)+N2(g) ΔH=-748 kJ·mol-1
2CO2(g)+N2(g) ΔH=-748 kJ·mol-1
①一定条件下,单位时间内不同温度下测定的NO转化率如图1所示。温度高于710K时,随温度的升高NO转化率降低的原因可能是____________________ 。
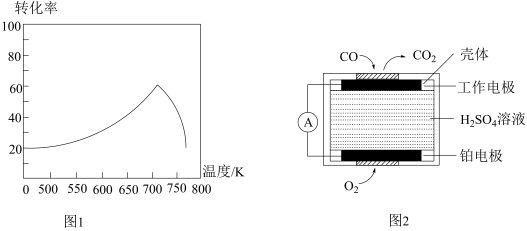
②已知:测定空气中NO和CO含量常用的方法有两种,方法1:电化学气敏传感器法。其中CO传感器的工作原理如图2所示,则工作电极的反应式为________________ ;方法2:氧化还原滴定法。用H2O2溶液吸收尾气,将氮氧化物转化为强酸,用酸碱中和滴定法测定强酸浓度。写出NO与H2O2溶液反应的离子方程式______________________ 。
(3)一定条件下,将CO和H2充入2L密闭容器中反应,可生成甲醚(CH3OCH3)。
4H2(g)+2CO(g) CH3OCH3(g)+H2O(g) △H<0
CH3OCH3(g)+H2O(g) △H<0
下列能判断反应达到平衡的是_______________ 。
A.υ(H2)=2υ(CO) B.容器内的压强不变
C.混合气体的密度不变 D.混合气体的平均相对分子质量不变
E.甲醚的浓度保持不变
(1)CO与Cl2在催化剂的作用下合成光气(COCl2)。某温度下,向2L的密闭容器中投入一定量的CO和Cl2,在催化剂的作用下发生反应:CO(g)+Cl2(g)
 COCl2(g) ΔH =a kJ/mol反应过程中测定的部分数据如下表:
COCl2(g) ΔH =a kJ/mol反应过程中测定的部分数据如下表:t/min | n(CO)/mol | n(Cl2)/mol |
0 | 1.2 | 0.6 |
1 | 0.9 | |
2 | 0.8 | |
4 | 0.2 |
①反应0~2min末的平均速率v(COCl2)=
②在2min~4min间,v(Cl2)正
③已知X、L可分别代表温度或压强,如图表示L一定时,CO的转化率随X的变化关系。
X代表的物理量是

(2)在催化剂作用下NO和CO转化为无毒气体:
2CO(g)+2NO(g)
 2CO2(g)+N2(g) ΔH=-748 kJ·mol-1
2CO2(g)+N2(g) ΔH=-748 kJ·mol-1①一定条件下,单位时间内不同温度下测定的NO转化率如图1所示。温度高于710K时,随温度的升高NO转化率降低的原因可能是

②已知:测定空气中NO和CO含量常用的方法有两种,方法1:电化学气敏传感器法。其中CO传感器的工作原理如图2所示,则工作电极的反应式为
(3)一定条件下,将CO和H2充入2L密闭容器中反应,可生成甲醚(CH3OCH3)。
4H2(g)+2CO(g)
 CH3OCH3(g)+H2O(g) △H<0
CH3OCH3(g)+H2O(g) △H<0下列能判断反应达到平衡的是
A.υ(H2)=2υ(CO) B.容器内的压强不变
C.混合气体的密度不变 D.混合气体的平均相对分子质量不变
E.甲醚的浓度保持不变
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐3】氯气是一种重要的化工原料。
(1)工业生产氯化物通常用由氧化物经氯化作用生成的方法,例如工业上常采用“加碳氯化”的方法以高钛渣(主要成分为 )为原料生产
)为原料生产 。
。
已知:
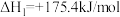 ;
;
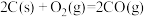
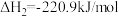 。
。
沸腾炉中“加碳氯化”生成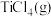 和
和 的热化学方程式:
的热化学方程式:___________ 。
(2) 合成有机物时会产生副产物
合成有机物时会产生副产物 。利用反应
。利用反应 可实现氯的循环利用。
可实现氯的循环利用。
①该反应的
___________ 0(填“>”“<”或“=”)。
②若反应物按物质的量 (
(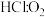 )在体积不变的密闭容器中发生该反应,下列叙述正确的是
)在体积不变的密闭容器中发生该反应,下列叙述正确的是___________ (填字母)。
A.当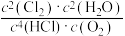 不变时,说明反应已达到平衡状态
不变时,说明反应已达到平衡状态
B.当 时,说明反应已达到平衡状态
时,说明反应已达到平衡状态
C.平衡后,继续按 的物质的量之比投入
的物质的量之比投入 和
和 ,再次达到新平衡时,
,再次达到新平衡时, 的转化率增大
的转化率增大
D.平衡后,分离出 ,可以提高
,可以提高 的平衡产率,并加快正反应速率
的平衡产率,并加快正反应速率
③下图是在两个不同温度 和
和 下,改变
下,改变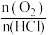 时
时 在平衡混合物中的体积分数的变化规律曲线。下列叙述正确的是
在平衡混合物中的体积分数的变化规律曲线。下列叙述正确的是___________ (填字母)。

A.a点未达到平衡,c点一定已经平衡
B.平衡常数: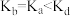
C.达到平衡时 的转化率大小为a>b>c
的转化率大小为a>b>c
D.若平衡常数K值变大,达新平衡前 始终减小
始终减小
(3)在一定温度下,以 为催化剂,氯苯(
为催化剂,氯苯(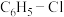 )和
)和 在
在 中发生平行反应,分别生成邻二氯苯(A)和对二氯苯(B),其反应的化学方程式如下:
中发生平行反应,分别生成邻二氯苯(A)和对二氯苯(B),其反应的化学方程式如下:
i.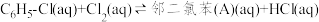
ii.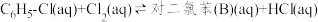
向盛有 含有
含有 的
的 的容器中加入
的容器中加入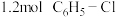 和
和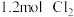 发生反应,忽略
发生反应,忽略 溶液体积的变化,达到平衡时生成邻二氯苯(A)和对二氯苯(B)的物质的量(n)随时间(t)变化的曲线如图所示。
溶液体积的变化,达到平衡时生成邻二氯苯(A)和对二氯苯(B)的物质的量(n)随时间(t)变化的曲线如图所示。

①该温度下,反应ii的化学平衡常数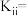
___________ 。
②工业生产上,提高生成邻二氯苯(A)反应选择性的关键因素是选择合适的___________ 。
(1)工业生产氯化物通常用由氧化物经氯化作用生成的方法,例如工业上常采用“加碳氯化”的方法以高钛渣(主要成分为
 )为原料生产
)为原料生产 。
。已知:

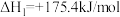 ;
;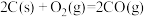
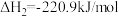 。
。沸腾炉中“加碳氯化”生成
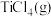 和
和 的热化学方程式:
的热化学方程式:(2)
 合成有机物时会产生副产物
合成有机物时会产生副产物 。利用反应
。利用反应 可实现氯的循环利用。
可实现氯的循环利用。①该反应的

②若反应物按物质的量
 (
(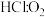 )在体积不变的密闭容器中发生该反应,下列叙述正确的是
)在体积不变的密闭容器中发生该反应,下列叙述正确的是A.当
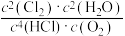 不变时,说明反应已达到平衡状态
不变时,说明反应已达到平衡状态B.当
 时,说明反应已达到平衡状态
时,说明反应已达到平衡状态C.平衡后,继续按
 的物质的量之比投入
的物质的量之比投入 和
和 ,再次达到新平衡时,
,再次达到新平衡时, 的转化率增大
的转化率增大D.平衡后,分离出
 ,可以提高
,可以提高 的平衡产率,并加快正反应速率
的平衡产率,并加快正反应速率③下图是在两个不同温度
 和
和 下,改变
下,改变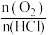 时
时 在平衡混合物中的体积分数的变化规律曲线。下列叙述正确的是
在平衡混合物中的体积分数的变化规律曲线。下列叙述正确的是
A.a点未达到平衡,c点一定已经平衡
B.平衡常数:
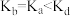
C.达到平衡时
 的转化率大小为a>b>c
的转化率大小为a>b>cD.若平衡常数K值变大,达新平衡前
 始终减小
始终减小(3)在一定温度下,以
 为催化剂,氯苯(
为催化剂,氯苯(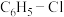 )和
)和 在
在 中发生平行反应,分别生成邻二氯苯(A)和对二氯苯(B),其反应的化学方程式如下:
中发生平行反应,分别生成邻二氯苯(A)和对二氯苯(B),其反应的化学方程式如下:i.
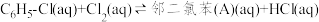
ii.
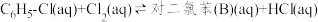
向盛有
 含有
含有 的
的 的容器中加入
的容器中加入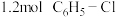 和
和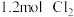 发生反应,忽略
发生反应,忽略 溶液体积的变化,达到平衡时生成邻二氯苯(A)和对二氯苯(B)的物质的量(n)随时间(t)变化的曲线如图所示。
溶液体积的变化,达到平衡时生成邻二氯苯(A)和对二氯苯(B)的物质的量(n)随时间(t)变化的曲线如图所示。
①该温度下,反应ii的化学平衡常数
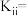
②工业生产上,提高生成邻二氯苯(A)反应选择性的关键因素是选择合适的
您最近一年使用:0次

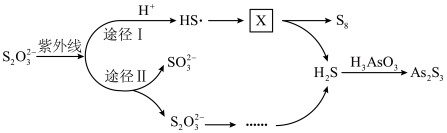
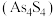 和雌黄
和雌黄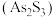 等形式存在,工业上常用雌黄制成浆状,通入
等形式存在,工业上常用雌黄制成浆状,通入 和单质硫。
和单质硫。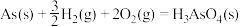

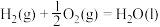

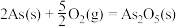

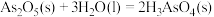 的
的
 去除酸性废水中
去除酸性废水中 的机理如下(“HS·”为自由基,“。”表示孤电子),方框中
的机理如下(“HS·”为自由基,“。”表示孤电子),方框中 的化学式为
的化学式为