名校
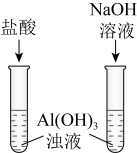
1 . 下列装置或操作能达到实验目的的是
| 装置或操作 |
|
|
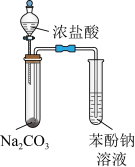
| 目的 | A.证明铝元素既有金属性又有非金属性 | B.验证碳酸的酸性比苯酚的强 |
| 装置或操作 |
|
|
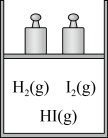
| 目的 | C.验证改变压强能破坏化学平衡状态 | D.鉴别苯和己烷 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
2 . 工业上利用“碘循环”吸收 ,同时制得
,同时制得 ,流程如图所示。下列说法正确的是
,流程如图所示。下列说法正确的是
 ,同时制得
,同时制得 ,流程如图所示。下列说法正确的是
,流程如图所示。下列说法正确的是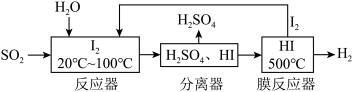
A.反应器中发生的反应离子方程式为: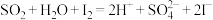 |
B.反应器中控制温度的目的是增大 的溶解度以加快吸收 的溶解度以加快吸收 |
| C.分离器中物质分离的方法为蒸馏 |
| D.膜反应器中,增大压强有利于提高平衡转化率 |
您最近半年使用:0次
名校
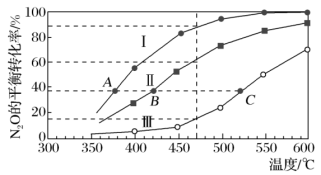
3 . 现有反应2N2O(g) 2N2(g)+O2(g),在四个恒容密闭容器中按下表充入气体进行反应,容器Ⅰ、Ⅱ、Ⅲ中N2O的平衡转化率如图所示。下列说法正确的是
2N2(g)+O2(g),在四个恒容密闭容器中按下表充入气体进行反应,容器Ⅰ、Ⅱ、Ⅲ中N2O的平衡转化率如图所示。下列说法正确的是
 2N2(g)+O2(g),在四个恒容密闭容器中按下表充入气体进行反应,容器Ⅰ、Ⅱ、Ⅲ中N2O的平衡转化率如图所示。下列说法正确的是
2N2(g)+O2(g),在四个恒容密闭容器中按下表充入气体进行反应,容器Ⅰ、Ⅱ、Ⅲ中N2O的平衡转化率如图所示。下列说法正确的是| 容器 | 容积/L | 起始物质的量/mol | ||
| N2O | N2 | O2 | ||
| Ⅰ | V1 | 0.1 | 0 | 0 |
| Ⅱ | 1.0 | 0.1 | 0 | 0 |
| Ⅲ | V3 | 0.1 | 0 | 0 |
| Ⅳ | 1.0 | 0.06 | 0.06 | 0.04 |

| A.该反应的正反应放热 |
| B.相同温度下,起始反应速率:v(Ⅰ)>v(Ⅱ) |
| C.图中A、B、C三点处,三个容器内的压强:pA(Ⅰ)<pB(Ⅱ)<pC(Ⅲ) |
| D.若Ⅳ在470℃进行反应,反应逆向进行 |
您最近半年使用:0次
2024-02-03更新
|
119次组卷
|
2卷引用:北京市十一学校2022-2023学年高三下学期1月月考化学试题
名校
解题方法
4 . CO(g)+H2O(g)  CO2(g)+H2(g) ΔH<0,在其他条件不变的情况下,表述正确的是
CO2(g)+H2(g) ΔH<0,在其他条件不变的情况下,表述正确的是
 CO2(g)+H2(g) ΔH<0,在其他条件不变的情况下,表述正确的是
CO2(g)+H2(g) ΔH<0,在其他条件不变的情况下,表述正确的是| A.加入催化剂,改变了反应的途径,反应的ΔH也随之改变 |
| B.改变压强,平衡不发生移动,反应放出的热量不变 |
| C.升高温度,反应速率加快,反应放出的热量不变 |
| D.保持该容器不变,同时增加1molCO和1molH2O,达平衡时,H2体积分数增大 |
您最近半年使用:0次
2024-01-26更新
|
100次组卷
|
2卷引用:北京市第五十中学2022-2023学年高二上学期期中考试化学试题
5 . 氢气是一种清洁能源,氢气的制取与储存是氢能源利用领域的研究热点。
I.制取氢气
(1)甲醇和水蒸气制取氢气的过程中有下列反应:
CH3OH(g) CO(g)+2H2(g) △H=+91 kJ·mol-1
CO(g)+2H2(g) △H=+91 kJ·mol-1
CO(g)+H2O(g) CO2(g)+H2 (g) △H=-4lkJ·mol-1
CO2(g)+H2 (g) △H=-4lkJ·mol-1
写出以甲醇为原料制取氢气的热化学方程式___________ 。
(2)理论上,能提高H2平衡产率的措施有___________ (写出一条即可)。
II.储存氢气
硼氢化钠(NaBH4) 是研究最广泛的储氢材料之一;
已知: i.B的电负性为2.0 H的电负性为2.1
ii.25℃下NaBH4 在水中的溶解度为55g,NaBO2在水中的溶解度为0.28g
(3)向NaBH4 水溶液中加入催化剂Ru/NGR后,能够迅速反应,生成偏硼酸钠(NaBO2) 和氢气。写出该反应的化学方程式___________ 。
(4)在研究浓度对催化剂Ru/NGR 活性的影响时,发现B 点后(见下图)增加NaBH4的浓度,制氢速率反而下降,推断可能的原因是___________ 。

(5)用惰性电极电解NaBO2 溶液可制得NaBH4, 实现物质的循环使用,制备装置如图所示。
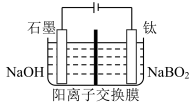
①钛电极的电极反应式是___________ ;
②电解过程中,阴极区溶液pH___________ 。(填“增大”“减小”或“不变”)
I.制取氢气
(1)甲醇和水蒸气制取氢气的过程中有下列反应:
CH3OH(g)
 CO(g)+2H2(g) △H=+91 kJ·mol-1
CO(g)+2H2(g) △H=+91 kJ·mol-1CO(g)+H2O(g)
 CO2(g)+H2 (g) △H=-4lkJ·mol-1
CO2(g)+H2 (g) △H=-4lkJ·mol-1写出以甲醇为原料制取氢气的热化学方程式
(2)理论上,能提高H2平衡产率的措施有
II.储存氢气
硼氢化钠(NaBH4) 是研究最广泛的储氢材料之一;
已知: i.B的电负性为2.0 H的电负性为2.1
ii.25℃下NaBH4 在水中的溶解度为55g,NaBO2在水中的溶解度为0.28g
(3)向NaBH4 水溶液中加入催化剂Ru/NGR后,能够迅速反应,生成偏硼酸钠(NaBO2) 和氢气。写出该反应的化学方程式
(4)在研究浓度对催化剂Ru/NGR 活性的影响时,发现B 点后(见下图)增加NaBH4的浓度,制氢速率反而下降,推断可能的原因是

(5)用惰性电极电解NaBO2 溶液可制得NaBH4, 实现物质的循环使用,制备装置如图所示。

①钛电极的电极反应式是
②电解过程中,阴极区溶液pH
您最近半年使用:0次
名校
6 . 气态醋酸中存在平衡:
 。实验测得压强分别
。实验测得压强分别 和
和 时,上述平衡体系中气体的平均摩尔质量(
时,上述平衡体系中气体的平均摩尔质量(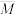 )随温度(T)的变化如下图所示。[已知:(
)随温度(T)的变化如下图所示。[已知:(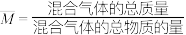 );
); ]
]
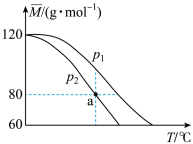
下列说法不正确 的是

 。实验测得压强分别
。实验测得压强分别 和
和 时,上述平衡体系中气体的平均摩尔质量(
时,上述平衡体系中气体的平均摩尔质量(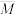 )随温度(T)的变化如下图所示。[已知:(
)随温度(T)的变化如下图所示。[已知:(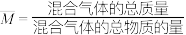 );
); ]
]
下列说法
A. |
B. |
C.a点时,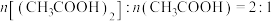 |
D.为了使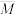 的值接近60,可采取高温、低压的实验条件 的值接近60,可采取高温、低压的实验条件 |
您最近半年使用:0次
7 . 对已经达到化学平衡状态的下列反应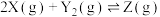
 ,减小容器体积时,对反应产生的影响是
,减小容器体积时,对反应产生的影响是
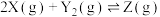
 ,减小容器体积时,对反应产生的影响是
,减小容器体积时,对反应产生的影响是| A.逆反应速率增大,正反应速率减小,平衡向逆反应方向移动 |
| B.逆反应速率减小,正反应速率增大,平衡向正反应方向移动 |
| C.正、逆反应速率都增大,平衡向逆反应方向移动 |
| D.正、逆反应速率都增大,平衡向正反应方向移动 |
您最近半年使用:0次
名校
8 . 二甲醚( )是重要的化工原料,可用水煤气(主要成分为CO和
)是重要的化工原料,可用水煤气(主要成分为CO和 )合成。其主要反应原理如下(a、b、c均为正值):
)合成。其主要反应原理如下(a、b、c均为正值):
①
 kJ⋅mol
kJ⋅mol
②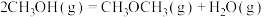
 kJ·mol
kJ·mol
③
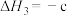 kJ⋅mol
kJ⋅mol
回答下列问题:
(1)总反应的热化学方程式: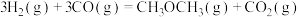

_______ kJ/mol。
(2)以下说法能说明反应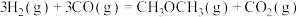 达到化学平衡状态的有
达到化学平衡状态的有_______ 。
a.恒温恒容条件下,气体的密度保持不变
b.恒温恒压条件下,气体的平均摩尔质量保持不变
c.绝热体系中,体系的温度保持不变
(3)生产二甲醚的过程中存在副反应: ,与甲醇脱水反应:
,与甲醇脱水反应: 形成竞争。将水煤气按一定进料比通入反应装置,选择合适的催化剂。在保持温度一定改变压强条件下测得二甲醚的选择性如下图所示。
形成竞争。将水煤气按一定进料比通入反应装置,选择合适的催化剂。在保持温度一定改变压强条件下测得二甲醚的选择性如下图所示。
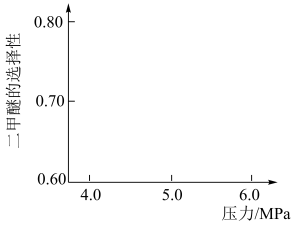
资料:二甲醚的选择性是指转化为二甲醚的CO在全部CO反应物中所占的比例。
分析:温度一定,随压强增大,二甲醚选择性增大的原因是_______ 。
 )是重要的化工原料,可用水煤气(主要成分为CO和
)是重要的化工原料,可用水煤气(主要成分为CO和 )合成。其主要反应原理如下(a、b、c均为正值):
)合成。其主要反应原理如下(a、b、c均为正值):①

 kJ⋅mol
kJ⋅mol
②
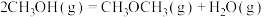
 kJ·mol
kJ·mol
③

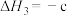 kJ⋅mol
kJ⋅mol
回答下列问题:
(1)总反应的热化学方程式:
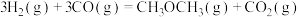

(2)以下说法能说明反应
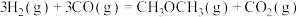 达到化学平衡状态的有
达到化学平衡状态的有a.恒温恒容条件下,气体的密度保持不变
b.恒温恒压条件下,气体的平均摩尔质量保持不变
c.绝热体系中,体系的温度保持不变
(3)生产二甲醚的过程中存在副反应:
 ,与甲醇脱水反应:
,与甲醇脱水反应: 形成竞争。将水煤气按一定进料比通入反应装置,选择合适的催化剂。在保持温度一定改变压强条件下测得二甲醚的选择性如下图所示。
形成竞争。将水煤气按一定进料比通入反应装置,选择合适的催化剂。在保持温度一定改变压强条件下测得二甲醚的选择性如下图所示。
资料:二甲醚的选择性是指转化为二甲醚的CO在全部CO反应物中所占的比例。
分析:温度一定,随压强增大,二甲醚选择性增大的原因是
您最近半年使用:0次
名校
解题方法
9 . 甲醇是重要的化工原料,发展前景广阔。研究表明CO2加氢可以合成甲醇。CO2和H2可发生如下两个反应:
Ⅰ.

Ⅱ.

(1)有利于提高反应Ⅰ中CO2的平衡转化率的措施有______ (填序号)。
a.使用催化剂 b.加压 c.增大CO2和H2的初始投料比
(2)研究温度对于甲醇产率的影响。在210℃~290℃,保持原料气中CO2和H2的投料比不变,按一定流速通过催化剂甲,主要发生反应Ⅰ,得到甲醇的实际产率、平衡产率与温度的关系如图。
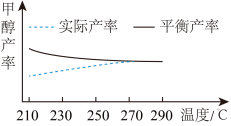
则
______ 0(填>、=或<),其依据是____________________ 。
(3)某实验控制压强一定,CO2和H2初始投料比一定,按一定流速通过催化剂乙,经过相同时间测得如下实验数据(反应未达到平衡状态)
(注:甲醇选择性是指转化的CO2中生成甲醇的百分比)
表中实验数据表明,升高温度,CO2的实际转化率提高而甲醇的选择性降低,其原因是_____________ 。
Ⅰ.


Ⅱ.


(1)有利于提高反应Ⅰ中CO2的平衡转化率的措施有
a.使用催化剂 b.加压 c.增大CO2和H2的初始投料比
(2)研究温度对于甲醇产率的影响。在210℃~290℃,保持原料气中CO2和H2的投料比不变,按一定流速通过催化剂甲,主要发生反应Ⅰ,得到甲醇的实际产率、平衡产率与温度的关系如图。

则

(3)某实验控制压强一定,CO2和H2初始投料比一定,按一定流速通过催化剂乙,经过相同时间测得如下实验数据(反应未达到平衡状态)
T(K) | CO2实际转化率(%) | 甲醇选择性(%)注 |
543 | 12.3 | 42.3 |
553 | 15.3 | 39.1 |
表中实验数据表明,升高温度,CO2的实际转化率提高而甲醇的选择性降低,其原因是
您最近半年使用:0次
名校
10 . 在某容积一定的密闭容器中,有下列可逆反应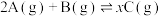 ,反应曲线(T表示温度,p表示压强,C%表示C的体积分数)如图Ⅰ、Ⅱ所示,试判断下列说法正确的是
,反应曲线(T表示温度,p表示压强,C%表示C的体积分数)如图Ⅰ、Ⅱ所示,试判断下列说法正确的是
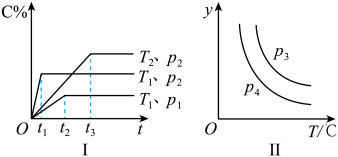
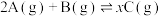 ,反应曲线(T表示温度,p表示压强,C%表示C的体积分数)如图Ⅰ、Ⅱ所示,试判断下列说法正确的是
,反应曲线(T表示温度,p表示压强,C%表示C的体积分数)如图Ⅰ、Ⅱ所示,试判断下列说法正确的是
A. | B.该反应 , , |
C. ,y轴表示B的平衡转化率 ,y轴表示B的平衡转化率 | D.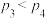 ,y轴表示混合气体的密度 ,y轴表示混合气体的密度 |
您最近半年使用:0次