在一定温度和催化剂的条件下,将(0.1mol NH3通入3L的恒容密闭容器中进行反应2NH3(g)=N2(g)+3H2(g)(初始容器内总压为200kPa),各物质的分压随时间的变化曲线如下图所示。下列说法错误的是


A.用H2的浓度变化表示0~t1时间内的反应速率v(H2)=0.02/t1mol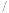 (L·min) (L·min) |
| B.混合气体的平均相对分子质量不再改变时,反应达平衡 |
| C.在该温度下的压强平衡常数为4800(kPa)2 |
| D.若t2时将容器体积迅速缩小至原来的一半,N2分压变化趋势的曲线是a |
更新时间:2024-01-22 07:53:01
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】一定温度下,向一个容积为3L的真空密闭容器中通入1molN2和3molH2,2min后,测得容器内的压强是开始时的0.8倍,则这段时间内V(H2)为( )
| A.0.2mol/(L·min) | B.0.6mol/(L·min) |
| C.0.1mol/(L·min) | D.0.3mol/(L·min) |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】在一定温度下,将 和
和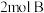 放入容积为
放入容积为 的某密闭容器中发生反应:
的某密闭容器中发生反应: 。
。 后达到平衡,测得容器内C的浓度为
后达到平衡,测得容器内C的浓度为 ,则下列叙述不正确的是
,则下列叙述不正确的是
 和
和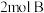 放入容积为
放入容积为 的某密闭容器中发生反应:
的某密闭容器中发生反应: 。
。 后达到平衡,测得容器内C的浓度为
后达到平衡,测得容器内C的浓度为 ,则下列叙述不正确的是
,则下列叙述不正确的是A.在 内该反应用D的浓度变化表示的反应速率为 内该反应用D的浓度变化表示的反应速率为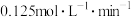 |
| B.平衡时A的转化率为25% |
| C.平衡时B的体积分数约为50% |
D.初始时的压强与平衡时的压强之比为 |
您最近半年使用:0次
单选题
|
适中
(0.65)
【推荐3】用 溶液氧化废水中的还原性污染物M,为研究降解效果,设计如下对比实验探究温度、浓度、pH对降解速率和效果的影响,实验测得M的浓度与时间的关系如图所示:
溶液氧化废水中的还原性污染物M,为研究降解效果,设计如下对比实验探究温度、浓度、pH对降解速率和效果的影响,实验测得M的浓度与时间的关系如图所示:
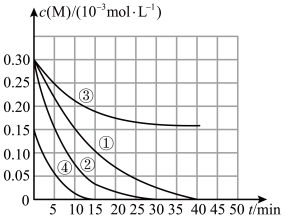
下列说法正确的是
 溶液氧化废水中的还原性污染物M,为研究降解效果,设计如下对比实验探究温度、浓度、pH对降解速率和效果的影响,实验测得M的浓度与时间的关系如图所示:
溶液氧化废水中的还原性污染物M,为研究降解效果,设计如下对比实验探究温度、浓度、pH对降解速率和效果的影响,实验测得M的浓度与时间的关系如图所示:实验编号 | 温度/ºC | pH |
① | 25 | 1 |
② | 45 | 1 |
③ | 25 | 7 |
④ | 25 | 1 |

下列说法正确的是
A.实验①中0~15min内M的降解速率为 |
| B.若其他条件相同,则实验①②说明升高温度,M的降解速率增大 |
| C.若其他条件相同,则实验①③说明pH越大,越有利于M的降解 |
| D.若其他条件相同,则实验①④说明M的浓度越小,降解的速率越快 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】向绝热恒容密闭容器中通入 和
和 ,在一定条件下发生反应
,在一定条件下发生反应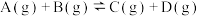 ,正反应速率随时间变化的示意图如图,下列结论正确的是
,正反应速率随时间变化的示意图如图,下列结论正确的是
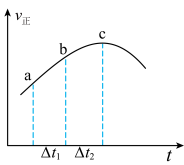
 和
和 ,在一定条件下发生反应
,在一定条件下发生反应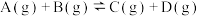 ,正反应速率随时间变化的示意图如图,下列结论正确的是
,正反应速率随时间变化的示意图如图,下列结论正确的是
A.气体 的浓度: 的浓度: 点小于 点小于 点 点 |
B.当 时,气体C的生成量:ab段小于bc段 时,气体C的生成量:ab段小于bc段 |
C. 点时: 点时: |
| D.体系压强不再变化,不能说明反应达到平衡状态 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】氮是生命的基础,氮及其化合物在生产生活中具有广泛应用。工业上用氨的催化氧化生产硝酸,其热化学方程式为4NH3(g)+5O2(g)  4NO(g)+6H2O(g)ΔH=-904 kJ·mol-1。生产硝酸的尾气中主要含有NO、NO2等大气污染物,可用石灰浆等碱性溶液吸收处理,并得到Ca(NO3)2、Ca(NO2)2等化工产品。对于反应4NH3(g)+5O2(g)
4NO(g)+6H2O(g)ΔH=-904 kJ·mol-1。生产硝酸的尾气中主要含有NO、NO2等大气污染物,可用石灰浆等碱性溶液吸收处理,并得到Ca(NO3)2、Ca(NO2)2等化工产品。对于反应4NH3(g)+5O2(g)  4NO(g)+6H2O(g),下列有关说法
4NO(g)+6H2O(g),下列有关说法不 正确的是
 4NO(g)+6H2O(g)ΔH=-904 kJ·mol-1。生产硝酸的尾气中主要含有NO、NO2等大气污染物,可用石灰浆等碱性溶液吸收处理,并得到Ca(NO3)2、Ca(NO2)2等化工产品。对于反应4NH3(g)+5O2(g)
4NO(g)+6H2O(g)ΔH=-904 kJ·mol-1。生产硝酸的尾气中主要含有NO、NO2等大气污染物,可用石灰浆等碱性溶液吸收处理,并得到Ca(NO3)2、Ca(NO2)2等化工产品。对于反应4NH3(g)+5O2(g)  4NO(g)+6H2O(g),下列有关说法
4NO(g)+6H2O(g),下列有关说法| A.该反应一定能自发进行 |
| B.该反应的正反应的活化能小于逆反应的活化能 |
| C.断裂1mol N—H键的同时断裂1molO—H键,说明该反应达到平衡状态 |
| D.达到平衡时,增大容器的体积,v(正)增加、v(逆)减小 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐3】恒温恒容的密闭容器中,在某催化剂表面上发生三氧化硫的分解反应:
 ,测得不同起始浓度和催化剂表面积下三氧化硫浓度随时间的变化,如表所示,下列说法不正确的是
,测得不同起始浓度和催化剂表面积下三氧化硫浓度随时间的变化,如表所示,下列说法不正确的是

 ,测得不同起始浓度和催化剂表面积下三氧化硫浓度随时间的变化,如表所示,下列说法不正确的是
,测得不同起始浓度和催化剂表面积下三氧化硫浓度随时间的变化,如表所示,下列说法不正确的是| 编号 | 时间/min
表面积/  | 0 | 20 | 40 | 60 | 80 |
| ① | x | 2.40 | 2.00 | 1.70 | 1.46 | 1.24 |
| ② | 2x | 1.20 | 0.80 | 0.56 | 0.46 | 0.40 |
| ③ | 2x | 2.40 | 1.40 | 0.70 | 0.40 | 0.40 |
A.实验①,0~20min的平均速率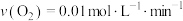 |
B.实验②,到达平衡状态时,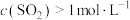 |
| C.其他条件不变,向容器中充入He增大压强,反应速率增大 |
D.此温度下,该反应的平衡常数为 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】在三个相同容器中各充入1molN2和3molH2,在不同条件下反应达到平衡,氨的体积分数随时间变化的曲线如图所示。下列说法中正确的是
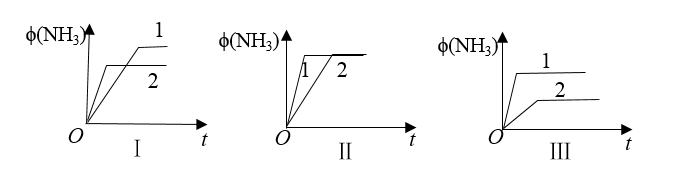

| A.图Ⅰ可能是不同压强对反应的影响,且p2>p1 |
| B.图Ⅱ可能是不同压强对反应的影响,且p1>p2 |
| C.图Ⅲ可能是不同温度对反应的影响,且T1>T2 |
| D.图Ⅱ可能是同温同压下不同催化剂对反应的影响,且催化剂性能1>2 |
您最近半年使用:0次
单选题
|
适中
(0.65)
【推荐2】一定条件下,发生反应: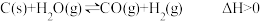 达到平衡后,下列说法错误的是
达到平衡后,下列说法错误的是
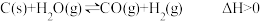 达到平衡后,下列说法错误的是
达到平衡后,下列说法错误的是| A.其它条件不变,升高温度,v(正)增大的程度比v(逆)增大的程度大,平衡向右移动 |
| B.恒温恒容条件下,充入稀有气体,v(正)、v(逆)不变,平衡不移动 |
| C.其它条件不变,增大压强,v(正)、v(逆)同倍数增大,平衡不移动 |
| D.恒温恒容条件下,加入碳粉,v(正)不变,v(逆)不变,平衡不移动 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】下列方案设计、现象和结论都正确的是
| 目的 | 方案设计 | 现象与结论 | |
| A | 验证压强对化学平衡的影响 | 先将注射器充满NO2气体,然后将活塞往里推压缩体积 | 观察到注射器内气体颜色加深,证明加压平衡朝生成NO2气体的方向移动 |
| B | 铜的电解精炼 | 待精炼的铜和纯铜连接外加直流电源的阳极和阴极,用硫酸铜溶液作电解质电解 | 阳极上铜逐渐溶解,阴极上铜逐渐析出,硫酸铜溶液浓度保持不变 |
| C | 制备[Cu(NH3)4]SO4·H2O晶体 | 向4mL 0.1mol/LCuSO4溶液中滴加氨水,先形成难溶物,并继续滴加沉淀溶解,然后蒸发溶剂析出晶体 | 反应过程中,NH3的N给出孤对电子,Cu2+接受电子对,形成了稳定的配位键[Cu(NH3)4]2+ |
| D | 除去锅炉水垢中的CaSO4 | 先用碳酸钠溶液浸泡水垢,然后再用盐酸除去 | 利用Ksp(CaSO4)> Ksp(CaCO3),实现沉淀的转化 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】{Ti12O18}团簇是比较罕见的一个穴醚无机类似物,我国科学家通过将{Rb@Ti12O18}和Cs+反应,测定笼内Cs+的浓度,计算Cs+取代Rb+反应的平衡常数(Keq),反应示意图和所测数据如图。有关说法不正确 的是
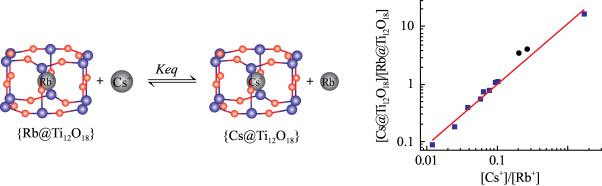
图中 表示平衡时铯离子浓度和铷离子浓度之比,其它类似
表示平衡时铯离子浓度和铷离子浓度之比,其它类似

图中
 表示平衡时铯离子浓度和铷离子浓度之比,其它类似
表示平衡时铯离子浓度和铷离子浓度之比,其它类似| A.离子半径:r(Cs+)>r(Rb+) |
| B.研究发现:Cs+的直径显著大于{Ti12O18}团簇表面的孔径且{Ti12O18}的骨架结构在Cs+交换过程中没有被破坏。据此推断:{Ti12O18}团簇表面的孔是柔性的 |
| C.Keq≈0.1 |
| D.{Ti12O18}团簇对于Cs+具有比Rb+大的亲和力 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】一定条件下,反应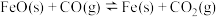 的平衡常数为0.5,在体积为2L的容器中充入
的平衡常数为0.5,在体积为2L的容器中充入
 、
、
 发生上述反应直至达到平衡,下列说法正确的是
发生上述反应直至达到平衡,下列说法正确的是
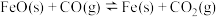 的平衡常数为0.5,在体积为2L的容器中充入
的平衡常数为0.5,在体积为2L的容器中充入
 、
、
 发生上述反应直至达到平衡,下列说法正确的是
发生上述反应直至达到平衡,下列说法正确的是A.该反应的平衡常数的表达式为: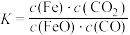 |
| B.CO的平衡转化率为80% |
C.达到平衡时再充入 和 和 各 各 ,平衡正向移动 ,平衡正向移动 |
| D.保持温度不变,将体系体积压缩,正、逆反应速率均加快而反应限度不变 |
您最近半年使用:0次

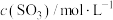
 充入
充入 和
和 ,发生反应:
,发生反应: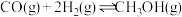 ,测得平衡混合物中
,测得平衡混合物中 的体积分数在不同压强下随温度的变化情况如图所示。下列说法正确的是
的体积分数在不同压强下随温度的变化情况如图所示。下列说法正确的是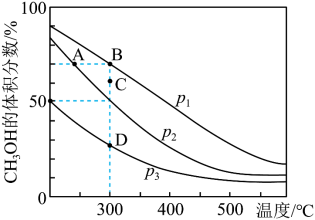

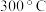 时,该反应的平衡常数
时,该反应的平衡常数
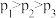
 、温度为
、温度为


