名校
1 . 在T℃时,向1L固定体积的密闭容器M中加入2molX和1molY,发生如下反应: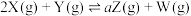
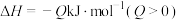 ;该反应达到平衡后,放出的热量为
;该反应达到平衡后,放出的热量为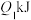 ,物质X的转化率为
,物质X的转化率为 ;若平衡后再升高温度,混合气体的平均相对分子质量减小。
;若平衡后再升高温度,混合气体的平均相对分子质量减小。
请回答下列问题:
(1)化学计量数 的值为
的值为___________ 。
(2)下列能说明该反应达到了化学平衡状态的是___________ 。
a.容器内压强一定
b.容器内气体的密度一定
c.容器内Z的分子数一定
d.容器内气体的质量一定
(3)维持T℃温度不变,若起始时向容器M中加入2molX、1molY和1molAr(稀有气体不参与反应),则反应达到平衡后放出的热量是___________ 。
(4)维持T℃温度不变,若在一个和原容器体积相等的恒压容器N中加入2molX和1molY,发生题给反应并达到平衡,则___________ (填“M”或“N”)容器中的反应先达到平衡状态,容器中X的质量分数M___________ N(填“>”、“<”或“=”)。
(5)已知:该反应的平衡常数随温度的变化情况如表所示:
若在某温度下,2molX和1molY在容器M中反应并达到平衡,X的平衡转化率为50%,则该温度为___________ ℃。
(6)维持T℃温度不变,若起始时向容器M中加入4molX和6molY,反应达到平衡时容器内的分子数目减少10%,则反应中放出的热量为___________ kJ。
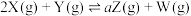
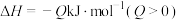 ;该反应达到平衡后,放出的热量为
;该反应达到平衡后,放出的热量为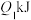 ,物质X的转化率为
,物质X的转化率为 ;若平衡后再升高温度,混合气体的平均相对分子质量减小。
;若平衡后再升高温度,混合气体的平均相对分子质量减小。请回答下列问题:
(1)化学计量数
 的值为
的值为(2)下列能说明该反应达到了化学平衡状态的是
a.容器内压强一定
b.容器内气体的密度一定
c.容器内Z的分子数一定
d.容器内气体的质量一定
(3)维持T℃温度不变,若起始时向容器M中加入2molX、1molY和1molAr(稀有气体不参与反应),则反应达到平衡后放出的热量是
(4)维持T℃温度不变,若在一个和原容器体积相等的恒压容器N中加入2molX和1molY,发生题给反应并达到平衡,则
(5)已知:该反应的平衡常数随温度的变化情况如表所示:
| 温度/℃ | 200 | 250 | 300 | 350 |
| 平衡常数K | 9.94 | 5.2 | 1 | 0.5 |
(6)维持T℃温度不变,若起始时向容器M中加入4molX和6molY,反应达到平衡时容器内的分子数目减少10%,则反应中放出的热量为
您最近半年使用:0次
2023-05-30更新
|
73次组卷
|
2卷引用:河南省南阳市镇平县第一高级中学2022-2023学年高二下学期5月月考化学试题
2023高三·全国·专题练习
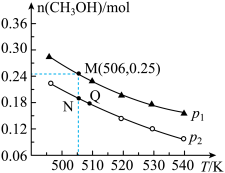
2 . 由CO2和H2合成CH3OH 的反应如下:CO2(g)+3H2(g)  CH3OH(g)+H2O(g) ΔH,在10L的恒容密闭容器中投入1molCO2和2.75molH2,在不同条件下发生上述反应,测得平衡时甲醇的物质的量随温度、压强的变化如图所示,则反应的ΔH
CH3OH(g)+H2O(g) ΔH,在10L的恒容密闭容器中投入1molCO2和2.75molH2,在不同条件下发生上述反应,测得平衡时甲醇的物质的量随温度、压强的变化如图所示,则反应的ΔH___________ (填“> ”或“<”),判断理由是___________ 。图中压强p1___________ ( “>”或“<”)p2,N点时,该反应的平衡常数K=___________ (计算结果保留2位小数)。
 CH3OH(g)+H2O(g) ΔH,在10L的恒容密闭容器中投入1molCO2和2.75molH2,在不同条件下发生上述反应,测得平衡时甲醇的物质的量随温度、压强的变化如图所示,则反应的ΔH
CH3OH(g)+H2O(g) ΔH,在10L的恒容密闭容器中投入1molCO2和2.75molH2,在不同条件下发生上述反应,测得平衡时甲醇的物质的量随温度、压强的变化如图所示,则反应的ΔH
您最近半年使用:0次
22-23高一下·上海·期末
3 . 工业合成氨
(1)合成氨的适宜条件探究:N2(g)+3H2(g) 2NH3(g) + Q(Q>0)
2NH3(g) + Q(Q>0)
∴合成氨的合理生产条件:① 使用___________ 为催化剂 ②一定程度的加压 ③温度控制在催化剂的活性温度(500℃) ④及时分离___________
(1)合成氨的适宜条件探究:N2(g)+3H2(g)
 2NH3(g) + Q(Q>0)
2NH3(g) + Q(Q>0)| 反应条件 | 对化学反应速率的影响 | 对平衡混合物中NH3含量的影响 | 化学反应速率与化学平衡综合考虑 |
| 增大压强 | 影响一致,应 | ||
| 升高温度 | 影响 | ||
| 使用催化剂 | 用合适催化剂有利于加快反应速率 | ||
| 增加反应物浓度 | 平衡向 | 影响一致应 |
您最近半年使用:0次
名校
4 . 肼( )是一种应用广泛的化工原料。工业上先合成氨气:
)是一种应用广泛的化工原料。工业上先合成氨气:
 ,再进一步制备肼。完成下列填空:
,再进一步制备肼。完成下列填空:
(1)合成氨需要选择合适的催化剂,分别选用A、B、C三种催化剂进行试验,所得结果如图所示(其他条件相同),则生产中适宜选择的催化剂是_______ (填“A”或“B”或“C”)

(2)一定条件下,对在密闭容器中进行的合成氨反应达平衡后,其他条件不变时,若同时压缩容器的体积和升高温度达新平衡后,与原平衡相比,请将有关物理量的变化的情况填入下表中(填“增大”、“减小”或“无法确定”)
(3)通常把拆开1mol某化学键所吸收的能量看成该化学键的键能。已知部分化学键的键能如下:
发射神舟飞船的长征火箭用了肼( ,气态)为燃料,若它在氧气(气态)中燃烧,生成
,气态)为燃料,若它在氧气(气态)中燃烧,生成 (气态)和
(气态)和 (气态)。该反应的热化学方程式为:
(气态)。该反应的热化学方程式为:_______ 。
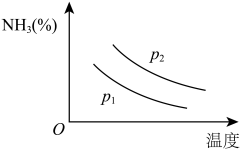
(4)氨主要用于生产化肥和硝酸。“十三五”期间,预计我国合成氨产量将保持稳中略增。下图是不同温度和不同压强下,反应达到平衡后,混合物中 含量(体积%)的变化情况,已知初始时
含量(体积%)的变化情况,已知初始时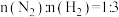 。判断
。判断 、
、 压强的大小关系,
压强的大小关系,
_______  (选填“>”、“<”或“=”)。
(选填“>”、“<”或“=”)。
(5)通过 传感器可监测
传感器可监测 的含量,其工作原理如图。
的含量,其工作原理如图。
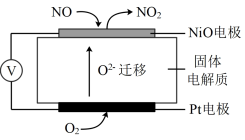
①Pt电极是电源的_______ (填“正”或“负”)极上发生的是_______ 反应(填“氧化”或“还原”)。
②写出NiO电极上的电极反应式:_______ 。
 )是一种应用广泛的化工原料。工业上先合成氨气:
)是一种应用广泛的化工原料。工业上先合成氨气:
 ,再进一步制备肼。完成下列填空:
,再进一步制备肼。完成下列填空:(1)合成氨需要选择合适的催化剂,分别选用A、B、C三种催化剂进行试验,所得结果如图所示(其他条件相同),则生产中适宜选择的催化剂是

(2)一定条件下,对在密闭容器中进行的合成氨反应达平衡后,其他条件不变时,若同时压缩容器的体积和升高温度达新平衡后,与原平衡相比,请将有关物理量的变化的情况填入下表中(填“增大”、“减小”或“无法确定”)
| 反应速率 | 平衡常数K | |
| 变化情况 |
| 化学键 | N—H | N—N | O=O | N≡N | O—H |
| 键能(kJ/mol) | 386 | 167 | 498 | 946 | 460 |
 ,气态)为燃料,若它在氧气(气态)中燃烧,生成
,气态)为燃料,若它在氧气(气态)中燃烧,生成 (气态)和
(气态)和 (气态)。该反应的热化学方程式为:
(气态)。该反应的热化学方程式为:(4)氨主要用于生产化肥和硝酸。“十三五”期间,预计我国合成氨产量将保持稳中略增。下图是不同温度和不同压强下,反应达到平衡后,混合物中
 含量(体积%)的变化情况,已知初始时
含量(体积%)的变化情况,已知初始时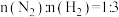 。判断
。判断 、
、 压强的大小关系,
压强的大小关系,
 (选填“>”、“<”或“=”)。
(选填“>”、“<”或“=”)。
(5)通过
 传感器可监测
传感器可监测 的含量,其工作原理如图。
的含量,其工作原理如图。
①Pt电极是电源的
②写出NiO电极上的电极反应式:
您最近半年使用:0次
5 . 某温度下,在2L恒容密闭容器中,X、Y、Z三种气体的物质的量随时间的变化曲线如图所示。
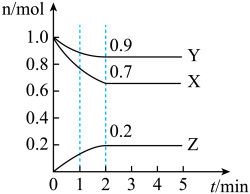
回答下列问题:
(1)2min内,气体Z的平均反应速率为___________  ;平衡时,气体Y的体积分数为
;平衡时,气体Y的体积分数为___________ %,气体Y的转化率为___________ %。
(2)该反应的化学方程式可以表示为___________ 。
(3)1min时,
___________ (填“>”或“<”或“=”,下同)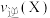 ;2min时,
;2min时,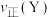
___________ 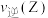 。
。
(4)反应达到平衡状态后,向容器中通入氩气,气体X的化学反应速率不变的原因是_______ 。
(5)若X、Y、Z均为气体(容器体积不变),下列能说明反应已达平衡的是______ (填字母)。
a.X、Y、Z三种气体的物质的量相等 b.混合气体的密度不随时间变化
c.容器内气体压强不变 d.反应速率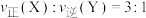

回答下列问题:
(1)2min内,气体Z的平均反应速率为
 ;平衡时,气体Y的体积分数为
;平衡时,气体Y的体积分数为(2)该反应的化学方程式可以表示为
(3)1min时,

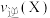 ;2min时,
;2min时,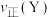
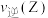 。
。(4)反应达到平衡状态后,向容器中通入氩气,气体X的化学反应速率不变的原因是
(5)若X、Y、Z均为气体(容器体积不变),下列能说明反应已达平衡的是
a.X、Y、Z三种气体的物质的量相等 b.混合气体的密度不随时间变化
c.容器内气体压强不变 d.反应速率
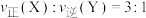
您最近半年使用:0次
2023高三·全国·专题练习
6 . 现代制备乙烯常用乙烷氧化裂解法,主反应为C2H6(g)+ O2(g)
O2(g) C2H4(g)+H2O(g) ΔH=−110kJ·mol-1,反应时还会生成CH4、CO、CO2等副产物(副反应均为放热反应),如图所示为温度对乙烷氧化裂解反应的影响。[乙烯选择性=
C2H4(g)+H2O(g) ΔH=−110kJ·mol-1,反应时还会生成CH4、CO、CO2等副产物(副反应均为放热反应),如图所示为温度对乙烷氧化裂解反应的影响。[乙烯选择性= ×100%;乙烯收率=乙烷转化率×乙烯选择性]
×100%;乙烯收率=乙烷转化率×乙烯选择性]________ ,反应的最佳温度为_________ 。
A.650℃ B.700℃ C.775℃ D.850℃
(2)工业上,保持体系总压强恒定在100kPa下进行该反应,且通常在乙烷和氧气的混合气体中掺入惰性气体(惰性气体的体积分数为70%),掺入惰性气体的目的是___________ 。
 O2(g)
O2(g) C2H4(g)+H2O(g) ΔH=−110kJ·mol-1,反应时还会生成CH4、CO、CO2等副产物(副反应均为放热反应),如图所示为温度对乙烷氧化裂解反应的影响。[乙烯选择性=
C2H4(g)+H2O(g) ΔH=−110kJ·mol-1,反应时还会生成CH4、CO、CO2等副产物(副反应均为放热反应),如图所示为温度对乙烷氧化裂解反应的影响。[乙烯选择性= ×100%;乙烯收率=乙烷转化率×乙烯选择性]
×100%;乙烯收率=乙烷转化率×乙烯选择性]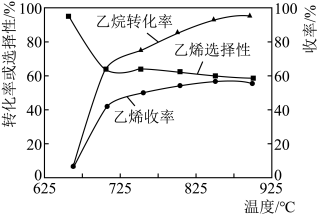
A.650℃ B.700℃ C.775℃ D.850℃
(2)工业上,保持体系总压强恒定在100kPa下进行该反应,且通常在乙烷和氧气的混合气体中掺入惰性气体(惰性气体的体积分数为70%),掺入惰性气体的目的是
您最近半年使用:0次
2023高三·全国·专题练习
7 . 二甲醚是一种重要的化工原料。在恒温恒压条件下,化工生产上利用二甲醚与氧气为原料制备合成气,反应原理如下:CH3OCH3(g)+ O2(g)⇌2CO(g)+3H2(g) ΔH=+72.4134kJ·mol-1。实际生产过程中常常添加一定量的水蒸气,其目的是
O2(g)⇌2CO(g)+3H2(g) ΔH=+72.4134kJ·mol-1。实际生产过程中常常添加一定量的水蒸气,其目的是___________ ;研究发现,所得平衡混合气体中H2的体积分数随 变化如图所示,试解释该曲线先变大后减小的原因:
变化如图所示,试解释该曲线先变大后减小的原因:___________ 。

 O2(g)⇌2CO(g)+3H2(g) ΔH=+72.4134kJ·mol-1。实际生产过程中常常添加一定量的水蒸气,其目的是
O2(g)⇌2CO(g)+3H2(g) ΔH=+72.4134kJ·mol-1。实际生产过程中常常添加一定量的水蒸气,其目的是 变化如图所示,试解释该曲线先变大后减小的原因:
变化如图所示,试解释该曲线先变大后减小的原因:
您最近半年使用:0次
名校
解题方法
8 . 一定温度下,在恒容的密闭容器内,将2molSO2和1molO2混合发生反应:2SO2(g)+O2(g) 2SO3(g) △H<0。回答下列问题:
2SO3(g) △H<0。回答下列问题:
(1)升高温度,混合气体的密度______ (填“变大”“变小”或“不变”)。
(2)若反应达到平衡后,再充入O2,平衡将______ (填“正向”“向”或“不”)移动,SO2的转化率______ (填“增大”“减小”或“不变”)。
(3)若反应达到平衡后,将c(SO2)、c(O2)、c(SO3)同时增大1倍,平衡将______ 移动。
(4)如图表示合成SO3反应在某段时间t0→t6中反应速率与时间的曲线图,t1、t3、t4时刻分别改变某一外界条件,它们依次为______ 、______ 、______ ;SO3的体积分数最小的平衡时间段是______ (填序号)。

 2SO3(g) △H<0。回答下列问题:
2SO3(g) △H<0。回答下列问题:(1)升高温度,混合气体的密度
(2)若反应达到平衡后,再充入O2,平衡将
(3)若反应达到平衡后,将c(SO2)、c(O2)、c(SO3)同时增大1倍,平衡将
(4)如图表示合成SO3反应在某段时间t0→t6中反应速率与时间的曲线图,t1、t3、t4时刻分别改变某一外界条件,它们依次为

您最近半年使用:0次
2023高三·全国·专题练习
9 . 乙苯催化脱氢制苯乙烯反应:

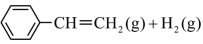 ΔH=+124 kJ·mol-1,工业上,通常在乙苯蒸气中掺混水蒸气(原料气中乙苯和水蒸气的物质的量之比为1∶9),控制反应温度600 ℃,并保持体系总压为常压的条件下进行反应。在不同反应温度下,乙苯的平衡转化率和某催化剂作用下苯乙烯的选择性(指除了H2以外的产物中苯乙烯的物质的量分数)变化如图,掺入水蒸气能提高乙苯的平衡转化率,解释说明该事实
ΔH=+124 kJ·mol-1,工业上,通常在乙苯蒸气中掺混水蒸气(原料气中乙苯和水蒸气的物质的量之比为1∶9),控制反应温度600 ℃,并保持体系总压为常压的条件下进行反应。在不同反应温度下,乙苯的平衡转化率和某催化剂作用下苯乙烯的选择性(指除了H2以外的产物中苯乙烯的物质的量分数)变化如图,掺入水蒸气能提高乙苯的平衡转化率,解释说明该事实___________
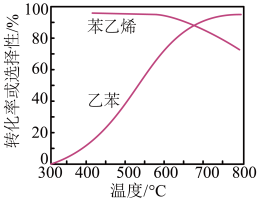


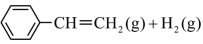 ΔH=+124 kJ·mol-1,工业上,通常在乙苯蒸气中掺混水蒸气(原料气中乙苯和水蒸气的物质的量之比为1∶9),控制反应温度600 ℃,并保持体系总压为常压的条件下进行反应。在不同反应温度下,乙苯的平衡转化率和某催化剂作用下苯乙烯的选择性(指除了H2以外的产物中苯乙烯的物质的量分数)变化如图,掺入水蒸气能提高乙苯的平衡转化率,解释说明该事实
ΔH=+124 kJ·mol-1,工业上,通常在乙苯蒸气中掺混水蒸气(原料气中乙苯和水蒸气的物质的量之比为1∶9),控制反应温度600 ℃,并保持体系总压为常压的条件下进行反应。在不同反应温度下,乙苯的平衡转化率和某催化剂作用下苯乙烯的选择性(指除了H2以外的产物中苯乙烯的物质的量分数)变化如图,掺入水蒸气能提高乙苯的平衡转化率,解释说明该事实
您最近半年使用:0次
2023高三·全国·专题练习
解题方法
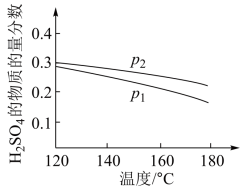
10 . 对反应:3SO2(g)+2H2O (g)=2H2SO4 (l)+S(s) ΔH2=−254 kJ·mol−1,在某一投料比时,两种压强下,H2SO4在平衡体系中物质的量分数随温度的变化关系如图所示。p2___________ p 1(填“>”或“<”),得出该结论的理由是___________

您最近半年使用:0次



