名校
解题方法
1 . Ⅰ.下图为工业合成氨的流程图:
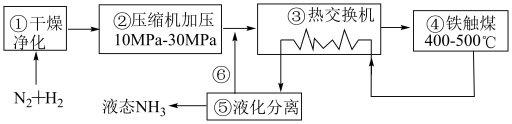
(1)⑥循环利用的物质是___________ ,①的气体若不进化,容易造成的问题是___________
(2)上述流程中能增加反应速率的是___________ ,能提高原料转化率的是___________ 。(填数字编号)
Ⅱ.某兴趣小组为研究“不同条件”对化学平衡的影响情况,进行了如下实验:(反应起始的温度和体积均相同):
(3)则:
___________  、
、
___________  (填“>”、“=”或“<”)
(填“>”、“=”或“<”)

(1)⑥循环利用的物质是
(2)上述流程中能增加反应速率的是
Ⅱ.某兴趣小组为研究“不同条件”对化学平衡的影响情况,进行了如下实验:(反应起始的温度和体积均相同):
| 序号 | 起始投入量 | 平衡转化率 | ||
 |  |  | ||
| ①恒温恒容 |  |  | 0 |  |
| ②绝热恒容 |  |  | 0 |  |
| ③恒温恒压 |  |  | 0 |  |
(3)则:

 、
、
 (填“>”、“=”或“<”)
(填“>”、“=”或“<”)
您最近一年使用:0次
名校
2 . 合成氨是人类科学技术上的一项重大突破,其反应原理为N2(g)+3H2(g) 2NH3(g) ΔH=-92.4kJ·mol-1.。一种工业合成氨的简式流程如图1所示:
2NH3(g) ΔH=-92.4kJ·mol-1.。一种工业合成氨的简式流程如图1所示:

步骤Ⅱ中制氢气的原理如下:
①CH4(g)+H2O(g) CO(g)+3H2(g) ΔH=+206.4kJ·mol-1
CO(g)+3H2(g) ΔH=+206.4kJ·mol-1
②CO(g)+H2O(g) CO2(g)+H2(g) ΔH=-41.2kJ·mol-1
CO2(g)+H2(g) ΔH=-41.2kJ·mol-1
(1)对于反应①,一定可以提高平衡体系中H2的百分含量,且能加快反应速率的措施是___________。
(2)图2表示500 ℃、60.0 MPa条件下,原料气投料比与平衡时NH3体积分数的关系。根据图中a点数据计算H2的平衡体积分数:___________ 。

(3)合成氨反应中正反应速率v正=k正c(N2)•c3(H2),逆反应速率v逆=k逆c2(NH3),k正、k逆为速率常数。平衡常数K与温度的关系如图。

①表示正反应的平衡常数K与温度变化的曲线为___________ (填L1或L2)。
②平衡时,合成氨反应的平衡常数K=___________ (用k正、k逆表示)。
(4)上述流程图中,使合成氨放出的能量得到充分利用的主要步骤是(填序号)___________ 。简述本流程中提高合成氨原料总转化率的方法:___________ (写出2条即可)。
(5)合成氨工业中,原料气(N2、H2及少量的CO、NH3的混合气)在进入合成塔前常用醋酸二氨合铜溶液来吸收原料气中的CO,其反应是[Cu(NH3)2CH3COO]+CO+NH3 [Cu(NH3)3]CH3COO·CO(正反应为放热反应)。必须除去原料气中CO的原因是
[Cu(NH3)3]CH3COO·CO(正反应为放热反应)。必须除去原料气中CO的原因是___________ 。
(6)相同温度下,有体积相同的甲、乙两个恒容密闭容器,甲容器中充入1 g N2和1 g H2,乙容器中充入2 g N2和2 g H2,分别进行合成氨反应。下列叙述中正确的是___________
 2NH3(g) ΔH=-92.4kJ·mol-1.。一种工业合成氨的简式流程如图1所示:
2NH3(g) ΔH=-92.4kJ·mol-1.。一种工业合成氨的简式流程如图1所示:
步骤Ⅱ中制氢气的原理如下:
①CH4(g)+H2O(g)
 CO(g)+3H2(g) ΔH=+206.4kJ·mol-1
CO(g)+3H2(g) ΔH=+206.4kJ·mol-1②CO(g)+H2O(g)
 CO2(g)+H2(g) ΔH=-41.2kJ·mol-1
CO2(g)+H2(g) ΔH=-41.2kJ·mol-1(1)对于反应①,一定可以提高平衡体系中H2的百分含量,且能加快反应速率的措施是___________。
| A.降低压强 | B.增大水蒸气浓度 | C.加入催化剂 | D.升高温度 |

(3)合成氨反应中正反应速率v正=k正c(N2)•c3(H2),逆反应速率v逆=k逆c2(NH3),k正、k逆为速率常数。平衡常数K与温度的关系如图。

①表示正反应的平衡常数K与温度变化的曲线为
②平衡时,合成氨反应的平衡常数K=
(4)上述流程图中,使合成氨放出的能量得到充分利用的主要步骤是(填序号)
(5)合成氨工业中,原料气(N2、H2及少量的CO、NH3的混合气)在进入合成塔前常用醋酸二氨合铜溶液来吸收原料气中的CO,其反应是[Cu(NH3)2CH3COO]+CO+NH3
 [Cu(NH3)3]CH3COO·CO(正反应为放热反应)。必须除去原料气中CO的原因是
[Cu(NH3)3]CH3COO·CO(正反应为放热反应)。必须除去原料气中CO的原因是(6)相同温度下,有体积相同的甲、乙两个恒容密闭容器,甲容器中充入1 g N2和1 g H2,乙容器中充入2 g N2和2 g H2,分别进行合成氨反应。下列叙述中正确的是___________
| A.化学反应速率:乙>甲 | B.平衡后N2的浓度:乙>甲 |
| C.H2的平衡转化率:甲>乙 | D.平衡后混合气体中H2的体积分数:乙>甲 |
您最近一年使用:0次
名校
解题方法
3 . 工业上常以黄铁矿( )为原料制备硫酸,硫酸是一种重要的工业原料,可用于制造肥料、药物、炸药、颜料、洗涤剂、蓄电池等。接触法制硫酸生产中的关键工序是
)为原料制备硫酸,硫酸是一种重要的工业原料,可用于制造肥料、药物、炸药、颜料、洗涤剂、蓄电池等。接触法制硫酸生产中的关键工序是 的催化氧化:
的催化氧化: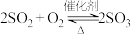 ,其流程如图所示:
,其流程如图所示:

(1)“吸收”过程中吸收液(浓硫酸)从上向下喷,目的是___________ 。
(2)“接触室”中,在温度为400~500℃时, 的催化氧化采用常压而不是高压,主要原因是
的催化氧化采用常压而不是高压,主要原因是___________ 。
(3)其催化氧化的能量变化如图所示,该过程的热化学方程式为___________ 。

已知: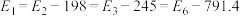
(4)为提高钒催化剂的综合性能,我国科学家对其进行了改良。不同催化剂下,温度和转化率关系如图所示,催化性能最佳的是___________ (填标号)。

(5)向体积可变的密闭容器中加入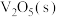 、
、 各0.6mol、
各0.6mol、 0.3mol,此时容器的体积为10L(忽略容器中固体体积),保持恒压的条件下分别在
0.3mol,此时容器的体积为10L(忽略容器中固体体积),保持恒压的条件下分别在 、
、 、
、 三种温度下进行反应,测得容器中
三种温度下进行反应,测得容器中 的转化率如图所示。
的转化率如图所示。

① 温度下反应速率最慢的原因可能是
温度下反应速率最慢的原因可能是___________ 。
② 温度时,反应达到平衡时容器的体积为
温度时,反应达到平衡时容器的体积为___________ L,反应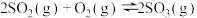 的平衡常数K=
的平衡常数K=___________ 。
 )为原料制备硫酸,硫酸是一种重要的工业原料,可用于制造肥料、药物、炸药、颜料、洗涤剂、蓄电池等。接触法制硫酸生产中的关键工序是
)为原料制备硫酸,硫酸是一种重要的工业原料,可用于制造肥料、药物、炸药、颜料、洗涤剂、蓄电池等。接触法制硫酸生产中的关键工序是 的催化氧化:
的催化氧化: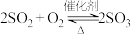 ,其流程如图所示:
,其流程如图所示:
(1)“吸收”过程中吸收液(浓硫酸)从上向下喷,目的是
(2)“接触室”中,在温度为400~500℃时,
 的催化氧化采用常压而不是高压,主要原因是
的催化氧化采用常压而不是高压,主要原因是(3)其催化氧化的能量变化如图所示,该过程的热化学方程式为

已知:
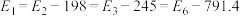
(4)为提高钒催化剂的综合性能,我国科学家对其进行了改良。不同催化剂下,温度和转化率关系如图所示,催化性能最佳的是

(5)向体积可变的密闭容器中加入
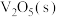 、
、 各0.6mol、
各0.6mol、 0.3mol,此时容器的体积为10L(忽略容器中固体体积),保持恒压的条件下分别在
0.3mol,此时容器的体积为10L(忽略容器中固体体积),保持恒压的条件下分别在 、
、 、
、 三种温度下进行反应,测得容器中
三种温度下进行反应,测得容器中 的转化率如图所示。
的转化率如图所示。
①
 温度下反应速率最慢的原因可能是
温度下反应速率最慢的原因可能是②
 温度时,反应达到平衡时容器的体积为
温度时,反应达到平衡时容器的体积为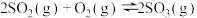 的平衡常数K=
的平衡常数K=
您最近一年使用:0次
2023-08-11更新
|
160次组卷
|
3卷引用:贵州省2024届高三8月入学考试化学试题



