名校
1 . 恒温下,反应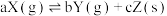 达到平衡状态,把容器容积缩小到原来的一半,且达到新的平衡状态时,X的物质的量浓度从0.1mol·L-1增大到0.19mol·L-1。下列判断中正确的是
达到平衡状态,把容器容积缩小到原来的一半,且达到新的平衡状态时,X的物质的量浓度从0.1mol·L-1增大到0.19mol·L-1。下列判断中正确的是
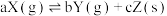 达到平衡状态,把容器容积缩小到原来的一半,且达到新的平衡状态时,X的物质的量浓度从0.1mol·L-1增大到0.19mol·L-1。下列判断中正确的是
达到平衡状态,把容器容积缩小到原来的一半,且达到新的平衡状态时,X的物质的量浓度从0.1mol·L-1增大到0.19mol·L-1。下列判断中正确的是| A.a>b | B.a<b+c | C.a=b+c | D.a<b |
您最近半年使用:0次
名校
解题方法
2 . 将玉米秸秆进行热化学裂解可制备出以CO、 、
、 、
、 为主要成分的生物质原料气,对原料气进行预处理后,可用于生产甲醇、乙醇等燃料。
为主要成分的生物质原料气,对原料气进行预处理后,可用于生产甲醇、乙醇等燃料。
(1)已知:几种常见共价键的键能如下表所示:
由此可计算反应 的焓变
的焓变
___________ kJ⋅mol 。
。
(2)若在恒容绝热的密闭容器中进行上述反应,下列说法正确的是___________(填标号)。
(3) 和
和 合成乙醇的反应为
合成乙醇的反应为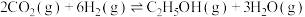 。将等物质的量的
。将等物质的量的 和
和 充入一刚性容器中,测得平衡时
充入一刚性容器中,测得平衡时 的体积分数随温度和压强的变化关系如图所示。
的体积分数随温度和压强的变化关系如图所示。
___________  (填“>、<”或“=”,下同)。判断依据是
(填“>、<”或“=”,下同)。判断依据是___________ 。
②a、b两点的平衡常数
___________  。
。
③已知Arrhenius经验公式为 (
( 为活化能,k为速率常数,R和C为常数),为探究m、n两种催化剂的催化效率,进行了实验探究,依据实验数据获得下图所示曲线。在n催化剂作用下,该反应的活化能
为活化能,k为速率常数,R和C为常数),为探究m、n两种催化剂的催化效率,进行了实验探究,依据实验数据获得下图所示曲线。在n催化剂作用下,该反应的活化能
___________ J⋅mol 。从图中信息获知催化效率较高的催化剂是
。从图中信息获知催化效率较高的催化剂是___________ (填“m”或“n”)。
 、
、 、
、 为主要成分的生物质原料气,对原料气进行预处理后,可用于生产甲醇、乙醇等燃料。
为主要成分的生物质原料气,对原料气进行预处理后,可用于生产甲醇、乙醇等燃料。(1)已知:几种常见共价键的键能如下表所示:
| 共价键 | C-H | C-O | C≡O | H-H | O-H |
键能(kJ⋅mol ) ) | 413 | 358 | 839 | 436 | 467 |
 的焓变
的焓变
 。
。(2)若在恒容绝热的密闭容器中进行上述反应,下列说法正确的是___________(填标号)。
| A.体系温度不再发生变化时,反应达到化学平衡状态 |
B.体系中若 和 和 的物质的量之比达到2∶1,则反应已达到平衡 的物质的量之比达到2∶1,则反应已达到平衡 |
C.加入催化剂,可以提高 的平衡产率 的平衡产率 |
| D.其它条件不变,增大CO的浓度,能提高H2的平衡转化率 |
(3)
 和
和 合成乙醇的反应为
合成乙醇的反应为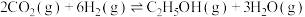 。将等物质的量的
。将等物质的量的 和
和 充入一刚性容器中,测得平衡时
充入一刚性容器中,测得平衡时 的体积分数随温度和压强的变化关系如图所示。
的体积分数随温度和压强的变化关系如图所示。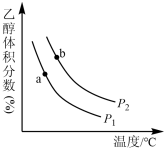

 (填“>、<”或“=”,下同)。判断依据是
(填“>、<”或“=”,下同)。判断依据是②a、b两点的平衡常数

 。
。③已知Arrhenius经验公式为
 (
( 为活化能,k为速率常数,R和C为常数),为探究m、n两种催化剂的催化效率,进行了实验探究,依据实验数据获得下图所示曲线。在n催化剂作用下,该反应的活化能
为活化能,k为速率常数,R和C为常数),为探究m、n两种催化剂的催化效率,进行了实验探究,依据实验数据获得下图所示曲线。在n催化剂作用下,该反应的活化能
 。从图中信息获知催化效率较高的催化剂是
。从图中信息获知催化效率较高的催化剂是
您最近半年使用:0次
3 . 某温度下气体反应体系达到化学平衡,其平衡常数K=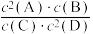 ,恒容时,若温度升高,C的浓度增加。下列说法正确的是
,恒容时,若温度升高,C的浓度增加。下列说法正确的是
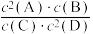 ,恒容时,若温度升高,C的浓度增加。下列说法正确的是
,恒容时,若温度升高,C的浓度增加。下列说法正确的是| A.其他条件不变,增大压强,平衡左移 |
B.该反应的热化学方程式为2A(g)+B(g) C(g)+2D(g) ΔH<0 C(g)+2D(g) ΔH<0 |
| C.增大c(A)、c(B),K增大 |
| D.平衡时,向体系中再加入C,逆反应速率逐渐增大 |
您最近半年使用:0次
名校
4 . 在一定温度下的可逆反应X(g) 2Y(g)
2Y(g)  >0,v正=k正c(X),v逆=k逆c2(Y)(k为速率常数),若在该温度下的k正=10k逆,下列说法错误的是
>0,v正=k正c(X),v逆=k逆c2(Y)(k为速率常数),若在该温度下的k正=10k逆,下列说法错误的是
 2Y(g)
2Y(g)  >0,v正=k正c(X),v逆=k逆c2(Y)(k为速率常数),若在该温度下的k正=10k逆,下列说法错误的是
>0,v正=k正c(X),v逆=k逆c2(Y)(k为速率常数),若在该温度下的k正=10k逆,下列说法错误的是| A.该温度下的平衡常数为10 |
| B.升高温度,k正增大的倍数小于k逆增大的倍数 |
| C.有利于测定X的相对分子质量的条件为高温低压 |
| D.恒压条件下,向平衡体系中充入惰性气体He,X的转化率增大 |
您最近半年使用:0次
2024-04-05更新
|
63次组卷
|
2卷引用:浙江省杭州市精诚联盟2023-2024学年高二上学期12月月考化学试题
5 . 完成下列问题
(1)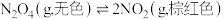 的平衡体系,降低温度,气体颜色变浅,则正反应是
的平衡体系,降低温度,气体颜色变浅,则正反应是___________ 热反应;若增大压强,平衡向___________ 移动(填“正反应方向”、“逆反应方向”或“不”),正反应速率___________ (填“增大”或“减小”)。
(2)某温度下,纯水的 为
为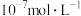 ,则此时
,则此时 为
为___________  ,若温度不变,滴入稀
,若温度不变,滴入稀 使
使 ,则由水电离出的
,则由水电离出的 为
为___________  ,某温度(T0℃)时,水的
,某温度(T0℃)时,水的 ,则该温度
,则该温度___________ (填“高于”、“低于”或“等于”)25℃其理由是___________ 。碳酸氢钠溶液显___________ 性,水解方程式表示为___________ 。
(1)
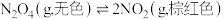 的平衡体系,降低温度,气体颜色变浅,则正反应是
的平衡体系,降低温度,气体颜色变浅,则正反应是(2)某温度下,纯水的
 为
为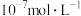 ,则此时
,则此时 为
为 ,若温度不变,滴入稀
,若温度不变,滴入稀 使
使 ,则由水电离出的
,则由水电离出的 为
为 ,某温度(T0℃)时,水的
,某温度(T0℃)时,水的 ,则该温度
,则该温度
您最近半年使用:0次
6 . Ⅰ.氮的固定是几百年来科学家一直研究的课题。
(1)下表列举了不同温度下大气固氮和工业固氮的部分化学平衡常数K的值。.
①分析数据可知:大气固氮反应属于__________ (填“吸热”或“放热”)反应。
②分析数据可知:人类不适合大规模模拟大气固氮的原因:__________ 。
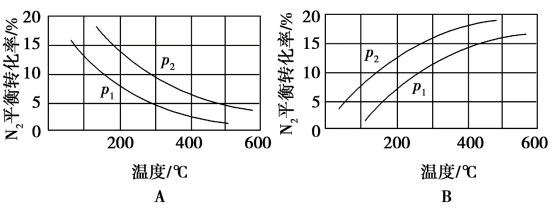
(2)工业固氮反应中,在其他条件相同时,分别测定 的平衡转化率在不同压强(
的平衡转化率在不同压强( 、
、 )下随温度变化的曲线,下图所示的图示中,正确的是
)下随温度变化的曲线,下图所示的图示中,正确的是______ (填“A”或“B”);比较 、
、 的大小关系:
的大小关系:__________ 。
Ⅱ.目前工业合成氨的原理是 。
。
(3)在一定温度下,将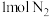 和
和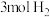 混合置于体积不变的密闭容器中发生反应。
混合置于体积不变的密闭容器中发生反应。
①下列描述能说明反应达到平衡状态的是__________ (填字母)。
A.单位时间内消耗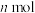 的
的 同时消耗
同时消耗 的
的
B. 、
、 、
、 的浓度相等
的浓度相等
C.混合气体的平均相对分子质量不变
D.混合气体的密度不变
②已知450℃时,某时刻测得 ,
, ,
, ,此时可逆反应
,此时可逆反应__________ 。
A.向正方向进行 B.向逆方向进行 C.处于平衡状态
(1)下表列举了不同温度下大气固氮和工业固氮的部分化学平衡常数K的值。.
| 反应 | 大气固氮 | 工业固氮 | |||
温度/℃ | 27 | 2000 | 25 | 400 | 450 |
平衡常数K |
| 0.1 |
| 0.507 | 0.152 |
②分析数据可知:人类不适合大规模模拟大气固氮的原因:
(2)工业固氮反应中,在其他条件相同时,分别测定
 的平衡转化率在不同压强(
的平衡转化率在不同压强( 、
、 )下随温度变化的曲线,下图所示的图示中,正确的是
)下随温度变化的曲线,下图所示的图示中,正确的是 、
、 的大小关系:
的大小关系:
Ⅱ.目前工业合成氨的原理是
 。
。(3)在一定温度下,将
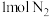 和
和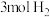 混合置于体积不变的密闭容器中发生反应。
混合置于体积不变的密闭容器中发生反应。①下列描述能说明反应达到平衡状态的是
A.单位时间内消耗
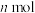 的
的 同时消耗
同时消耗 的
的
B.
 、
、 、
、 的浓度相等
的浓度相等C.混合气体的平均相对分子质量不变
D.混合气体的密度不变
②已知450℃时,某时刻测得
 ,
, ,
, ,此时可逆反应
,此时可逆反应A.向正方向进行 B.向逆方向进行 C.处于平衡状态
您最近半年使用:0次
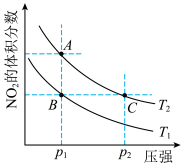
7 . 反应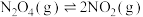
 ,在温度为
,在温度为 、
、 时,平衡体系中
时,平衡体系中 的体积分数随压强的变化曲线如图所示。下列说法正确的是。
的体积分数随压强的变化曲线如图所示。下列说法正确的是。
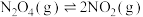
 ,在温度为
,在温度为 、
、 时,平衡体系中
时,平衡体系中 的体积分数随压强的变化曲线如图所示。下列说法正确的是。
的体积分数随压强的变化曲线如图所示。下列说法正确的是。
| A.A、C两点的反应速率:A>C |
| B.A、C两点气体的颜色:A深,C浅 |
| C.A、C两点气体的平均相对分子质量:A>C |
| D.由状态B到状态A,可以用加热的方法 |
您最近半年使用:0次
8 . 对于任何一个化学平衡体系,采取以下措施,一定会使平衡发生移动的是
| A.加入一种反应物 | B.加入催化剂 |
| C.增大体系压强 | D.升高温度 |
您最近半年使用:0次
9 . 探究CH3OH合成反应化学平衡的影响因素,有利于提高CH3OH的产率。以CO2、H2为原料合成CH3OH涉及的主要反应如下:
Ⅰ.CO2(g)+3H2(g)⇌CH3OH(g)+H2O(g) ΔH1=-49.5kJ·mol-1
Ⅱ.CO(g)+2H2(g)⇌CH3OH(g) ΔH2=-90.4kJ·mol-1
Ⅲ.CO2(g)+H2(g)⇌CO(g)+H2O(g) ΔH3=+40.9kJ·mol-1
(1)不同压强下,按照n(CO2)∶n(H2)=1∶3投料,实验测定CO2的平衡转化率和CH3OH的平衡产率随温度的变化关系如图所示。

其中纵坐标表示CO2平衡转化率的是图_____ (填“甲”或“乙”);压强p1、p2、p3由大到小的顺序为_____ ;图乙中T1温度时,三条曲线几乎交于一点的原因是_____ 。
(2)为同时提高CO2的平衡转化率和CH3OH的平衡产率,应选择的反应条件为_____(填标号)。
(3)反应ⅠCO2(g)+3H2(g)=CH3OH(g)+H2O(g)。最近采用真空封管法制备的磷化硼纳米颗粒,在发展非金属催化剂实现CO2电催化还原制备甲醇方向取得重要进展,该反应历程如图所示:
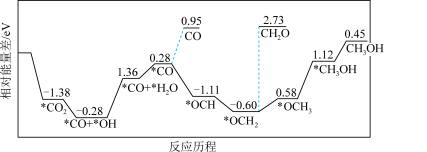
容易得到的副产物有CO和CH2O,其中相对较少的副产物为_____ ;上述合成甲醇的反应速率较慢,要使反应速率加快,主要降低下列变化中_____ (填字母)的能量变化。(双选)
A.*OCH3→*CH3OH B.*CO→*COH C.*OCH2→*OCH3 D.*CO+*OH→*CO+*H2O
Ⅰ.CO2(g)+3H2(g)⇌CH3OH(g)+H2O(g) ΔH1=-49.5kJ·mol-1
Ⅱ.CO(g)+2H2(g)⇌CH3OH(g) ΔH2=-90.4kJ·mol-1
Ⅲ.CO2(g)+H2(g)⇌CO(g)+H2O(g) ΔH3=+40.9kJ·mol-1
(1)不同压强下,按照n(CO2)∶n(H2)=1∶3投料,实验测定CO2的平衡转化率和CH3OH的平衡产率随温度的变化关系如图所示。

其中纵坐标表示CO2平衡转化率的是图
(2)为同时提高CO2的平衡转化率和CH3OH的平衡产率,应选择的反应条件为_____(填标号)。
| A.低温、高压 | B.高温、低压 | C.低温、低压 | D.高温、高压 |
(3)反应ⅠCO2(g)+3H2(g)=CH3OH(g)+H2O(g)。最近采用真空封管法制备的磷化硼纳米颗粒,在发展非金属催化剂实现CO2电催化还原制备甲醇方向取得重要进展,该反应历程如图所示:

容易得到的副产物有CO和CH2O,其中相对较少的副产物为
A.*OCH3→*CH3OH B.*CO→*COH C.*OCH2→*OCH3 D.*CO+*OH→*CO+*H2O
您最近半年使用:0次
解题方法
10 . 下列叙述与对应的图示相符合的是
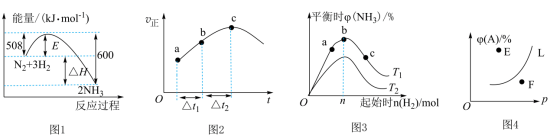

A.图1为 反应过程中的能量变化图,利用勒夏特列原理能解释工业上选择 反应过程中的能量变化图,利用勒夏特列原理能解释工业上选择 左右合成氨比室温更有利 左右合成氨比室温更有利 |
B.图2为在绝热恒容密闭容器中通入 和 和 ,反应 ,反应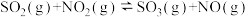 的 的 图,由图可知该反应为放热反应 图,由图可知该反应为放热反应 |
C.图3为合成氨反应中,保持其他条件不变,起始时 用量、反应温度对反应的影响图,则图中温度 用量、反应温度对反应的影响图,则图中温度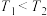 , , 、 、 、 、 三点均处于平衡状态,反应物 三点均处于平衡状态,反应物 的平衡转化率:a<b<c 的平衡转化率:a<b<c |
D.图4为反应 平衡时 平衡时 的体积分数与反应压强的关系图,则 的体积分数与反应压强的关系图,则 点: 点: |
您最近半年使用:0次