解题方法
1 . 在一定条件下,一定量的X在恒容密闭容器中发生反应: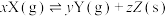
 ,达到平衡时,Y的浓度与温度和容器容积的关系如图所示,下列判断正确的是
,达到平衡时,Y的浓度与温度和容器容积的关系如图所示,下列判断正确的是
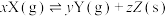
 ,达到平衡时,Y的浓度与温度和容器容积的关系如图所示,下列判断正确的是
,达到平衡时,Y的浓度与温度和容器容积的关系如图所示,下列判断正确的是
A. |
B. |
| C.在M点,投入适量Z,逆反应速率增大 |
| D.在M点,增大X的浓度,X的平衡质量分数增大 |
您最近半年使用:0次
名校
2 . 已知:
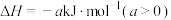 。恒温恒容下,在10L的密闭容器中加入
。恒温恒容下,在10L的密闭容器中加入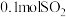 和
和 ,经过2min达到平衡状态,反应放热
,经过2min达到平衡状态,反应放热 。下列判断正确的是
。下列判断正确的是

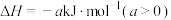 。恒温恒容下,在10L的密闭容器中加入
。恒温恒容下,在10L的密闭容器中加入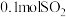 和
和 ,经过2min达到平衡状态,反应放热
,经过2min达到平衡状态,反应放热 。下列判断正确的是
。下列判断正确的是A.在2min内,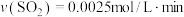 |
B.若再充入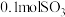 ,达到平衡后 ,达到平衡后 的质量分数会减小 的质量分数会减小 |
C.在1min时,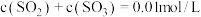 |
D.若恒温恒压下,在10L的密闭容器中加入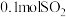 和 和 ,平衡后又反应放热小于0.025akJ ,平衡后又反应放热小于0.025akJ |
您最近半年使用:0次
解题方法
3 . 化工原料异丁烯( )可由异丁烷(
)可由异丁烷( )直接催化脱氢制得,反应方程式为
)直接催化脱氢制得,反应方程式为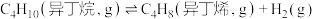
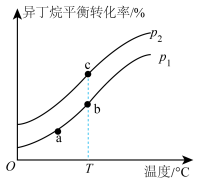
 。一定条件下,温度、压强对异丁烷平衡转化率的影响如图所示(假设起始时异丁烯的物质的量为xmol且
。一定条件下,温度、压强对异丁烷平衡转化率的影响如图所示(假设起始时异丁烯的物质的量为xmol且 ),下列说法正确的是
),下列说法正确的是
 )可由异丁烷(
)可由异丁烷( )直接催化脱氢制得,反应方程式为
)直接催化脱氢制得,反应方程式为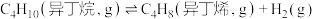
 。一定条件下,温度、压强对异丁烷平衡转化率的影响如图所示(假设起始时异丁烯的物质的量为xmol且
。一定条件下,温度、压强对异丁烷平衡转化率的影响如图所示(假设起始时异丁烯的物质的量为xmol且 ),下列说法正确的是
),下列说法正确的是
A.压强: | B.反应速率: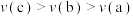 |
C.平衡常数: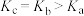 | D.异丁烯( )的质量分数: )的质量分数: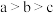 |
您最近半年使用:0次
解题方法
4 . 在一体积可变的密闭容器中,加入一定量的X、Y,发生反应mX(g) nY(g) ΔH=QkJ/mol。反应达到平衡时,Y的物质的量浓度与温度、气体体积的关系如下表所示:
nY(g) ΔH=QkJ/mol。反应达到平衡时,Y的物质的量浓度与温度、气体体积的关系如下表所示:
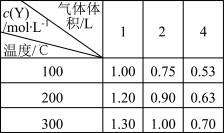
下列说法正确的是
 nY(g) ΔH=QkJ/mol。反应达到平衡时,Y的物质的量浓度与温度、气体体积的关系如下表所示:
nY(g) ΔH=QkJ/mol。反应达到平衡时,Y的物质的量浓度与温度、气体体积的关系如下表所示:
下列说法正确的是
| A.m<n |
| B.Q<0 |
| C.温度不变,压强增大,Y的质量分数减小 |
| D.体积不变,温度升高,平衡向逆反应方向移动 |
您最近半年使用:0次
名校
5 . 恒温恒压下向密闭容器中充入4mol SO2和2mol O2,反应如下:2SO2(g)+O2(g) 2SO3(g) ΔH<0;2min时反应达到平衡,生成1.4mol SO3,同时放出热量Q kJ。则下列分析
2SO3(g) ΔH<0;2min时反应达到平衡,生成1.4mol SO3,同时放出热量Q kJ。则下列分析不正确 的是
 2SO3(g) ΔH<0;2min时反应达到平衡,生成1.4mol SO3,同时放出热量Q kJ。则下列分析
2SO3(g) ΔH<0;2min时反应达到平衡,生成1.4mol SO3,同时放出热量Q kJ。则下列分析| A.若反应开始时容器体积为2L,则0~2min内v(SO3)>0.35mol/(L·min) |
| B.2min后向容器中再通入一定量的SO3气体,重新达到平衡时,SO2的含量不变 |
| C.若把条件“恒温恒压”改为“绝热恒压”,则平衡后n(SO3)>1.4mol |
| D.若把条件“恒温恒压”改为“恒温恒容”,则平衡时放出热量小于Q kJ |
您最近半年使用:0次
解题方法
6 . 反应mA(s)+nB(g) eC(g)+fD(g),反应过程中,当其它条件不变时,C的百分含量(C%)与温度(T)和压强(P)的关系如下图,下列叙述正确的是
eC(g)+fD(g),反应过程中,当其它条件不变时,C的百分含量(C%)与温度(T)和压强(P)的关系如下图,下列叙述正确的是

 eC(g)+fD(g),反应过程中,当其它条件不变时,C的百分含量(C%)与温度(T)和压强(P)的关系如下图,下列叙述正确的是
eC(g)+fD(g),反应过程中,当其它条件不变时,C的百分含量(C%)与温度(T)和压强(P)的关系如下图,下列叙述正确的是
| A.到平衡后,加入催化剂则C%增大 |
| B.化学方程式中n>e+f |
| C.达到平衡后,若升温,平衡左移 |
| D.达到平衡后,增加A的量有利于平衡向右移动 |
您最近半年使用:0次
7 . 已知可逆反应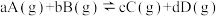 ,在其他条件不变时,C的物质的量分数随温度(T)或压强(P)的变化如下图所示,下列说法正确的是
,在其他条件不变时,C的物质的量分数随温度(T)或压强(P)的变化如下图所示,下列说法正确的是
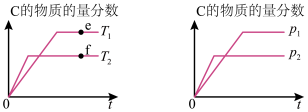
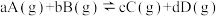 ,在其他条件不变时,C的物质的量分数随温度(T)或压强(P)的变化如下图所示,下列说法正确的是
,在其他条件不变时,C的物质的量分数随温度(T)或压强(P)的变化如下图所示,下列说法正确的是
| A.反应达到平衡后,添加合适的催化剂,D的百分含量增加 |
B.e、f点对应的化学反应速率: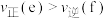 |
C.平衡常数K: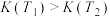 , ,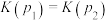 |
D. , ,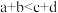 |
您最近半年使用:0次
名校
解题方法
8 . 下列叙述与图对应的是
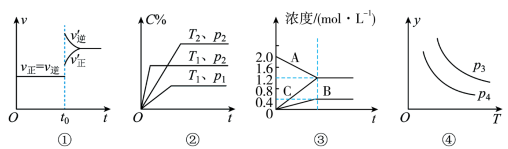

| A.对于达到平衡状态的反应:N2(g)+3H2(g)⇌2NH3(g),图①表示在t0时刻充入了一定量的NH3,平衡逆向移动 |
| B.由图②可知,P2>P1、T1>T2,满足反应:2A(g)+B(g)⇌2C(g) △H<0 |
| C.图③表示的反应方程式为:2A=3B+C |
| D.对于反应2X(g)+3Y(g)⇌3Z(g) △H>0,图④y轴可以表示Y的百分含量 |
您最近半年使用:0次
名校
9 . 一定温度下,把2.5molA和2.5molB混合盛入容积为2L的密闭容器里,发生如下反应:3A(g)+B(s)⇌xC(g)+2D(g),经5s反应达平衡,在此5s内C的平均反应速率为0.1mol·L-1·s-1,同时生成1molD,下列叙述中不正确 的是
| A.反应达到平衡状态时A的转化率为60% |
| B.x=2 |
| C.减小容器的体积,反应物A的百分含量变小 |
| D.反应达到平衡状态时,相同条件下容器内气体的压强与起始时压强比为5∶6 |
您最近半年使用:0次
2022-10-26更新
|
74次组卷
|
2卷引用:山东省临沂市平邑县第一中学2022-2023学年高二上学期10月月考化学试题
10 . 下列叙述与图像对应符合的是
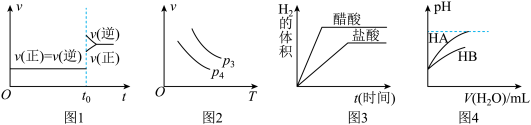

A.图1表示达到平衡状态的N2(g)+3H2(g) 2NH3(g) ΔH>0在t0时刻升高温度,平衡逆向移动 2NH3(g) ΔH>0在t0时刻升高温度,平衡逆向移动 |
B.对于反应2X(g)+3Y(g) 3Z(g) ΔH<0,图2中y轴可以表示Y的百分含量 3Z(g) ΔH<0,图2中y轴可以表示Y的百分含量 |
| C.图3表示等体积,等pH值的盐酸和醋酸溶液分别与过量的Mg反应 |
| D.图4表示常温下,稀释HA、HB两种酸的稀溶液时,溶液pH随加水量的变化,则HB酸性强 |
您最近半年使用:0次



