解题方法
1 . 回答下列问题。
(1)已知可逆反应: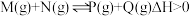 ,请回答下列问题:
,请回答下列问题:
①在某温度下,反应物的起始浓度分别为: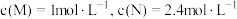 ;达到平衡后,M的转化率为
;达到平衡后,M的转化率为 ,此时N的转化率为
,此时N的转化率为_______ ;平衡常数是多少?(写出计算过程)
②若反应温度升高,M的转化率_______ (填“增大”“减小”或“不变”;)
③若反应温度不变,反应物的起始浓度分别为: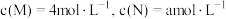 ;达到平衡后,
;达到平衡后,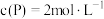 ,则
,则
_______ ;
(2)用酸性 溶液与
溶液与 溶液反应来探究“外界条件对化学反应速率的影响”。
溶液反应来探究“外界条件对化学反应速率的影响”。
实验前先用酸性 标准溶液滴定未知浓度的草酸。
标准溶液滴定未知浓度的草酸。
反应原理: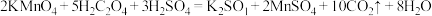 。
。
实验操作:取 待测
待测 溶液放入锥形瓶中,用
溶液放入锥形瓶中,用 酸性
酸性 标准溶液进行滴定。重复上述滴定操作2~3次,并记录数据。
标准溶液进行滴定。重复上述滴定操作2~3次,并记录数据。
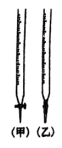
①滴定时,用_______ 滴定管盛装标准酸性 溶液(填“甲”或“乙”滴定终点的现象为
溶液(填“甲”或“乙”滴定终点的现象为_______ 。
②实验时记录的实验数据如下,试计算所测 溶液的浓度为
溶液的浓度为_______  。
。
(1)已知可逆反应:
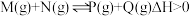 ,请回答下列问题:
,请回答下列问题:①在某温度下,反应物的起始浓度分别为:
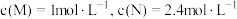 ;达到平衡后,M的转化率为
;达到平衡后,M的转化率为 ,此时N的转化率为
,此时N的转化率为②若反应温度升高,M的转化率
③若反应温度不变,反应物的起始浓度分别为:
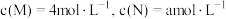 ;达到平衡后,
;达到平衡后,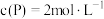 ,则
,则
(2)用酸性
 溶液与
溶液与 溶液反应来探究“外界条件对化学反应速率的影响”。
溶液反应来探究“外界条件对化学反应速率的影响”。实验前先用酸性
 标准溶液滴定未知浓度的草酸。
标准溶液滴定未知浓度的草酸。反应原理:
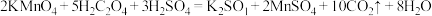 。
。实验操作:取
 待测
待测 溶液放入锥形瓶中,用
溶液放入锥形瓶中,用 酸性
酸性 标准溶液进行滴定。重复上述滴定操作2~3次,并记录数据。
标准溶液进行滴定。重复上述滴定操作2~3次,并记录数据。
①滴定时,用
 溶液(填“甲”或“乙”滴定终点的现象为
溶液(填“甲”或“乙”滴定终点的现象为②实验时记录的实验数据如下,试计算所测
 溶液的浓度为
溶液的浓度为 。
。| 实验次数编号 | 待测液体积 | 滴入的标准液体积 |
| 1 | 20.00 | 16.05 |
| 2 | 20.00 | 15.95 |
| 3 | 20.00 | 16.00 |
您最近一年使用:0次
23-24高二·全国·假期作业
2 . 回答下列问题。
(I)载人飞船中通过如下过程实现O2再生:
①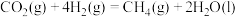

②

(1)已知18g液态水完全气化要吸收44kJ的热量,则1molCH4完全燃烧生成气态水时放出___________ kJ热量。
(II)工业上可用CO和H2合成甲醇: 。一定条件下向2L的密闭容器中充入1molCO和2molH2发生反应,CO的平衡转化率与温度、压强的关系如图所示:
。一定条件下向2L的密闭容器中充入1molCO和2molH2发生反应,CO的平衡转化率与温度、压强的关系如图所示:

(2)在T1和p1条件下,由D点到A点过程中,正、逆反应速率之间的关系:v正___________ v逆(填“>”“<”或“=”);B点和C点的逆反应速率的关系:v逆(B)___________ v正(C)(填“>”“<”或“=”)。
(3)该反应的
___________ 0(填“>”或“<”);生产中有利于增大CO平衡转化率的措施有___________ (写出1条即可)。
(4)若p2=100kPa,B点的Kp=___________ 。(结果保留2位有效数字;Kp表示分压平衡常数,分压=总压 物质的量分数)。
物质的量分数)。
(I)载人飞船中通过如下过程实现O2再生:
①
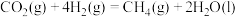

②


(1)已知18g液态水完全气化要吸收44kJ的热量,则1molCH4完全燃烧生成气态水时放出
(II)工业上可用CO和H2合成甲醇:
 。一定条件下向2L的密闭容器中充入1molCO和2molH2发生反应,CO的平衡转化率与温度、压强的关系如图所示:
。一定条件下向2L的密闭容器中充入1molCO和2molH2发生反应,CO的平衡转化率与温度、压强的关系如图所示:
(2)在T1和p1条件下,由D点到A点过程中,正、逆反应速率之间的关系:v正
(3)该反应的

(4)若p2=100kPa,B点的Kp=
 物质的量分数)。
物质的量分数)。
您最近一年使用:0次
23-24高二·全国·假期作业
3 . 合成氨工业对化学工业和国防工业具有重要意义。工业合成氨生产示意图如图所示。
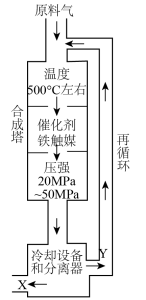
(1)图中条件选定的主要原因是_______ (填字母编号)。
A.温度、压强对化学平衡的影响
B.催化剂铁触媒在该温度时活性大
C.工业生产受动力、材料、设备等条件的限制
(2)工业生产中氮气与氢气按物质的量之比为1∶2.8进行投料,合成塔压强p恒定。若起始时氮气通入量为x mol,一段时间后测得氮气的平衡转化率为80%,用平衡分压代替平衡浓度表示平衡常数的
_______ (用p表示,气体分压=总压×物质的量分数)。
(3)合成氨反应通常控制在20~50MPa的压强和500℃左右的温度,若进入合成塔的氮气和氢气的体积比为1∶3,经科学测定,在相应条件下氮气和氢气反应所得氨的平衡浓度(体积分数)如表所示:
而实际流程从合成塔出来的混合气体中含有氨约为15%,这表明_______ 。
A.表中所测数据有明显误差 B.生产条件控制不当
C.氨的分解速率大于预测值 D.合成塔中的反应并未达到平衡
该流程控制含氨约为15%的原因是_______ 。

(1)图中条件选定的主要原因是
A.温度、压强对化学平衡的影响
B.催化剂铁触媒在该温度时活性大
C.工业生产受动力、材料、设备等条件的限制
(2)工业生产中氮气与氢气按物质的量之比为1∶2.8进行投料,合成塔压强p恒定。若起始时氮气通入量为x mol,一段时间后测得氮气的平衡转化率为80%,用平衡分压代替平衡浓度表示平衡常数的

(3)合成氨反应通常控制在20~50MPa的压强和500℃左右的温度,若进入合成塔的氮气和氢气的体积比为1∶3,经科学测定,在相应条件下氮气和氢气反应所得氨的平衡浓度(体积分数)如表所示:
| 压强 | 20MPa | 60MPa |
| 500℃ | 19.1 | 42.2 |
A.表中所测数据有明显误差 B.生产条件控制不当
C.氨的分解速率大于预测值 D.合成塔中的反应并未达到平衡
该流程控制含氨约为15%的原因是
您最近一年使用:0次
解题方法
4 . 某温度下,可逆反应: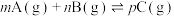 的平衡常数为K,下列对K的说法正确的是
的平衡常数为K,下列对K的说法正确的是
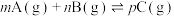 的平衡常数为K,下列对K的说法正确的是
的平衡常数为K,下列对K的说法正确的是A.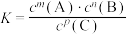 |
B.如果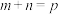 ,则 ,则 |
| C.K值越大,表明该反应越有利于C的生成,平衡时反应物的转化率越大 |
D.增大压强缩小反应器的容积到原来的一半,达到新的平衡时C的浓度为原平衡的1.5倍则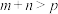 |
您最近一年使用:0次
2023-12-14更新
|
112次组卷
|
2卷引用:贵州省贵阳市三新改革联盟校2023-2024学年高二上学期10月月考化学试题
解题方法
5 . 在不同温度下,向2L密闭容器中加入0.5mol NO和0.5mol活性炭,发生反应:2NO(g)+C(s)  N2(g)+CO2(g) ΔH<0,5min后反应达到平衡,平衡数据如下:
N2(g)+CO2(g) ΔH<0,5min后反应达到平衡,平衡数据如下:
下列有关说法正确的是
 N2(g)+CO2(g) ΔH<0,5min后反应达到平衡,平衡数据如下:
N2(g)+CO2(g) ΔH<0,5min后反应达到平衡,平衡数据如下:| 温度/℃ | n(C)/mol | n(CO2)/mol |
| T1 | 0.15 | |
| T2 | 0.375 |
A.T1℃时,该反应的平衡常数K=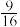 |
| B.T1℃时,5min时CO2的反应速率为0.015mol·L-1·min-1 |
| C.由上述信息可推知:T1>T2 |
| D.T2℃时,反应达到平衡后再通入NO,c(N2):c(NO)增大 |
您最近一年使用:0次
2023-12-14更新
|
197次组卷
|
2卷引用:浙江省杭州市“六县九校”联盟2023-2024学年高二上学期11月期中考试化学试题
名校
6 . T℃时,在一固定容积的密闭容器中发生反应: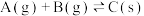
 ,按照不同配比充入A、B,达到平衡时容器中A、B浓度变化如图中曲线(实线)所示,下列判断正确的是
,按照不同配比充入A、B,达到平衡时容器中A、B浓度变化如图中曲线(实线)所示,下列判断正确的是
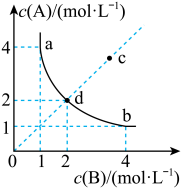
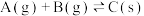
 ,按照不同配比充入A、B,达到平衡时容器中A、B浓度变化如图中曲线(实线)所示,下列判断正确的是
,按照不同配比充入A、B,达到平衡时容器中A、B浓度变化如图中曲线(实线)所示,下列判断正确的是
| A.T℃时,该反应的平衡常数值为4 | B.c点没有达到平衡,此时反应向逆向进行 |
| C.若c点为平衡点,则此时容器内的温度高于T℃ | D.T℃时,直线cd上的点均为平衡状态 |
您最近一年使用:0次
2023-12-08更新
|
640次组卷
|
43卷引用:四川省遂宁二中2018-2019学年高二上学期半期考试化学试题
四川省遂宁二中2018-2019学年高二上学期半期考试化学试题四川省攀枝花市第十五中学2019-2020学年高二上学期期中考试化学试题鲁科版(2019)选择性必修1 第2章 化学反应的方向、限度与速率 第2节 化学反应的限度辽宁省实验中学、大连八中、大连二十四中、鞍山一中、东北育才学校五校协作体2020-2021学年高二上学期期末化学试题重庆市第七中学校2021-2022学年高二上学期第一次月考化学试题河南省新蔡县第一高级中学2021-2022学年高二10月月考化学试题山东省济南市历城第二中学2022-2023学年高二上学期期末线上测试化学试题广东省梅州市兴宁市沐彬中学2021-2022学年高二下学期期中考试化学试题山西省大同市第一中学校2023-2024学年高二上学期12月月考化学试题河南省郑州市登封市第一高级中学2023-2024学年高二上学期期末考试化学试题2016届河北邯郸第一中学高三一轮收官考试一理综化学卷2016届山东省济南外国语学校高三上学期12月模拟化学试卷2016届江西南昌二中、临川一中等高三4月联考二理综化学试卷2015-2016学年湖北省枣阳市高中高二下期中化学试卷2017届天津市红桥区高三上学期期末考试(下学期开学考试)化学试卷天津市耀华中学2018届高三上学期第二次月考化学试题山东省泰安市宁阳一中2018-2019学年高二上学期阶段性考试三(12月)化学试题【全国百强校】福建省厦门外国语学校2018-2019学年高二下学期第一次月考化学试题黑龙江省大庆实验中学2019-2020学年高二上学期第一次月考化学试题江西省赣州市寻乌中学2019-2020学年高二上学期第二次段考化学试题河北省石家庄市第二中学2019-2020学年高一下学期期末模拟考试化学试题(已下线)第16讲 化学平衡-2021年高考化学一轮复习名师精讲练四川省成都龙泉第二中学2021届高三上学期九月月考化学试题辽宁省大连市一〇三中学2021届高三上学期第二阶段模拟考试化学试题云南省楚雄天人中学2020-2021学年高二上学期12月月考化学试题(已下线)课时38 化学平衡常规图像-2022年高考化学一轮复习小题多维练(全国通用)湖南省长沙市宁乡市2021-2022学年高三11月调研考试化学试题广西柳州市第三中学2021-2022学年高二下学期4月月考化学试题河北省廊坊市2021-2022学年上学期高三年级9月调研考试化学试题重庆市石柱中学校2021-2022学年高二上学期第一次月考化学试题湖北省巴东县第三高级中学2022-2023学年高二上学期第一次月考化学试题黑龙江省齐齐哈尔市普高联谊校2022-2023学年高二上学期期中考试化学试题广东省深圳市6校联盟2022-2023学年高二上学期期中考试化学试题山东省青岛第二中学2020-2021学年高二上学期期末化学试题 广东省佛山市顺德区第一中学2022-2023学年高二上学期期中考试化学试题(已下线)第七章 化学反应速率与化学平衡 第41练 化学平衡状态 化学平衡常数山东省青岛第二中学2023-2024学年高二上学期期中考试化学试卷广东省佛山市顺德区容山中学2023-2024学年高二上学期期中考试化学试题山东省青岛第二中学2023-2024学年高二上学期期中考试化学试题(已下线)题型13 化学平衡常数的计算及应用-2024年高考化学二轮热点题型归纳与变式演练(新高考通用)2015届山东省青岛市高三下学期一模考试理综化学试卷湖南省天壹名校联盟.宁乡市2021-2022学年高三11月调研考试化学试题新疆克拉玛依克拉玛依市独山子第二中学2021-2022学年高三上学期12月月考化学试题
名校
7 . 一定温度下,在体积可变的反应器中充入足量 ,发生反应:
,发生反应: ,达到平衡1时测得气体压强为
,达到平衡1时测得气体压强为 ,浓度为
,浓度为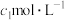 。保持温度不变,将体积压缩至原来的一半,保持压缩后体积不变,达到平衡2时测得气体压强为
。保持温度不变,将体积压缩至原来的一半,保持压缩后体积不变,达到平衡2时测得气体压强为 ,浓度为
,浓度为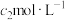 。下列推断正确的是
。下列推断正确的是
 ,发生反应:
,发生反应: ,达到平衡1时测得气体压强为
,达到平衡1时测得气体压强为 ,浓度为
,浓度为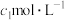 。保持温度不变,将体积压缩至原来的一半,保持压缩后体积不变,达到平衡2时测得气体压强为
。保持温度不变,将体积压缩至原来的一半,保持压缩后体积不变,达到平衡2时测得气体压强为 ,浓度为
,浓度为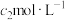 。下列推断正确的是
。下列推断正确的是A.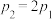 , , | B. , , |
C.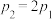 , , | D. , , |
您最近一年使用:0次
2023-11-22更新
|
100次组卷
|
3卷引用:寒假作业03 化学平衡-【寒假分层作业】2024年高二化学寒假培优练(人教版2019)
(已下线)寒假作业03 化学平衡-【寒假分层作业】2024年高二化学寒假培优练(人教版2019)山东省部分名校2023-2024学年高二上学期11月期中调研考试化学试题安徽省淮北市第一中学2023-2024学年高二下学期寒假自主学习质量评估化学试题
解题方法
8 . 一定温度下,向密闭容器中加入足量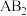 ,发生反应
,发生反应 。达到平衡状态后,测得
。达到平衡状态后,测得 ,保持温度不变,将容器的容积扩大一倍,达到新平衡时
,保持温度不变,将容器的容积扩大一倍,达到新平衡时 为
为
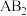 ,发生反应
,发生反应 。达到平衡状态后,测得
。达到平衡状态后,测得 ,保持温度不变,将容器的容积扩大一倍,达到新平衡时
,保持温度不变,将容器的容积扩大一倍,达到新平衡时 为
为A. | B. | C. | D. |
您最近一年使用:0次
2023-11-14更新
|
108次组卷
|
3卷引用:河南省新乡市2023-2024学年高二上学期期中考试化学试题
河南省新乡市2023-2024学年高二上学期期中考试化学试题(已下线)寒假作业03 化学平衡-【寒假分层作业】2024年高二化学寒假培优练(人教版2019)河南省郑州学森实验学校2023-2024学年高二上学期1月月考 化学试题
23-24高二上·全国·期中
解题方法
9 . 已知二甲醚是一种重要的清洁燃料,可以通过CH3OH分子间脱水制得:2CH3OH(g) CH3OCH3(g)+H2O(g)△H=23.5kJ•mol﹣1.在T1℃,恒容密闭容器中建立上述平衡,体系中各组分浓度随时间变化如图所示。请回答下列问题:
CH3OCH3(g)+H2O(g)△H=23.5kJ•mol﹣1.在T1℃,恒容密闭容器中建立上述平衡,体系中各组分浓度随时间变化如图所示。请回答下列问题:
(1)该条件下反应平衡常数表达式K=___________ ,在T1℃时,该反应的平衡常数为___________ ,达到平衡时n(CH3OH):n(CH3OCH3):n(H2O)=___________ 。
(2)相同条件下,若改变起始浓度,某时刻各组分浓度依次为c(CH3OH)=0.4mol•L﹣1、c(H2O)=0.6mol•L﹣1、c(CH3OCH3)=1.2mol•L﹣1,此时正、逆反应速率的大小:v (正)___________ v (逆)(填“>”、“<”或“=”),反应向___________ 进行(填“正反应方向”或“逆反应方向”)。

 CH3OCH3(g)+H2O(g)△H=23.5kJ•mol﹣1.在T1℃,恒容密闭容器中建立上述平衡,体系中各组分浓度随时间变化如图所示。请回答下列问题:
CH3OCH3(g)+H2O(g)△H=23.5kJ•mol﹣1.在T1℃,恒容密闭容器中建立上述平衡,体系中各组分浓度随时间变化如图所示。请回答下列问题:(1)该条件下反应平衡常数表达式K=
(2)相同条件下,若改变起始浓度,某时刻各组分浓度依次为c(CH3OH)=0.4mol•L﹣1、c(H2O)=0.6mol•L﹣1、c(CH3OCH3)=1.2mol•L﹣1,此时正、逆反应速率的大小:v (正)

您最近一年使用:0次
10 . 已知可逆反应: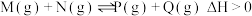 。在某温度下,反应物的起始浓度分别为
。在某温度下,反应物的起始浓度分别为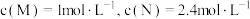 。达到平衡后,
。达到平衡后, 的转化率为
的转化率为 。请回答下列问题:
。请回答下列问题:
(1)此时 的转化率为
的转化率为___________ 。
(2)若温度升高,则 的转化率
的转化率___________ (填“增大”、“减小”或“不变”)。
(3)若反应温度不变,反应物的起始浓度分别为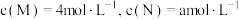 ;达到平衡后,
;达到平衡后,
___________ 。
(4)若反应温度不变,反应物的起始浓度为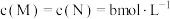 ,达到平衡后,
,达到平衡后, 的转化率为
的转化率为___________ (已知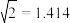 )。
)。
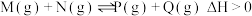 。在某温度下,反应物的起始浓度分别为
。在某温度下,反应物的起始浓度分别为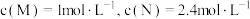 。达到平衡后,
。达到平衡后, 的转化率为
的转化率为 。请回答下列问题:
。请回答下列问题:(1)此时
 的转化率为
的转化率为(2)若温度升高,则
 的转化率
的转化率(3)若反应温度不变,反应物的起始浓度分别为
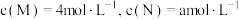 ;达到平衡后,
;达到平衡后,
(4)若反应温度不变,反应物的起始浓度为
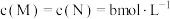 ,达到平衡后,
,达到平衡后, 的转化率为
的转化率为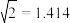 )。
)。
您最近一年使用:0次



