名校
解题方法
1 . 氢气既是一种优质的能源,又是一种重要化工原料,高纯氢的制备是目前的研究热点。
(1)甲烷水蒸气催化重整是制备高纯氢的方法之一,甲烷和水蒸气反应的热化学方程式是:
CH2(g)+2H2O(g)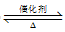 CO2(g)+4H2(g) △H=+165.0kJ·mol-1
CO2(g)+4H2(g) △H=+165.0kJ·mol-1
已知反应器中存在如下反应过程:
I.CH4(g)+H2O(g) CO(g)+3H2(g) △H1=+206.4kJ·mol-1
CO(g)+3H2(g) △H1=+206.4kJ·mol-1
II.CO(g)+H2O(g) CO2(g)+H2(g) △H2
CO2(g)+H2(g) △H2
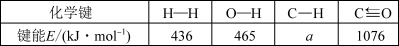
根据上述信息计算:a=___ 、△H2=___ 。
(2)某温度下,4molH2O和lmolCH4在体积为2L的刚性容器内同时发生I、II反应,达平衡时,体系中n(CO)=bmol、n(CO2)=dmol,则该温度下反应I的平衡常数K值为___ (用字母表示)。
(3)欲增大CH4转化为H2的平衡转化率,可采取的措施有___ (填标号)。
A.适当增大反应物投料比武n(H2O):n(CH4)
B.提高压强
C.分离出CO2
(4)H2用于工业合成氨:N2+3H2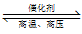 2NH3。将n(N2):n(H2)=1:3的混合气体,匀速通过装有催化剂的反应器反应,反应器温度变化与从反应器排出气体中NH3的体积分数φ(NH3)关系如图,反应器温度升高NH3的体积分数φ(NH3)先增大后减小的原因是
2NH3。将n(N2):n(H2)=1:3的混合气体,匀速通过装有催化剂的反应器反应,反应器温度变化与从反应器排出气体中NH3的体积分数φ(NH3)关系如图,反应器温度升高NH3的体积分数φ(NH3)先增大后减小的原因是___ 。

某温度下,n(N2):n(H2)=1:3的混合气体在刚性容器内发生反应,起始气体总压为2×l07Pa,平衡时总压为开始的90%,则H2的转化率为___ ,气体分压(p分)=气体总压(p总)×体积分数,用某物质的平衡分压代替物质的量浓度也可以表示化学平衡常数(记作Kp),此温度下,该反应的化学平衡常数Kp=___ (分压列计算式、不化简)。
(1)甲烷水蒸气催化重整是制备高纯氢的方法之一,甲烷和水蒸气反应的热化学方程式是:
CH2(g)+2H2O(g)
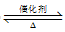 CO2(g)+4H2(g) △H=+165.0kJ·mol-1
CO2(g)+4H2(g) △H=+165.0kJ·mol-1已知反应器中存在如下反应过程:
I.CH4(g)+H2O(g)
 CO(g)+3H2(g) △H1=+206.4kJ·mol-1
CO(g)+3H2(g) △H1=+206.4kJ·mol-1II.CO(g)+H2O(g)
 CO2(g)+H2(g) △H2
CO2(g)+H2(g) △H2
根据上述信息计算:a=
(2)某温度下,4molH2O和lmolCH4在体积为2L的刚性容器内同时发生I、II反应,达平衡时,体系中n(CO)=bmol、n(CO2)=dmol,则该温度下反应I的平衡常数K值为
(3)欲增大CH4转化为H2的平衡转化率,可采取的措施有
A.适当增大反应物投料比武n(H2O):n(CH4)
B.提高压强
C.分离出CO2
(4)H2用于工业合成氨:N2+3H2
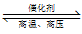 2NH3。将n(N2):n(H2)=1:3的混合气体,匀速通过装有催化剂的反应器反应,反应器温度变化与从反应器排出气体中NH3的体积分数φ(NH3)关系如图,反应器温度升高NH3的体积分数φ(NH3)先增大后减小的原因是
2NH3。将n(N2):n(H2)=1:3的混合气体,匀速通过装有催化剂的反应器反应,反应器温度变化与从反应器排出气体中NH3的体积分数φ(NH3)关系如图,反应器温度升高NH3的体积分数φ(NH3)先增大后减小的原因是
某温度下,n(N2):n(H2)=1:3的混合气体在刚性容器内发生反应,起始气体总压为2×l07Pa,平衡时总压为开始的90%,则H2的转化率为
您最近一年使用:0次
2020-01-02更新
|
607次组卷
|
7卷引用:福建省莆田二中2020-2021学年高三上学期期中检测化学试题
福建省莆田二中2020-2021学年高三上学期期中检测化学试题四省八校2020届高三上学期第一次教学质量检测理综化学试题2020届高三《新题速递·化学》1月第02期(考点11-13)【百强校】江西省南昌市第十中学2020届高三下学期综合模拟考试化学试题(已下线)考点06 化学能与热能-2020年高考化学命题预测与模拟试题分类精编广西壮族自治区桂林市第十八中学2021届高三上学期第一次月考理综化学试题(已下线)04 化学反应原理综合题型集训之多重平衡中的Kp计算(解析)-备战2023年高考化学大题逐空突破系列(全国通用)
名校
解题方法
2 . 下列图像能正确地表达可逆反应3A(g)+B(g)⇌2C(g)(ΔH<0)的是
A.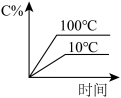 | B.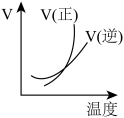 |
C. | D.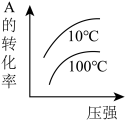 |
您最近一年使用:0次
2019-12-16更新
|
503次组卷
|
21卷引用:福建省长泰县第一中学2020届高三上学期期中考试化学试题
福建省长泰县第一中学2020届高三上学期期中考试化学试题(已下线)2010年河南省郑州外国语学校全真模拟(二)(理科综合)化学部分2017届山东省枣庄三中高三上学期9月质检化学试卷2018届高三一轮复习化学:微考点55-平衡移动与结果判断福建省永安市第九中学2022-2023学年高二上学期期中考试化学(选考)试题(已下线)2010-2011学年广东省白云中学高二下学期期中考试化学试卷(已下线)2011-2012学年辽宁省沈阳同泽女中高二上学期期中考试化学试卷(已下线)2011-2012学年山东省济宁市重点中学高二上学期期中考试化学试卷(已下线)2013-2014学年河北省遵化市高二上学期期中质量检测化学试卷2014-2015浙江省严州中学高二下学期4月阶段性测试化学试卷2015-2016学年河北邯郸魏县一中、曲周县一中高二上期中化学试卷湖南省湘潭、岳阳两校2015-2016学年高二上第三次联考化学卷2016-2017学年江西省南昌市第二中学高二上学期期末考试化学试卷(已下线)2018年9月18日 《每日一题》人教选修4-化学平衡移动的分析山东省德州市夏津一中2018-2019学年高二上学期第一次月考化学试题陕西省蓝田县焦岱中学2018-2019学年高二上学期第一次月考化学试题湖南省岳阳市岳阳县一中、汨罗市一中2019-2020学年高二10月联考化学试题陕西省咸阳市西藏民族大学附属中学2019-2020学年高二上学期期中考试化学试题山西省怀仁市重点中学2019-2020学年高二上学期期末考试化学试题云南省楚雄市楚雄实验中学2018—2019学年高二上学期9月月考化学试题湖北省黄冈市麻城市实验高中2020-2021学年高二上学期10月月考化学试题
11-12高二上·吉林长春·阶段练习
名校
3 . 密闭容器中有如下反应:L(s)+aG(g)  bR(g),温度和压强对该反应的影响如图所示,其中压强p1<p2,由此可判断( )
bR(g),温度和压强对该反应的影响如图所示,其中压强p1<p2,由此可判断( )

 bR(g),温度和压强对该反应的影响如图所示,其中压强p1<p2,由此可判断( )
bR(g),温度和压强对该反应的影响如图所示,其中压强p1<p2,由此可判断( )
| A.正反应为放热反应 |
| B.G的转化率随温度升高而减小 |
| C.化学方程式中的计量数a>b |
| D.增大压强,容器内气体质量不变 |
您最近一年使用:0次
2019-09-02更新
|
727次组卷
|
11卷引用:2012届福建省厦门外国语学校高三上学期10月份月考化学试卷
(已下线)2012届福建省厦门外国语学校高三上学期10月份月考化学试卷(已下线)2011-2012学年福建省福州文博中学高二下学期期中考试化学试卷2016届湖北省襄阳市保康县第一中学高三上学期期中测试化学试卷(已下线)2011-2012年吉林省长春外国语学校高二上学期第一次月考化学试卷(已下线)2011-2012学年江西省白鹭洲中学高二上学期期中考试化学(理)试卷(已下线)2012-2013学年安徽省舒城晓天中学高二上学期第一次月考化学试卷黑龙江省大庆铁人中学2019-2020学年高二上学期入学考试化学试题天津市静海区大邱庄中学等四校2019-2020学年高二10联考化学试题河南省三门峡市第一高级中学2020-2021学年高二上学期9月月考化学试题河北省衡水市武强中学2021-2022学年高二下学期期中考试化学试题广东省广州市第十七中学2022-2023学年高二上学期期中考试化学试题
10-11高三上·福建泉州·期末
名校
4 . 在10L密闭容器中,A、B、C三种气态物质构成了可逆反应的体系,当在某一温度时,A、B、C物质的量与时间的关系如图1,C的百分含量与温度的关系如图2。
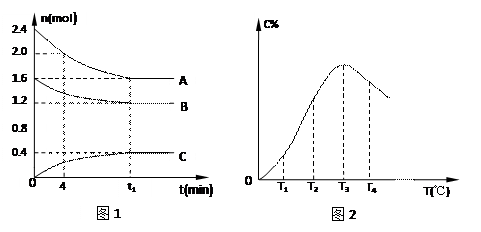
下列分析不正确的是

下列分析不正确的是
| A.0~4分钟时,A的平均反应速率为0.02mol/(L·min) |
B.该反应的平衡常数表达式 |
| C.由T1向T2变化时,V正 > V逆 |
| D.此反应的正反应为放热反应 |
您最近一年使用:0次
2019-01-30更新
|
759次组卷
|
6卷引用:福建省泉州市四校2010届高三上学期期末联考(化学)
(已下线)福建省泉州市四校2010届高三上学期期末联考(化学)(已下线)2015届山西大学附中高三上学期期中化学试卷2017届四川省广元市苍溪县高三零诊理综化学试卷(已下线)山东省济南市2019-2020年高三10月月考化学试题湖南师范大学附属中学2021届高三上学期第二次月考化学试题河北省保定市曲阳县第一高级中学2020-2021学年高二上学期第二次月考化学试题
名校
5 . T ℃时,在2 L密闭容器中使X(g)与Y(g)发生反应生成Z(g)。反应过程中X、Y、Z的物质的量的变化如图1所示;若保持其他条件不变,温度分别为T1和T2时,Z的百分含量与时间的关系如图2所示。则下列结论正确的是
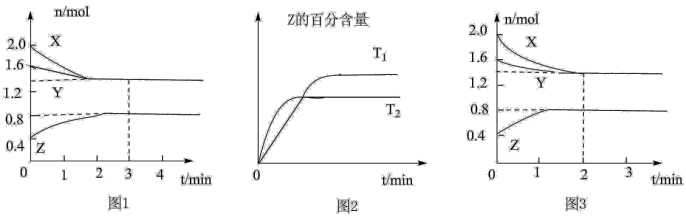

| A.容器中发生的反应可表示为3X(g)+Y(g) ==2Z(g) |
| B.反应进行的前3 min内,用X表示的反应速率v(X)=0.2 mol·L-1·min-1 |
| C.若改变反应条件,使反应进程如图3所示,则改变的条件是增大压强 |
| D.保持其他条件不变,升高温度,反应的化学平衡常数K减小 |
您最近一年使用:0次
名校
6 . 燃煤脱硫可减少SO2尾气的排放,燃煤脱硫技术受到各界科研人员的关注。一种燃煤脱硫技术的原理是:CaO(s)+3CO(g)+SO2(g) CaS(s)+3CO2(g)△H=-394.0kJ/mol,保持其他条件不变,不同温度下起始CO物质的量与平衡时体系中CO2的体积分数的关系如图所示(T表示温度)。下列有关说法正确的是
CaS(s)+3CO2(g)△H=-394.0kJ/mol,保持其他条件不变,不同温度下起始CO物质的量与平衡时体系中CO2的体积分数的关系如图所示(T表示温度)。下列有关说法正确的是
 CaS(s)+3CO2(g)△H=-394.0kJ/mol,保持其他条件不变,不同温度下起始CO物质的量与平衡时体系中CO2的体积分数的关系如图所示(T表示温度)。下列有关说法正确的是
CaS(s)+3CO2(g)△H=-394.0kJ/mol,保持其他条件不变,不同温度下起始CO物质的量与平衡时体系中CO2的体积分数的关系如图所示(T表示温度)。下列有关说法正确的是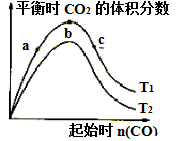
| A.T1比T2高 |
| B.b点SO2转化率最高 |
| C.b点后曲线下降是因CO体积分数升高 |
| D.减小压强可提高CO、SO2转化率 |
您最近一年使用:0次
2018-03-19更新
|
500次组卷
|
7卷引用:【全国百强校】福建省三明市第一中学2019届高三上学期第二次月考化学试题
【全国百强校】福建省三明市第一中学2019届高三上学期第二次月考化学试题河南省天一大联考2017届高三阶段性测试(三)(A)化学试题2020届高考化学二轮复习提升练习《 化学反应反应速率与反应平衡》(已下线)专题讲座(五)反应速率、平衡图像题解题策略(练) — 2022年高考化学一轮复习讲练测(新教材新高考)(已下线)第七章 化学反应速率与化学平衡 第44练 化学反应速率、平衡的常规图像内蒙古第一机械制造(集团)有限公司第一中学2019-2020学年高二10月月考化学试题四川省凉山彝族自治州2022-2023学年高二上学期期末检测化学试题
9-10高二下·广东东莞·期末
名校
7 . 在密闭容器中,对于可逆反应:A(?)+3B(?) 2C(g),平衡时C的体积分数与温度和压强的关系如图所示,下列判断正确的是
2C(g),平衡时C的体积分数与温度和压强的关系如图所示,下列判断正确的是

 2C(g),平衡时C的体积分数与温度和压强的关系如图所示,下列判断正确的是
2C(g),平衡时C的体积分数与温度和压强的关系如图所示,下列判断正确的是
| A.若正反应方向△H<0,则T1>T2 | B.压强增大时,混合气体的平均相对分子质量减小 |
| C.A一定为气体 | D.B一定为气体 |
您最近一年使用:0次
2018-01-16更新
|
628次组卷
|
19卷引用:2011届福建省三明一中高三上学期第三次月考化学试卷
(已下线)2011届福建省三明一中高三上学期第三次月考化学试卷(已下线)2015届山西大学附中高三上学期期中化学试卷(已下线)第六单元 化学反应速率和化学平衡测试题-2021年高考化学一轮复习名师精讲练【学科网名师堂】天津市七校联考2022届高三第二次质量调查化学试题(已下线)2010年广东省东莞市高二第二学期期末考试化学A卷(已下线)2011-2012学年广东省中山市高二下学期期末考试化学试卷(已下线)2013-2014四川省宜昌市部分市级示范高中春季期中考试高二化学试卷(已下线)2013-2014广东汕头市金山中学第一学期期末高二化学试卷2015-2016学年广东省湛江市高二上学期期末质检化学试卷2015-2016学年湖北省武汉三十九中高二上学期期末化学试卷河南省濮阳市2016-2017学年高二下学期升级(期末)考试(A卷)化学试题河北省张家口市第一中学2016-2017学年高一(衔接班)下学期期末考试(理)化学试题陕西省黄陵中学高新部2016-2017学年高一下学期期末考试化学试题广东省佛山市第一中学2017-2018学年高二上学期期中考试化学试题广东省普宁市华美实验学校2017-2018学年高二上学期第二次月考化学试题吉林省吉化第一高级中学校2017-2018学年高二上学期期末考试化学试题北京市通州区2019-2020学年高二下学期期末考试化学试题广东省台山市华侨中学2020-2021学年高二上学期第一次月考化学试题江西省吉安三中2021-2022学年高二上学期10月第一次段考化学试题
名校
8 . 如图所示,与对应的叙述相符的是


| A.图甲表示反应:4CO(g) +2NO2(g)==N2(g) +4CO2(g) ΔH<0,在其他条件不变的情况下,改变起始物CO的物质的量对此反应平衡的影响,则有T1<T2,b点处NO2的转化率最大 |
| B.图乙表示某条件对2A(g) +B(g)==3C(g)的影响,乙一定使用了催化剂 |
| C.图丙表示的某可逆反应是吸热反应,该图表明催化剂能同时改变正逆反应的活化能 |
D.图丁表示等量NO2在容积相同的恒容密闭容器中,不同温度下分别发生反应:2NO2(g) N2O4(g),相同时间后测得NO2含量的曲线,则该反应的ΔH>0 N2O4(g),相同时间后测得NO2含量的曲线,则该反应的ΔH>0 |
您最近一年使用:0次
2017-12-04更新
|
425次组卷
|
4卷引用:福建省三明市第一中学2018届高三上学期第二次月考化学试题



