1 . 为实现“双碳”目标,某科研所研究二氧化碳制备甲醇技术可实现二氧化碳资源化利用、降低碳排放。回答下列问题:
(1)在一定条件下,合成甲醇的过程中主要发生以下反应:
Ⅰ.CO2(g)+3H2(g) CH3OH(g)+H2O(g) △H1
CH3OH(g)+H2O(g) △H1
Ⅱ.CO2(g)+H2(g) CO(g)+H2O(g) △H2=+41kJ•mol-1
CO(g)+H2O(g) △H2=+41kJ•mol-1
Ⅲ.CO(g)+2H2(g) CH3OH(g) △H3=-90.5kJ•mol-1
CH3OH(g) △H3=-90.5kJ•mol-1
反应Ⅰ的△H1=_______ ;增大反应体系的压强(缩小容积),n(CH3OH)_______ (填“变大”“变小”或“不变”)。
(2)在3.0MPa和催化剂下,向1L密闭容器中充入1molCO2和3molH2,平衡时CO2的转化率与CH3OH、CO的选择性随温度的变化如图所示。
[CH3OH或CO的选择性=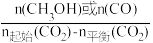 ×100%]
×100%]

图中X曲线代表_______ (填化学式)的选择性;150~250℃之间,以反应______ (填“Ⅰ”或“Ⅱ”)为主。
(3)在上述条件下,反应在200℃时,反应Ⅲ的浓度平衡常数Kc=_______ L2•mol-2(用计算式表示);250℃时,反应达到平衡时测得H2的物质的量为2.0mol,CH3OH的物质的量为0.25mol,则反应Ⅱ的压强平衡常数Kp=_______ (以分压表示,分压=总压×物质的量分数)。
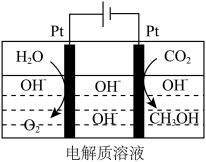
(4)该科研所除在催化剂下用氢气还原二氧化碳制取甲醇外,还研究用如图装置电解法制取甲醇。写出阴极上发生反应的电极反应式_______ 。
(1)在一定条件下,合成甲醇的过程中主要发生以下反应:
Ⅰ.CO2(g)+3H2(g)
 CH3OH(g)+H2O(g) △H1
CH3OH(g)+H2O(g) △H1Ⅱ.CO2(g)+H2(g)
 CO(g)+H2O(g) △H2=+41kJ•mol-1
CO(g)+H2O(g) △H2=+41kJ•mol-1Ⅲ.CO(g)+2H2(g)
 CH3OH(g) △H3=-90.5kJ•mol-1
CH3OH(g) △H3=-90.5kJ•mol-1反应Ⅰ的△H1=
(2)在3.0MPa和催化剂下,向1L密闭容器中充入1molCO2和3molH2,平衡时CO2的转化率与CH3OH、CO的选择性随温度的变化如图所示。
[CH3OH或CO的选择性=
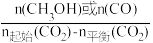 ×100%]
×100%]
图中X曲线代表
(3)在上述条件下,反应在200℃时,反应Ⅲ的浓度平衡常数Kc=
(4)该科研所除在催化剂下用氢气还原二氧化碳制取甲醇外,还研究用如图装置电解法制取甲醇。写出阴极上发生反应的电极反应式

您最近半年使用:0次
2 . 以乙烯、丙烯为代表的低碳烯烃是化学工业的最基本原料。回答下列问题:
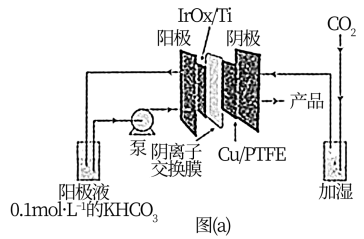
(1)一种电解还原CO2制乙烯的装置如图(a)所示,阴极上生成乙烯的电极反应式为___________ 。
(2)丙烷脱氢制烯烃反应及其常压下平衡常数自然对数值lnKp随温度(T)的变化如图(b)所示:

主反应:
Ⅰ.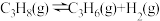
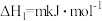
副反应:
Ⅱ.

Ⅲ.
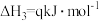
Ⅳ.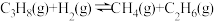

①图中属于吸热反应的是___________ (填标号)。
② =
=___________  。
。
③若只发生反应Ⅱ,则在w点时(若总压强为1MPa)丙烷的转化率为___________ (已知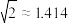 )。
)。
(3)甲醇乙烯烷基化制备丙烯主要反应有:
Ⅰ.

Ⅱ.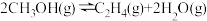
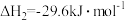
Ⅲ.
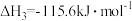
在总压强为0.2MPa,起始时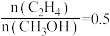 时,平衡时各物质的物质的量分数(yi)随温度变化如图(c)所示;起始时不同的
时,平衡时各物质的物质的量分数(yi)随温度变化如图(c)所示;起始时不同的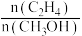 与平衡时各物质的物质的量分数(yi)之间的关系如图(d)所示。
与平衡时各物质的物质的量分数(yi)之间的关系如图(d)所示。
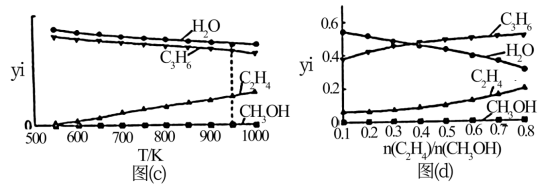
①图(c)中丙烯分压最大值不超过___________ MPa;温度高于550K时,随温度升高,yi(C2H4)不断增大的原因是___________ 。
②图(d)中随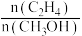 的增大,yi(H2O)不断减小的原因是
的增大,yi(H2O)不断减小的原因是___________ 。
③下列说法正确的是___________ (填字母)。
A.恒温下改变压强,丙烯的平衡产率不变
B.生产丙烯时,升高温度有利于丙烯的生成
C.实际生产中改进催化剂的选择性有利于提高丙烯的产率
D.其它条件不变时,适当增大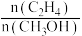 ,有利于提高丙烯的平衡产率
,有利于提高丙烯的平衡产率
(1)一种电解还原CO2制乙烯的装置如图(a)所示,阴极上生成乙烯的电极反应式为

(2)丙烷脱氢制烯烃反应及其常压下平衡常数自然对数值lnKp随温度(T)的变化如图(b)所示:

主反应:
Ⅰ.
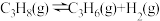
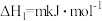
副反应:
Ⅱ.


Ⅲ.

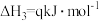
Ⅳ.
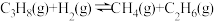

①图中属于吸热反应的是
②
 =
= 。
。③若只发生反应Ⅱ,则在w点时(若总压强为1MPa)丙烷的转化率为
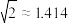 )。
)。(3)甲醇乙烯烷基化制备丙烯主要反应有:
Ⅰ.


Ⅱ.
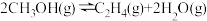
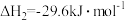
Ⅲ.

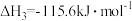
在总压强为0.2MPa,起始时
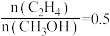 时,平衡时各物质的物质的量分数(yi)随温度变化如图(c)所示;起始时不同的
时,平衡时各物质的物质的量分数(yi)随温度变化如图(c)所示;起始时不同的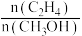 与平衡时各物质的物质的量分数(yi)之间的关系如图(d)所示。
与平衡时各物质的物质的量分数(yi)之间的关系如图(d)所示。
①图(c)中丙烯分压最大值不超过
②图(d)中随
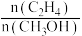 的增大,yi(H2O)不断减小的原因是
的增大,yi(H2O)不断减小的原因是③下列说法正确的是
A.恒温下改变压强,丙烯的平衡产率不变
B.生产丙烯时,升高温度有利于丙烯的生成
C.实际生产中改进催化剂的选择性有利于提高丙烯的产率
D.其它条件不变时,适当增大
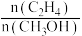 ,有利于提高丙烯的平衡产率
,有利于提高丙烯的平衡产率
您最近半年使用:0次
2021-09-04更新
|
304次组卷
|
2卷引用:湖北省九师联盟2022届高三上学期8月开学考化学试题
3 . 下列图示与对应的叙述不相符的是
A.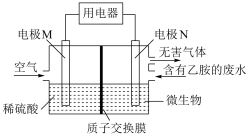 微生物燃料电池,可将工业废水中的乙胺(CH3CH2NH2)转化成环境友好的物质(M、N均为铂电极),N电极的电极反应式为2CH3CH2NH2+8H2O-30e-== 4CO2↑+N2↑+30H+ |
B. 反应xA(g)+yB(g)  zC(g)的ΔH>0,当n(A)/n(B)=2时,A、B的转化率之比为2:1 zC(g)的ΔH>0,当n(A)/n(B)=2时,A、B的转化率之比为2:1 |
C.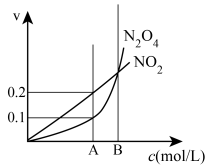 恒温恒容条件下,发生的可逆反应2NO2(g)  N2O4(g)中,各物质的浓度与其消耗速率之间的关系,其中A点对应的状态为化学平衡状态 N2O4(g)中,各物质的浓度与其消耗速率之间的关系,其中A点对应的状态为化学平衡状态 |
D.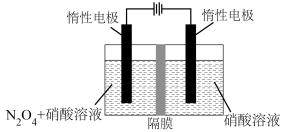 利用N2O4制备N2O5的装置(隔膜只允许H+通过,不允许H2O分子通过),其阳极的电极反应式为N2O4+2HNO3 —2e-== 2N2O5+2H+ |
您最近半年使用:0次
4 . (一)以四甲基氯化铵[(CH3)4NCl]水溶液为原料,通过电解法可以制备四甲基氢氧化铵[(CH3)4NOH],装置如图所示。
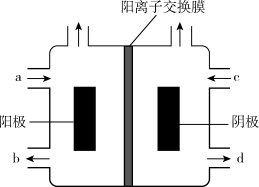
(1)收集到(CH3)4NOH的区域是_______ (填a、b、c或d)。
(2)写出电池总反应_______ 。
(二)乙酸乙酯一般通过乙酸和乙醇酯化合成:CH3COOH(l)+C2H5OH(l)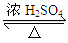 CH3COOC2H5(l)+H2O(l) ΔH=-2.7kJ·mol-1
CH3COOC2H5(l)+H2O(l) ΔH=-2.7kJ·mol-1
已知纯物质和相关恒沸混合物的常压沸点如下表:
请完成:
(1)关于该反应,下列说法不合理 的是_______ 。
A.反应体系中硫酸有催化作用
B.因为化学方程式前后物质的化学计量数之和相等,所以反应的ΔS等于零
C.因为反应的△H 接近于零,所以温度变化对平衡转化率的影响大
D.因为反应前后都是液态物质,所以压强变化对化学平衡的影响可忽略不计
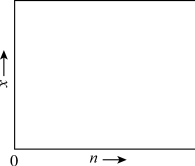
(2)一定温度下该反应的平衡常数K=4.0。若按化学方程式中乙酸和乙醇的化学计量数比例投料,则乙酸乙酯的平衡产率y =_______ ;若乙酸和乙醇的物质的量之比为n : 1,相应平衡体系中乙酸乙酯的物质的量分数为x,请在图中绘制x随n变化的示意图(计算时不计副反应)_______ 。
(3)工业上多采用乙酸过量的方法,将合成塔中乙酸、乙醇和硫酸混合液加热至110℃左右发生酯化反应并回流,直到塔顶温度达到70~71℃,开始从塔顶出料。控制乙酸过量的作用有_______ 。
(4)近年,科学家研究了乙醇催化合成乙酸乙酯的新方法:2C2H5OH(g) CH3COOC2H5(g)+2H2(g)
CH3COOC2H5(g)+2H2(g)
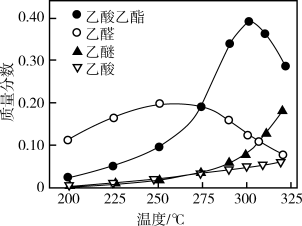
在常压下反应,冷凝收集,测得常温下液体收集物中主要产物的质量分数如图所示。关于该方法,下列推测合理的是_______ 。
A.反应温度不宜超过300℃
B.增大体系压强,有利于提高乙醇平衡转化率
C.在催化剂作用下,乙醛是反应历程中的中间产物
D.提高催化剂的活性和选择性,减少乙醚、乙烯等副产物是工艺的关键

(1)收集到(CH3)4NOH的区域是
(2)写出电池总反应
(二)乙酸乙酯一般通过乙酸和乙醇酯化合成:CH3COOH(l)+C2H5OH(l)
 CH3COOC2H5(l)+H2O(l) ΔH=-2.7kJ·mol-1
CH3COOC2H5(l)+H2O(l) ΔH=-2.7kJ·mol-1已知纯物质和相关恒沸混合物的常压沸点如下表:
| 纯物质 | 沸点/℃ | 恒沸混合物(质量分数) | 沸点/℃ |
| 乙醇 | 78.3 | 乙酸乙酯(0.92)+水(0.08) | 70.4 |
| 乙酸 | 117.9 | 乙酸乙酯(0.69)+乙醇(0.31) | 71.8 |
| 乙酸乙酯 | 77.1 | 乙酸乙酯(0.83)+乙醇(0.08) +水(0.09) | 70.2 |
请完成:
(1)关于该反应,下列说法
A.反应体系中硫酸有催化作用
B.因为化学方程式前后物质的化学计量数之和相等,所以反应的ΔS等于零
C.因为反应的△H 接近于零,所以温度变化对平衡转化率的影响大
D.因为反应前后都是液态物质,所以压强变化对化学平衡的影响可忽略不计
(2)一定温度下该反应的平衡常数K=4.0。若按化学方程式中乙酸和乙醇的化学计量数比例投料,则乙酸乙酯的平衡产率y =

(3)工业上多采用乙酸过量的方法,将合成塔中乙酸、乙醇和硫酸混合液加热至110℃左右发生酯化反应并回流,直到塔顶温度达到70~71℃,开始从塔顶出料。控制乙酸过量的作用有
(4)近年,科学家研究了乙醇催化合成乙酸乙酯的新方法:2C2H5OH(g)
 CH3COOC2H5(g)+2H2(g)
CH3COOC2H5(g)+2H2(g)在常压下反应,冷凝收集,测得常温下液体收集物中主要产物的质量分数如图所示。关于该方法,下列推测合理的是

A.反应温度不宜超过300℃
B.增大体系压强,有利于提高乙醇平衡转化率
C.在催化剂作用下,乙醛是反应历程中的中间产物
D.提高催化剂的活性和选择性,减少乙醚、乙烯等副产物是工艺的关键
您最近半年使用:0次
2018-11-09更新
|
2237次组卷
|
4卷引用:浙江省普通高校招生选考科目2018年4月考试化学试题
浙江省普通高校招生选考科目2018年4月考试化学试题三轮冲刺2020届高三化学考题必刷——有机物制备类探究实验题山东省滕州市第一中学2020届高三3月线上模拟考试化学试题(已下线)专题20.化学反应原理综合应用-十年(2012-2021)高考化学真题分项汇编(浙江专用)
5 . 丙烯是重要的有机化工原料,丁烯催化裂解法是一种重要的丙烯生产法,生产过程中会有生成乙烯的副反应发生。
反应如下:I主反应,3C4H8(g)=4C3H6(g) △H1
II副反应: C4H8(g)=2C2H4(g) △H2
(1) 已知丁烯的燃烧热△H3=-akJ/mol 丙烯的燃烧热△H4=-bkJ/mol。 计算: △H1=____ kJ/mol
(2) 以ZSM-5分子筛作为催化剂,测得上述两反应的平衡体系中,各组分的质量分数(w%)随温度(T) 和压强(p)变化的趋势分别如图1和图2所示:
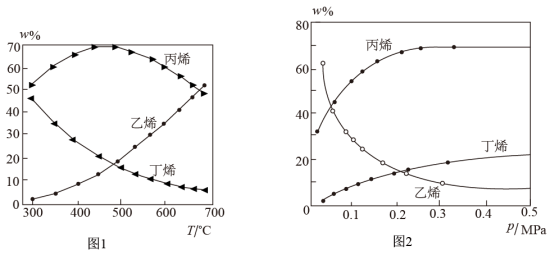
① 下列说法正确的是______ 。
A.随温度升高反应II的正反应速率增大,逆反应速率减小
B.温度可影响产物的选择性
C.根据350℃时各物质的质量分数可知,反应I的活化能低于反应II
D.制备丙烯适宜的温度和压强分别为600℃,0.5Mpa
②若某温度下反应达到平衡时C4H8、C3H6、C2H4的体积分数分别为20%、70%、10%,平衡时总压强为P,请计算该温度下反应的平衡常数Kp=_______ (Kp为用气体的分压表示的平衡常数,分压=气体的体积分数×体系总压)
③图2 中,随压强增大,平衡体系中丙烯的质量分数呈上升趋势,从平衡角度解释其原因是__________________ 。
(3) 在恒温恒容体系中,充入一定量的丁烯,转化率随时间的变化如图。在实际生产中,通常在恒压条件下以氮气作为反应体系的稀释剂,请在下图中画出恒压条件丁烯的转化率随时间变化由线_______ 。
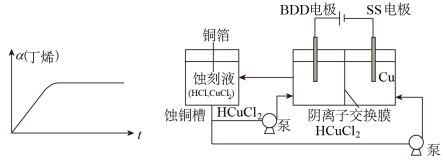
(4) 有研究者用HCl和CuCl2的混合液做蚀刻液,浸泡铜板可制备印刷电路板,蚀铜结束会产生大量含HCuC12废液。采用如图所示装置可直接从水中电解产生具有强氧化性的氢氧自由基(HO·),再进一步反应可实现阳极区蚀刻液再生的目的。
阳极区发生的反应为:_____________ ,H++CuCl2-+ HO·=Cu2++2Cl-+H2O
反应如下:I主反应,3C4H8(g)=4C3H6(g) △H1
II副反应: C4H8(g)=2C2H4(g) △H2
(1) 已知丁烯的燃烧热△H3=-akJ/mol 丙烯的燃烧热△H4=-bkJ/mol。 计算: △H1=
(2) 以ZSM-5分子筛作为催化剂,测得上述两反应的平衡体系中,各组分的质量分数(w%)随温度(T) 和压强(p)变化的趋势分别如图1和图2所示:

① 下列说法正确的是
A.随温度升高反应II的正反应速率增大,逆反应速率减小
B.温度可影响产物的选择性
C.根据350℃时各物质的质量分数可知,反应I的活化能低于反应II
D.制备丙烯适宜的温度和压强分别为600℃,0.5Mpa
②若某温度下反应达到平衡时C4H8、C3H6、C2H4的体积分数分别为20%、70%、10%,平衡时总压强为P,请计算该温度下反应的平衡常数Kp=
③图2 中,随压强增大,平衡体系中丙烯的质量分数呈上升趋势,从平衡角度解释其原因是
(3) 在恒温恒容体系中,充入一定量的丁烯,转化率随时间的变化如图。在实际生产中,通常在恒压条件下以氮气作为反应体系的稀释剂,请在下图中画出恒压条件丁烯的转化率随时间变化由线

(4) 有研究者用HCl和CuCl2的混合液做蚀刻液,浸泡铜板可制备印刷电路板,蚀铜结束会产生大量含HCuC12废液。采用如图所示装置可直接从水中电解产生具有强氧化性的氢氧自由基(HO·),再进一步反应可实现阳极区蚀刻液再生的目的。
阳极区发生的反应为:
您最近半年使用:0次



