名校
解题方法
1 . 可逆反应aA(g)+bB(s) cC(g)+dD(g),其他条件不变,C的物质的量分数和温度(T)或压强(p)的关系如图所示,其中正确的是
cC(g)+dD(g),其他条件不变,C的物质的量分数和温度(T)或压强(p)的关系如图所示,其中正确的是

 cC(g)+dD(g),其他条件不变,C的物质的量分数和温度(T)或压强(p)的关系如图所示,其中正确的是
cC(g)+dD(g),其他条件不变,C的物质的量分数和温度(T)或压强(p)的关系如图所示,其中正确的是
| A.使用催化剂C的物质的量分数增加 |
| B.已知T2>T1,升高温度能提高A的转化率 |
| C.已知p2>p1,则化学计量数:a<c+d |
| D.若该反应在恒容中进行,通入氦气(不参与反应),使压强增大,将加快该反应的速率 |
您最近半年使用:0次
名校
2 . 已知某可逆反应mA(g)+ nB(g) p C(g);在密闭容器中进行,下图表示在不同反应时间t、温度T和压强P与反应物B在混合气体中的百分含量B%的关系曲线,由曲线分析,下列判断正确的是
p C(g);在密闭容器中进行,下图表示在不同反应时间t、温度T和压强P与反应物B在混合气体中的百分含量B%的关系曲线,由曲线分析,下列判断正确的是

 p C(g);在密闭容器中进行,下图表示在不同反应时间t、温度T和压强P与反应物B在混合气体中的百分含量B%的关系曲线,由曲线分析,下列判断正确的是
p C(g);在密闭容器中进行,下图表示在不同反应时间t、温度T和压强P与反应物B在混合气体中的百分含量B%的关系曲线,由曲线分析,下列判断正确的是
| A.T1<T2、P1>P2、m+n>P,ΔH <0 |
| B.T1>T2、P1<P2、m+n<P,ΔH >0 |
| C.T1<T2、P1>P2、m+n<P,ΔH <0 |
| D.T1>T2、P1<P2、m+n>P,ΔH >0 |
您最近半年使用:0次
2022-12-21更新
|
1060次组卷
|
34卷引用:广东省阳东广雅学校2017-2018学年高二11月月考化学试题
广东省阳东广雅学校2017-2018学年高二11月月考化学试题广西壮族自治区百色市田阳高中2019-2020学年高二上学期12月月考理科综合化学试题四川省资阳市2019-2020学年高二上学期期末质量检测化学试题黑龙江省鹤岗市第一中学2019-2020学年高一下学期期末考试化学试题(已下线)第17讲 化学平衡计算与图像-2021年高考化学一轮复习名师精讲练(已下线)第2章 章末检测-2020-2021学年高二化学同步课堂帮帮帮(人教版选修4)河南省洛阳市孟津县第二高级中学2020-2021学年高二上学期9月月考化学试题(已下线)【南昌新东方】6. 南昌十七中 颜毅吉林省通化县综合高级中学2020-2021学年高二上学期期中考试化学试题西藏自治区拉萨市第二高级中学2019-2020学年高二上学期期末考试化学试题甘肃省会宁县第一中学2020-2021学年高二上学期期中考试化学(理)试题河北省唐山市遵化市2020-2021学年高二上学期期中考试化学试题广东省梅州市2020-2021学年高二上学期第二次质检考试化学试题四川省射洪中学校2020-2021学年高二上学期第三次月考化学试题云南省玉溪第二中学2020-2021学年高二上学期期中质量检测化学试题江西省赣州市信丰中学2020-2021学年高二上学期入学考试化学试题山西省沁源县第一中学2020-2021学年高二下学期开学考试化学试题河南省许昌市第三中学2020-2021学年高二3月月考化学试题(已下线)专题讲座(五)反应速率、平衡图像题解题策略(讲) — 2022年高考化学一轮复习讲练测(新教材新高考)山西省太原市山西英才学校2021-2022学年高二上学期月考化学试题湖北省襄阳市南漳县第二中学2021-2022学年高二上学期10月考化学试题广东省执信中学番禺附属学校2021-2022学年高二上学期期中考试化学试题吉林省辉南县第一中学2021-2022学年高二上学期第三次月考化学试题江西省丰城市第九中学2022-2023学年高二上学期入学质量检测化学试题河南省洛阳市新安县第一高级中学2021-2022学年高二上学期10月月考化学试题陕西省安康市汉滨区五里高级中学2021-2022学年高二上学期期中考试化学试题河南宏力学校2021-2022学年高二上学期期中考试化学试题广西贺州市钟山县钟山中学2020-2021学年高二下学期第三次月考理科化学试题天津市南仓中学2022-2023学年高二上学期1月期末考试化学试题新疆阿克苏市实验中学2022-2023学年高二上学期期末考试化学试题(已下线)第七章 化学反应速率与化学平衡 第44讲 化学反应速率、平衡的常规图像四川省青神中学校2022-2023学年高二下学期3月月考化学试题江西省抚州市2023-2024学年高二上学期学生学业质量监测化学试题江西省新余市第一中学2023-2024学年高二下学期开学考试化学试题
名校
解题方法
3 .  在KI溶液中存在下列平衡:
在KI溶液中存在下列平衡:
 。某
。某 、KI混合溶液中,
、KI混合溶液中, 的物质的量浓度
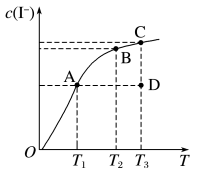
的物质的量浓度 与温度T的关系如图所示(曲线上任何一点都表示平衡状态)。下列说法不正确的是
与温度T的关系如图所示(曲线上任何一点都表示平衡状态)。下列说法不正确的是
 在KI溶液中存在下列平衡:
在KI溶液中存在下列平衡:
 。某
。某 、KI混合溶液中,
、KI混合溶液中, 的物质的量浓度
的物质的量浓度 与温度T的关系如图所示(曲线上任何一点都表示平衡状态)。下列说法不正确的是
与温度T的关系如图所示(曲线上任何一点都表示平衡状态)。下列说法不正确的是
A.该反应 |
B.若在 、 、 温度下,反应的平衡常数分别为 温度下,反应的平衡常数分别为 、 、 ,则 ,则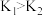 |
C.若反应进行到状态D时,一定有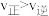 |
D.状态A与状态B相比,状态A的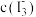 大 大 |
您最近半年使用:0次
2022-11-27更新
|
262次组卷
|
9卷引用:【市级联考】山东省烟台市2019届高三上学期期末考试化学试题
【市级联考】山东省烟台市2019届高三上学期期末考试化学试题【全国百强校】福建省厦门市双十中学2018-2019学年高二下学期第一次月考化学试题黑龙江省牡丹江市东宁市第一中学2020-2021学年高二上学期第一次月考化学试题河北省衡水市第十四中学2020-2021学年高二上学期三调考试(校内)化学试题黑龙江省实验中学2021-2022学年高二上学期期中考试化学试题黑龙江省哈尔滨市第二十四中学2022-2023学年高二10月月考化学试题四川省成都市树德中学2022-2023学年高二上学期11月阶段性测试化学试题吉林省延边第二中学2022-2023学年高二上学期期末考试化学试题新疆阿克苏市实验中学2022-2023学年高二上学期期末考试化学试题
名校
解题方法
4 . 利用 和
和 在催化剂的作用下合成甲醇,发生反应:
在催化剂的作用下合成甲醇,发生反应: 。在体积一定的密闭容器中按物质的量之比
。在体积一定的密闭容器中按物质的量之比 充入
充入 和
和 ,测得平衡混合物中
,测得平衡混合物中 的体积分数在不同压强下随温度的变化情况如图(a)所示。现有两个体积相同的恒容密闭容器甲和乙,向甲中加入1molCO和2mol
的体积分数在不同压强下随温度的变化情况如图(a)所示。现有两个体积相同的恒容密闭容器甲和乙,向甲中加入1molCO和2mol ,向乙中加入2molCO和4mol
,向乙中加入2molCO和4mol ,测得不同温度下
,测得不同温度下 的平衡转化率如图(b)所示。
的平衡转化率如图(b)所示。
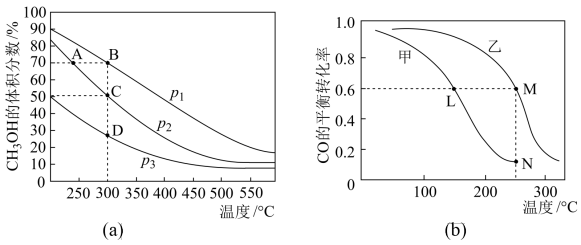
(1)反应的
_______ 0(填“>”“<”或“=”,后同),
_______  。
。
(2)达到平衡时,反应速率:A点_______ B点。平衡常数:C点_______ D点。
(3)在C点时,CO的转化率为_______ 。
(4)L、M两点容器内压强:
_______ 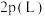 。
。
 和
和 在催化剂的作用下合成甲醇,发生反应:
在催化剂的作用下合成甲醇,发生反应: 。在体积一定的密闭容器中按物质的量之比
。在体积一定的密闭容器中按物质的量之比 充入
充入 和
和 ,测得平衡混合物中
,测得平衡混合物中 的体积分数在不同压强下随温度的变化情况如图(a)所示。现有两个体积相同的恒容密闭容器甲和乙,向甲中加入1molCO和2mol
的体积分数在不同压强下随温度的变化情况如图(a)所示。现有两个体积相同的恒容密闭容器甲和乙,向甲中加入1molCO和2mol ,向乙中加入2molCO和4mol
,向乙中加入2molCO和4mol ,测得不同温度下
,测得不同温度下 的平衡转化率如图(b)所示。
的平衡转化率如图(b)所示。
(1)反应的


 。
。(2)达到平衡时,反应速率:A点
(3)在C点时,CO的转化率为
(4)L、M两点容器内压强:

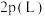 。
。
您最近半年使用:0次
9-10高二下·重庆·期末
名校
解题方法
5 . 温度为T时,在2 L容积不变的密闭容器中使X(g)与Y(g)发生反应生成Z(g)。反应过程中X、Y、Z的浓度变化如图1所示;若保持其他条件不变,温度分别为T1和T2时,Y的体积分数与时间的关系如图2所示。则下列结论错误 的是
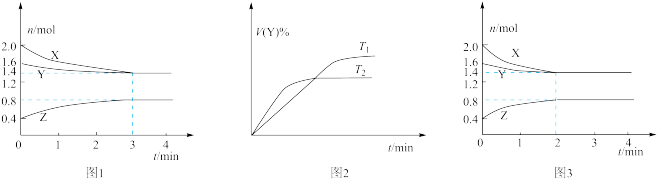

A.容器中发生的反应可表示为:3X(g)+Y(g) 2Z(g) 2Z(g) |
| B.若改变反应条件,使反应进程如图3所示,则改变的条件是使用催化剂 |
| C.反应进行的前3 min内,用X表示的反应速率v(X)=0.1 mol·L-1·min-1 |
| D.保持其他条件不变,升高温度,平衡逆向移动 |
您最近半年使用:0次
2022-10-22更新
|
74次组卷
|
6卷引用:09-10年万州二中高二下学期期末考试化学卷
(已下线)09-10年万州二中高二下学期期末考试化学卷(已下线)2011届四川省资阳市资阳中学高三第一次高考模拟(理综)化学部分(已下线)2013-2014黑龙江省鹤岗一中高一下学期期末考试化学试卷(已下线)2014~2015学年江西四校9月联考高二化学试卷北京市顺义牛栏山第一中学2022-2023学年高二上学期10月月考化学试题北京市顺义区第一中学2023-2024学年高二上学期10月月考化学试题
2019高三·全国·专题练习
名校
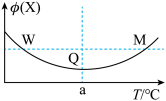
6 . 在某恒家密闭容器中充入一定量的X和Y发生反应: 反应过程中持续升高温度,测得混合体系中X的体积分数与温度的关系如图所示,下列推断正确的是
反应过程中持续升高温度,测得混合体系中X的体积分数与温度的关系如图所示,下列推断正确的是
 反应过程中持续升高温度,测得混合体系中X的体积分数与温度的关系如图所示,下列推断正确的是
反应过程中持续升高温度,测得混合体系中X的体积分数与温度的关系如图所示,下列推断正确的是
| A.M点时,Y的转化率最大 |
| B.升高温度,平衡逆向移动 |
| C.平衡后充入Z,达到新平衡时Z的体积分数增大 |
| D.W、M两点Y的正反应速率相同 |
您最近半年使用:0次
2022-10-18更新
|
233次组卷
|
8卷引用:专题7.2 化学平衡状态 化学平衡移动(练)-《2020年高考一轮复习讲练测》
(已下线)专题7.2 化学平衡状态 化学平衡移动(练)-《2020年高考一轮复习讲练测》河北省鸡泽县第一中学2020-2021学年高二上学期第一次月考化学试题(已下线)第23讲 化学平衡状态 化学平衡的移动(精练)-2021年高考化学一轮复习讲练测成都市实验外国语学校(西区)2020-2021学年高二上学期化学学科期中测试卷黑龙江省哈尔滨市宾县第一中学2021届高三上学期第三次月考化学试题重庆市第七中学校2020-2021学年高二上学期12月考化学试题江西省抚州市临川第二中学2022-2023学年高二上学期第一次月考化学试题黑龙江省佳木斯市第一中学2023-2024学年高二上学期10月月考化学试题
名校
解题方法
7 . 一定温度下,在2L的密闭容器中,X、Y、Z三种气体的物质的量随时间t(单位为分钟)变化的曲线如图,下列描述正确的是
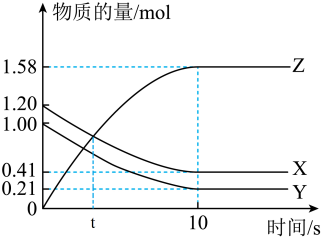

| A.t分钟时该反应达到化学平衡状态 |
B.反应开始到10分钟,用X表示的反应速率为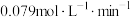 |
| C.反应开始到10分钟时,Y的转化率为79.0% |
D.反应的化学方程式为: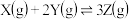 |
您最近半年使用:0次
2022-10-08更新
|
513次组卷
|
6卷引用:【全国校级联考】浙江省温州市十五校联合体2017-2018学年高一下学期期中联考化学试题
8 . 利用I2O5可消除CO污染,反应为I2O5(s)+5CO(g)⇌5CO2(g)+I2(s)。不同温度下,向装有足量的I2O5 固体的2L恒容密闭容器中通入2mol CO,测得CO的体积分数 (CO)随时间t变化曲线如图。
(CO)随时间t变化曲线如图。
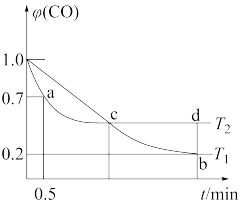
(1)此反应的平衡常数表达式____________ 。
(2)到a点时表示的化学反应速率v(CO)=____________ 。
(3)b点时CO的转化率____________ 。
(4)Kb_______ Kd(填“大于”“小于”或“等于”),原因是_______________ 。
(5)此反应的ΔH________ 0(填“大于”“小于”或“等于”)。
 (CO)随时间t变化曲线如图。
(CO)随时间t变化曲线如图。
(1)此反应的平衡常数表达式
(2)到a点时表示的化学反应速率v(CO)=
(3)b点时CO的转化率
(4)Kb
(5)此反应的ΔH
您最近半年使用:0次
9 . I.据报道,我国在南海北部神狐海域进行的可燃冰(甲烷的水合物)试采获得成功。甲烷是一种重要的化工原料。
(1)甲烷重整是提高甲烷利用率的重要方式,除部分氧化外还有以下两种:
水蒸气重整:CH4(g)+H2O(g) CO(g)+3H2(g) △H1=+205.9kJ·mol-1①
CO(g)+3H2(g) △H1=+205.9kJ·mol-1①
CO(g)+H2O(g) CO2(g)+H2(g) △H2=-41.2kJ·mol-1②
CO2(g)+H2(g) △H2=-41.2kJ·mol-1②
二氧化碳重整:CH4(g)+CO2(g) 2CO(g)+2H2(g) △H3③
2CO(g)+2H2(g) △H3③
则反应①自发进行的条件是____ ,△H3=____ kJ·mol-1。
II.氮的固定一直是科学家研究的重要课题,合成氨则是人工固氮比较成熟的技术,其原理为N2(g)+3H2(g) 2NH3(g)。
2NH3(g)。
(2)在不同温度、压强和相同催化剂条件下,初始N2、H2分别为0.1mol、0.3mol时,平衡后混合物中氮的体积分数(φ)如图所示。
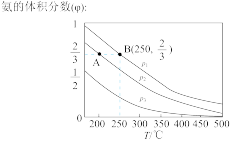
①其中,p1、p2和p3由大到小的顺序是____ ,其原因是____ 。
②若分别用VA(N2)和VB(N2)表示从反应开始至达平衡状态A、B时的化学反应速率,则VA(N2)____ VB(N2)(填“>”“<”或“=”)。
③若在250℃、p1为104Pa条件下,反应达到平衡时容器的体积为1L,则该条件下B点N2的分压p(N2)为_____ Pa(分压=总压×物质的量分效,保留一位小数)。
III.以连二硫酸根(S2O )为媒介,使用间接电化学法也可处理燃煤烟气中的NO,装置如图所示:
)为媒介,使用间接电化学法也可处理燃煤烟气中的NO,装置如图所示:
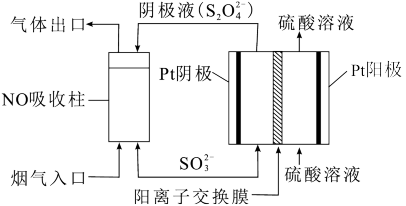
(3)①阴极区的电极反应式为____ 。
②NO吸收转化后的主要产物为NH ,若通电时电路中转移了0.3mole-,则此通电过程中理论上吸收的NO在标况下的体积为
,若通电时电路中转移了0.3mole-,则此通电过程中理论上吸收的NO在标况下的体积为____ mL。
(1)甲烷重整是提高甲烷利用率的重要方式,除部分氧化外还有以下两种:
水蒸气重整:CH4(g)+H2O(g)
 CO(g)+3H2(g) △H1=+205.9kJ·mol-1①
CO(g)+3H2(g) △H1=+205.9kJ·mol-1①CO(g)+H2O(g)
 CO2(g)+H2(g) △H2=-41.2kJ·mol-1②
CO2(g)+H2(g) △H2=-41.2kJ·mol-1②二氧化碳重整:CH4(g)+CO2(g)
 2CO(g)+2H2(g) △H3③
2CO(g)+2H2(g) △H3③则反应①自发进行的条件是
II.氮的固定一直是科学家研究的重要课题,合成氨则是人工固氮比较成熟的技术,其原理为N2(g)+3H2(g)
 2NH3(g)。
2NH3(g)。(2)在不同温度、压强和相同催化剂条件下,初始N2、H2分别为0.1mol、0.3mol时,平衡后混合物中氮的体积分数(φ)如图所示。

①其中,p1、p2和p3由大到小的顺序是
②若分别用VA(N2)和VB(N2)表示从反应开始至达平衡状态A、B时的化学反应速率,则VA(N2)
③若在250℃、p1为104Pa条件下,反应达到平衡时容器的体积为1L,则该条件下B点N2的分压p(N2)为
III.以连二硫酸根(S2O
 )为媒介,使用间接电化学法也可处理燃煤烟气中的NO,装置如图所示:
)为媒介,使用间接电化学法也可处理燃煤烟气中的NO,装置如图所示:
(3)①阴极区的电极反应式为
②NO吸收转化后的主要产物为NH
 ,若通电时电路中转移了0.3mole-,则此通电过程中理论上吸收的NO在标况下的体积为
,若通电时电路中转移了0.3mole-,则此通电过程中理论上吸收的NO在标况下的体积为
您最近半年使用:0次
2022-09-22更新
|
107次组卷
|
8卷引用:广东省揭阳市2018高三高考第一次模拟考试理综化学试题
广东省揭阳市2018高三高考第一次模拟考试理综化学试题云南省昆明市寻甸一中2020届高三第一次全真模拟考试理综化学试题甘肃省高台县第一中学2020届高三上学期期中考试化学试题山西省太原市第五中学2021-2022学年上学期高三第四次模块诊断化学试题(已下线)一轮巩固卷10-【赢在高考·黄金20卷】备战2022年高考化学模拟卷(全国卷专用)(已下线)专题12 化学反应原理综合题—2022年高考化学二轮复习讲练测(全国版)-练习福建泉州实验中学2021-2022学年高三上学期12月月考化学试题福建省宁德第一中学2022-2023学年高二上学期第二次月考化学试题
名校
10 . 给定物质A、B、C的量,在一定条件下发生反应,建立如下化学平衡: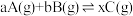 ,符合下图所示的关系(c%表示平衡混合气中产物C的百分含量。T表示温度,P表示压强)。在图中,Y轴是指
,符合下图所示的关系(c%表示平衡混合气中产物C的百分含量。T表示温度,P表示压强)。在图中,Y轴是指
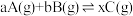 ,符合下图所示的关系(c%表示平衡混合气中产物C的百分含量。T表示温度,P表示压强)。在图中,Y轴是指
,符合下图所示的关系(c%表示平衡混合气中产物C的百分含量。T表示温度,P表示压强)。在图中,Y轴是指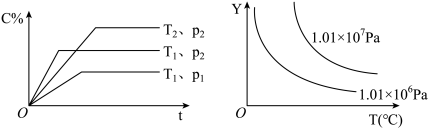
| A.反应物A的百分含量 | B.平衡混合气的总物质的量 | C.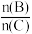 比值 比值 | D.反应物B的平衡转化率 |
您最近半年使用:0次
2022-09-13更新
|
670次组卷
|
4卷引用:福建省厦门第一中学2020-2021学年高二上学期期中考试化学试题



