10-11高二下·浙江嘉兴·阶段练习
名校
1 . 反应:L(s)+aG(g) bR(g)达到平衡时,温度和压强对该反应的影响如图所示:图中压强p1>p2,x轴表示温度,y轴表示平衡混合气中G的体积分数。据此可判断( )
bR(g)达到平衡时,温度和压强对该反应的影响如图所示:图中压强p1>p2,x轴表示温度,y轴表示平衡混合气中G的体积分数。据此可判断( )

 bR(g)达到平衡时,温度和压强对该反应的影响如图所示:图中压强p1>p2,x轴表示温度,y轴表示平衡混合气中G的体积分数。据此可判断( )
bR(g)达到平衡时,温度和压强对该反应的影响如图所示:图中压强p1>p2,x轴表示温度,y轴表示平衡混合气中G的体积分数。据此可判断( )
| A.上述反应是放热反应 | B.上述反应是吸热反应 |
| C.a+1>b | D.a+1<b |
您最近一年使用:0次
2019-10-11更新
|
63次组卷
|
3卷引用:安徽省阜阳市阜南县实验中学2019-2020学年高一下学期6月月考化学试题
安徽省阜阳市阜南县实验中学2019-2020学年高一下学期6月月考化学试题(已下线)2010—2011学年浙江省海盐元济高级中学高二3月月考化学试卷宁夏青铜峡市高级中学(吴忠中学分校)2019-2020学年高二上学期第一次月考化学试题
11-12高二上·江西赣州·期中
名校
2 . 可逆反应mA(固)+nB(气)⇌pC(气)+qD(气),反应过程中其它条件不变时C的百分含量C%与温度(T)和压强(P)的关系如图所示,下列叙述中正确的是
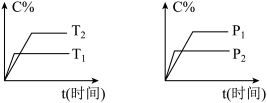

| A.达到平衡后,使用催化剂,C%将增大 |
| B.达到平衡后,若升高温度、化学平衡向逆反应方向移动 |
| C.方程式中n>p+q |
| D.达到平衡后,增加A的量有利于化学平衡向正反应方向移动 |
您最近一年使用:0次
2019-10-05更新
|
1842次组卷
|
39卷引用:安徽省六安市二中2018-2019学年高二第一学期10月月考化学试题
安徽省六安市二中2018-2019学年高二第一学期10月月考化学试题(已下线)2014-2015学年吉林延边二中高二9月阶段考试化学试卷2015-2016学年浙江台州中学高二上第三次统练化学试卷2016-2017学年河北省定州二中高二上学期第一次月考化学试卷2016-2017学年宁夏吴忠中学高二下学期第一次月考化学试卷【全国百强校】甘肃省静宁县第一中学2018-2019学年高二上学期10月月考化学试题【校级联考】广东省汕头市达濠华侨中学、东厦中学2018-2019学年高二(理)上学期阶段测试(二)化学试题湖北省恩施州巴东县第二高级中学2019-2020学年高一下学期网课质量检测化学试题江西省上饶市横峰中学2020-2021学年高二上学期第一次月考化学(统招班)试题安徽省怀宁县第二中学2021-2022学年高二上学期期中考试化学试题云南省文山州广南县第二中学校2021-2022学年高二上学期12月考试化学试题黑龙江省虎林市高级中学2023-2024学年高二上学期第一次月考化学试题(已下线)2011-2012学年江西省兴国县将军中学高二上学期期中考试化学试卷(已下线)2011-2012学年内蒙古包头三十三中高二上学期期末考试化学试卷(已下线)2012-2013学年黑龙江省集贤县第一中学高二上学期期末考试化学试卷(已下线)2014-2015学年云南省玉溪市第一中学高二上学期期中考试化学试卷2014-2015学年内蒙古巴彦淖尔市一中高二上学期期中化学试卷2014-2015学年福建省晋江市季延中学高二下学期期中考试化学试卷2016-2017学年甘肃省嘉峪关市酒钢三中高二上学期期末考试化学试卷四川省泸州泸县第五中学2018届高三上学期期末考试理综化学试题吉林省吉林地区普通高中友好学校联合体2017-2018学年高二上学期期末考试化学试题甘肃省白银市会宁县第一中学2019-2020学年高二上学期期中考试化学(理)试题广东省广州市第八十九中学2019-2020学年高二上学期期中考试化学试题湖南省永州市宁远县第一中学2019-2020学年高二上学期期中考试化学试题福建省莆田四中2019-2020学年高二上学期期中考试化学试题山东省德州市陵城区第一中学2019-2020学年高二上学期期中考试化学试题云南省曲靖市陆良县第十中学2019-2020学年高二上学期期末考试化学试题甘肃省兰州大学附属中学(33中)2019-2020学年高二上学期期中考试化学试题广西桂林市第十八中学2019-2020学年高二下学期期中考试化学试题甘肃省天水市武山县三校2020-2021学年高二上学期期中联考化学试题 吉林省吉化第一高级中学校2020-2021学年高二上学期期末考试化学试题宁夏固原市隆德县2020-2021学年高二上学期期末考试化学试题湖南省湘潭电机子弟中学2019-2020学年高二下学期期中考试化学(理)试题河南省登封市第一高级中学2019-2020学年高二上学期期中考试化学试题广东省汕尾市2021-2022学年高一年级下学期期末考试化学试题广东省江门广雅中学2022-2023学年高二上学期期中考试化学试题浙江省宁波市奉化区2022-2023学年高二上学期期末联考化学试题辽宁省名校联盟2023-2024学年高二上学期期初考试化学试题辽宁省锦州市黑山县名校联盟试2023-2024学年高二上学期开学考试化学试题
名校
3 . 根据下列图示所得出的结论正确的是( )
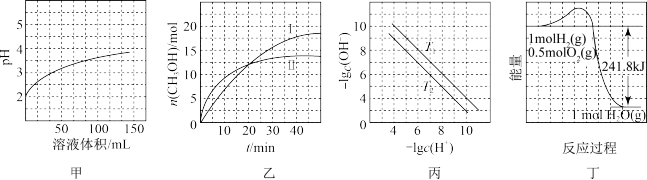

| A.图甲表示1 mL pH=2某一元酸溶液加水稀释时,pH随溶液总体积的变化曲线,说明该酸是强酸 |
B.图乙表示恒容密闭容器中其他条件相同时改变温度,反应CO2(g)+3H2(g)  CH3OH(g)+H2O(g)中n(CH3OH)随时间的变化曲线,说明反应平衡常数KⅠ>KⅡ CH3OH(g)+H2O(g)中n(CH3OH)随时间的变化曲线,说明反应平衡常数KⅠ>KⅡ |
| C.图丙表示不同温度下水溶液中-lg c(H+)、-lg c(OH-)变化曲线,说明T1>T2 |
| D.图丁表示1 mol H2和0.5 mol O2反应生成1 mol H2O过程中的能量变化曲线,说明H2的燃烧热是241.8 kJ·mol-1 |
您最近一年使用:0次
2019-03-04更新
|
1120次组卷
|
6卷引用:安徽省合肥市肥东县高级中学2020届高三5月调研考试理科综合化学试题
名校
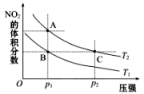
4 . 反应2NO2(g)  N2O4(g) ΔH=-57kJ·mol-1,在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化曲线如图所示。下列说法正确的为( )
N2O4(g) ΔH=-57kJ·mol-1,在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化曲线如图所示。下列说法正确的为( )
 N2O4(g) ΔH=-57kJ·mol-1,在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化曲线如图所示。下列说法正确的为( )
N2O4(g) ΔH=-57kJ·mol-1,在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化曲线如图所示。下列说法正确的为( )
| A.A、C两点气体的颜色:A深,C浅 |
| B.A、C两点的反应速率:A>C |
| C.A、C两点气体的平均相对分子质量:A>C |
| D.由状态A到状态B,可以采用降温的方法 |
您最近一年使用:0次
2018-12-19更新
|
103次组卷
|
2卷引用:安徽省淮北市树人高级中学2020-2021学年高二上学期第一次联考化学试题
2018高二上·全国·专题练习
名校
5 . 在密闭容器中投入一定量的A和B发生反应:mA(g)+nB(g) pC(g)+qD(g)。
pC(g)+qD(g)。
(1)若开始时加入A物质m mol,欲使A与B的转化率相等,则加入B物质________ mol。
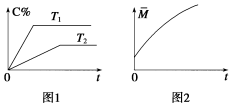
(2)相同的压强下,充入一定量的A、B后,在不同温度下C的百分含量与时间的关系如图1所示。则T1(填“>”、“<”或“=”)______ T2,该反应正反应方向的ΔH(填“>”、“<”或“=”)______ 0。
(3)一定条件下,从正反应开始至达到化学平衡的过程中,混合气体的平均相对分子质量随时间的变化如图2所示,测得达到平衡时A、B、C、D的物质的量均为1 mol。
①若在恒温恒容的条件下,向该平衡体系中再通入A、B、C、D各1 mol,则体系中气体的平均相对分子质量(填“增大”、“减小”、“不变”或“无法确定”)__________ 。
②若恒温恒压的条件下,向原平衡体系中再通入A、B、C、D各1 mol,则体系中气体的密度(填“增大”、“减小”、“不变”或“无法确定”)__________ 。
 pC(g)+qD(g)。
pC(g)+qD(g)。
(1)若开始时加入A物质m mol,欲使A与B的转化率相等,则加入B物质
(2)相同的压强下,充入一定量的A、B后,在不同温度下C的百分含量与时间的关系如图1所示。则T1(填“>”、“<”或“=”)
(3)一定条件下,从正反应开始至达到化学平衡的过程中,混合气体的平均相对分子质量随时间的变化如图2所示,测得达到平衡时A、B、C、D的物质的量均为1 mol。
①若在恒温恒容的条件下,向该平衡体系中再通入A、B、C、D各1 mol,则体系中气体的平均相对分子质量(填“增大”、“减小”、“不变”或“无法确定”)
②若恒温恒压的条件下,向原平衡体系中再通入A、B、C、D各1 mol,则体系中气体的密度(填“增大”、“减小”、“不变”或“无法确定”)
您最近一年使用:0次
2018-09-26更新
|
254次组卷
|
6卷引用:安徽省蚌埠田家炳中学2020-2021学年高二10月月考化学试题
名校
6 . 反应N2O4(g) 2NO2(g) △H=+57 kJ·mol-1,在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化曲线如图所示。下列说法正确的是
2NO2(g) △H=+57 kJ·mol-1,在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化曲线如图所示。下列说法正确的是

 2NO2(g) △H=+57 kJ·mol-1,在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化曲线如图所示。下列说法正确的是
2NO2(g) △H=+57 kJ·mol-1,在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化曲线如图所示。下列说法正确的是
| A.a、c两点的反应速率:a>c |
| B.a、c两点气体的颜色:a深,c浅 |
| C.b、c两点的转化率:b>c |
| D.由b点到a点,可以用加热的方法 |
您最近一年使用:0次
2018-07-25更新
|
3282次组卷
|
11卷引用:安徽省阜阳市第三中学2018-2019学年高一下学期第二次调研考试化学试题
安徽省阜阳市第三中学2018-2019学年高一下学期第二次调研考试化学试题安徽省宣城市郎溪县郎溪中学2018-2019学年高二上学期直升部返校考化学试题吉林省长春汽车经济开发区第六中学2018-2019学年高二上学期第一次月考化学试题福建省福州第三中学2022-2023学年高二上学期半期考试化学试题福建省漳州市正兴学校2023-2024学年高二上学期10月月考化学试卷【全国校级联考】辽宁省抚顺市六校2017-2018学年高一下学期期末考试化学试题四川省成都市外国语学校2019届高三上学期开学考试化学试题福建省莆田市私立一中2019-2020学年高二上学期期中考试化学试题夯基提能2020届高三化学选择题对题专练——选修四化学反应原理——化学反应速率及其影响因素专练(已下线)2.3.3 温度对化学平衡的影响(基础练)——2020-2021学年高二化学上学期十分钟同步课堂专练(苏教版选修4)黑龙江省大庆市东风中学2021-2022学年高二上学期期中考试化学试题
名校
7 . 在其他条件不变时,只改变某一条件,化学反应aA(g)+bB(g) cC(g)的平衡的变化图像如下(图中p表示压强,T表示温度,n表示物质的量,α表示平衡转化率),据此分析下列说法正确的是
cC(g)的平衡的变化图像如下(图中p表示压强,T表示温度,n表示物质的量,α表示平衡转化率),据此分析下列说法正确的是

 cC(g)的平衡的变化图像如下(图中p表示压强,T表示温度,n表示物质的量,α表示平衡转化率),据此分析下列说法正确的是
cC(g)的平衡的变化图像如下(图中p表示压强,T表示温度,n表示物质的量,α表示平衡转化率),据此分析下列说法正确的是
| A.在图像反应Ⅰ中,说明正反应为吸热反应 |
| B.在图像反应Ⅰ中,若p1>p2,则此反应的ΔS>0 |
| C.在图像反应Ⅱ中,说明该正反应为吸热反应 |
| D.在图像反应Ⅲ中,若T1>T2,则该反应能自发进行 |
您最近一年使用:0次
2017-11-14更新
|
2250次组卷
|
17卷引用:安徽省宣城二中2020-2021学年高二上学期第一次月考化学试题
安徽省宣城二中2020-2021学年高二上学期第一次月考化学试题山西省临猗县临晋中学2020-2021学年高二9月月考化学试题河北承德第一中学2020-2021学年高一下学期第三次月考化学试题天津市西青区杨柳青第一中学2021--2022 学年高三上学期第一次阶段检测化学试题广西河池市八校2021-2022学年高二下学期第二次联考化学试题云南省会泽县实验高级中学校2021-2022学年高二下学期4月月考理科综合化学试题福建省德化一中、永安一中、漳平一中三校协作2023-2024学年高二上学期12月联考化学试题湖南省嘉禾一中、临武一中2017-2018学年高二上学期期中联考化学试题【区级联考】天津市武清区2018-2019学年高二上学期期中质量调查化学试题2019年秋高三化学复习强化练习——化学反应的方向及判断2020届高三化学选修4二轮专题练——化学反应的方向和限度【选择精编25题】四川省内江市2019-2020学年高二上学期期末检测化学试题江西省南昌市八一中学、洪都中学等4校2021-2022学年高二上学期期中联考化学试题天津市外国语大学附属外国语学校2021-2022学年高二上学期期中阶段性检测化学试题(已下线)专题七 化学反应速率与化学平衡 能力提升检测卷(测)-2023年高考化学一轮复习讲练测(新教材新高考)天津市崇化中学2022-2023学年高二 上学期阶段性质量监测化学试卷天津市第一百中学、咸水沽第一中学2023-2024学年高二上学期期中联考化学试题
10-11高二下·安徽滁州·阶段练习
名校
解题方法
8 . 对于反应A(g)+2B(g) 2C(g),在压强相同的条件下,若生成物C的含量w(C)与时间t的关系如图所示。则下列结论正确的是
2C(g),在压强相同的条件下,若生成物C的含量w(C)与时间t的关系如图所示。则下列结论正确的是
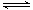 2C(g),在压强相同的条件下,若生成物C的含量w(C)与时间t的关系如图所示。则下列结论正确的是
2C(g),在压强相同的条件下,若生成物C的含量w(C)与时间t的关系如图所示。则下列结论正确的是
| A.T1>T2,正反应放热 |
| B.T1<T2 ,正反应放热 |
| C.T1>T2 ,正反应吸热 |
| D.T1<T2 ,正反应吸热 |
您最近一年使用:0次
2016-12-09更新
|
1109次组卷
|
9卷引用:2010-2011学年安徽省天长市关塘中学高二下学期月考化学试题
(已下线)2010-2011学年安徽省天长市关塘中学高二下学期月考化学试题甘肃省武威第十八中学2019-2020学年高二上学期第二次月考化学试题江西省南昌市新建县第一中学2019-2020学年高二上学期第一次月考化学试题(共建部)安徽省芜湖市2019-2020学年高二上学期期末考试化学(理)试题新疆阿勒泰地区2020-2021学年高二上学期期末考试化学试题山西省汾阳市汾阳中学2020-2021学年高二下学期开学考试化学试题湖北省十堰市区县普通高中联合体2021-2022学年高二上学期期中联考化学试题吉林省长春市清蒲中学2021-2022学年高二上学期期末考试化学试题吉林省长春市清蒲中学2021-2022学年高二上学期期末考试化学试题
9 . 可逆反应m A(s)+n B(g) e C(g)+f D(g),反应过程中,当其他条件不变时,C的体积分数φ(C)在不同温度和不同压强的条件下随时间的变化如图所示。下列叙述正确的是
e C(g)+f D(g),反应过程中,当其他条件不变时,C的体积分数φ(C)在不同温度和不同压强的条件下随时间的变化如图所示。下列叙述正确的是
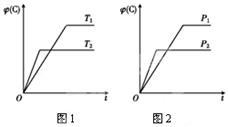
 e C(g)+f D(g),反应过程中,当其他条件不变时,C的体积分数φ(C)在不同温度和不同压强的条件下随时间的变化如图所示。下列叙述正确的是
e C(g)+f D(g),反应过程中,当其他条件不变时,C的体积分数φ(C)在不同温度和不同压强的条件下随时间的变化如图所示。下列叙述正确的是
| A.平衡后,若使用催化剂,C的体积分数将增大 |
| B.平衡后,若温度升高,化学平衡向正反应方向移动 |
| C.平衡后,增加A的质量化学平衡向正反应方向移动 |
| D.化学方程式中,化学计量数的关系为n<e +f |
您最近一年使用:0次
2016-09-22更新
|
474次组卷
|
4卷引用:安徽省定远重点中学2017-2018学年高一下学期教学段考化学试题



