名校
1 . 我国向世界郑重承诺:2030年前实现碳达峰,2060年前实现碳中和。而研发二氧化碳捕捉和碳利用技术则是关键,其中 催化加氢合成甲酸(反应为:
催化加氢合成甲酸(反应为: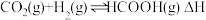 )是一种很有前景的方法,且生成的甲酸是重要化工原料。回答下列问题:
)是一种很有前景的方法,且生成的甲酸是重要化工原料。回答下列问题:
(1)已知: 时,部分物质的相对能量如表所示。
时,部分物质的相对能量如表所示。
则
_________  ,此条件下
,此条件下 的燃烧热
的燃烧热
________ (填“大于”、“小于”或“等于”) 的燃烧热
的燃烧热 。
。
(2) 催化加氢合成甲酸的过程中,不断升高温度,下列图像正确的是________(填选项字母)。
催化加氢合成甲酸的过程中,不断升高温度,下列图像正确的是________(填选项字母)。
(3)恒容密闭容器中充入一定量的 和
和 去合成
去合成 ,下列示意图正确且能说明该反应进行到
,下列示意图正确且能说明该反应进行到 时刻达到平衡状态的是___________(填选项字母)。
时刻达到平衡状态的是___________(填选项字母)。
(4)恒温、恒容的密闭容器中充入 ,
,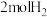 和
和 (不参与反应)发生反应合成甲酸,测得反应过程中体系压强随时间的变化曲线如图所示。
(不参与反应)发生反应合成甲酸,测得反应过程中体系压强随时间的变化曲线如图所示。
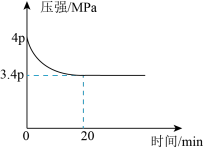
① ,用
,用 表示的化学反应速率为
表示的化学反应速率为___________ 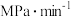 ;
;
②此反应的分压平衡常数
___________ ( 为以分压表示的平衡常数,
为以分压表示的平衡常数,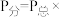 物质的量分数;用含P的式子表示)。
物质的量分数;用含P的式子表示)。
 催化加氢合成甲酸(反应为:
催化加氢合成甲酸(反应为: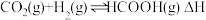 )是一种很有前景的方法,且生成的甲酸是重要化工原料。回答下列问题:
)是一种很有前景的方法,且生成的甲酸是重要化工原料。回答下列问题:(1)已知:
 时,部分物质的相对能量如表所示。
时,部分物质的相对能量如表所示。| 物质 |  |  |  |
相对能量/( ) ) |  | 0 |  |

 ,此条件下
,此条件下 的燃烧热
的燃烧热
 的燃烧热
的燃烧热 。
。(2)
 催化加氢合成甲酸的过程中,不断升高温度,下列图像正确的是________(填选项字母)。
催化加氢合成甲酸的过程中,不断升高温度,下列图像正确的是________(填选项字母)。A.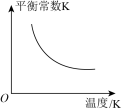 | B.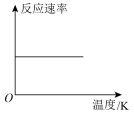 | C.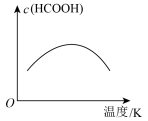 | D. |
(3)恒容密闭容器中充入一定量的
 和
和 去合成
去合成 ,下列示意图正确且能说明该反应进行到
,下列示意图正确且能说明该反应进行到 时刻达到平衡状态的是___________(填选项字母)。
时刻达到平衡状态的是___________(填选项字母)。A.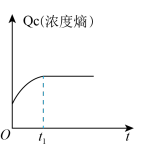 | B. | C. | D. |
(4)恒温、恒容的密闭容器中充入
 ,
,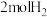 和
和 (不参与反应)发生反应合成甲酸,测得反应过程中体系压强随时间的变化曲线如图所示。
(不参与反应)发生反应合成甲酸,测得反应过程中体系压强随时间的变化曲线如图所示。
①
 ,用
,用 表示的化学反应速率为
表示的化学反应速率为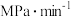 ;
;②此反应的分压平衡常数

 为以分压表示的平衡常数,
为以分压表示的平衡常数,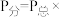 物质的量分数;用含P的式子表示)。
物质的量分数;用含P的式子表示)。
您最近一年使用:0次
名校
解题方法
2 . 关于煤的处理是工业重要的生产工艺,从煤的气化到液化是重要环节。
(1)煤的气化是重要的制氢途径,在一定温度下,向体积固定的密闭容器中加入足量的C(s)和 ,起始压强为0.2MPa时,下列反应生成水煤气:
,起始压强为0.2MPa时,下列反应生成水煤气:
Ⅰ.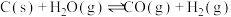

Ⅱ.
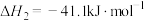
①下列说法正确的是_______ 。
A.平衡时升高温度,反应Ⅰ的平衡逆向移动 B.混合气体的密度保持不变时,说明反应体系已达到平衡
C.平衡时 的体积分数可能大于
的体积分数可能大于 D.将炭块粉碎,可加快反应速率
D.将炭块粉碎,可加快反应速率
②反应平衡时, 的转化率为50%,CO的物质的量为0.1mol。此时,整个体系
的转化率为50%,CO的物质的量为0.1mol。此时,整个体系_______ (填“吸收”或“放出”)热量_______ kJ,反应Ⅰ的平衡常数
_______ MPa(以分压表示,分压=总压×物质的量分数)。
(2)掺杂硒的纳米氧化亚铜催化剂可用于工业上水煤气合成甲醇,实现煤的间接液化,其反应为
 。向起始温度为:125℃的5L恒容密闭容器中充入2mol CO和
。向起始温度为:125℃的5L恒容密闭容器中充入2mol CO和 发生反应,体系总压强(p)与时间(t)的关系如图2中曲线Ⅰ所示,曲线Ⅱ为只改变某一条件的变化曲线。
发生反应,体系总压强(p)与时间(t)的关系如图2中曲线Ⅰ所示,曲线Ⅱ为只改变某一条件的变化曲线。
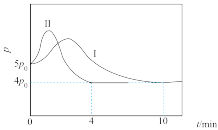
①曲线Ⅱ所对应的改变的条件可能为_______ 。
②体系总压强先增大的原因为_______ ,后减小的原因为_______ 。
③该条件下 的平衡转化率为
的平衡转化率为_______ %(结果保留三位有效数字)。
(1)煤的气化是重要的制氢途径,在一定温度下,向体积固定的密闭容器中加入足量的C(s)和
 ,起始压强为0.2MPa时,下列反应生成水煤气:
,起始压强为0.2MPa时,下列反应生成水煤气:Ⅰ.
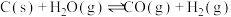

Ⅱ.

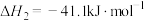
①下列说法正确的是
A.平衡时升高温度,反应Ⅰ的平衡逆向移动 B.混合气体的密度保持不变时,说明反应体系已达到平衡
C.平衡时
 的体积分数可能大于
的体积分数可能大于 D.将炭块粉碎,可加快反应速率
D.将炭块粉碎,可加快反应速率②反应平衡时,
 的转化率为50%,CO的物质的量为0.1mol。此时,整个体系
的转化率为50%,CO的物质的量为0.1mol。此时,整个体系
(2)掺杂硒的纳米氧化亚铜催化剂可用于工业上水煤气合成甲醇,实现煤的间接液化,其反应为

 。向起始温度为:125℃的5L恒容密闭容器中充入2mol CO和
。向起始温度为:125℃的5L恒容密闭容器中充入2mol CO和 发生反应,体系总压强(p)与时间(t)的关系如图2中曲线Ⅰ所示,曲线Ⅱ为只改变某一条件的变化曲线。
发生反应,体系总压强(p)与时间(t)的关系如图2中曲线Ⅰ所示,曲线Ⅱ为只改变某一条件的变化曲线。
①曲线Ⅱ所对应的改变的条件可能为
②体系总压强先增大的原因为
③该条件下
 的平衡转化率为
的平衡转化率为
您最近一年使用:0次
解题方法
3 . 一定温度下,在甲、乙、丙三个体积均为1L的恒容密闭容器中发生甲醇合成二甲醚的反应: ,起始时各物质的物质的量及平衡时各物质的物质的量如表所示。下列说法错误的是
,起始时各物质的物质的量及平衡时各物质的物质的量如表所示。下列说法错误的是
 ,起始时各物质的物质的量及平衡时各物质的物质的量如表所示。下列说法错误的是
,起始时各物质的物质的量及平衡时各物质的物质的量如表所示。下列说法错误的是| 容器 | 温度/℃ | 起始物质的量/mol | 平衡物质的量/mol | |
 |  |  | ||
| 甲 | 387 | 0.20 | 0.080 | 0.080 |
| 乙 | 387 | 0.40 | ||
| 丙 | 207 | 0.20 | 0.090 | 0.090 |
| A.该反应的正反应为放热反应 |
| B.甲容器中反应比丙容器中反应达到平衡状态所需时间长 |
C.平衡时,甲、乙容器中 的转化率相同 的转化率相同 |
D.若起始时向甲容器中充入 、 、 和 和 ,则反应向正反应方向进行 ,则反应向正反应方向进行 |
您最近一年使用:0次
名校
解题方法
4 . 将二氧化碳转化为甲醇等液体燃料是理想的能源补充形式。二氧化碳加氢制甲醇的反应原理为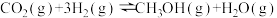 ,
, 。回答下列问题:
。回答下列问题:
(1)不同温度下,向2L的恒容密闭容器中充入1molCO2和3molH2反应相同一段时间,得到以下关系图:
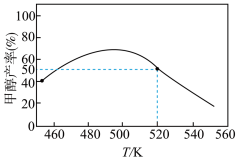
520K时,若增加CO2的浓度,能___________ (填“提高”或“降低”)H2的转化率,此时该反应的平衡常数K=___________ 。在该温度下,再向容器中加入H2和CH3OH(g)各1mol,平衡将___________ (填“正向移动”“逆向移动”或“不移动”)。
(2)在温度t1、t2、t3下,分别将等物质的量的CO2和H2投入到三个等容容器中发生上述反应,平衡时CH3OH(g)的物质的量分数与温度﹑压强的关系如下图所示:
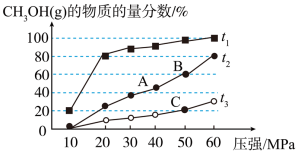
①由上图可知t1、t2、t3的大小关系为___________ 。
②下列说法正确的是___________ (填标号)。
A.采取加压、增大c(H2)、加入合适的催化剂等措施,都能提高CO2的转化率
B.平衡常数:KB>KC
C.在t1温度、20MPa状态下再通入等物质的量的CO2和H2,达新平衡时H2的体积分数减小
D.t3温度下,混合气体的密度不随时间的变化而变化说明反应已达平衡
(3)工业上可利用CO(g)和H2O(g)来制氢气。已知反应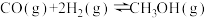
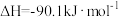 ;则利用CO(g)和H2O(g)来制氢气的热化学方程式为
;则利用CO(g)和H2O(g)来制氢气的热化学方程式为___________ 。
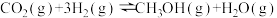 ,
, 。回答下列问题:
。回答下列问题:(1)不同温度下,向2L的恒容密闭容器中充入1molCO2和3molH2反应相同一段时间,得到以下关系图:

520K时,若增加CO2的浓度,能
(2)在温度t1、t2、t3下,分别将等物质的量的CO2和H2投入到三个等容容器中发生上述反应,平衡时CH3OH(g)的物质的量分数与温度﹑压强的关系如下图所示:

①由上图可知t1、t2、t3的大小关系为
②下列说法正确的是
A.采取加压、增大c(H2)、加入合适的催化剂等措施,都能提高CO2的转化率
B.平衡常数:KB>KC
C.在t1温度、20MPa状态下再通入等物质的量的CO2和H2,达新平衡时H2的体积分数减小
D.t3温度下,混合气体的密度不随时间的变化而变化说明反应已达平衡
(3)工业上可利用CO(g)和H2O(g)来制氢气。已知反应
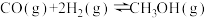
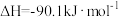 ;则利用CO(g)和H2O(g)来制氢气的热化学方程式为
;则利用CO(g)和H2O(g)来制氢气的热化学方程式为
您最近一年使用:0次
名校
5 . 现有下列四个图像:
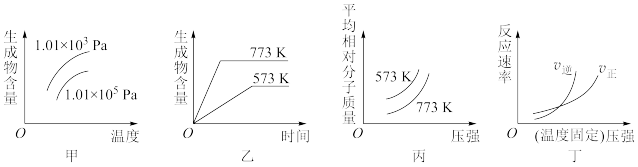
下列反应中全部符合上述图像的反应是

下列反应中全部符合上述图像的反应是
| A.N2(g)+3H2(g)⇌2NH3(g) ΔH1<0 |
| B.2SO3(g)⇌2SO2(g)+O2(g) ΔH2>0 |
| C.4NH3(g)+5O2(g)⇌4NO(g)+6H2O(g) ΔH3<0 |
| D.H2(g)+CO(g)⇌C(s)+H2O(g) ΔH4>0 |
您最近一年使用:0次
2021-12-28更新
|
638次组卷
|
45卷引用:2015-2016学年安徽省宣城郎溪中学高二上学期第三次月考化学试卷
2015-2016学年安徽省宣城郎溪中学高二上学期第三次月考化学试卷(已下线)2011届山东省潍坊市诸城一中高三12月阶段测试化学试卷(已下线)2014-2015学年河南省汝州市高二上学期第一次月考化学试卷2015-2016学年贵州省思南中学高二上二次月考化学试卷2016届陕西省蒲城尧山补习学校高三上学期第四次质检化学试卷2015-2016学年辽宁师大附中高一下学期6月月考化学试卷2016-2017学年辽宁省大连市第二十中学高二上9月月考化学试卷2017届湖北省武钢三中高三上学期11月月考化学试卷山东省德州市夏津一中2018-2019学年高二上学期第一次月考化学试题【全国百强校】甘肃省静宁县第一中学2018-2019学年高二上学期10月月考化学试题江西省赣州市南康中学2019-2020学年高二上学期第一次月考化学试题河南省兰考县第三高级中学卫星试验部2020-2021学年高二上学期第一次月考化学试题辽宁省联合校2020-2021学年高二上学期第一次月考化学试题江西省南昌市第十中学2020-2021学年高二上学期第一次月考化学试题河南省洛阳市豫西名校2021-2022学年高二上学期第一次联考化学试题云南省丽江市第一高级中学2021-2022学年高二上学期元月考化学试题江苏省徐州市睢宁县第一中学2021-2022学年高二下学期第一次月考化学试题湖北省竹溪县第二高级中学2021-2022学年高二上学期12月月考化学试题(已下线)2011-2012年黑龙江双鸭山一中高二上学期期中考试化学试卷(已下线)2012-2013学年山东省威海市高二上学期期末考试化学试卷(已下线)2014-2015学年湖南省衡阳市第八中学高二上学期期中考试化学试卷2015-2016学年黑龙江省红兴隆第一高级中学高二上期中理科化学试卷2015-2016学年陕西省西安第七十中学高二上学期期中测试化学试卷2016-2017学年黑龙江省铁人中学高二上开学测化学卷2018版化学(苏教版)高考总复习专题七题型冲关--巧解平衡及速率图像题甘肃省兰州第一中学2017-2018学年高二上学期期中考试化学(理)试题湖北省华中师范大学第一附属中学2018届高三上学期期中考试化学试题2018-2019学年鲁科版高中化学选修四:第2章检测题江西省上饶市第二中学2018-2019学年高二上学期期中考试化学试题【市级联考】湖南省娄底市2018-2019学年高二上学期期中考试化学试题江苏省泰州市第二中学2017-2018学年高二上学期期中考试化学试题云南省大理市下关一中2018-2019学年高二上学期期中考试化学试题【校级联考】湖北省宜昌市协作体2018-2019学年高二上学期期末考试化学试题山东省济南外国语学校三箭分校2019-2020学年高二上学期期中考试化学试题黑龙江省齐齐哈尔市第八中学2019-2020学年高二上学期期中考试化学试题甘肃省定西市岷县第二中学2019-2020学年高二上学期期中考试化学试题福建省建瓯市芝华中学2019-2020学年高二上学期期中考试化学(1-2班)试题江西省南昌市进贤一中2019-2020学年高二上学期期末考试化学试题甘肃省兰州市第十中学、民族中学2019-2020学年高二上学期期末考试化学试题广西钦州市2019-2020学年高二下学期期末教学质量监测化学试题辽宁省大连市第一中学2021-2022学年高二上学期学情反馈(一)化学试题湖北省十堰市2016-2017学年高二上学期期末调研考试化学试题黑龙江省哈尔滨市德强高中2021-2022学年高二上学期期中考试化学试题江苏省盐城市大丰区新丰中学2021-2022学年高二上学期期中考试化学(选修)试题(已下线)第10讲 影响化学平衡的因素(word讲义)-【帮课堂】2022-2023学年高二化学同步精品讲义(人教2019选择性必修1)
名校
解题方法
6 . 下列图示与对应的叙述不相符的是
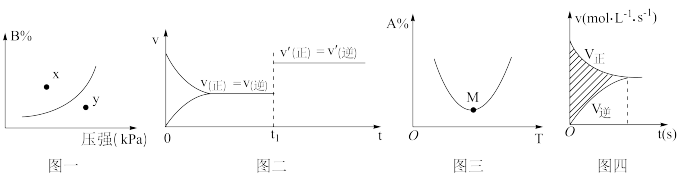

A.图一表示反应: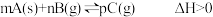 ,在一定温度下,平衡时B的体积分数(B%)与压强变化的关系,则x点时 ,在一定温度下,平衡时B的体积分数(B%)与压强变化的关系,则x点时 正> 正> 逆 逆 |
B.图二是可逆反应: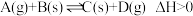 的速率时间图象,则在t1时刻改变条件可能是加入催化剂 的速率时间图象,则在t1时刻改变条件可能是加入催化剂 |
C.图三表示对于化学反应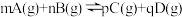 ,A的百分含量与温度(T)的变化情况,则该反应的 ,A的百分含量与温度(T)的变化情况,则该反应的 |
| D.图四所示图中的阴影部分面积的含义是反应物的物质的量减少量 |
您最近一年使用:0次
名校
7 . 分别在T1℃、T2℃、T3℃时,向三个500mL的恒容密闭容器中均充入1molN2和2.5molH2,发生反应:N2(g)+3H2(g) 2NH3(g) △H<0。实验测得反应tmin时N2的体积分数如图所示。下列说法正确的是
2NH3(g) △H<0。实验测得反应tmin时N2的体积分数如图所示。下列说法正确的是
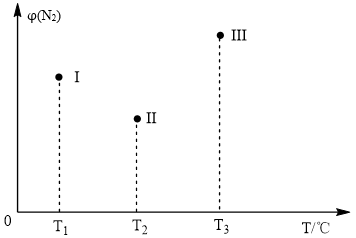
 2NH3(g) △H<0。实验测得反应tmin时N2的体积分数如图所示。下列说法正确的是
2NH3(g) △H<0。实验测得反应tmin时N2的体积分数如图所示。下列说法正确的是
| A.tmin时,Ⅱ和Ⅲ一定达到平衡 |
| B.2v(NH3)=3v(H2)时,三容器均达平衡状态 |
| C.平衡后容器Ⅰ中混合气体平均相对分子质量最小 |
| D.已知tmin时,Ⅲ中c(N2)=1mol•L-1,此时反应平衡常数K=0.5 |
您最近一年使用:0次
2021-11-14更新
|
171次组卷
|
4卷引用:安徽省亳州市涡阳县第二中学2022-2023学年高二上学期教学检测化学试题
名校
解题方法
8 . 下列图示与对应的叙述相符的是


A.图1表示反应: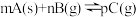  在一定温度下,B的平衡转化率(B%)与压强变化的关系如图所示,则x点正反应速率大于逆反应速率 在一定温度下,B的平衡转化率(B%)与压强变化的关系如图所示,则x点正反应速率大于逆反应速率 |
B.图2是可逆反应:  的速率时间图像,在t1时刻改变条件只能是加入催化剂 的速率时间图像,在t1时刻改变条件只能是加入催化剂 |
C.图3表示对于化学反应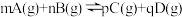 ,A的百分含量与温度(T)的变化情况,则该反应的 ,A的百分含量与温度(T)的变化情况,则该反应的 |
| D.图4所示图中的阴影部分面积的含义是该物质物质的量的变化量 |
您最近一年使用:0次
2021-11-13更新
|
1012次组卷
|
11卷引用:安徽省黄山市屯溪第一中学2023-2024学年高一上学期11月月考 化学试题
安徽省黄山市屯溪第一中学2023-2024学年高一上学期11月月考 化学试题湖北省襄阳市第五中学2022-2023学年高二上学期9月化学试题安徽省芜湖市安徽师范大学附属中学2022-2023学年高二上学期期中考查化学试题湖北省恩施市第一中学2022-2023学年高二上学期11月月考化学试题安徽省黄山市2022-2023学年高二上学期期末考试化学试题河南省南阳市第一中学校2022-2023学年高二上学期第二次月考化学试题辽宁省东北育才中学少儿部2023-2024学年高二上学期第一次月考化学试题重庆市三峡名校联盟2023-2024学年高二上学期12月月考化学试题江苏省江阴市华士高级中学2023-2024学年高二上学期12月学情调研化学(选修)试卷湖北省华中师范大学第一附属中学2021-2022学年高二上学期期中检测化学试题黑龙江省哈尔滨市德强学校2022-2023学年高二上学期期末考试化学试题
名校
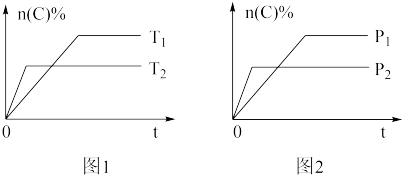
9 . 可逆反应aA(g)+cC(g) bB(s)+dD(g)ΔH,其他条件不变,C的物质的量分数和温度(T)或压强(P)关系如图,其中不正确的是
bB(s)+dD(g)ΔH,其他条件不变,C的物质的量分数和温度(T)或压强(P)关系如图,其中不正确的是
 bB(s)+dD(g)ΔH,其他条件不变,C的物质的量分数和温度(T)或压强(P)关系如图,其中不正确的是
bB(s)+dD(g)ΔH,其他条件不变,C的物质的量分数和温度(T)或压强(P)关系如图,其中不正确的是 
| A.升高温度、增大压强,平衡都向正反应方向移动 |
| B.使用催化剂,C的物质的量分数不变 |
| C.化学方程式系数a+c>b+d |
| D.ΔH>0,升高温度平衡常数K值增大 |
您最近一年使用:0次
2021-04-06更新
|
649次组卷
|
4卷引用:安徽省安庆市第十中学2020-2021学年高二下学期第一次月考化学试题
安徽省安庆市第十中学2020-2021学年高二下学期第一次月考化学试题湖南省临澧县第一中学2021-2022学年高二上学期第一次阶段性考试化学试题(已下线)专题2.2.4 化学平衡图像(备作业)-【上好课】2021-2022学年高二化学同步备课系列(人教版2019选择性必修1)(已下线)2.2.3 影响化学平衡的因素(素养提优B练)-2021-2022学年高二化学课时过关提优AB练(人教版2019选择性必修1)
10 . 体积均为1.0L的甲、乙两个恒容密闭容器,向甲中加入0.1molCO2和0.3mol碳粉,向乙中加入0.4molCO,在不同温度下发生反应:CO2(g)+C(s) 2CO(g)。达到平衡时CO的物质的量浓度随温度的变化如图所示。下列说法正确的是
2CO(g)。达到平衡时CO的物质的量浓度随温度的变化如图所示。下列说法正确的是
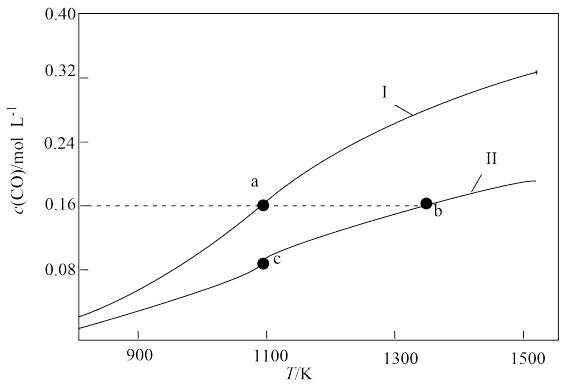
 2CO(g)。达到平衡时CO的物质的量浓度随温度的变化如图所示。下列说法正确的是
2CO(g)。达到平衡时CO的物质的量浓度随温度的变化如图所示。下列说法正确的是
| A.曲线II对应的是乙容器 |
| B.a、b两点对应平衡体系中的压强之比:pa:pb<14:9 |
C.b点对应的平衡体系中,CO的体积分数小于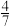 |
| D.900K时,起始时向容器乙中加入CO、CO2、碳粉各1mol,此时v正﹥v逆 |
您最近一年使用:0次
2020-12-23更新
|
1864次组卷
|
3卷引用:安徽省舒城中学2020-2021学年高二上学期第三次月考化学试题



