名校
1 . 下列实验操作能达到相应实验目的的是
| 选项 | 实验操作 | 实验目的 |
| A | 将二氧化硫气体通入紫色石蕊试液中,观察溶液颜色查化 | 证明二氧化硫具有漂白性 |
| B | 向2mL1mol·L-1NaOH溶液中先加入3滴1mol·L-1FeCl3溶液.再加入3滴1mol·L-1MgCl2溶液 | 证明 Ksp[Mg(OH)2]>Ksp[Fe(OH)3] |
| C | 相同温度下,向两支盛有相同体积不同浓度H2O2溶液的试管中分别滴入适量相同浓度的CuSO4溶液和FeCl3溶液 | 探究Cu2+、Fe3+对H2O2分解速率的影响 |
| D | 向2mL品红溶液和2mL加入少许醋酸的品红溶液中分别滴入3滴含NaClO的“84”消毒液,观察红色褪色快慢 | 证明随溶液pH减小,“84”消毒液的氧化能力增强 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2016-12-09更新
|
965次组卷
|
6卷引用:湖南省长沙市第一中学2018届高三上学期晚自习测试(一)化学试题
湖南省长沙市第一中学2018届高三上学期晚自习测试(一)化学试题2016届辽宁省部分重点高中协作校高三下模拟理综化学试卷甘肃省张掖市2018届高三第一次质量检测考试理综化学试题甘肃省张掖市2022-2023学年高三上学期第一次诊断考试化学试题黑龙江省大庆铁人中学2022-2023学年高三上学期第一次月考化学试题(已下线)专题24 实验分析设计型选择题-2023年高考化学毕业班二轮热点题型归纳与变式演练(新高考专用)
名校
解题方法
2 . 下列根据实验操作和现象所得出的结论正确的是
| 选项 | 实验操作 | 实验现象 | 结论 |
| A | 向两份蛋白质溶液中分别滴加饱和NaCl 溶液和CuSO4溶液 | 均有固体析出 | 蛋白质均发生变性 |
| B | 向溶液X 中先滴加稀硝酸,再滴加Ba(NO3)2溶液 | 出现白色沉淀 | 溶液X 中一定含有SO42- |
| C | 向一定浓度的Na2SiO3溶液中通入适量CO2气体 | 出现白色沉淀 | H2SiO3的酸性比H2CO3的酸性强 |
| D | 向浓度均为0. 1 mol·L-1NaCl 和NaI 混合溶液中滴加少量AgNO3溶液 | 出现黄色沉淀 | Ksp(AgCl)>Ksp(AgI) |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2016-12-09更新
|
244次组卷
|
4卷引用:2017届湖南省石门一中高三上学期9月月考化学试卷
名校
3 . t ℃时Ag2CrO4在水中的沉淀溶解平衡曲线如图所示。下列说法正确的是
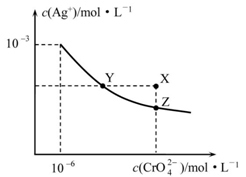

| A.在t ℃时,Ag2CrO4的Ksp=1×10-9 |
| B.X点有Ag2CrO4沉淀生成 |
| C.通过加热蒸发可以使溶液由Y点变到Z点 |
| D.在饱和Ag2CrO4溶液中加入K2CrO4,可使溶液由Y点变到X点最终变到Z点 |
您最近一年使用:0次
2016-12-09更新
|
330次组卷
|
3卷引用:2016届湖南省益阳市高三下学期4月调研理综化学试卷
4 . 下列有关实验操作、现象和解释或结论都正确的是
| 选项 | 实验操作 | 现象 | 解释或结论 |
| A | 向某溶液中先滴加氯水,再滴加少量KSCN溶液 | 溶液变成血红色 | 溶液中含有Fe2+ |
| B | AgCl沉淀中滴入稀KI溶液 | 有黄色沉淀出现 | AgI比AgCl更难溶 |
| C | Al箔插入稀HNO3中 | 无现象 | Al箔表面被HNO3氧化,形成致密的氧化膜 |
| D | 淀粉与稀H2SO4共热,再加银氨溶液水浴加热 | 无银镜生成 | 淀粉水解产物无还原性 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
5 . 高铁酸钾(K2FeO4)是一种高效多功能水处理剂,具有极强的氧化性。
(1)已知:4 +10H2O ⇌4Fe(OH) 3+8OH-+3O2↑。K2FeO4在处理水的过程中所起的作用有
+10H2O ⇌4Fe(OH) 3+8OH-+3O2↑。K2FeO4在处理水的过程中所起的作用有___ 。
同浓度的高铁酸钾在pH为4.74、7.00、11.50的水溶液中最稳定的是pH=_______ 的溶液。
(2)高铁酸钾有以下几种常见制备方法:

①干法制备K2FeO4的反应中,氧化剂与还原剂的物质的量之比为___________ 。
②湿法制备中,若Fe(NO3)3加入过量,在碱性介质中K2FeO4与Fe3+发生氧化还原反应生成K3FeO4,此反应的离子方程式:___________________________________ 。
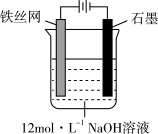
③制备中间产物Na2FeO4,可采用的装置如图所示,则阳极的电极反应式为_______________ 。
(3)比亚迪双模电动汽车使用高铁电池供电,其总反应为:3Zn+2K2FeO4+8H2O 3Zn(OH)(OH)2+2Fe(OH)3+4KOH 放电时负极附近pH变化
3Zn(OH)(OH)2+2Fe(OH)3+4KOH 放电时负极附近pH变化_______________ ,正极反应为:____________________ 。
(4)25℃时,CaFeO4的Ksp=4.54×l0-9,若要使1000 L含有2.0×l0-4 mol·L-l K2FeO4的废水中的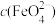 有沉淀产生,理论上至少加入Ca(OH)2的物质的量为
有沉淀产生,理论上至少加入Ca(OH)2的物质的量为________ mol。
(1)已知:4
 +10H2O ⇌4Fe(OH) 3+8OH-+3O2↑。K2FeO4在处理水的过程中所起的作用有
+10H2O ⇌4Fe(OH) 3+8OH-+3O2↑。K2FeO4在处理水的过程中所起的作用有同浓度的高铁酸钾在pH为4.74、7.00、11.50的水溶液中最稳定的是pH=
(2)高铁酸钾有以下几种常见制备方法:

①干法制备K2FeO4的反应中,氧化剂与还原剂的物质的量之比为
②湿法制备中,若Fe(NO3)3加入过量,在碱性介质中K2FeO4与Fe3+发生氧化还原反应生成K3FeO4,此反应的离子方程式:
③制备中间产物Na2FeO4,可采用的装置如图所示,则阳极的电极反应式为

(3)比亚迪双模电动汽车使用高铁电池供电,其总反应为:3Zn+2K2FeO4+8H2O
 3Zn(OH)(OH)2+2Fe(OH)3+4KOH 放电时负极附近pH变化
3Zn(OH)(OH)2+2Fe(OH)3+4KOH 放电时负极附近pH变化(4)25℃时,CaFeO4的Ksp=4.54×l0-9,若要使1000 L含有2.0×l0-4 mol·L-l K2FeO4的废水中的
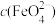 有沉淀产生,理论上至少加入Ca(OH)2的物质的量为
有沉淀产生,理论上至少加入Ca(OH)2的物质的量为
您最近一年使用:0次
6 . 下列有关实验操作、现象和结论都正确的是
| 实验操作 | 现象和结论 | |
| A | 在平衡3KSCN + FeCl3 Fe(SCN)3+3KC1的溶液中加入少量KCl溶液 Fe(SCN)3+3KC1的溶液中加入少量KCl溶液 | 溶液红色变浅,平衡逆向移动 |
| B | 向AgI沉淀中滴入KCl溶液 | 有白色沉生成,Ksp(AgCl)<Ksp(AgI) |
| C | 把C12通入品红溶液中 | 溶液褪色,C12具有漂白性 |
| D | 向Fe(NO3)2溶液中滴入硫酸酸化的H2O2溶液 | 溶液变为黄色,氧化性:H2O2> Fe3+ |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
7 . 结合下表回答下列问题:
(1)CuCl2溶液中含有少量的FeCl2和FeCl3,为得到纯净的CuCl2·2H2O晶体,可先加入适量氯水,发生的离子反应为_____________________ ;再加入____________ ,调至pH=4,此时溶液中的c(Fe3+)=___________ ;过滤后,将所得滤液低温蒸发、浓缩结晶,可得到CuCl2•2H2O晶体.
(2)在空气中直接加热CuCl2•2H2O晶体得不到纯的无水CuCl2,由CuCl2•2H2O晶体得到纯的无水CuCl2的合理方法是_____________________ 。
| 物 质 | Fe(OH)2 | Cu(OH)2 | Fe(OH)3 |
| 溶度积/25℃ | 8.0×10-16 | 2.2×10-20 | 4.0×10-38 |
| 完全沉淀时的pH范围 | ≥9.6 | ≥6.4 | 3~4 |
(2)在空气中直接加热CuCl2•2H2O晶体得不到纯的无水CuCl2,由CuCl2•2H2O晶体得到纯的无水CuCl2的合理方法是
您最近一年使用:0次
8 . 下列叙述错误的是
| A.在加热搅拌条件下加入MgO,可除去MgCl2溶液中的Fe3+ |
| B.pH=4.5的番茄汁中c(H+)是pH=6.5的牛奶中c(H+)的100倍 |
| C.常温下,CH3COONa和CH3COOH的混合溶液中(pH=7):C(Na+)=c(CH3COO―)>c(CH3COOH)>c(H+)=c(OH―) |
| D.常温下,Cd(OH)2和Co(OH)2的混合悬浊液中,c(Cd@+)是c(Co)的3.5倍。已知:KSP(Cd(OH)2)=7.2×10-15, KSP(Co(OH)2)=1.8×10-15 |
您最近一年使用:0次
2016-12-09更新
|
190次组卷
|
4卷引用:2015届湖南省五市十校高三下学期3月模拟考试理综化学试卷
9 . 已知:Fe(OH)3和Al(OH)3沉淀的生成与溶解的pH如下表
向FeCl3、Al2(SO4)3的混合溶液中逐滴加入Ba(OH)2溶液,形成沉淀的情况如下图所示。以下推断错误的是

| 氢氧化物 | 溶液pH | |||
| 开始沉淀 | 沉淀完全 | 沉淀开始溶解 | 沉淀完全溶解 | |
| Fe(OH)3 | 2.3 | 3.4 | ___ | ___ |
| Al(OH)3 | 3.3 | 5.2 | 7.8 | 12.8 |

A.AB段可能发生的反应是:2Ba2++ 3OH-+ 2 + Al3++ 2Ba2+=2BaSO4 + Al3++ 2Ba2+=2BaSO4 +Al(OH)3 +Al(OH)3 |
| B.C点对应的沉淀是:Fe(OH)3和BaSO4 |
C.OA段可能发生的反应是:3Ba2++ 6OH-+ 3 + Al3++Fe3+=3BaSO4 + Al3++Fe3+=3BaSO4 +Fe(OH)3 +Fe(OH)3 +Al(OH)3 +Al(OH)3 |
D.据图计算原溶液中:c(Cl-) =c(SO ) ) |
您最近一年使用:0次
10 . 下列有关说法正确的是
| A.配制Fe(NO3)2溶液时,为了防止Fe2+水解可向溶液中加入适量的稀硝酸 |
| B.向饱和Na2CO3溶液中加少量BaSO4粉末,过滤,向洗净的沉淀中加稀盐酸,有气泡产生,则Ksp(BaCO3)<Ksp(BaSO4) |
| C.过量的铁在氯气中燃烧可生成氯化亚铁 |
D.已知I2可溶于KI形成KI3,向两支盛有KI3溶液的试管中,分别滴加淀粉溶液和AgNO3溶液,前者溶液变蓝,后者有黄色沉淀,说明KI3溶液中存在平衡:I3- I2+I- I2+I- |
您最近一年使用:0次



