1 .  是一种用途广泛的磁性材料,以
是一种用途广泛的磁性材料,以 为原料制备
为原料制备 并获得副产物
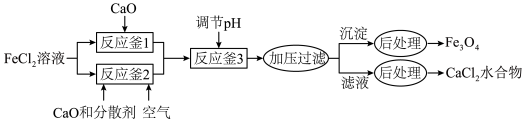
并获得副产物 水合物的工艺如下。
水合物的工艺如下。
 时各物质溶度积见下表:
时各物质溶度积见下表:
回答下列问题:
(1) 中
中 元素的化合价是
元素的化合价是 和
和_______ 。 的核外电子排布式为
的核外电子排布式为_______ 。
(2)反应釜1中的反应需在隔绝空气条件下进行,其原因是_______ 。
(3)反应釜2中,加入 和分散剂的同时通入空气。
和分散剂的同时通入空气。
①反应的离子方程式为_______ 。
②为加快反应速率,可采取的措施有_______ 。(写出两项即可)。
(4)①反应釜3中, 时,
时, 浓度为
浓度为 ,理论上
,理论上 不超过
不超过_______ 。
②称取 水合物
水合物 ,加水溶解,加入过量
,加水溶解,加入过量 ,将所得沉淀过滤洗涤后,溶于热的稀硫酸中,用
,将所得沉淀过滤洗涤后,溶于热的稀硫酸中,用 标准溶液滴定,消耗
标准溶液滴定,消耗 。滴定达到终点的现象为
。滴定达到终点的现象为_______ ,该副产物中 的质量分数为
的质量分数为_______ 。
 是一种用途广泛的磁性材料,以
是一种用途广泛的磁性材料,以 为原料制备
为原料制备 并获得副产物
并获得副产物 水合物的工艺如下。
水合物的工艺如下。
 时各物质溶度积见下表:
时各物质溶度积见下表:| 物质 |  |  |  |
溶度积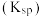 |  |  |  |
(1)
 中
中 元素的化合价是
元素的化合价是 和
和 的核外电子排布式为
的核外电子排布式为(2)反应釜1中的反应需在隔绝空气条件下进行,其原因是
(3)反应釜2中,加入
 和分散剂的同时通入空气。
和分散剂的同时通入空气。①反应的离子方程式为
②为加快反应速率,可采取的措施有
(4)①反应釜3中,
 时,
时, 浓度为
浓度为 ,理论上
,理论上 不超过
不超过②称取
 水合物
水合物 ,加水溶解,加入过量
,加水溶解,加入过量 ,将所得沉淀过滤洗涤后,溶于热的稀硫酸中,用
,将所得沉淀过滤洗涤后,溶于热的稀硫酸中,用 标准溶液滴定,消耗
标准溶液滴定,消耗 。滴定达到终点的现象为
。滴定达到终点的现象为 的质量分数为
的质量分数为
您最近一年使用:0次
2023-09-28更新
|
4425次组卷
|
4卷引用:2023年重庆市高考化学试卷
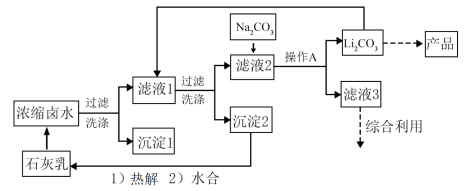
2 . 全球对锂资源的需求不断增长,“盐湖提锂”越来越受到重视。某兴趣小组取盐湖水进行浓缩和初步除杂后,得到浓缩卤水(含有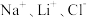 和少量
和少量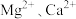 ),并设计了以下流程通过制备碳酸锂来提取锂。
),并设计了以下流程通过制备碳酸锂来提取锂。
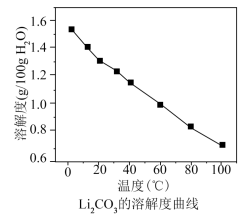
 时相关物质的参数如下:
时相关物质的参数如下:
 的溶解度:
的溶解度: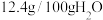
回答下列问题:
(1)“沉淀1”为___________ 。
(2)向“滤液1”中加入适量固体 的目的是
的目的是___________ 。
(3)为提高 的析出量和纯度,“操作A”依次为
的析出量和纯度,“操作A”依次为___________ 、___________ 、洗涤。
(4)有同学建议用“侯氏制碱法”的原理制备 。查阅资料后,发现文献对常温下的
。查阅资料后,发现文献对常温下的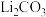 有不同的描述:①是白色固体;②尚未从溶液中分离出来。为探究
有不同的描述:①是白色固体;②尚未从溶液中分离出来。为探究 的性质,将饱和
的性质,将饱和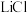 溶液与饱和
溶液与饱和 溶液等体积混合,起初无明显变化,随后溶液变浑浊并伴有气泡冒出,最终生成白色沉淀。上述现象说明,在该实验条件下
溶液等体积混合,起初无明显变化,随后溶液变浑浊并伴有气泡冒出,最终生成白色沉淀。上述现象说明,在该实验条件下
___________ (填“稳定”或“不稳定”),有关反应的离子方程式为___________ 。
(5)他们结合(4)的探究结果,拟将原流程中向“滤液2”加入 改为通入
改为通入 。这一改动能否达到相同的效果,作出你的判断并给出理由
。这一改动能否达到相同的效果,作出你的判断并给出理由___________ 。
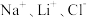 和少量
和少量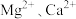 ),并设计了以下流程通过制备碳酸锂来提取锂。
),并设计了以下流程通过制备碳酸锂来提取锂。
 时相关物质的参数如下:
时相关物质的参数如下: 的溶解度:
的溶解度: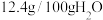
| 化合物 | 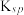 |
 |  |
 | 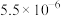 |
 | 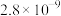 |
 | 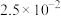 |

回答下列问题:
(1)“沉淀1”为
(2)向“滤液1”中加入适量固体
 的目的是
的目的是(3)为提高
 的析出量和纯度,“操作A”依次为
的析出量和纯度,“操作A”依次为(4)有同学建议用“侯氏制碱法”的原理制备
 。查阅资料后,发现文献对常温下的
。查阅资料后,发现文献对常温下的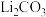 有不同的描述:①是白色固体;②尚未从溶液中分离出来。为探究
有不同的描述:①是白色固体;②尚未从溶液中分离出来。为探究 的性质,将饱和
的性质,将饱和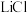 溶液与饱和
溶液与饱和 溶液等体积混合,起初无明显变化,随后溶液变浑浊并伴有气泡冒出,最终生成白色沉淀。上述现象说明,在该实验条件下
溶液等体积混合,起初无明显变化,随后溶液变浑浊并伴有气泡冒出,最终生成白色沉淀。上述现象说明,在该实验条件下
(5)他们结合(4)的探究结果,拟将原流程中向“滤液2”加入
 改为通入
改为通入 。这一改动能否达到相同的效果,作出你的判断并给出理由
。这一改动能否达到相同的效果,作出你的判断并给出理由
您最近一年使用:0次
2022-07-12更新
|
8753次组卷
|
14卷引用:2022年湖北省高考真题化学试题
2022年湖北省高考真题化学试题(已下线)专题15 工艺流程题-2022年高考真题模拟题分项汇编(已下线)2022年湖北省高考真题变式题16-19江苏省响水中学2022-2023学年高三上学期开学测试化学试题(已下线)专题17 化工流程综合题-备战2023年高考化学母题题源解密(广东卷)湖北省武汉市第一中学2022-2023学年高三上学期9月开学考试化学试题(已下线)易错点26 沉淀溶解平衡-备战2023年高考化学考试易错题四川省内江市第六中学2022- 2023学年高三上学期第二次月考化学试题(已下线)热点情景汇编-专题十 工艺流程中的新工艺(已下线)专题18 工艺流程题(已下线)专题18 工艺流程题(已下线)专题13 工艺流程综合题-2023年高考化学真题题源解密(新高考专用)(已下线)专题13 工艺流程综合题-2023年高考化学真题题源解密(全国通用)(已下线)考点47 无机工艺流程(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)
真题
名校
3 . 以软锰矿粉(含MnO2及少量Fe、Al、Si、Ca、Mg等的氧化物)为原料制备电池级MnO2。
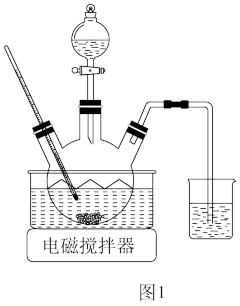
(1)浸取。将一定量软锰矿粉与Na2SO3、H2SO4溶液中的一种配成悬浊液,加入到三颈瓶中(图1),70℃下通过滴液漏斗缓慢滴加另一种溶液,充分反应,过滤。滴液漏斗中的溶液是___ ;MnO2转化为Mn2+的离子方程式为___ 。
(2)除杂。向已经除去Fe、Al、Si的MnSO4溶液(pH约为5)中加入NH4F溶液,溶液中的Ca2+、Mg2+形成氟化物沉淀。若沉淀后上层清液中c(F-)=0.05mol·L-1,则 =
=___ 。[Ksp(MgF2)=5×10-11,Ksp(CaF2)=5×10-9]
(3)制备MnCO3。在搅拌下向100mL1mol·L-1MnSO4溶液中缓慢滴加1mol·L-1NH4HCO3溶液,过滤、洗涤、干燥,得到MnCO3固体。需加入NH4HCO3溶液的体积约为___ 。
(4)制备MnO2。MnCO3经热解、酸浸等步骤可制备MnO2。MnCO3在空气气流中热解得到三种价态锰的氧化物,锰元素所占比例(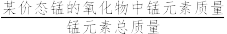 ×100%)随热解温度变化的曲线如图2所示。已知:MnO与酸反应生成Mn2+;Mn2O3氧化性强于Cl2,加热条件下Mn2O3在酸性溶液中转化为MnO2和Mn2+。
×100%)随热解温度变化的曲线如图2所示。已知:MnO与酸反应生成Mn2+;Mn2O3氧化性强于Cl2,加热条件下Mn2O3在酸性溶液中转化为MnO2和Mn2+。
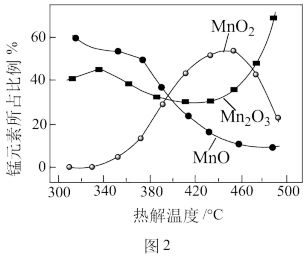
为获得较高产率的MnO2,请补充实验方案:取一定量MnCO3置于热解装置中,通空气气流,___ ,固体干燥,得到MnO2。(可选用的试剂:1mol·L-1H2SO4溶液、2mol·L-1HCl溶液、BaCl2溶液、AgNO3溶液)。
(1)浸取。将一定量软锰矿粉与Na2SO3、H2SO4溶液中的一种配成悬浊液,加入到三颈瓶中(图1),70℃下通过滴液漏斗缓慢滴加另一种溶液,充分反应,过滤。滴液漏斗中的溶液是

(2)除杂。向已经除去Fe、Al、Si的MnSO4溶液(pH约为5)中加入NH4F溶液,溶液中的Ca2+、Mg2+形成氟化物沉淀。若沉淀后上层清液中c(F-)=0.05mol·L-1,则
 =
=(3)制备MnCO3。在搅拌下向100mL1mol·L-1MnSO4溶液中缓慢滴加1mol·L-1NH4HCO3溶液,过滤、洗涤、干燥,得到MnCO3固体。需加入NH4HCO3溶液的体积约为
(4)制备MnO2。MnCO3经热解、酸浸等步骤可制备MnO2。MnCO3在空气气流中热解得到三种价态锰的氧化物,锰元素所占比例(
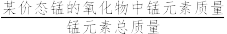 ×100%)随热解温度变化的曲线如图2所示。已知:MnO与酸反应生成Mn2+;Mn2O3氧化性强于Cl2,加热条件下Mn2O3在酸性溶液中转化为MnO2和Mn2+。
×100%)随热解温度变化的曲线如图2所示。已知:MnO与酸反应生成Mn2+;Mn2O3氧化性强于Cl2,加热条件下Mn2O3在酸性溶液中转化为MnO2和Mn2+。
为获得较高产率的MnO2,请补充实验方案:取一定量MnCO3置于热解装置中,通空气气流,
您最近一年使用:0次
2022-01-04更新
|
6541次组卷
|
7卷引用:2021年新高考江苏化学高考真题
2021年新高考江苏化学高考真题(已下线)黄金卷3-【赢在高考·黄金20卷】备战2022年高考化学模拟卷(江苏卷)江苏省盐城市阜宁中学2021-2022学年高三下学期第三次综合测试化学试题(已下线)押江苏卷第17题 化学实验综合题 -备战2022年高考化学临考题号押题(江苏卷)(已下线)易错点34 化学实验方案的设计与评价-备战2023年高考化学考试易错题(已下线)专题19 实验综合题(已下线)专题19 实验综合题
4 . 实验室以工业废渣(主要含CaSO4·2H2O,还含少量SiO2、Al2O3、Fe2O3)为原料制取轻质CaCO3和(NH4)2SO4晶体,其实验流程如下:
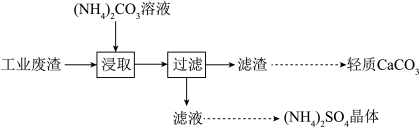
(1)室温下,反应CaSO4(s)+ (aq)⇌CaCO3(s)+
(aq)⇌CaCO3(s)+ (aq)达到平衡,则溶液中
(aq)达到平衡,则溶液中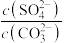 =
=________ [Ksp(CaSO4)=4.8×10−5,Ksp(CaCO3)=3×10−9]。
(2)将氨水和NH4HCO3溶液混合,可制得(NH4)2CO3溶液,其离子方程式为________ ;浸取废渣时,向(NH4)2CO3溶液中加入适量浓氨水的目的是________ 。
(3)废渣浸取在如图所示的装置中进行。控制反应温度在60~70 ℃,搅拌,反应3小时。温度过高将会导致CaSO4的转化率下降,其原因是________ ;保持温度、反应时间、反应物和溶剂的量不变,实验中提高CaSO4转化率的操作有________ 。
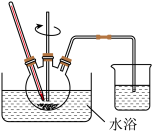
(4)滤渣水洗后,经多步处理得到制备轻质CaCO3所需的CaCl2溶液。设计以水洗后的滤渣为原料,制取CaCl2溶液的实验方案:______ [已知pH=5时Fe(OH)3和Al(OH)3沉淀完全;pH=8.5时Al(OH)3开始溶解。实验中必须使用的试剂:盐酸和Ca(OH)2]。

(1)室温下,反应CaSO4(s)+
 (aq)⇌CaCO3(s)+
(aq)⇌CaCO3(s)+ (aq)达到平衡,则溶液中
(aq)达到平衡,则溶液中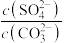 =
=(2)将氨水和NH4HCO3溶液混合,可制得(NH4)2CO3溶液,其离子方程式为
(3)废渣浸取在如图所示的装置中进行。控制反应温度在60~70 ℃,搅拌,反应3小时。温度过高将会导致CaSO4的转化率下降,其原因是

(4)滤渣水洗后,经多步处理得到制备轻质CaCO3所需的CaCl2溶液。设计以水洗后的滤渣为原料,制取CaCl2溶液的实验方案:
您最近一年使用:0次
2019-06-10更新
|
5874次组卷
|
7卷引用:2019年江苏省高考化学试题
2019年江苏省高考化学试题2020届高考化学二轮复习大题精准训练 —— 制备类无机工艺流程题专题3.2 非金属及其化合物(疑难突破)——巅峰冲刺2020年高考化学二轮专项提升江苏省徐州市第一中学2019-2020学年高二下学期开学收心检测化学试题(已下线)专题6.1 无机化工流程题(疑难突破)——巅峰冲刺2020年高考化学二轮专项提升内蒙古四子王旗第一中学2021届高三上学期1月月考化学试题(已下线)工业流程题
真题
名校
5 . 某小组以CoCl2·6H2O、NH4Cl、H2O2、液氨、氯化铵为原料,在活性炭催化下合成了橙黄色晶体X。为测定其组成,进行如下实验。
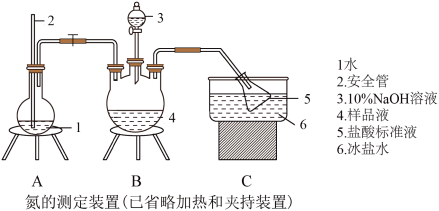
①氨的测定:精确称取wgX,加适量水溶解,注入如图所示的三颈瓶中,然后逐滴加入足量10%NaOH溶液,通入水蒸气,将样品溶液中的氨全部蒸出,用V1mLc1mol·L—1的盐酸溶液吸收。蒸氨结束后取下接收瓶,用c2mol·L—1NaOH标准溶液滴定过剩的HCl,到终点时消耗V2mLNaOH溶液。
②氯的测定:准确称取样品X,配成溶液后用AgNO3标准溶液滴定,K2CrO4溶液为指示剂,至出现砖红色沉淀不再消失为终点(Ag2CrO4为砖红色)。
回答下列问题:
(1)装置中安全管的作用原理是_________ 。
(2)用NaOH标准溶液滴定过剩的HCl时,应使用_____ 式滴定管,可使用的指示剂为________ 。
(3)样品中氨的质量分数表达式为____________ 。
(4)测定氨前应该对装置进行气密性检验,若气密性不好测定结果将___ (填“偏高”或“偏低”)。
(5)测定氯的过程中,使用棕色滴定管的原因是___________ ;滴定终点时,若溶液中c(Ag+)=2.0×10—5mol·L—1,c(CrO42—)为______ mol·L—1。(已知:Ksp(Ag2CrO4)=1.12×10—12)
(6)经测定,样品X中钴、氨、氯的物质的量之比为1:6:3,钴的化合价为______ ,制备X的化学方程式为____________________ ;X的制备过程中温度不能过高的原因是__________________ 。

①氨的测定:精确称取wgX,加适量水溶解,注入如图所示的三颈瓶中,然后逐滴加入足量10%NaOH溶液,通入水蒸气,将样品溶液中的氨全部蒸出,用V1mLc1mol·L—1的盐酸溶液吸收。蒸氨结束后取下接收瓶,用c2mol·L—1NaOH标准溶液滴定过剩的HCl,到终点时消耗V2mLNaOH溶液。
②氯的测定:准确称取样品X,配成溶液后用AgNO3标准溶液滴定,K2CrO4溶液为指示剂,至出现砖红色沉淀不再消失为终点(Ag2CrO4为砖红色)。
回答下列问题:
(1)装置中安全管的作用原理是
(2)用NaOH标准溶液滴定过剩的HCl时,应使用
(3)样品中氨的质量分数表达式为
(4)测定氨前应该对装置进行气密性检验,若气密性不好测定结果将
(5)测定氯的过程中,使用棕色滴定管的原因是
(6)经测定,样品X中钴、氨、氯的物质的量之比为1:6:3,钴的化合价为
您最近一年使用:0次
2016-12-09更新
|
3782次组卷
|
11卷引用:2014年全国普通高等学校招生统一考试理科综合能力测试化学(新课标Ⅱ卷)
2014年全国普通高等学校招生统一考试理科综合能力测试化学(新课标Ⅱ卷)2016届黑龙江省哈尔滨第六中学高三上期中测试化学试卷2016届山东省泰安一中高三5月模拟一理综化学试卷2016届山东省泰安一中高三5月高考拉练一模理综化学试卷四川省成都市龙泉第二中学2019-2020学年高三上学期1月月考理科综合化学试题2020届高考化学二轮复习大题精准训练——定量分析实验中成分的测定【懂做原理题】2020届高三化学选修4二轮专题练——沉淀溶解平衡常数及相关计算【精编25题】甘肃省西北师范大学附属中学2019-2020学年高二上学期期中考试化学试题云南省玉溪市通海县第三中学2021-2022学年高二上学期期末考试化学试题云南省玉溪市峨山县第一中学2022-2023学年高二上学期期中考试化学试题(已下线)实验综合题



