名校
解题方法
1 . 下列各组离子在指定溶液中一定能大量共存的是
A.滴入甲基橙显红色的溶液: 、 、 、 、 、 、 |
B.室温下,水电离的 mol/L的溶液: mol/L的溶液: 、 、 、 、 、 、 |
C.室温下, 的溶液: 的溶液: 、 、 、 、 、 、 |
D.室温下,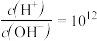 的溶液: 的溶液: 、 、 、 、 、 、 |
您最近一年使用:0次
2022-12-29更新
|
368次组卷
|
2卷引用:辽宁省大连市2022-2023学年高二上学期期末考试化学试题
名校
解题方法
2 . 常温下,下列各组离子一定能大量共存的是
A.0.1mol•L-1的NaHCO3溶液中:Fe3+、K+、Cl-、 |
B.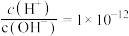 的溶液中:K+、Na+、 的溶液中:K+、Na+、 、 、 |
C.滴加KSCN溶液显红色的溶液中: 、K+、Cl-、I- 、K+、Cl-、I- |
D.水电离产生的c(OH-)=1.0×10-12mol•L-1的溶液中:Na+、Al3+、Cl-、 |
您最近一年使用:0次
名校
解题方法
3 . 已知水的电离平衡曲线如图所示:
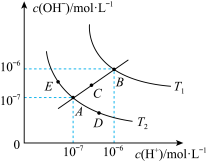
试回答下列问题:
(1)图中
_______  (用“>”、“<”、“=”回答)
(用“>”、“<”、“=”回答)
(2)图中五点的 间的关系是
间的关系是_______ 。
(3)若从A点到E点,可采用的措施是_______ 。
a.升温 b.加入少量的盐酸 c.加入少量的NaOH溶液
(4)点E对应的温度下,将 的NaOH溶液与
的NaOH溶液与 的
的 溶液混合,若所得混合溶液的
溶液混合,若所得混合溶液的 ,则NaOH溶液与
,则NaOH溶液与 溶液的体积比为
溶液的体积比为_______ 。
(5)点B对应的温度下,若100体积 的某强酸溶液与1体积
的某强酸溶液与1体积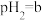 的某强碱溶液混合后溶液呈中性,则混合前,该强酸的
的某强碱溶液混合后溶液呈中性,则混合前,该强酸的 与强碱的
与强碱的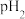 之间应满足的关系是
之间应满足的关系是_______ 。
(6)写出用pH试纸测溶液pH的操作_______ 。

试回答下列问题:
(1)图中

 (用“>”、“<”、“=”回答)
(用“>”、“<”、“=”回答)(2)图中五点的
 间的关系是
间的关系是(3)若从A点到E点,可采用的措施是
a.升温 b.加入少量的盐酸 c.加入少量的NaOH溶液
(4)点E对应的温度下,将
 的NaOH溶液与
的NaOH溶液与 的
的 溶液混合,若所得混合溶液的
溶液混合,若所得混合溶液的 ,则NaOH溶液与
,则NaOH溶液与 溶液的体积比为
溶液的体积比为(5)点B对应的温度下,若100体积
 的某强酸溶液与1体积
的某强酸溶液与1体积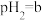 的某强碱溶液混合后溶液呈中性,则混合前,该强酸的
的某强碱溶液混合后溶液呈中性,则混合前,该强酸的 与强碱的
与强碱的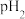 之间应满足的关系是
之间应满足的关系是(6)写出用pH试纸测溶液pH的操作
您最近一年使用:0次
2022-11-10更新
|
345次组卷
|
3卷引用:山东省菏泽市2022-2023学年高二上学期期中考试(B)化学试题
4 . 下列说法正确的是
| A.电解、电离、电镀、电化学腐蚀这些过程都需要通电后才能进行 |
B.298K时,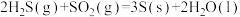 能自发进行,则其△H<0 能自发进行,则其△H<0 |
| C.镀锌铁板是利用了外加电流的阴极保护法来达到防止腐蚀的目的 |
| D.将纯水加热至较高温度,Kw变大、pH变小、呈酸性 |
您最近一年使用:0次
名校
解题方法
5 . 常温下,下列关于电解质溶液的正确判断是
A.在pH=12的溶液中,Al3+、Cl-、CO 、Na+可以大量共存 、Na+可以大量共存 |
B.在pH=0的溶液中,Na+、NO 、SO 、SO 、K+可以大量共存 、K+可以大量共存 |
C.由水电离出的氢离子浓度为1.0×10-12mol•L-1溶液中,K+、Cl-、HCO 、Na+可以大量共存 、Na+可以大量共存 |
| D.由0.1mol•L-1一元酸HA溶液的pH=3,可推知NaA溶液存在A-+H2O⇌HA+OH- |
您最近一年使用:0次
名校
解题方法
6 . 常温,下列各组离子在指定溶液中能大量共存的是
A.pH=1的溶液中: I-、NO 、SO 、SO 、Na+ 、Na+ |
B.由水电离的c(H+)=1×10-14 mol•L-1的溶液中:Ca2+、K+、Cl-、HCO |
C.c(H+)/c(OH-)=1012的溶液中: NH 、Al3+、NO 、Al3+、NO 、Cl- 、Cl- |
D.能使KSCN溶液变红的溶液中:SO 、HCO 、HCO 、Na+、Cl- 、Na+、Cl- |
您最近一年使用:0次
7 . T℃时,在20.00mL0.10mol·L-1的一元酸HR溶液中滴入0.10mol·L-1NaOH溶液,溶液pH与NaOH溶液体积的关系如图所示。
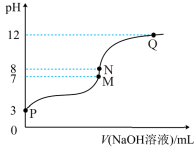
下列说法不正确的是( )

下列说法不正确的是( )
| A..T℃时,HR电离常数Ka≈1.0×10-5 |
| B.M点对应的NaOH溶液体积为20.00mL |
| C.N点与Q点所示溶液中水的电离程度:N>Q |
| D.M点所示溶液中c(Na+)=c(R-) |
您最近一年使用:0次
2020-03-26更新
|
669次组卷
|
6卷引用:广东省兴宁一中2020届高三年级3月质量检测考试(全国I卷)理综化学试题



