T℃时,在20.00mL0.10mol·L-1的一元酸HR溶液中滴入0.10mol·L-1NaOH溶液,溶液pH与NaOH溶液体积的关系如图所示。
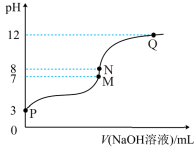
下列说法不正确的是( )

下列说法不正确的是( )
| A..T℃时,HR电离常数Ka≈1.0×10-5 |
| B.M点对应的NaOH溶液体积为20.00mL |
| C.N点与Q点所示溶液中水的电离程度:N>Q |
| D.M点所示溶液中c(Na+)=c(R-) |
更新时间:2020-03-26 09:13:04
|
相似题推荐
单选题
|
较易
(0.85)
解题方法
【推荐1】下列说法错误的是( )
A.0.1mol/L 的硫酸铵溶液中:C(NH )>C(SO )>C(SO ) ) |
| B.25°C 时 pH=2 的醋酸溶液中水电离出的 C(H+)=10-12mol/L |
| C.配制 FeCl3溶液,应加少量盐酸 |
| D.将 Al2(SO4)3溶液蒸干,灼烧得 Al2O3 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐2】25℃时,在 溶液中滴入
溶液中滴入 溶液,溶液pH与NaOH溶液体积的关系如图所示。下列说法正确的是
溶液,溶液pH与NaOH溶液体积的关系如图所示。下列说法正确的是
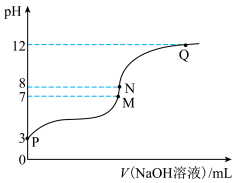
 溶液中滴入
溶液中滴入 溶液,溶液pH与NaOH溶液体积的关系如图所示。下列说法正确的是
溶液,溶液pH与NaOH溶液体积的关系如图所示。下列说法正确的是
| A.M点加入的NaOH溶液的体积为20.00mL |
| B.M、N、Q三点中水的电离程度最大的是Q点 |
C.25℃时, 的电离平衡常数 的电离平衡常数 |
| D.M点到N点过程中水的离子积常数增大 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐3】下列各组离子在指定的溶液中能大量共存的是
A.常温下,水电离的c(OH-)=1×10-12mol·L-1的溶液中:NH 、Fe2+、SO 、Fe2+、SO 、NO 、NO |
B.能使酚酞变红的溶液中:Na+、Ba2+、HC2O 、Cl- 、Cl- |
C.加铝能够产生氢气的溶液:Al3+、Mg2+、S2O 、AlO 、AlO |
D.常温下, =10-10mol·L-1的溶液中:K+、Na+、I-、SO =10-10mol·L-1的溶液中:K+、Na+、I-、SO |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐1】下列叙述正确的是
A.NaHCO3的电离方程式为 |
| B.pH=11的氨水溶液稀释10倍后pH=10 |
| C.NaOH溶液中通入CO2气体至过量,水的电离程度先增大后减小 |
| D.升高温度,NaOH溶液的pH不变 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐2】已知某温度下,K(HCN)=6.2×10-10、K(HF)=6.8×10-4、K(CH3COOH)=1.8×10-5、K(HNO2)=6.4×10-6。物质的量浓度都为0.1 mol/L的下列溶液中,c(H+)浓度由大到小的次序是( )
| A.HCN>HNO2>CH3COOH>HF | B.HF>CH3COOH>HNO2>HCN |
| C.HCN>CH3COOH>HF>HNO2 | D.CH3COOH>HCN>HF>HNO2 |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐3】高氯酸、硫酸、硝酸和盐酸都是强酸,其酸性在水溶液中差别不大。下表是某温度下这四种酸在冰醋酸中的电离常数,由表格数据判断以下说法中不正确的是
酸 | HClO4 | H2SO4 | HCl | HNO3 |
Ka | 1.6×10-5 | 6.3×10-9 | 1.6×10-9 | 4.2×10-10 |
| A.相同条件下在冰醋酸中,硝酸是这四种酸中最弱的酸 |
| B.在冰醋酸中,这四种酸都没有完全电离 |
C.在冰醋酸中,硫酸的电离方程式为H2SO4⇌H++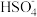 、 、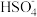 ⇌H++ ⇌H++ |
| D.电解质的强弱与所处的溶剂无关 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐1】对于常温下 的乙酸溶液,下列说法正确的是
的乙酸溶液,下列说法正确的是
 的乙酸溶液,下列说法正确的是
的乙酸溶液,下列说法正确的是A. |
| B.加水稀释到原体积的10倍后溶液pH变为4 |
| C.加入少量乙酸钠固体,溶液pH降低 |
D.乙酸的电离方程式为 |
您最近一年使用:0次
单选题
|
较易
(0.85)
解题方法
【推荐2】表1是元素周期表的一部分:
 时,用浓度为
时,用浓度为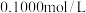 的NaOH溶液分别滴定
的NaOH溶液分别滴定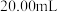 浓度均为
浓度均为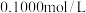 的两种酸HX、
的两种酸HX、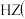 忽略体积变化
忽略体积变化 ,实验数据如表
,实验数据如表
下列判断正确的是
| 氧 | X |
| Y | Z |
 时,用浓度为
时,用浓度为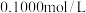 的NaOH溶液分别滴定
的NaOH溶液分别滴定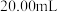 浓度均为
浓度均为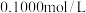 的两种酸HX、
的两种酸HX、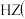 忽略体积变化
忽略体积变化 ,实验数据如表
,实验数据如表| 数据编号 | 滴入NaOH溶液的体积 | 溶液pH | |
| HX | HZ | ||
| ① | 0 | 3 | 1 |
| ② | 20.00 | a | 7 |
A.表格中 |
B.HX和HZ等体积混合后 |
| C.Y和Z两元素的简单氢化物受热分解,前者分解温度高 |
D.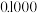  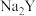 的水溶液中: 的水溶液中: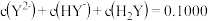  |
您最近一年使用:0次



