名校
解题方法
1 . 回答下列有关水的电离及电解质溶液问题:
(1)某温度时,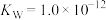 ,该条件下测出
,该条件下测出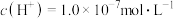 ,溶液呈
,溶液呈_______ (填“酸性”“碱性”或“中性”),若该溶液为碱溶液,则由 电离出来的
电离出来的 为
为_______  。
。
(2)将少量碳酸钠固体加入盐酸中,溶液中水的电离平衡_______ (填“向左”“向右”或“不”,下同)移动。在新制氯水中加入少量NaCl固体,水的电离平衡_______ 移动。
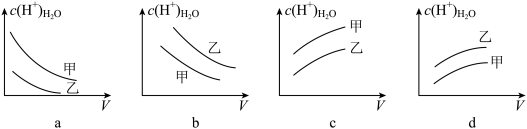
(3)将NaOH(甲)、 (乙)等物质的量浓度的水溶液加水稀释,下图水电离出的
(乙)等物质的量浓度的水溶液加水稀释,下图水电离出的 与加入水的体积
与加入水的体积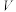 的关系正确的是
的关系正确的是_______ 。
(4)25℃时,pH=4的盐酸中水的电离程度_______ (填“大于”“小于”或“等于”)pH=10的 溶液中水的电离程度。
溶液中水的电离程度。
(1)某温度时,
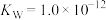 ,该条件下测出
,该条件下测出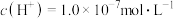 ,溶液呈
,溶液呈 电离出来的
电离出来的 为
为 。
。(2)将少量碳酸钠固体加入盐酸中,溶液中水的电离平衡
(3)将NaOH(甲)、
 (乙)等物质的量浓度的水溶液加水稀释,下图水电离出的
(乙)等物质的量浓度的水溶液加水稀释,下图水电离出的 与加入水的体积
与加入水的体积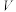 的关系正确的是
的关系正确的是
(4)25℃时,pH=4的盐酸中水的电离程度
 溶液中水的电离程度。
溶液中水的电离程度。
您最近一年使用:0次
2023-01-14更新
|
251次组卷
|
3卷引用:四川省绵阳市高中2022-2023学年高二理科突击班下学期3月月考化学试题
四川省绵阳市高中2022-2023学年高二理科突击班下学期3月月考化学试题山东省文登第一中学2022-2023学年高二上学期1月期末考试化学试题(已下线)专题06 电离平衡 水的电离和溶液的pH-【好题汇编】备战2023-2024学年高二化学上学期期末真题分类汇编(人教版2019)
解题方法
2 . 回答下列问题:
(1)已知100℃时,水的离子积常数为 ,该温度下,有pH=11的NaOH溶液100mL,要使它的pH变为10(体积变化忽略不计):
,该温度下,有pH=11的NaOH溶液100mL,要使它的pH变为10(体积变化忽略不计):
①如果加入蒸馏水,应加___________ mL;
②如果加入pH=9的NaOH溶液,应加___________ mL;
③如果加入0.01 的盐酸,应加
的盐酸,应加___________ mL。
(2)在t℃时,测得0.01 NaOH溶液的pH=11,0.1
NaOH溶液的pH=11,0.1 的HA溶液中
的HA溶液中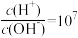 。回答下列问题:
。回答下列问题:
①该温度下,水的离子积常数Kw=___________ ;
②该温度下,0.1 的HA溶液中由水电离出的c(H+)=
的HA溶液中由水电离出的c(H+)=___________  。
。
(3)①明矾溶液呈___________ (填“酸性”“中性”或“碱性”),原因是___________ (用离子方程式表示);
②将氯化铁溶液蒸干灼烧得到的固体物质是___________ (填化学式)。
(1)已知100℃时,水的离子积常数为
 ,该温度下,有pH=11的NaOH溶液100mL,要使它的pH变为10(体积变化忽略不计):
,该温度下,有pH=11的NaOH溶液100mL,要使它的pH变为10(体积变化忽略不计):①如果加入蒸馏水,应加
②如果加入pH=9的NaOH溶液,应加
③如果加入0.01
 的盐酸,应加
的盐酸,应加(2)在t℃时,测得0.01
 NaOH溶液的pH=11,0.1
NaOH溶液的pH=11,0.1 的HA溶液中
的HA溶液中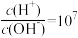 。回答下列问题:
。回答下列问题:①该温度下,水的离子积常数Kw=
②该温度下,0.1
 的HA溶液中由水电离出的c(H+)=
的HA溶液中由水电离出的c(H+)= 。
。(3)①明矾溶液呈
②将氯化铁溶液蒸干灼烧得到的固体物质是
您最近一年使用:0次
3 . I.(1)25℃时,10L水中含H+的个数为________ 个(设阿伏加 德罗常数为NA,下同。),1g水中含H+的个数为________ 个。
(2)某温度(t℃)时,水的Kw=1×10-12,则该温度________ 25℃(填“>”“<”或“=”),该温度下,c(H+)=1×10-7mol·L-1的溶液呈________ (填“酸性”“碱性”或“中性”);若该溶液中只存在NaOH溶质,则由H2O电离出来的c(OH-)=________ mol·L-1。
II.氯化铁主要用于金属蚀刻、污水处理,具有效果好、价格便宜等优点。请回答下列有关氯化铁的问题:
(1)用FeCl3作净水剂的原理用化学用语解释为________ ,配制FeCl3溶液时需要加入少量的浓盐酸,其作用为________ 。
(2)25℃时,Ksp[Fe(OH)3]=4.0×10-38。Fe3+发生水解反应Fe3++3H2O Fe(OH)3+3H+,该反应的平衡常数为
Fe(OH)3+3H+,该反应的平衡常数为______________ 。
(2)某温度(t℃)时,水的Kw=1×10-12,则该温度
II.氯化铁主要用于金属蚀刻、污水处理,具有效果好、价格便宜等优点。请回答下列有关氯化铁的问题:
(1)用FeCl3作净水剂的原理用化学用语解释为
(2)25℃时,Ksp[Fe(OH)3]=4.0×10-38。Fe3+发生水解反应Fe3++3H2O
 Fe(OH)3+3H+,该反应的平衡常数为
Fe(OH)3+3H+,该反应的平衡常数为
您最近一年使用:0次



