1 . 化学电池不仅可以作为电源将化学能转化为电能,还可以通过对电池电动势的测定求出电池反应的平衡常数。例如,将酸碱中和反应作为电池反应,可以设计出相应的电池,并由其电动势求出中和反应平衡常数及水的离子积。现将两个氢电极(以Pt 作为导电的惰性金属,以氢气作为参与电极反应的物质,可以是生成氢气,也可以是消耗氢气)分别置于酸性水溶液( H+)和碱性水溶液(OH-)中构成电池,使电池反应为酸碱中和反应。
(1)酸溶液中的氢电极A和碱溶液中的氢电极B,为电池正极是___________ (填 A或B) ;
(2)A, B上分别发生的电极反应为:A极:___________ ;B极:___________ ;
(3)总反应式为___________ ,该反应的平衡常数K与水的离子积Kw的关系是___________ 。
(1)酸溶液中的氢电极A和碱溶液中的氢电极B,为电池正极是
(2)A, B上分别发生的电极反应为:A极:
(3)总反应式为
您最近一年使用:0次
名校
解题方法
2 . 下列叙述正确的是
| A.无论是纯水,还是酸性、碱性或中性稀溶液,在常温下,其c(H+)·c(OH-)=1×10-14 |
| B.c(H+)=1×10-7 mol·L-1的溶液一定是中性溶液 |
| C.0.2 mol·L-1 CH3COOH溶液中的c(H+)是0.1 mol·L-1 CH3COOH溶液中的c(H+)的2倍 |
| D.任何浓度的溶液都可以用pH来表示其酸碱性的强弱 |
您最近一年使用:0次
2022-04-11更新
|
232次组卷
|
18卷引用:江苏省启东中学2019-2020学年高二上学期第一次质量检测化学试题
江苏省启东中学2019-2020学年高二上学期第一次质量检测化学试题(已下线)2011-2012年江西省吉安一中高二上学期期中考试化学(理)试题(已下线)2014届高考化学二轮复习提分训练 专题7水溶液中的离子平衡练习卷(已下线)2014年高二化学人教版选修四 12水的电离 溶液的酸碱性练习卷(已下线)2014-2015学年山西省山大附中高二上学期期中化学试卷2015-2016学年辽宁省实验中学高一下学期期末考试化学卷2016-2017学年陕西省西安一中高二上期中化学试卷甘肃省临夏中学2016-2017学年高二上学期期末考试化学试题西藏自治区拉萨中学2017-2018学年高二上学期第二次月考理综化学试题安徽省定远重点中学2018-2019学年高二上学期第三次月考化学试题云南省丘北县第二中学2018-2019学年高二下学期6月份考试化学试题陕西省西安中学2019-2020学年高二12月月考化学试题陕西省黄陵中学2019-2020学年高二上学期期末考试(重点班)化学试题(已下线)3.2.1 溶液的酸碱性(备作业)-【上好课】2021-2022学年高二化学同步备课系列(苏教版2019选择性必修1)云南省玉溪市通海县第一中学2021-2022学年高二上学期期末考试化学试题云南省玉溪市通海县第三中学2021-2022学年高二上学期期末考试化学试题(已下线)3.1.1 水的电离和溶液的酸碱性-【帮课堂】2022-2023学年高二化学同步精品讲义(沪科版2020选择性必修第一册)贵州省威宁彝族回族苗族自治县第八中学2023-2024学年高二上学期期中考试化学试卷
3 . 水是“生命之基质”,是“永远值得探究的物质”。
(1)关于反应H2(g)+ O2(g)=H2O(l),下列说法不正确的是
O2(g)=H2O(l),下列说法不正确的是______
A. 焓变ΔH<0,熵变ΔS<0
B. 可以把反应设计成原电池,实现能量的转化
C. 一定条件下,若观察不到水的生成,说明该条件下反应不能自发进行
D. 选用合适的催化剂,有可能使反应在常温常压下以较快的速率进行
(2)根据H2O的成键特点,画出与图中H2O分子直接相连的所有氢键(O—H…O)______ 。

(3)水在高温高压状态下呈现许多特殊的性质。当温度、压强分别超过临界温度(374.2℃)、临界压强(22.1MPa)时的水称为超临界水。
①与常温常压的水相比。高温高压液态水的离子积会显著增大。解释其原因______ 。
②如果水的离子积Kw从10×10-14增大到1.0×10-10,则相应的电离度是原来的______ 倍。
③超临界水能够与氧气等氧化剂以任意比例互溶,由此发展了超临界水氧化技术。一定实验条件下,测得乙醇的超临界水氧化结果如图所示,其中x为以碳元素计算的物质的量分数,t为反应时间。

下列说法合理的是______
A. 乙醇的超临界水氧化过程中,一氧化碳是中间产物,二氧化碳是最终产物
B. 在550℃条件下,反应时间大于15s时,乙醇氧化为二氧化碳已趋于完全
C. 乙醇的超临界水氧化过程中,乙醇的消耗速率或二氧化碳的生成速率都可以用来表示反应的速率,而且两者数值相等
D. 随温度升高,xCO峰值出现的时间提前,且峰值更高,说明乙醇的氧化速率比一氧化碳氧化速率的增长幅度更大
(4)以铂阳极和石墨阴极设计电解池,通过电解NH4HSO4溶液产生(NH4)2S2O8,再与水反应得到H2O2;其中生成的NH4HSO4可以循环使用。
①阳极的电极反应式是______ 。
②制备H2O2的总反应方程式是______ 。
(1)关于反应H2(g)+
 O2(g)=H2O(l),下列说法不正确的是
O2(g)=H2O(l),下列说法不正确的是A. 焓变ΔH<0,熵变ΔS<0
B. 可以把反应设计成原电池,实现能量的转化
C. 一定条件下,若观察不到水的生成,说明该条件下反应不能自发进行
D. 选用合适的催化剂,有可能使反应在常温常压下以较快的速率进行
(2)根据H2O的成键特点,画出与图中H2O分子直接相连的所有氢键(O—H…O)

(3)水在高温高压状态下呈现许多特殊的性质。当温度、压强分别超过临界温度(374.2℃)、临界压强(22.1MPa)时的水称为超临界水。
①与常温常压的水相比。高温高压液态水的离子积会显著增大。解释其原因
②如果水的离子积Kw从10×10-14增大到1.0×10-10,则相应的电离度是原来的
③超临界水能够与氧气等氧化剂以任意比例互溶,由此发展了超临界水氧化技术。一定实验条件下,测得乙醇的超临界水氧化结果如图所示,其中x为以碳元素计算的物质的量分数,t为反应时间。

下列说法合理的是
A. 乙醇的超临界水氧化过程中,一氧化碳是中间产物,二氧化碳是最终产物
B. 在550℃条件下,反应时间大于15s时,乙醇氧化为二氧化碳已趋于完全
C. 乙醇的超临界水氧化过程中,乙醇的消耗速率或二氧化碳的生成速率都可以用来表示反应的速率,而且两者数值相等
D. 随温度升高,xCO峰值出现的时间提前,且峰值更高,说明乙醇的氧化速率比一氧化碳氧化速率的增长幅度更大
(4)以铂阳极和石墨阴极设计电解池,通过电解NH4HSO4溶液产生(NH4)2S2O8,再与水反应得到H2O2;其中生成的NH4HSO4可以循环使用。
①阳极的电极反应式是
②制备H2O2的总反应方程式是
您最近一年使用:0次
4 . (1)某温度(t℃)时,测得0.01mol/L的NaOH溶液的pH=11,则该温度下水的KW=_______ 。在此温度下,将pH=a的NaOH溶液Va L与pH=b的H2SO4溶液Vb L混合,若所得混合液为中性,且a+b=12,则Va:Vb=___________ 。
(2)25℃时,0.1mol/L的HaA溶液中c(H+)/c(OH-)=1010,请回答下列问题:
①HaA是___________ (填“强电解质”或“弱电解质”)。
②在加水稀释HaA溶液的过程中,随着水量的增加而增大的是__________ (填字母)
A.c(HaA) B.c(H+)/c(HaA) C.c(H+)与c(OH-)的乘积 D.c(OH-)
③NanA溶液显__________ (填“酸性”、“中性”或“碱性”),理由是(用离子方程式表示)____________ 。
(2)25℃时,0.1mol/L的HaA溶液中c(H+)/c(OH-)=1010,请回答下列问题:
①HaA是
②在加水稀释HaA溶液的过程中,随着水量的增加而增大的是
A.c(HaA) B.c(H+)/c(HaA) C.c(H+)与c(OH-)的乘积 D.c(OH-)
③NanA溶液显
您最近一年使用:0次
2016-07-12更新
|
308次组卷
|
2卷引用:2015-2016学年江苏省泰州中学高一创新班下期末化学试卷
5 . 根据下列图示所得出的结论不正确的是


A.图甲是常温下用 的 的 溶液分别滴定 溶液分别滴定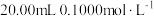 一元酸 一元酸 、 、 的滴定曲线,说明 的滴定曲线,说明 的酸性大于 的酸性大于 |
B.图乙表示温度在 和 和 时水溶液中 时水溶液中 和 和 的关系,则阴影部分M内任意一点均满足 的关系,则阴影部分M内任意一点均满足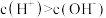 |
C.图丙表示改变平衡体系 的某一条件后,v(正)、v(逆)的变化情况,可推知 的某一条件后,v(正)、v(逆)的变化情况,可推知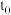 时刻改变的条件是升高温度 时刻改变的条件是升高温度 |
D.图丁表示炭黑作用下 生成活化氧过程中能量变化情况,说明每活化一个氧分子放出 生成活化氧过程中能量变化情况,说明每活化一个氧分子放出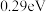 能量 能量 |
您最近一年使用:0次
2022-06-28更新
|
246次组卷
|
2卷引用:江苏省徐州市2021-2022学年高二下学期期末抽测化学试题



